

Структура белка – это трехмерное расположение атомов в молекуле с аминокислотной цепью . Белки — это полимеры , в частности полипептиды , образованные из последовательностей аминокислот , которые являются мономерами полимера. Мономер одной аминокислоты также можно назвать остатком , который указывает на повторяющуюся единицу полимера. Белки образуются из аминокислот, подвергающихся реакциям конденсации , в которых аминокислоты теряют одну молекулу воды за каждую реакцию , чтобы прикрепиться друг к другу пептидной связью . По соглашению цепь длиной менее 30 аминокислот часто идентифицируется как пептид , а не белок. [1] Чтобы иметь возможность выполнять свою биологическую функцию, белки складываются в одну или несколько определенных пространственных конформаций, управляемых рядом нековалентных взаимодействий , таких как водородные связи , ионные взаимодействия , силы Ван-дер-Ваальса и гидрофобная упаковка. Чтобы понять функции белков на молекулярном уровне, часто необходимо определить их трехмерную структуру . Это тема научной области структурной биологии , которая использует такие методы, как рентгеновская кристаллография , ЯМР-спектроскопия , криоэлектронная микроскопия (крио-ЭМ) и интерферометрия двойной поляризации , для определения структуры белков.
Размер белковых структур варьируется от десятков до нескольких тысяч аминокислот. [2] По физическому размеру белки классифицируются как наночастицы размером от 1 до 100 нм. Из белковых субъединиц могут образовываться очень большие белковые комплексы . Например, многие тысячи молекул актина собираются в микрофиламент .
Белок обычно претерпевает обратимые структурные изменения при выполнении своей биологической функции. Альтернативные структуры одного и того же белка называются разными конформациями , а переходы между ними — конформационными изменениями .
Существует четыре различных уровня структуры белка.
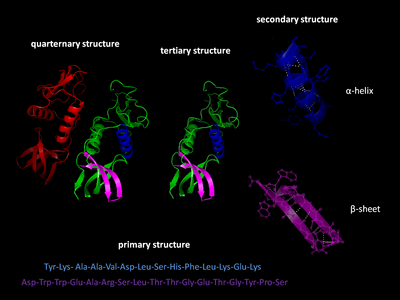
Первичная структура белка относится к последовательности аминокислот в полипептидной цепи. Первичная структура удерживается вместе пептидными связями , которые образуются в процессе биосинтеза белка . Два конца полипептидной цепи называются карбоксильным концом (С-конец) и аминоконцом (N-конец) в зависимости от природы свободной группы на каждом конце. Подсчет остатков всегда начинается с N-конца (NH 2 -группы), который является концом, на котором аминогруппа не участвует в пептидной связи. Первичная структура белка определяется геном, соответствующим белку. Определенная последовательность нуклеотидов в ДНК транскрибируется в мРНК , которая считывается рибосомой в процессе, называемом трансляцией . Последовательность аминокислот в инсулине была открыта Фредериком Сэнгером , установившим, что белки имеют определяющие аминокислотные последовательности. [3] [4] Последовательность белка уникальна для этого белка и определяет структуру и функцию белка. Последовательность белка можно определить такими методами, как деградация по Эдману или тандемная масс-спектрометрия . Однако часто он считывается непосредственно из последовательности гена с помощью генетического кода . При обсуждении белков строго рекомендуется использовать слова «аминокислотные остатки», поскольку при образовании пептидной связи теряется молекула воды , и поэтому белки состоят из аминокислотных остатков. Посттрансляционные модификации, такие как фосфорилирование и гликозилирование , обычно также считаются частью первичной структуры и не могут быть считаны из гена. Например, инсулин состоит из 51 аминокислоты в 2 цепях. Одна цепь содержит 31 аминокислоту, а другая — 20 аминокислот.
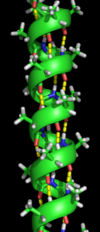
Вторичная структура относится к очень регулярным локальным субструктурам реальной основной цепи полипептида. Два основных типа вторичной структуры, α-спираль и β-цепь или β-листы , были предложены в 1951 году Лайнусом Полингом . [5] Эти вторичные структуры определяются характером водородных связей между пептидными группами основной цепи. Они имеют правильную геометрию и ограничены конкретными значениями двугранных углов ψ и φ на графике Рамачандрана . И α-спираль, и β-лист представляют собой способ насыщения всех доноров и акцепторов водородных связей в пептидном остове. Некоторые части белка упорядочены, но не образуют регулярных структур. Их не следует путать со случайным клубком — развернутой полипептидной цепью, лишенной какой-либо фиксированной трехмерной структуры. Несколько последовательных вторичных структур могут образовывать « супервторичную единицу ». [6]
Третичная структура относится к трехмерной структуре, созданной одной молекулой белка (одной полипептидной цепью ). Он может включать один или несколько доменов . α-спирали и β-складчатые листы свернуты в компактную глобулярную структуру . Складывание обусловлено неспецифическими гидрофобными взаимодействиями , захоронением гидрофобных остатков из воды , но структура стабильна только тогда, когда части белкового домена зафиксированы на месте специфическими третичными взаимодействиями, такими как солевые мостики , водородные связи, и плотная упаковка боковых цепей и дисульфидных связей . Дисульфидные связи в цитозольных белках встречаются крайне редко, поскольку цитозоль ( внутриклеточная жидкость) обычно является восстановительной средой.
Четвертичная структура — это трехмерная структура, состоящая из агрегации двух или более отдельных полипептидных цепей (субъединиц), которые действуют как единая функциональная единица ( мультимер ). Образующийся мультимер стабилизируется теми же нековалентными взаимодействиями и дисульфидными связями, что и третичная структура. Существует множество возможных организаций четвертичной структуры. [7] Комплексы двух или более полипептидов (т.е. нескольких субъединиц) называются мультимерами . В частности, его можно было бы назвать димером , если он содержит две субъединицы, тримером , если он содержит три субъединицы, тетрамером , если он содержит четыре субъединицы, и пентамером , если он содержит пять субъединиц, и так далее. Субъединицы часто связаны друг с другом операциями симметрии , такими как ось 2-го порядка в димере. Мультимеры, состоящие из идентичных субъединиц, обозначаются префиксом «гомо-», а мультимеры, состоящие из разных субъединиц, обозначаются префиксом «гетеро-», например, гетеротетрамер, такой как два альфа и два бета. цепочки гемоглобина .

Белки часто описывают как состоящие из нескольких структурных единиц. Эти единицы включают домены, мотивы и складки. Несмотря на то, что в эукариотических системах экспрессируется около 100 000 различных белков , различных доменов, структурных мотивов и складок гораздо меньше.
Структурный домен — это элемент общей структуры белка, который является самостабилизирующимся и часто сворачивается независимо от остальной части белковой цепи. Многие домены не являются уникальными для белковых продуктов одного гена или одного семейства генов , а вместо этого появляются в различных белках. Домены часто называют и выделяют, потому что они играют важную роль в биологической функции белка, которому они принадлежат; например, « кальцийсвязывающий домен кальмодулина ». Поскольку они независимо стабильны, домены можно «обменять» с помощью генной инженерии между одним белком и другим, чтобы создать химеры . Консервативная комбинация нескольких доменов, которые встречаются в разных белках, таких как домен протеинтирозинфосфатазы и пара доменов C2 , была названа «супердоменом», который может развиваться как единая единица. [8]
Структурные и последовательность мотивов относятся к коротким сегментам трехмерной структуры белка или аминокислотной последовательности, которые были обнаружены в большом количестве различных белков .
Третичные белковые структуры могут иметь несколько вторичных элементов в одной и той же полипептидной цепи. Супервторичная структура относится к определенной комбинации элементов вторичной структуры , таких как единицы β-α-β или мотив спираль-поворот-спираль . Некоторые из них можно также назвать структурными мотивами.
Складка белка относится к общей архитектуре белка, такой как пучок спирали , β-цилиндр , складка Россмана или различные «складки», представленные в базе данных структурной классификации белков . [9] Родственной концепцией является топология белка .
Белки не являются статичными объектами, а скорее населяют ансамбли конформационных состояний . Переходы между этими состояниями обычно происходят на наномасштабах и связаны с функционально значимыми явлениями, такими как аллостерическая передача сигналов [10] и ферментативный катализ . [11] Динамика белков и конформационные изменения позволяют белкам функционировать как наноразмерные биологические машины внутри клеток, часто в форме мультибелковых комплексов . [12] Примеры включают моторные белки , такие как миозин , который отвечает за сокращение мышц , кинезин , который перемещает груз внутри клеток от ядра по микротрубочкам , и динеин , который перемещает груз внутри клеток к ядру и вызывает аксонемное биение подвижные реснички и жгутики . «По сути, [подвижная ресничка] представляет собой наномашину, состоящую, возможно, из более чем 600 белков в молекулярных комплексах, многие из которых также функционируют независимо как наномашины... Гибкие линкеры позволяют соединенным ими мобильным белковым доменам рекрутировать свое связывание партнеров и индуцируют дальнюю аллостерию посредством динамики белковых доменов ». [13]

Белки часто рассматривают как относительно стабильные третичные структуры , которые претерпевают конформационные изменения под воздействием взаимодействия с другими белками или в результате ферментативной активности. Однако белки могут иметь различную степень стабильности, а некоторые из менее стабильных вариантов являются белками с внутренней неупорядоченностью . Эти белки существуют и функционируют в относительно «неупорядоченном» состоянии, лишенном стабильной третичной структуры . В результате их трудно описать единой фиксированной третичной структурой . Конформационные ансамбли были разработаны как способ обеспечить более точное и «динамическое» представление конформационного состояния внутренне неупорядоченных белков . [15] [14]
Файлы белковых ансамблей представляют собой представление белка, который можно считать имеющим гибкую структуру. Для создания этих файлов необходимо определить, какие из различных теоретически возможных конформаций белка действительно существуют. Один из подходов заключается в применении вычислительных алгоритмов к данным о белках, чтобы попытаться определить наиболее вероятный набор конформаций для файла ансамбля . Существует несколько методов подготовки данных для базы данных белковых ансамблей, которые делятся на две общие методологии – подходы пула и молекулярной динамики (МД) (показаны на рисунке). Подход на основе пула использует аминокислотную последовательность белка для создания огромного пула случайных конформаций. Затем этот пул подвергается дополнительной вычислительной обработке, в результате которой создается набор теоретических параметров для каждой конформации на основе структуры. Из этого пула отобраны конформационные подмножества, средние теоретические параметры которых близко соответствуют известным экспериментальным данным для этого белка. Альтернативный подход молекулярной динамики учитывает одновременно несколько случайных конформаций и подвергает их всем экспериментальным данным. Здесь экспериментальные данные служат ограничениями на конформации (например, известные расстояния между атомами). Принимаются только конформации, которым удается оставаться в пределах, установленных экспериментальными данными. Этот подход часто применяет большие объемы экспериментальных данных к конформациям, что является очень сложной вычислительной задачей. [14]
Конформационные ансамбли были созданы для ряда высокодинамичных и частично развернутых белков, таких как Sic1 / Cdc4 , [16] p15 PAF , [17] MKK7 , [18] Бета-синуклеин [19] и P27 [20].
При трансляции полипептиды покидают рибосому в основном в виде случайной спирали и сворачиваются в свое нативное состояние . [21] [22] Обычно считается, что окончательная структура белковой цепи определяется ее аминокислотной последовательностью ( догма Анфинсена ). [23]
Термодинамическая стабильность белков представляет собой разницу в свободной энергии между свернутым и развернутым состояниями белка. Эта разница свободной энергии очень чувствительна к температуре, поэтому изменение температуры может привести к разворачиванию или денатурации. Денатурация белка может привести к потере функции и потере нативного состояния. Свободная энергия стабилизации растворимых глобулярных белков обычно не превышает 50 кДж/моль. [ нужна цитата ] Принимая во внимание большое количество водородных связей, которые имеют место для стабилизации вторичных структур, а также стабилизации внутреннего ядра посредством гидрофобных взаимодействий, свободная энергия стабилизации проявляется как небольшая разница между большими числами. [24]


Около 90% белковых структур, доступных в Банке данных белков, были определены методом рентгеновской кристаллографии . [25] Этот метод позволяет измерить трехмерное (3-D) распределение плотности электронов в белке в кристаллическом состоянии и тем самым сделать вывод о трехмерных координатах всех атомов , которые необходимо определить с определенным разрешением. . Примерно 7% известных белковых структур были получены методами ядерного магнитного резонанса (ЯМР). [26] Для более крупных белковых комплексов криоэлектронная микроскопия может определить структуру белка. Разрешение обычно ниже, чем у рентгеновской кристаллографии или ЯМР, но максимальное разрешение постоянно увеличивается. Этот метод по-прежнему особенно ценен для очень больших белковых комплексов, таких как белки оболочки вируса и амилоидные волокна.
Общий состав вторичной структуры можно определить с помощью кругового дихроизма . Колебательную спектроскопию также можно использовать для характеристики конформации пептидов, полипептидов и белков. [27] Двумерная инфракрасная спектроскопия стала ценным методом исследования структур гибких пептидов и белков, которые невозможно изучить другими методами. [28] [29] Более качественную картину структуры белка часто получают с помощью протеолиза , который также полезен для скрининга более кристаллизующихся образцов белка. Новые реализации этого подхода, включая быстрый параллельный протеолиз (FASTpp) , позволяют исследовать структурированную фракцию и ее стабильность без необходимости очистки. [30] После того, как структура белка определена экспериментально, дальнейшие детальные исследования могут быть проведены вычислительным путем с использованием молекулярно-динамического моделирования этой структуры. [31]
База данных о структурах белков — это база данных, которая моделируется на основе различных экспериментально определенных структур белков. Целью большинства баз данных о структурах белков является организация и аннотирование белковых структур, предоставляя биологическому сообществу полезный доступ к экспериментальным данным. Данные, включенные в базы данных структур белков, часто включают трехмерные координаты, а также экспериментальную информацию, такую как размеры и углы элементарных ячеек для структур, определенных рентгеновской кристаллографией . Хотя большинство примеров (в данном случае либо белков, либо определений конкретной структуры белка) также содержат информацию о последовательностях, а некоторые базы данных даже предоставляют средства для выполнения запросов на основе последовательностей, основным атрибутом базы данных структуры является структурная информация, тогда как базы данных последовательностей фокусируются на информацию о последовательности и не содержат структурной информации для большинства записей. Базы данных о структурах белков имеют решающее значение для многих усилий в вычислительной биологии , таких как разработка лекарств на основе структуры , как при разработке используемых вычислительных методов, так и при предоставлении большого набора экспериментальных данных, используемых некоторыми методами для обеспечения понимания функции белка. [32]
Белковые структуры можно группировать на основе их структурного сходства, топологического класса или общего эволюционного происхождения. База данных структурной классификации белков [33] и база данных CATH [34] предоставляют две разные структурные классификации белков. Когда структурное сходство велико, два белка, возможно, разошлись от общего предка [35] , и общая структура белков считается свидетельством гомологии . Сходство структур затем можно использовать для группировки белков в суперсемейства белков . [36] Если общая структура значительна, но общая доля мала, общий фрагмент может быть следствием более драматического эволюционного события, такого как горизонтальный перенос генов , и объединение белков, разделяющих эти фрагменты, в суперсемейства белков больше не оправдано. [35] Топологию белка также можно использовать для классификации белков. Теория узлов и топология цепей — это две концепции топологии, разработанные для классификации складок белка на основе пересечения цепей и внутрицепочечных контактов соответственно.
Создать последовательность белка гораздо проще, чем определить структуру белка. Однако структура белка дает гораздо больше информации о функции белка, чем его последовательность. Поэтому был разработан ряд методов компьютерного предсказания структуры белка по его последовательности. [37] Методы предсказания ab initio используют только последовательность белка. Методы моделирования потоков и гомологии позволяют построить трехмерную модель белка неизвестной структуры на основе экспериментальных структур эволюционно родственных белков, называемых семейством белков .
{{cite book}}: |journal=игнорируется ( помощь )