

Первичная структура белка — это линейная последовательность аминокислот в пептиде или белке . [1] Обычно первичную структуру белка описывают, начиная с аминоконцевого (N) конца и заканчивая карбоксильным (C) концом. Биосинтез белка чаще всего осуществляется рибосомами в клетках. Пептиды также можно синтезировать в лаборатории. Первичные структуры белков можно секвенировать непосредственно или вывести из последовательностей ДНК .
Аминокислоты полимеризуются посредством пептидных связей с образованием длинной основной цепи , вдоль которой выступают различные боковые цепи аминокислот. В биологических системах белки производятся во время трансляции рибосомами клетки . Некоторые организмы также могут создавать короткие пептиды путем нерибосомального пептидного синтеза , в котором часто используются аминокислоты, отличные от стандартных 20, и которые могут подвергаться циклизации, модификации и сшиванию.
Пептиды можно синтезировать химическим путем с помощью ряда лабораторных методов. Химические методы обычно синтезируют пептиды в порядке, противоположном (начиная с С-конца) биологическому синтезу белка (начиная с N-конца).
Последовательность белка обычно обозначается в виде строки букв, в которой перечислены аминокислоты, начиная с аминоконца и до карбоксильного конца. Для обозначения 20 встречающихся в природе аминокислот, а также смесей или неоднозначных аминокислот можно использовать трехбуквенный или однобуквенный код (аналогично нотации нуклеиновых кислот ). [1] [2] [3]
Пептиды можно секвенировать непосредственно или вывести из последовательностей ДНК . В настоящее время существуют большие базы данных последовательностей , в которых сопоставляются известные последовательности белков.
В общем, полипептиды представляют собой неразветвленные полимеры, поэтому их первичную структуру часто можно определить с помощью последовательности аминокислот вдоль их основной цепи. Однако белки могут сшиваться, чаще всего за счет дисульфидных связей , а первичная структура также требует указания сшивающих атомов, например, указания цистеинов , участвующих в дисульфидных связях белка. Другие сшивки включают десмозин .
Хиральные центры полипептидной цепи могут подвергаться рацемизации . Хотя это не меняет последовательность, оно влияет на химические свойства последовательности. В частности, L -аминокислоты, обычно встречающиеся в белках, могут спонтанно изомеризоваться по атому с образованием D -аминокислот, которые не могут быть расщеплены большинством протеаз . Кроме того, пролин может образовывать стабильные транс-изомеры по пептидной связи.
Кроме того, белок может подвергаться множеству посттрансляционных модификаций , которые кратко суммированы здесь.
N-концевая аминогруппа полипептида может быть модифицирована ковалентно, например,
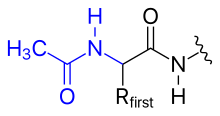
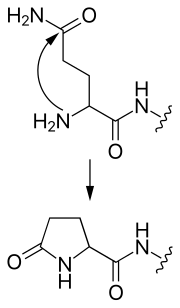
С-концевая карбоксилатная группа полипептида также может быть модифицирована, например,
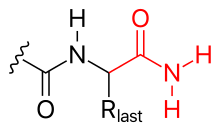
Наконец, боковые цепи пептида также могут быть модифицированы ковалентно, например,
Большинство модификаций полипептидов, перечисленных выше, происходят посттрансляционно , т.е. после того, как белок был синтезирован на рибосоме , обычно происходящей в эндоплазматическом ретикулуме , субклеточной органелле эукариотической клетки.
Многие другие химические реакции (например, цианилирование) применялись химиками к белкам, хотя они не обнаружены в биологических системах.
Помимо перечисленных выше, наиболее важной модификацией первичной структуры является расщепление пептидов (путем химического гидролиза или протеазами ). Белки часто синтезируются в неактивной форме-предшественнике; обычно N-концевой или C-концевой сегмент блокирует активный центр белка, подавляя его функцию. Белок активируется путем отщепления ингибирующего пептида.
Некоторые белки даже способны расщеплять себя. Обычно гидроксильная группа серина (редко треонина) или тиоловая группа остатка цистеина атакует карбонильный углерод предыдущей пептидной связи, образуя тетраэдрически связанное промежуточное соединение [классифицируемое как гидроксиоксазолидин (Ser/Thr) или гидрокситиазолидин ((Ser/Thr) или гидрокситиазолидин ( Cys) промежуточный]. Это промежуточное соединение имеет тенденцию вернуться в амидную форму, вытесняя атакующую группу, поскольку свободная энергия обычно благоприятствует амидной форме (предположительно из-за сильной резонансной стабилизации пептидной группы). Однако дополнительные молекулярные взаимодействия могут сделать амидную форму менее стабильной; вместо этого аминогруппа удаляется, в результате чего вместо пептидной связи образуется сложноэфирная (Ser/Thr) или тиоэфирная (Cys) связь. Эта химическая реакция называется NO-ацильным сдвигом.
Эфирно-тиоэфирную связь можно разрешить несколькими способами:
Сжатие аминокислотных последовательностей является сравнительно сложной задачей. Существующие специализированные компрессоры аминокислотных последовательностей уступают компрессорам последовательностей ДНК, главным образом из-за характеристик данных. Например, моделировать инверсии сложнее из-за обратной потери информации (от аминокислот к последовательности ДНК). Текущий компрессор данных без потерь, обеспечивающий более высокий уровень сжатия, — AC2. [5] AC2 смешивает различные контекстные модели с использованием нейронных сетей и кодирует данные с помощью арифметического кодирования.
Предположение о том, что белки представляют собой линейные цепочки α-аминокислот, было высказано почти одновременно двумя учеными на одной и той же конференции в 1902 году, 74-м собрании Общества немецких ученых и врачей, проходившем в Карлсбаде. Франц Хофмайстер сделал это предложение утром, основываясь на своих наблюдениях за биуретовой реакцией в белках. Через несколько часов за Хофмейстером последовал Эмиль Фишер , накопивший множество химических данных, подтверждающих модель пептидной связи. Для полноты картины: предположение о наличии в белках амидных связей было сделано еще в 1882 г. французским химиком Э. Гримо. [6]
Несмотря на эти данные и более поздние доказательства того, что протеолитически расщепленные белки дают только олигопептиды, идея о том, что белки представляют собой линейные, неразветвленные полимеры аминокислот, не была принята сразу. Некоторые уважаемые ученые, такие как Уильям Эстбери, сомневались, что ковалентные связи достаточно сильны, чтобы удерживать вместе такие длинные молекулы; они боялись, что тепловые колебания расшатают такие длинные молекулы. Герман Штаудингер столкнулся с подобными предрассудками в 1920-х годах, когда утверждал, что каучук состоит из макромолекул . [6]
Таким образом, возникло несколько альтернативных гипотез. Гипотеза коллоидных белков утверждала, что белки представляют собой коллоидные совокупности более мелких молекул. Эта гипотеза была опровергнута в 1920-х годах измерениями ультрацентрифугирования Теодора Сведберга , которые показали, что белки имеют четко определенную, воспроизводимую молекулярную массу, и электрофоретическими измерениями Арне Тиселиуса , которые показали, что белки представляют собой отдельные молекулы. Вторая гипотеза, гипотеза циклола , выдвинутая Дороти Ринч , предполагала, что линейный полипептид претерпел химическую циклольную перегруппировку C=O + HN C(OH)-N, которая сшивала его основные амидные группы, образуя двумерную ткань . Другие первичные структуры белков были предложены различными исследователями, такими как модель дикетопиперазина Эмиля Абдерхальдена и модель пиррола/пиперидина Троэнсегаарда в 1942 году. Хотя эти альтернативные модели никогда не пользовались большим доверием, они были окончательно опровергнуты, когда Фредерик Сэнгер успешно секвенировал инсулин [ когда ? ] и кристаллографическим определением миоглобина и гемоглобина Максом Перутцем и Джоном Кендрю [ когда? ] .
Можно сказать, что любой гетерополимер с линейной цепью имеет «первичную структуру» по аналогии с использованием этого термина для белков, но такое использование встречается редко по сравнению с чрезвычайно распространенным использованием в отношении белков. В РНК , которая также имеет обширную вторичную структуру , линейную цепь оснований обычно называют просто «последовательностью», как и в ДНК (которая обычно образует линейную двойную спираль с небольшой вторичной структурой). Другие биологические полимеры, такие как полисахариды, также могут считаться имеющими первичную структуру, хотя их использование не является стандартным.
Первичная структура биологического полимера во многом определяет трехмерную форму ( третичная структура ). Последовательность белка можно использовать для прогнозирования локальных особенностей , таких как сегменты вторичной структуры или трансмембранные области. Однако сложность сворачивания белка в настоящее время не позволяет предсказать третичную структуру белка только на основе его последовательности. Знание структуры сходной гомологичной последовательности (например, члена одного и того же семейства белков ) позволяет с высокой точностью предсказать третичную структуру путем моделирования гомологии . Если доступна полноразмерная последовательность белка, можно оценить его общие биофизические свойства , такие как изоэлектрическая точка .
Семейства последовательностей часто определяются путем кластеризации последовательностей , а проекты структурной геномики направлены на создание набора репрезентативных структур, чтобы охватить пространство последовательностей возможных неизбыточных последовательностей.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )