
Альтернативный сплайсинг , или альтернативный сплайсинг РНК , или дифференциальный сплайсинг , представляет собой альтернативный процесс сплайсинга во время экспрессии генов , который позволяет одному гену кодировать несколько белков . В этом процессе определенные экзоны гена могут быть включены или исключены из окончательной процессированной информационной РНК (мРНК), полученной из этого гена. [1] Это означает, что экзоны соединяются в разных комбинациях, что приводит к образованию разных (альтернативных) цепей мРНК. Следовательно, белки , транслированные с альтернативно сплайсированных мРНК, обычно содержат различия в своей аминокислотной последовательности и, часто, в своих биологических функциях (см. рисунок).
Биологически значимый альтернативный сплайсинг происходит как нормальное явление у эукариот , где он увеличивает количество белков, которые могут кодироваться геномом. [1] Широко распространено мнение, что у людей около 95% мультиэкзонных генов подвергаются альтернативному сплайсингу с образованием функциональных альтернативных продуктов из одного и того же гена [2], но многие ученые считают, что большинство наблюдаемых вариантов сплайсинга происходят из-за ошибок сплайсинга. а фактическое количество биологически значимых альтернативно сплайсированных генов намного ниже. [3] [4]
Альтернативный сплайсинг позволяет регулируемую генерацию множества мРНК и белковых продуктов из одного гена. [5]
Наблюдается множество способов альтернативного сплайсинга, из которых наиболее распространенным является пропуск экзона . В этом случае конкретный экзон может быть включен в мРНК при одних условиях или в определенных тканях и исключен из мРНК в других. [1]
Производство альтернативно сплайсированных мРНК регулируется системой транс-действующих белков, которые связываются с цис-действующими сайтами на самом первичном транскрипте . Такие белки включают активаторы сплайсинга, которые способствуют использованию определенного сайта сплайсинга, и репрессоры сплайсинга, которые уменьшают использование определенного сайта. Механизмы альтернативного сплайсинга весьма разнообразны, и постоянно находятся новые примеры, особенно за счет использования методов с высокой пропускной способностью. Исследователи надеются полностью выяснить регуляторные системы, участвующие в сплайсинге, чтобы можно было предсказать альтернативные продукты сплайсинга данного гена в определенных условиях («варианты сплайсинга») с помощью «кода сплайсинга». [6] [7]
Аномальные изменения в сплайсинге также участвуют в заболеваниях ; большая часть генетических нарушений человека возникает в результате сплайсинга вариантов. [6] Считается, что аномальные варианты сплайсинга также способствуют развитию рака, [8] [9] [10] [11] и гены факторов сплайсинга часто мутируют при различных типах рака. [11]
Альтернативный сплайсинг впервые был обнаружен в 1977 году. [ 12] [13] Аденовирус производит пять первичных транскриптов в начале своего инфекционного цикла, до репликации вирусной ДНК, и еще один позже, после начала репликации ДНК. Ранние первичные транскрипты продолжают производиться после начала репликации ДНК. Дополнительный первичный транскрипт, образующийся на поздних стадиях инфекции, имеет большой размер и составляет 5/6 генома аденовируса размером 32 т.п.н. Это намного больше, чем любая из отдельных мРНК аденовируса, присутствующих в инфицированных клетках. Исследователи обнаружили, что первичный транскрипт РНК, продуцируемый аденовирусом типа 2 на поздней стадии, подвергался сплайсингу разными способами, в результате чего образовывались мРНК, кодирующие различные вирусные белки. Кроме того, первичный транскрипт содержал несколько сайтов полиаденилирования , что давало разные 3'-концы процессированным мРНК. [14] [15] [16]
В 1981 году был охарактеризован первый пример альтернативного сплайсинга транскрипта нормального эндогенного гена . [14] Было обнаружено , что ген, кодирующий гормон щитовидной железы кальцитонин, альтернативно сплайсируется в клетках млекопитающих. Первичный транскрипт этого гена содержит 6 экзонов; мРНК кальцитонина содержит экзоны 1–4 и заканчивается после сайта полиаденилирования в экзоне 4. Другая мРНК образуется из этой пре-мРНК путем пропуска экзона 4 и включает экзоны 1–3, 5 и 6. Она кодирует белок, известный как CGRP ( пептид, родственный гену кальцитонина ). [17] [18] Примеры альтернативного сплайсинга транскриптов генов иммуноглобина у млекопитающих наблюдались также в начале 1980-х годов. [14] [19]
С тех пор у эукариот было обнаружено множество других примеров биологически значимого альтернативного сплайсинга. [1] «Рекордсменом» по альтернативному сплайсингу является ген D. melanogaster под названием Dscam , который потенциально может иметь 38 016 вариантов сплайсинга. [20]
В 2021 году было обнаружено, что геном аденовируса 2 типа, аденовируса, в котором впервые был идентифицирован альтернативный сплайсинг, способен продуцировать гораздо большее разнообразие мРНК, чем считалось ранее. [21] Используя технологию секвенирования нового поколения, исследователи смогли обновить транскриптом аденовируса человека типа 2 и представить ошеломляющую уникальную мРНК 904, вырабатываемую вирусом посредством сложной схемы альтернативного сплайсинга. Было показано, что очень немногие из этих вариантов сращивания функциональны, и авторы поднимают этот вопрос в своей статье.


Общепризнаны пять основных способов альтернативного сплайсинга. [1] [2] [6] [22]
Помимо этих основных способов альтернативного сплайсинга, существуют два других основных механизма, с помощью которых разные мРНК могут генерироваться из одного и того же гена; несколько промоторов и несколько сайтов полиаденилирования . Использование нескольких промоторов правильно описывается как механизм регуляции транскрипции , а не как альтернативный сплайсинг; начиная транскрипцию в разных точках, можно генерировать транскрипты с разными 5'-экзонами. На другом конце несколько сайтов полиаденилирования обеспечивают разные 3'-конечные точки транскрипта. Оба этих механизма обнаруживаются в сочетании с альтернативным сплайсингом и обеспечивают дополнительное разнообразие мРНК, полученных из гена. [1] [6]
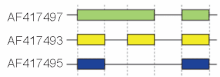
Эти режимы описывают основные механизмы сплайсинга, но могут оказаться недостаточными для описания сложных событий сплайсинга. Например, на рисунке справа показаны 3 сплайс-формы гена мышиной гиалуронидазы 3. Сравнение экзонной структуры, показанной в первой строке (зеленый), со структурой во второй строке (желтый), показывает сохранение интрона, тогда как сравнение второй и третьей сплайс-формы (желтый и синий) демонстрирует пропуск экзона. Недавно была предложена модельная номенклатура для однозначного обозначения всех возможных схем сплайсинга. [22]

Когда пре-мРНК транскрибируется с ДНК , она включает несколько интронов и экзонов . (У нематод среднее число составляет 4–5 экзонов и интронов; у плодовой мухи Drosophila в одной транскрибируемой пре-мРНК может быть более 100 интронов и экзонов.) Экзоны, которые должны сохраниться в мРНК , определяются в процессе сплайсинга. . Регуляция и выбор сайтов сплайсинга осуществляются с помощью транс-действующих белков-активаторов сплайсинга и белков-репрессоров сплайсинга, а также цис-действующих элементов внутри самой пре-мРНК, таких как экзонные усилители сплайсинга и экзонные сайленсеры сплайсинга.
Типичный эукариотический ядерный интрон имеет консенсусные последовательности, определяющие важные области. Каждый интрон имеет последовательность GU на своем 5'-конце. Около 3'-конца имеется участок разветвления. Нуклеотид в точке ветвления всегда представляет собой букву А; консенсус вокруг этой последовательности несколько различается. У людей консенсусная последовательность сайта ветвления представляет собой yUnAy. [24] За местом ветвления следует серия пиримидинов – полипиримидиновый тракт – затем AG на 3'-конце. [6]
Сплайсинг мРНК осуществляется комплексом РНК и белка, известным как сплайсосома , содержащим мяРНП , обозначенные U1, U2 , U4, U5 и U6 (U3 не участвует в сплайсинге мРНК). [25] U1 связывается с 5'-GU, а U2 с помощью белковых факторов U2AF связывается с точкой ветвления А внутри сайта ветвления. Комплекс на этой стадии известен как комплекс сплайсосомы А. Формирование комплекса А обычно является ключевым шагом в определении концов интрона, который необходимо отсоединить, и определения концов экзона, который необходимо сохранить. [6] (Номенклатура U обусловлена высоким содержанием уридина).
Комплекс U4,U5,U6 связывается, и U6 заменяет позицию U1. U1 и U4 уходят. Оставшийся комплекс затем осуществляет две реакции переэтерификации . При первой переэтерификации 5'-конец интрона отщепляется от верхнего экзона и соединяется с сайтом ветвления А посредством 2',5'- фосфодиэфирной связи. При второй переэтерификации 3'-конец интрона отщепляется от нижестоящего экзона, и два экзона соединяются фосфодиэфирной связью. Затем интрон высвобождается в форме лариата и разрушается. [1]

Сплайсинг регулируется транс-действующими белками (репрессорами и активаторами) и соответствующими цис-действующими регуляторными сайтами (сайленсерами и энхансерами) на пре-мРНК. Однако, учитывая сложность альтернативного сплайсинга, следует отметить, что эффекты фактора сплайсинга часто зависят от положения. То есть фактор сплайсинга, который служит активатором сплайсинга при связывании с интронным энхансерным элементом, может служить репрессором при связывании со своим сплайсинговым элементом в контексте экзона, и наоборот. [26] Вторичная структура транскрипта пре-мРНК также играет роль в регуляции сплайсинга, например, путем объединения элементов сплайсинга или маскировки последовательности, которая в противном случае служила бы связывающим элементом для фактора сплайсинга. [27] [28] Вместе эти элементы образуют «код сплайсинга», который определяет, как будет происходить сплайсинг в различных клеточных условиях. [29] [30]
Существует два основных типа элементов последовательности цис-действующей РНК, присутствующих в пре-мРНК, и они имеют соответствующие транс-действующие РНК-связывающие белки . Сайленсеры сплайсинга - это сайты, с которыми связываются белки-репрессоры сплайсинга, что снижает вероятность того, что соседний сайт будет использоваться в качестве соединения сплайсинга. Они могут быть расположены в самом интроне (интронные сайленсеры сплайсинга, ISS) или в соседнем экзоне ( экзонные сайленсеры сплайсинга , ESS). Они различаются по последовательности, а также по типам белков, которые с ними связываются. Большинство репрессоров сплайсинга представляют собой гетерогенные ядерные рибонуклеопротеины (hnRNP), такие как hnRNPA1 и белок, связывающий полипиримидиновый тракт (PTB). [6] [29] Усилители сплайсинга — это сайты, с которыми связываются белки-активаторы сплайсинга, что увеличивает вероятность того, что близлежащий сайт будет использоваться в качестве соединения сплайсинга. Они также могут возникать в интроне (интронные энхансеры сплайсинга, ISE) или экзоне ( экзонные энхансеры сплайсинга , ESE). Большинство белков-активаторов, которые связываются с ISE и ESE, являются членами семейства белков SR . Такие белки содержат мотивы узнавания РНК и домены, богатые аргинином и серином (RS). [6] [29]

В общем, детерминанты сплайсинга работают взаимозависимо, в зависимости от контекста, так что правила, управляющие регулированием сплайсинга, образуют код сплайсинга. [30] Присутствие определенного элемента последовательности цис-действующей РНК может увеличить вероятность того, что близлежащий сайт будет сплайсирован в некоторых случаях, но уменьшить вероятность в других случаях, в зависимости от контекста. Контекст, в котором действуют регуляторные элементы, включает контекст цис-действия, который устанавливается наличием других особенностей последовательности РНК, и контекст транс-действия, который устанавливается клеточными условиями. Например, некоторые элементы последовательности цис-действующей РНК влияют на сплайсинг только в том случае, если несколько элементов присутствуют в одной и той же области, чтобы установить контекст. В качестве другого примера, цис-действующий элемент может оказывать противоположные эффекты на сплайсинг, в зависимости от того, какие белки экспрессируются в клетке (например, нейрональные или ненейрональные PTB). Адаптивная значимость сплайсинга сайленсеров и энхансеров подтверждена исследованиями, показывающими, что в генах человека существует сильный отбор против мутаций, которые производят новые сайленсеры или разрушают существующие энхансеры. [31] [32]
Метилирование ДНК CpG показало роль в регулировании альтернативного сплайсинга у социальных насекомых. [33] [34] У медоносных пчел ( Apis mellifera ) метилирование ДНК CpG, по-видимому, регулирует пропуск экзонов на основании первых нескольких геномных исследований [35] [36] после того, как стал доступен геном медоносной пчелы. [37] Метилирование CpG ДНК более широко регулирует альтернативный сплайсинг, влияет не только на пропуск экзонов, но также на удержание интронов и другие события сплайсинга. [38]

Пре-мРНК гена dsx D. melanogaster содержат 6 экзонов. У самцов экзоны 1,2,3,5 и 6 соединяются, образуя мРНК, которая кодирует белок, регулирующий транскрипцию, необходимый для развития самцов. У женщин экзоны 1,2,3 и 4 соединяются, и сигнал полиаденилирования в экзоне 4 вызывает расщепление мРНК в этой точке. Полученная мРНК представляет собой белок, регулирующий транскрипцию, необходимый для развития самок. [39]
Это пример пропуска экзона. Интрон выше экзона 4 имеет полипиримидиновый тракт , который плохо соответствует консенсусной последовательности , поэтому белки U2AF плохо связываются с ним без помощи активаторов сплайсинга. Поэтому этот 3'-акцепторный сайт сплайсинга не используется у самцов. Однако самки производят активатор сплайсинга Трансформатор (Тра) (см. ниже). Белок SR Tra2 вырабатывается у представителей обоих полов и связывается с ESE в экзоне 4; если Tra присутствует, он связывается с Tra2 и вместе с другим белком SR образует комплекс, который помогает белкам U2AF связываться со слабым полипиримидиновым трактом. U2 рекрутируется в соответствующую точку ветвления, и это приводит к включению экзона 4 в мРНК. [39] [40]
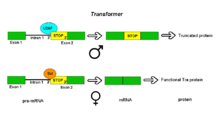
Пре-мРНК гена трансформера (Tra) Drosophila melanogaster подвергаются альтернативному сплайсингу посредством режима альтернативного акцепторного сайта. Ген Tra кодирует белок, который экспрессируется только у женщин. Первичный транскрипт этого гена содержит интрон с двумя возможными акцепторными сайтами. У самцов используется верхний акцепторный сайт. Это приводит к включению в обрабатываемый транскрипт более длинной версии экзона 2, включая ранний стоп-кодон . Полученная мРНК кодирует укороченный белковый продукт, который неактивен. Самки производят главный белок определения пола Sex Lethal (Sxl). Белок Sxl представляет собой репрессор сплайсинга, который связывается с ISS в РНК транскрипта Tra вблизи вышестоящего акцепторного сайта, предотвращая связывание белка U2AF с полипиримидиновым трактом. Это предотвращает использование этого соединения, смещая связывание сплайсосомы к нижележащему акцепторному сайту. Сплайсинг в этой точке обходит стоп-кодон, который вырезается как часть интрона. Полученная мРНК кодирует активный белок Tra, который сам по себе является регулятором альтернативного сплайсинга других генов, связанных с полом (см. dsx выше). [1]

Множественные изоформы белка рецептора Fas производятся путем альтернативного сплайсинга. Две обычно встречающиеся у человека изоформы производятся по механизму пропуска экзона. мРНК, включающая экзон 6, кодирует мембраносвязанную форму рецептора Fas, которая способствует апоптозу или запрограммированной гибели клеток. Повышенная экспрессия рецептора Fas в клетках кожи, хронически подвергающихся воздействию солнца, и отсутствие экспрессии в клетках рака кожи позволяют предположить, что этот механизм может быть важен для устранения предраковых клеток у людей. [41] Если экзон 6 пропущен, полученная мРНК кодирует растворимый белок Fas, который не способствует апоптозу. Включение или пропуск экзона зависит от двух антагонистических белков: TIA-1 и белка, связывающего полипиримидиновый тракт (PTB).
Этот механизм является примером определения экзонов при сплайсинге. Сплайсосома собирается на интроне, и субъединицы snRNP сворачивают РНК так, что 5'- и 3'-концы интрона соединяются. Однако недавно изученные примеры, подобные этому, показывают, что между концами экзона также существуют взаимодействия. В этом конкретном случае эти взаимодействия определения экзонов необходимы, чтобы обеспечить связывание основных факторов сплайсинга до сборки сплайсосом на двух фланкирующих интронах. [42]

ВИЧ , ретровирус , вызывающий СПИД у людей, продуцирует единственный первичный транскрипт РНК, который альтернативно сплайсируется несколькими способами с образованием более 40 различных мРНК. [43] Равновесие среди дифференциально сплайсированных транскриптов обеспечивает наличие множества мРНК, кодирующих различные продукты, необходимые для размножения вируса. [44] Один из дифференциально сплайсированных транскриптов содержит ген tat , в котором экзон 2 представляет собой кассетный экзон, который может быть пропущен или включен. Включение tat-экзона 2 в РНК регулируется конкуренцией между репрессором сплайсинга hnRNP A1 и SR-белком SC35. Внутри экзона 2 экзонная последовательность сайленсера сплайсинга (ESS) и экзонная последовательность энхансера сплайсинга (ESE) перекрываются. Если белок-репрессор А1 связывается с ESS, он инициирует совместное связывание нескольких молекул А1, распространяясь на 5'-донорный сайт выше экзона 2 и предотвращая связывание основного фактора сплайсинга U2AF35 с полипиримидиновым трактом. Если SC35 связывается с ESE, он предотвращает связывание A1 и поддерживает 5'-донорный сайт в доступном состоянии для сборки сплайсосомы. Конкуренция между активатором и репрессором обеспечивает продукцию обоих типов мРНК (с экзоном 2 и без него). [43]
Подлинный альтернативный сплайсинг происходит как в генах, кодирующих белок, так и в некодирующих генах, с образованием множества продуктов (белков или некодирующих РНК). Внешняя информация необходима для того, чтобы решить, какой продукт будет произведен, учитывая последовательность ДНК и исходный транскрипт. Поскольку методы регуляции наследуются, это открывает новые способы влияния мутаций на экспрессию генов. [10]
Альтернативный сплайсинг может обеспечить эволюционную гибкость. Одна точечная мутация может привести к тому, что данный экзон будет иногда исключен или включен в транскрипт во время сплайсинга, что позволит производить новую изоформу белка без потери исходного белка. [1] Исследования выявили внутренне неупорядоченные области (см. Внутренне неструктурированные белки ), обогащенные неконститутивными экзонами [45], что позволяет предположить, что изоформы белков могут демонстрировать функциональное разнообразие из-за изменения функциональных модулей внутри этих областей. Такое функциональное разнообразие, достигаемое изоформами, отражается в моделях их экспрессии и может быть предсказано с помощью подходов машинного обучения. [46] [47] Сравнительные исследования показывают, что альтернативный сплайсинг предшествовал многоклеточному развитию в эволюции, и предполагают, что этот механизм мог быть использован для помощи в развитии многоклеточных организмов. [48]
Исследования, основанные на проекте «Геном человека» и других методах секвенирования генома, показали, что у человека лишь примерно на 30% больше генов, чем у круглого червя Caenorhabditis elegans , и лишь примерно в два раза больше, чем у мухи Drosophila melanogaster . Это открытие привело к предположению, что воспринимаемая большая сложность людей или позвоночных в целом может быть связана с более высокой скоростью альтернативного сплайсинга у людей, чем у беспозвоночных. [49] [50] Однако исследование образцов из 100 000 меток экспрессируемых последовательностей (EST) каждого из человека, мыши, крысы, коровы, мухи ( D. melanogaster ), червя ( C. elegans ) и растения Arabidopsis thaliana обнаружило не было больших различий в частоте альтернативно сплайсированных генов среди людей и других протестированных животных. [51] Другое исследование, однако, предположило, что эти результаты являются артефактом разного количества EST, доступных для разных организмов. Когда они сравнили частоты альтернативного сплайсинга в случайных подмножествах генов каждого организма, авторы пришли к выводу, что у позвоночных действительно более высокий уровень альтернативного сплайсинга, чем у беспозвоночных. [52]
Изменения в механизме процессинга РНК могут привести к неправильному сплайсингу нескольких транскриптов, в то время как однонуклеотидные изменения в сайтах сплайсинга или цис-действующих регуляторных сайтах сплайсинга могут привести к различиям в сплайсинге одного гена и, следовательно, в мРНК, продуцируемой из транскрипты мутантного гена. Исследование 2005 года, включающее вероятностный анализ, показало, что более 60% мутаций , вызывающих заболевания человека, влияют на сплайсинг, а не непосредственно на кодирующие последовательности. [53] Более недавнее исследование показывает, что треть всех наследственных заболеваний, вероятно, имеют компонент сплайсинга. [26] Независимо от точного процента, существует ряд заболеваний, связанных со сплайсингом. [54] Как описано ниже, ярким примером заболеваний, связанных со сплайсингом, является рак.
Аномально сплайсированные мРНК также обнаруживаются в большом количестве раковых клеток. [8] [9] [11] Комбинированный анализ РНК-Seq и протеомики выявил поразительную дифференциальную экспрессию изоформ сплайсинга ключевых белков в важных путях рака. [55] Не всегда ясно, способствуют ли такие аберрантные модели сплайсинга раковому росту или являются просто следствием клеточных аномалий, связанных с раком. Было показано, что для некоторых типов рака, таких как колоректальный рак и рак простаты, количество ошибок сплайсинга на рак сильно различается в зависимости от конкретного рака; это явление называется нестабильностью транскриптома . [56] [57] Кроме того, было показано, что нестабильность транскриптома коррелирует со сниженным уровнем экспрессии генов факторов сплайсинга. Было продемонстрировано, что мутация DNMT3A способствует гематологическим злокачественным новообразованиям , и что клеточные линии с мутацией DNMT3A демонстрируют нестабильность транскриптома по сравнению с их изогенными аналогами дикого типа. [58]
Фактически, в раковых клетках действительно наблюдается снижение альтернативного сплайсинга по сравнению с нормальными, а типы сплайсинга различаются; например, раковые клетки демонстрируют более высокий уровень задержки интронов, чем нормальные клетки, но более низкий уровень пропуска экзонов. [59] Некоторые различия в сплайсинге раковых клеток могут быть связаны с высокой частотой соматических мутаций в генах факторов сплайсинга, [11] а некоторые могут быть результатом изменений в фосфорилировании транс-действующих факторов сплайсинга. [10] Другие могут быть вызваны изменениями в относительном количестве вырабатываемых факторов сплайсинга; например, было показано, что клетки рака молочной железы имеют повышенные уровни фактора сплайсинга SF2/ASF . [60] Одно исследование показало, что относительно небольшой процент (383 из более чем 26 000) альтернативных вариантов сплайсинга встречался значительно чаще в опухолевых клетках, чем в нормальных клетках, что позволяет предположить, что существует ограниченный набор генов, которые при неправильном сплайсинге способствуют развитию опухоли. [61] Однако считается, что вредные последствия неправильного сплайсинга транскриптов обычно защищаются и устраняются с помощью клеточного механизма посттранскрипционного контроля качества, называемого нонсенс-опосредованным распадом мРНК [NMD]. [62]
Одним из примеров специфического варианта сплайсинга, связанного с раком, является один из генов DNMT человека . Три гена DNMT кодируют ферменты, которые добавляют к ДНК метильные группы — модификация, которая часто оказывает регуляторное воздействие. Несколько мРНК DNMT3B с аномальным сплайсингом обнаружены в опухолях и линиях раковых клеток. В двух отдельных исследованиях экспрессия двух из этих аномально сплайсированных мРНК в клетках млекопитающих вызвала изменения в паттернах метилирования ДНК в этих клетках. Клетки с одной из аномальных мРНК также росли в два раза быстрее, чем контрольные клетки, что указывает на прямой вклад этого продукта в развитие опухоли. [10]
Другой пример — протоонкоген Рон ( MST1R ) . Важным свойством раковых клеток является их способность перемещаться и проникать в нормальные ткани. Было обнаружено, что продукция аномально сплайсированного транскрипта Рона связана с повышенными уровнями SF2/ASF в клетках рака молочной железы. Аномальная изоформа белка Ron, кодируемая этой мРНК, приводит к подвижности клеток . [60]
Сверхэкспрессия усеченного сплайсингового варианта гена FOSB – ΔFosB – в определенной популяции нейронов прилежащего ядра была идентифицирована как причинный механизм, участвующий в индукции и поддержании зависимости от наркотиков и естественных вознаграждений . [63] [64] [65] [66]
Недавние провокационные исследования указывают на ключевую функцию структуры хроматина и модификаций гистонов в альтернативной регуляции сплайсинга. Эти открытия позволяют предположить, что эпигенетическая регуляция определяет не только то, какие части генома экспрессируются, но и то, как они соединяются. [67]
Транскриптомный анализ альтернативного сплайсинга обычно выполняется с помощью высокопроизводительного секвенирования РНК. Чаще всего с помощью секвенирования короткого считывания, например, с помощью приборов Illumina. Но еще более информативным является длительное секвенирование, например, с помощью инструментов Nanopore или PacBio. Анализ всего транскриптома может, например, использоваться для измерения количества отклонений альтернативного сплайсинга, например, в когорте рака. [68]
Технологии глубокого секвенирования использовались для проведения полногеномного анализа как необработанных, так и обработанных мРНК; тем самым давая представление об альтернативном сплайсинге. Например, результаты использования глубокого секвенирования показывают, что у людей примерно 95% транскриптов мультиэкзонных генов подвергаются альтернативному сплайсингу, при этом ряд транскриптов пре-мРНК сплайсируются тканеспецифичным образом. [2] Функциональная геномика и вычислительные подходы, основанные на множественном обучении, также были разработаны для интеграции данных РНК-секвенирования для прогнозирования функций альтернативно сплайсированных изоформ. [47] Глубокое секвенирование также помогло обнаружить in vivo временные лариаты , которые высвобождаются во время сплайсинга, определить последовательности сайтов ветвления и крупномасштабное картирование точек ветвления в транскриптах пре-мРНК человека. [69]
Исторически альтернативно сплайсированные транскрипты были обнаружены путем сравнения последовательностей EST , но это требует секвенирования очень большого количества EST. Большинство библиотек EST происходят из очень ограниченного числа тканей, поэтому тканеспецифичные варианты сплайсинга в любом случае могут быть пропущены. Однако были разработаны высокопроизводительные подходы к исследованию сплайсинга, такие как анализ на основе микрочипов ДНК , анализы связывания РНК и глубокое секвенирование . Эти методы можно использовать для скрининга полиморфизмов или мутаций внутри или вокруг элементов сплайсинга, которые влияют на связывание белков. В сочетании с анализами сплайсинга, включая анализы репортерных генов in vivo , можно затем проанализировать функциональные эффекты полиморфизмов или мутаций на сплайсинг транскриптов пре-мРНК. [26] [29] [70]
В микрочиповом анализе использовались массивы фрагментов ДНК, представляющие отдельные экзоны ( например, экзонный микрочип Affymetrix ) или границы экзонов/экзонов ( например, массивы от ExonHit или Jivan ). Затем массив исследуют меченой кДНК из представляющих интерес тканей. кДНК зонда связываются с ДНК экзонов, которые включены в мРНК в ткани их происхождения, или с ДНК с границы, где соединяются два экзона. Это может выявить наличие определенных альтернативно сплайсированных мРНК. [71]
CLIP ( сшивка и иммунопреципитация ) использует УФ-излучение для связывания белков с молекулами РНК в ткани во время сплайсинга. Затем интересующий транс-действующий регуляторный белок сплайсинга осаждают с использованием специфических антител. Когда РНК, прикрепленная к этому белку, выделяется и клонируется, она обнаруживает целевые последовательности для этого белка. [7] Другим методом идентификации РНК-связывающих белков и картирования их связывания с транскриптами пре-мРНК является «Оценка геномных аптамеров на микрочипах по сдвигу (MEGAshift)».net [72] Этот метод включает в себя адаптацию «Систематической эволюции лигандов». методом экспоненциального обогащения (SELEX)» [73] вместе со считыванием на основе микроматрицы. Использование метода MEGAshift позволило лучше понять регуляцию альтернативного сплайсинга, позволив идентифицировать последовательности в транскриптах пре-мРНК, окружающих альтернативно сплайсированные экзоны, которые опосредуют связывание с различными факторами сплайсинга, такими как ASF/SF2 и PTB. [74] Этот подход также использовался для определения взаимосвязи между вторичной структурой РНК и связыванием факторов сплайсинга. [28]
Использование репортерных анализов позволяет найти белки сплайсинга, участвующие в конкретном событии альтернативного сплайсинга, путем конструирования репортерных генов, которые будут экспрессировать один из двух различных флуоресцентных белков в зависимости от происходящей реакции сплайсинга. Этот метод использовался для выделения мутантов, влияющих на сплайсинг, и, таким образом, для идентификации новых белков-регуляторов сплайсинга, инактивированных в этих мутантах. [7]
Недавние достижения в предсказании структуры белков способствовали разработке новых инструментов для аннотации генома и анализа альтернативного сплайсинга. Например, isoform.io, платформа, основанная на предсказаниях структуры белков, оценила сотни тысяч изоформ генов, кодирующих человеческие белки, собранных в результате многочисленных экспериментов по секвенированию РНК в различных тканях человека. Этот всесторонний анализ привел к идентификации многочисленных изоформ с более точно предсказанной структурой и потенциально превосходящими функциями по сравнению с каноническими изоформами в последней базе данных генов человека. Интегрируя структурные предсказания с данными экспрессии и эволюции, этот подход продемонстрировал потенциал предсказания структуры белка как инструмента для уточнения аннотации генома человека. [75]
Существует коллекция альтернативных баз данных сплайсинга. [76] [77] [78] Эти базы данных полезны для поиска генов, имеющих пре-мРНК, подвергающихся альтернативному сплайсингу и событиям альтернативного сплайсинга, или для изучения функционального воздействия альтернативного сплайсинга.
НЕСМОТРЯ НА ЗНАЧИМОСТЬ МНОГОЧИСЛЕННЫХ ПСИХОСОЦИАЛЬНЫХ ФАКТОРОВ, ПО СВОЕЙ ОСНОВЕ, НАРКОТИКИЯ ВКЛЮЧАЕТ БИОЛОГИЧЕСКИЙ ПРОЦЕСС: способность многократного воздействия злоупотребляемого наркотика вызывать изменения в уязвимом мозге, которые приводят к компульсивному поиску и приему наркотиков, и потеря контроля над употреблением наркотиков, определяющая состояние наркомании. ... Большой объем литературы продемонстрировал, что такая индукция ΔFosB в нейронах NAc D1-типа увеличивает чувствительность животного к лекарству, а также к естественным вознаграждениям и способствует самостоятельному приему лекарства, предположительно посредством процесса положительного подкрепления.
ΔFosB является важным фактором транскрипции, участвующим в молекулярных и поведенческих путях развития зависимости после неоднократного воздействия наркотиков. Образование ΔFosB во многих областях мозга и молекулярный путь, ведущий к образованию комплексов AP-1, хорошо изучены. Установление функционального назначения ΔFosB позволило продолжить определение некоторых ключевых аспектов его молекулярных каскадов, включая такие эффекторы, как GluR2 (87,88), Cdk5 (93) и NFkB (100). Более того, многие из этих выявленных молекулярных изменений теперь напрямую связаны со структурными, физиологическими и поведенческими изменениями, наблюдаемыми после хронического воздействия наркотиков (60,95,97,102). Новые горизонты исследований по изучению молекулярной роли ΔFosB были открыты эпигенетическими исследованиями, а недавние достижения проиллюстрировали роль ΔFosB, действующего на ДНК и гистоны, действительно как
молекулярный переключатель
(34). Благодаря нашему лучшему пониманию ΔFosB при зависимости, стало возможным оценить потенциал привыкания современных лекарств (119), а также использовать его в качестве биомаркера для оценки эффективности терапевтических вмешательств (121,122,124). Некоторые из этих предлагаемых мер имеют ограничения (125) или находятся на начальной стадии разработки (75). Однако есть надежда, что некоторые из этих предварительных результатов могут привести к созданию инновационных методов лечения, которые крайне необходимы при зависимости.
По этим причинам ΔFosB считается первичным и причинным фактором транскрипции в создании новых нейронных связей в центре вознаграждения, префронтальной коре и других областях лимбической системы. Это отражается в повышенном, стабильном и продолжительном уровне чувствительности к кокаину и другим наркотикам, а также в склонности к рецидивам даже после длительных периодов воздержания. Эти недавно построенные сети функционируют очень эффективно, используя новые пути, как только злоупотребляемые наркотиками продолжают приниматься.