Метионин (символ Met или M ) [ 3] ( / mɪ ˈ θ aɪ ə n iː n / ) [4] является незаменимой аминокислотой для человека.
Как предшественник других заменимых аминокислот, таких как цистеин и таурин , универсальных соединений, таких как SAM-e , и важного антиоксиданта глутатиона , метионин играет важную роль в метаболизме и здоровье многих видов, включая людей. Метионин также участвует в ангиогенезе и различных процессах, связанных с транскрипцией ДНК, эпигенетической экспрессией и регуляцией генов.
Метионин был впервые выделен в 1921 году Джоном Говардом Мюллером . [5] Он кодируется кодоном AUG. Он был назван Сатору Одаке в 1925 году, как сокращение от его структурного описания 2-амино-4-( метилтио ) бутановая кислота. [6]
Метионин (сокращенно Met или M ; кодируется кодоном AUG) — это α- аминокислота , которая используется в биосинтезе белков . Она содержит карбоксильную группу ( которая находится в депротонированной форме −COO − в биологических условиях pH ), аминогруппу (которая находится в протонированной форме −NH +
3образуется в биологических условиях pH), расположенный в α-положении по отношению к карбоксильной группе, и боковой цепи S - метилтиоэфира , что классифицирует его как неполярную алифатическую аминокислоту. [ необходима цитата ]
В ядерных генах эукариот и архей метионин кодируется стартовым кодоном , то есть он указывает на начало кодирующей области и является первой аминокислотой, образующейся в зарождающемся полипептиде во время трансляции мРНК . [7]
Цистеин и метионин являются двумя серосодержащими протеиногенными аминокислотами . За исключением немногих исключений, когда метионин может действовать как окислительно-восстановительный сенсор (например, сульфоксид метионина [8] ), остатки метионина не играют каталитической роли. [9] Это контрастирует с остатками цистеина, где тиоловая группа играет каталитическую роль во многих белках. [ 9] Тиоэфир в метионине, однако, играет незначительную структурную роль из-за эффекта стабильности взаимодействий S/π между атомом серы боковой цепи и ароматическими аминокислотами в одной трети всех известных структур белков. [9] Это отсутствие сильной роли отражено в экспериментах, где небольшой эффект наблюдается в белках, где метионин заменен норлейцином , прямой углеводородной аминокислотой боковой цепи, в которой отсутствует тиоэфир. [10] Было высказано предположение, что норлейцин присутствовал в ранних версиях генетического кода, но метионин проник в окончательную версию генетического кода из-за того, что он используется в кофакторе S -аденозилметионине (SAM-e). [11] Эта ситуация не уникальна и могла иметь место с орнитином и аргинином . [12]
Метионин — одна из двух аминокислот, кодируемых одним кодоном (AUG) в стандартном генетическом коде ( триптофан , кодируемый UGG, является другим). В отражении эволюционного происхождения его кодона, другие кодоны AUN кодируют изолейцин , который также является гидрофобной аминокислотой. В митохондриальном геноме нескольких организмов, включая метазоа и дрожжи , кодон AUA также кодирует метионин. В стандартном генетическом коде AUA кодирует изолейцин, а соответствующая тРНК ( ileX в Escherichia coli ) использует необычное основание лизидин (бактерии) или агматидин (археи) для дискриминации AUG. [13] [14]
Кодон метионина AUG также является наиболее распространенным стартовым кодоном. «Стартовый» кодон — это сообщение для рибосомы , которое сигнализирует об инициации трансляции белка с мРНК, когда кодон AUG находится в консенсусной последовательности Козака . Как следствие, метионин часто включается в N -концевую позицию белков у эукариот и архей во время трансляции, хотя его можно удалить путем посттрансляционной модификации . У бактерий производное N -формилметионина используется в качестве начальной аминокислоты. [ необходима цитата ]
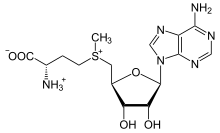
Производное метионина S -аденозилметионин (SAM-e) является кофактором , который служит в основном донором метильной группы . SAM-e состоит из молекулы аденозила (через 5′ углерод), присоединенной к сере метионина, что делает его катионом сульфония (т. е. три заместителя и положительный заряд). Сера действует как мягкая кислота Льюиса (т. е. донор/электрофил), которая позволяет переносить S -метильную группу в кислородную, азотную или ароматическую систему, часто с помощью других кофакторов, таких как кобаламин (витамин B 12 у людей). Некоторые ферменты используют SAM-e для инициирования радикальной реакции; они называются радикальными ферментами SAM-e . В результате переноса метильной группы получается S -аденозилгомоцистеин. У бактерий он либо восстанавливается путем метилирования, либо восстанавливается путем удаления аденина и гомоцистеина, в результате чего соединение дигидроксипентандион спонтанно превращается в аутоиндуктор-2 , который выводится как побочный продукт или сигнал кворума. [ необходима цитата ]
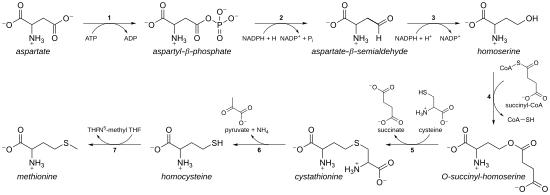
Как незаменимая аминокислота, метионин не синтезируется de novo у людей и других животных, которые должны потреблять метионин или содержащие метионин белки. У растений и микроорганизмов биосинтез метионина относится к семейству аспартата , наряду с треонином и лизином (через диаминопимелат , но не через α-аминоадипат ). Основная часть образуется из аспарагиновой кислоты , в то время как сера может поступать из цистеина , метантиола или сероводорода . [9]
Путь с использованием цистеина называется « путем транссульфурирования », тогда как путь с использованием сероводорода (или метантиола) называется «путем прямого сульфурирования».
Цистеин производится аналогичным образом, а именно он может быть получен из активированного серина и либо из гомоцистеина («обратный путь транссульфурирования»), либо из сероводорода («прямой путь сульфурирования»); активированный серин обычно представляет собой O -ацетилсерин (через CysK или CysM в E. coli ), но в Aeropyrum pernix и некоторых других археях используется O -фосфосерин. [15] CysK и CysM являются гомологами, но принадлежат к кладе PLP-складки типа III. [ требуется ссылка ]
Ферменты, участвующие в пути транссульфурирования E. coli биосинтеза метионина: [ необходима ссылка ]

Хотя млекопитающие не могут синтезировать метионин, они все равно могут использовать его в различных биохимических путях:
Метионин преобразуется в S -аденозилметионин (SAM-e) с помощью (1) метионин-аденозилтрансферазы . [ необходима цитата ]
SAM-e служит донором метильной группы во многих (2) реакциях метилтрансферазы и преобразуется в S- аденозилгомоцистеин (SAH). [ необходима цитата ]
(3) Аденозилгомоцистеиназа цистеин.
Метионин может быть регенерирован из гомоцистеина посредством (4) метионинсинтазы в реакции, требующей витамина B12 в качестве кофактора . [ необходима цитата ]
Гомоцистеин также может быть реметилирован с использованием глицинбетаина ( N , N , N -триметилглицин, TMG) в метионин через фермент бетаин-гомоцистеинметилтрансферазу (EC2.1.1.5, BHMT). BHMT составляет до 1,5% всех растворимых белков печени, и последние данные свидетельствуют о том, что он может оказывать большее влияние на гомеостаз метионина и гомоцистеина, чем метионинсинтаза. [ необходима цитата ]
Гомоцистеин может преобразовываться в цистеин.
Эта аминокислота также используется растениями для синтеза этилена . Этот процесс известен как цикл Ян или цикл метионина.
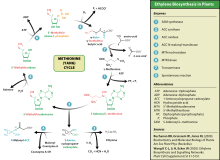
Распад метионина нарушается при следующих метаболических заболеваниях : [ необходима ссылка ]
Промышленный синтез объединяет акролеин , метантиол и цианид, что дает гидантоин . [16] Рацемический метионин также может быть синтезирован из диэтилфталимидомалонат натрия путем алкилирования хлорэтилметилсульфидом (ClCH 2 CH 2 SCH 3 ) с последующим гидролизом и декарбоксилированием. Также см. Метанол. [17]
Существуют неубедительные клинические данные о добавках метионина. [18] Диетическое ограничение метионина может привести к заболеваниям костей. [18]
Добавки метионина могут принести пользу тем, кто страдает от отравления медью . [19]
В ряде исследований показано, что избыточное потребление метионина, донора метильной группы при метилировании ДНК , связано с ростом рака. [20] [21]
Совет по пищевым продуктам и питанию Института медицины США установил рекомендуемые нормы потребления (RDA) незаменимых аминокислот в 2002 году. Для метионина в сочетании с цистеином для взрослых в возрасте 19 лет и старше — 19 мг/кг массы тела в день. [22]
Это составляет около 1,33 грамма в день для человека весом 70 килограммов. [ необходима цитата ]
Высокий уровень метионина можно найти в яйцах, мясе и рыбе; семенах кунжута, бразильских орехах и некоторых других семенах растений; и зерновых культурах. Большинство фруктов и овощей содержат очень мало метионина. Большинство бобовых , хотя и богаты белком, содержат мало метионина. Белки без достаточного количества метионина не считаются полноценными белками . [23] По этой причине рацемический метионин иногда добавляют в качестве ингредиента в корма для домашних животных . [24]
Потеря метионина связана с поседением волос в старческом возрасте. Его недостаток приводит к накоплению перекиси водорода в волосяных фолликулах , снижению эффективности тирозиназы и постепенной потере цвета волос. [25] Метионин повышает внутриклеточную концентрацию глутатиона , тем самым способствуя антиоксидантно-опосредованной защите клеток и окислительно-восстановительной регуляции. Он также защищает клетки от потери черных клеток, вызванной дофамином, путем связывания окислительных метаболитов. [26]
Метионин является промежуточным продуктом в биосинтезе цистеина , карнитина , таурина , лецитина , фосфатидилхолина и других фосфолипидов . Неправильное преобразование метионина может привести к атеросклерозу [27] из-за накопления гомоцистеина .
DL -метионин иногда дают собакам в качестве добавки; он помогает снизить вероятность образования камней в почках у собак. Известно также, что метионин увеличивает выделение хинидина с мочой, подкисляя мочу. Аминогликозидные антибиотики, используемые для лечения инфекций мочевыводящих путей, лучше всего работают в щелочных условиях, а подкисление мочи из-за использования метионина может снизить его эффективность. Если собака находится на диете, которая подкисляет мочу, метионин не следует использовать. [28]
Метионин разрешен в качестве добавки к органическому корму для птицы в соответствии с сертифицированной органической программой США. [29]
Метионин можно использовать в качестве нетоксичного пестицида против гигантских гусениц- парусников, которые являются серьезными вредителями апельсиновых культур. [30]