Вирус простого герпеса 1 и 2 ( ВПГ-1 и ВПГ-2 ), также известный под своими таксономическими названиями Альфагерпесвирус человека 1 и Альфагерпесвирус человека 2 , являются двумя членами семейства Herpesviridae человека , набора вирусов, которые в большинстве случаев вызывают вирусные инфекции. людей . [1] [2] И ВПГ-1, и ВПГ-2 очень распространены и заразны . Они могут распространяться, когда инфицированный человек начинает выделять вирус .
По состоянию на 2016 год около 67% населения мира в возрасте до 50 лет были больны ВПГ-1. [3] По оценкам, в США около 47,8% и 11,9% больных ВПГ-1 и ВПГ-2 соответственно, хотя реальная распространенность может быть намного выше. [4] Поскольку инфекция может передаваться при любом интимном контакте, она является одной из наиболее распространенных инфекций, передающихся половым путем . [5]
У многих из инфицированных симптомы никогда не проявляются. [6] Симптомы, когда они возникают, могут включать водянистые волдыри на коже или слизистых оболочках рта, губ, носа, половых органов [1] или глаз ( кератит простого герпеса ). [7] Поражения заживают, образуя струпья, характерные для герпетической болезни. Иногда во время вспышек вирусы вызывают легкие или атипичные симптомы. Однако они также могут вызывать более тяжелые формы простого герпеса . Как нейротропные и нейроинвазивные вирусы , ВПГ-1 и -2 персистируют в организме, скрываясь от иммунной системы в телах клеток нейронов , особенно в сенсорных ганглиях. После первоначального или первичного заражения у некоторых инфицированных людей наблюдаются спорадические эпизоды реактивации вируса или вспышки. Во время вспышки вирус в нервной клетке становится активным и транспортируется через аксон нейрона на кожу, где происходит репликация и выделение вируса, что может вызвать новые язвы. [8]
ВПГ-1 и ВПГ-2 передаются при контакте с инфицированным человеком, у которого наблюдается реактивация вируса. ВПГ-1 и ВПГ-2 периодически выделяются, чаще всего бессимптомно. [ нужна цитата ]
В исследовании людей с первым эпизодом генитальной инфекции ВПГ-1, проведенном в 2022 году, выделение ВПГ-1 из половых органов было обнаружено в 12% дней в течение 2 месяцев и значительно снизилось до 7% дней в течение 11 месяцев. В большинстве случаев выделения из половых органов протекали бессимптомно; Поражения гениталий и полости рта, а также выделения из полости рта встречались редко. [9]
Большинство случаев передачи ВПГ-2 половым путем происходит в периоды бессимптомного выделения вируса . [10] Бессимптомная реактивация означает, что вирус вызывает атипичные, едва заметные или труднозаметные симптомы, которые не идентифицируются как активная герпетическая инфекция, поэтому заражение вирусом возможно даже при отсутствии активных волдырей или язв ВПГ. В одном исследовании ежедневные образцы мазков из половых органов выявляли ВПГ-2 в среднем в 12–28% дней среди тех, у кого была вспышка, и в 10% дней среди людей с бессимптомной инфекцией (отсутствие предшествующих вспышек), причем многие из этих эпизодов происходит без видимой вспышки («субклиническое выделение»). [11]
В другом исследовании 73 пациента были рандомизированы для приема валацикловира в дозе 1 г в день или плацебо в течение 60 дней каждый в рамках двухфакторной перекрестной схемы . Ежедневный мазок из области гениталий самостоятельно собирали для обнаружения ВПГ-2 с помощью полимеразной цепной реакции, чтобы сравнить влияние валацикловира и плацебо на бессимптомное выделение вируса у иммунокомпетентных, серопозитивных по ВПГ-2 субъектов без истории симптоматической инфекции генитального герпеса. Исследование показало, что валацикловир значительно снижает выделение вируса в субклинические дни по сравнению с плацебо, демонстрируя снижение на 71%; У 84% испытуемых не было выделений при приеме валацикловира по сравнению с 54% испытуемых, принимавших плацебо. Около 88% пациентов, принимавших валацикловир, не имели выявленных признаков или симптомов по сравнению с 77% пациентов, принимавших плацебо. [12]
Большую часть передачи вируса простого герпеса 2 типа может составлять субклиническое выделение. [11] Исследования дискордантных партнеров (один инфицирован ВПГ-2, другой нет) показывают, что уровень передачи составляет примерно 5–8,9 на 10 000 сексуальных контактов, при этом использование презервативов значительно снижает риск заражения. [13] Атипичные симптомы часто объясняются другими причинами, например дрожжевой инфекцией . [14] [15] ВПГ-1 часто передается перорально в детстве. Он также может передаваться половым путем, включая контакт со слюной, например, при поцелуях и оральном сексе . [16] Исторически ВПГ-2 в основном передавался половым путем, но уровень генитальных инфекций ВПГ-1 увеличился за последние несколько десятилетий. [14]
Оба вируса также могут передаваться вертикально во время родов. [17] [18] Однако риск передачи минимален, если у матери нет симптомов и нет волдырей во время родов. Риск значителен, когда мать впервые заражается вирусом на поздних сроках беременности, что отражает высокую вирусную нагрузку. [19] Хотя большинство вирусных ЗППП не могут передаваться через предметы, поскольку вирус быстро погибает вне организма, ВПГ может сохраняться до 4,5 часов на поверхностях и передаваться через полотенца, зубные щетки, чашки, столовые приборы и т. д. [20] [21] [22] [23]
Вирусы простого герпеса могут поражать участки кожи, контактировавшие с инфицированным человеком. Примером этого является герпетический панирей , представляющий собой герпесную инфекцию на пальцах рук; его обычно обнаруживали на руках хирургов-стоматологов до того, как они начали регулярно использовать перчатки при лечении пациентов. Рукопожатие с инфицированным человеком не передает это заболевание. [24] Генитальная инфекция ВПГ-2 увеличивает риск заражения ВИЧ . [25]
ВПГ был модельным вирусом для многих исследований в области молекулярной биологии. Например, один из первых функциональных промоторов у эукариот был обнаружен у ВПГ ( гена тимидинкиназы ), а вирионный белок VP16 является одним из наиболее изученных активаторов транскрипции . [26]
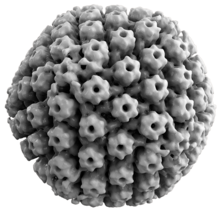

Все вирусы герпеса животных имеют некоторые общие свойства. Структура вирусов герпеса состоит из относительно большого двухцепочечного линейного ДНК- генома , заключенного в икосаэдрическую белковую клетку, называемую капсидом , которая обернута липидным бислоем , называемым оболочкой . Оболочка соединена с капсидом посредством тегумента . Эта полная частица известна как вирион . [27] ВПГ-1 и ВПГ-2 каждый содержат по меньшей мере 74 гена (или открытые рамки считывания , ORF) в своих геномах, [28] хотя предположения по поводу скученности генов допускают наличие до 84 уникальных генов, кодирующих белок, с помощью 94 предполагаемых ORF. [29] Эти гены кодируют различные белки, участвующие в формировании капсида, тегумента и оболочки вируса, а также в контроле репликации и инфекционности вируса. Эти гены и их функции обобщены в таблице ниже. [ нужна цитата ]
Геномы ВПГ-1 и ВПГ-2 сложны и содержат две уникальные области, называемые длинной уникальной областью (UL ) и короткой уникальной областью (US ) . Из 74 известных ORF UL содержит 56 вирусных генов, тогда как US содержит только 12. [28] Транскрипция генов ВПГ катализируется РНК-полимеразой II инфицированного хозяина. [28] Непосредственно ранние гены , которые кодируют белки, например ICP22 [30] , которые регулируют экспрессию ранних и поздних вирусных генов, первыми экспрессируются после заражения. Далее следует ранняя экспрессия генов, позволяющая синтезировать ферменты , участвующие в репликации ДНК , и вырабатывать определенные гликопротеины оболочки . Экспрессия поздних генов происходит последней; эта группа генов преимущественно кодирует белки, образующие частицу вириона. [28]
Пять белков из ( UL ) образуют вирусный капсид — UL6 , UL18, UL35, UL38 и основной капсидный белок UL19. [27]
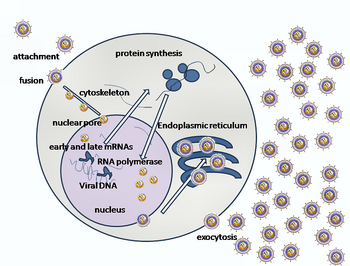
Проникновение ВПГ в клетку-хозяина предполагает связывание нескольких гликопротеинов на поверхности оболочечного вируса с их трансмембранными рецепторами на поверхности клетки. Многие из этих рецепторов затем втягиваются клеткой внутрь, что, как полагают, открывает кольцо из трех гетеродимеров gHgL, стабилизирующих компактную конформацию гликопротеина gB, так что он выскакивает наружу и прокалывает клеточную мембрану. [31] Оболочка, покрывающая вирусную частицу, затем сливается с клеточной мембраной, образуя пору, через которую содержимое вирусной оболочки попадает в клетку-хозяина. [ нужна цитата ]
Последовательные стадии проникновения HSV аналогичны стадиям проникновения других вирусов . Сначала комплементарные рецепторы на вирусе и поверхности клетки сближают вирусную и клеточную мембраны. Взаимодействие этих молекул затем образует стабильную входную пору, через которую содержимое вирусной оболочки попадает в клетку-хозяина. Вирус также может подвергаться эндоцитозу после связывания с рецепторами, и слияние может происходить на эндосоме . На электронных микрофотографиях видно, что внешние листки вирусного и клеточного липидного бислоя слились; [32] это полуслияние может происходить на обычном пути входа или обычно может быть остановленным состоянием, которое с большей вероятностью будет захвачено, чем механизм временного входа. [ нужна цитата ]
В случае вируса герпеса первоначальные взаимодействия происходят, когда два гликопротеина вирусной оболочки, называемые гликопротеином C (gC) и гликопротеином B (gB), связываются с полисахаридом клеточной поверхности , называемым гепарансульфатом . Затем основной белок, связывающий рецептор, гликопротеин D (gD), специфически связывается по крайней мере с одним из трех известных входных рецепторов. [33] Эти клеточные рецепторы включают медиатор входа герпесвируса ( HVEM ), нектин -1 и 3-O-сульфат гепарансульфата. Рецепторы нектина обычно вызывают межклеточную адгезию, обеспечивая прочную точку прикрепления вируса к клетке-хозяину. [31] Эти взаимодействия сближают поверхности мембран и позволяют другим гликопротеинам, встроенным в вирусную оболочку, взаимодействовать с другими молекулами клеточной поверхности. Связавшись с HVEM, gD меняет свою конформацию и взаимодействует с вирусными гликопротеинами H (gH) и L (gL), которые образуют комплекс. Взаимодействие этих мембранных белков может привести к состоянию гемифузии. Взаимодействие gB с комплексом gH/gL создает входную пору для вирусного капсида. [32] gB взаимодействует с гликозаминогликанами на поверхности клетки-хозяина. [ нужна цитата ]
После того как вирусный капсид попадает в цитоплазму клетки , он начинает экспрессировать вирусный белок ICP27. ICP27 представляет собой белок-регулятор, который вызывает нарушение синтеза белка-хозяина и использует его для репликации вируса. ICP27 связывается с клеточным ферментом серин-аргининпротеинкиназой 1, SRPK1 . Образование этого комплекса вызывает сдвиг SRPK1 из цитоплазмы в ядро, и вирусный геном транспортируется в ядро клетки . [34] После прикрепления к ядру в поре входа в ядро капсид выбрасывает содержимое ДНК через портал капсида. Капсидный портал образован 12 копиями портального белка UL6, расположенными в виде кольца; белки содержат последовательность аминокислот лейциновой молнии , которая позволяет им прилипать друг к другу. [35] Каждый икосаэдрический капсид содержит единственный портал, расположенный в одной вершине . [36] [37] ДНК выходит из капсида в виде одного линейного сегмента. [38]
ВПГ уклоняется от иммунной системы посредством вмешательства в презентацию антигена MHC класса I на поверхности клетки путем блокирования транспортера, связанного с процессингом антигена (TAP), индуцируемого секрецией ICP-47 ВПГ. В клетке-хозяине TAP транспортирует переваренные пептиды эпитопов вирусного антигена из цитозоля в эндоплазматический ретикулум, позволяя этим эпитопам объединяться с молекулами MHC класса I и презентироваться на поверхности клетки. Представление вирусного эпитопа с MHC класса I является необходимым условием для активации цитотоксических Т-лимфоцитов (CTL), основных эффекторов клеточно-опосредованного иммунного ответа против инфицированных вирусом клеток. ICP-47 предотвращает инициацию CTL-ответа на ВПГ, позволяя вирусу выживать в хозяине в течение длительного периода. [39] ВПГ обычно вызывает цитопатический эффект (ЦПЭ) в течение 24–72 часов после заражения в пермиссивных клеточных линиях, что наблюдается по классическому образованию бляшек. Однако также сообщалось о клинических изолятах HSV-1, которые не показали CPE в культурах клеток Vero и A549 в течение нескольких пассажей с низким уровнем экспрессии вирусного белка. Вероятно, эти изоляты HSV-1 эволюционируют в сторону более «загадочной» формы, вызывая хроническую инфекцию, тем самым раскрывая еще одну стратегию уклонения от иммунной системы хозяина, помимо латентности нейронов. [40]

После заражения клетки вырабатывается каскад белков вируса герпеса, называемый немедленным-ранним, ранним и поздним. Исследования с использованием проточной цитометрии на другом члене семейства вирусов герпеса, герпесвирусе, ассоциированном с саркомой Капоши , указывают на возможность дополнительной литической стадии , отсроченной-поздней. [41] Эти стадии литической инфекции, особенно поздние литические, отличаются от латентной стадии. В случае ВПГ-1 белковые продукты не выявляются в латентном периоде, тогда как они обнаруживаются во время литического цикла. [ нужна цитата ]
Ранние транскрибируемые белки используются в регуляции генетической репликации вируса. При попадании в клетку белок α-TIF присоединяется к вирусной частице и способствует немедленной и ранней транскрипции . Белок отключения хозяина вириона (VHS или UL41) очень важен для репликации вируса. [42] Этот фермент отключает синтез белка в организме хозяина, разрушает мРНК хозяина , помогает в репликации вируса и регулирует экспрессию генов вирусных белков. Вирусный геном немедленно перемещается в ядро, но белок VHS остается в цитоплазме. [43] [44]
Поздние белки образуют капсид и рецепторы на поверхности вируса. Упаковка вирусных частиц, включая геном , ядро и капсид, происходит в ядре клетки. Здесь конкатемеры вирусного генома разделяются путем расщепления и помещаются в образовавшиеся капсиды. ВПГ-1 подвергается процессу первичной и вторичной оболочки. Первичная оболочка образуется путем отпочкования во внутренней ядерной мембране клетки. Затем он сливается с внешней ядерной мембраной. Вирус приобретает свою окончательную оболочку путем отпочкования в цитоплазматических пузырьках . [45]
ВПГ могут персистировать в спокойной, но стойкой форме, известной как латентная инфекция, особенно в нервных ганглиях . [1] Кольцевая ДНК генома ВПГ находится в ядре клетки в виде эписомы . [46] ВПГ-1 имеет тенденцию локализоваться в тройничных ганглиях , а ВПГ-2 — в сакральных ганглиях , но это лишь исторические тенденции. Во время латентной инфекции клетки ВПГ экспрессируют РНК , связанную с латентным транскриптом (LAT) . LAT регулирует геном клетки-хозяина и вмешивается в естественные механизмы гибели клеток. Поддерживая клетки-хозяева, экспрессия LAT сохраняет резервуар вируса, что обеспечивает последующие, обычно симптоматические, периодические рецидивы или «вспышки», характерные для нелатентного периода. Независимо от того, являются ли рецидивы симптоматическими или нет, происходит выделение вируса для заражения нового хозяина. [ нужна цитата ]
Белок, обнаруженный в нейронах, может связываться с ДНК вируса герпеса и регулировать латентный период . ДНК вируса герпеса содержит ген белка ICP4, который является важным трансактиватором генов, связанных с литической инфекцией при ВПГ-1. [47] Элементы, окружающие ген ICP4, связывают белок, известный как фактор рестриктивного молчания нейронов нейронов человека (NRSF) или фактор транскрипции подавления репрессорных элементов человека (REST) . При связывании с элементами вирусной ДНК деацетилирование гистонов происходит поверх последовательности гена ICP4 , чтобы предотвратить инициацию транскрипции этого гена, тем самым предотвращая транскрипцию других вирусных генов, участвующих в литическом цикле. [47] [48] Другой белок ВПГ обращает вспять ингибирование синтеза белка ICP4. ICP0 диссоциирует NRSF от гена ICP4 и, таким образом, предотвращает замалчивание вирусной ДНК. [49]
Геном ВПГ охватывает около 150 000 пар оснований и состоит из двух уникальных сегментов, названных уникальным длинным (UL) и уникальным коротким (US), а также терминальных инвертированных повторов , обнаруженных на двух концах, называемых длинным повтором (RL) и коротким повтором (RL). РС). На дальних концах RS также обнаружены незначительные элементы «терминальной избыточности» (α). Общая схема представляет собой RL-UL-RL-α-RS-US-RS-α, где каждая пара повторов инвертирует друг друга. Затем вся последовательность инкапсулируется в терминальный прямой повтор. Каждая длинная и короткая части имеют свои собственные точки начала репликации : OriL расположен между UL28 и UL30, а OriS расположен в паре рядом с RS. [50] Поскольку сегменты L и S могут быть собраны в любом направлении, их можно свободно инвертировать друг относительно друга, образуя различные линейные изомеры. [51]
Гены ВПГ экспрессируются в трех временных классах: немедленно-ранние (IE или α), ранние (E или β) и поздние (γ) гены. Однако прогрессирование экспрессии вирусных генов происходит скорее постепенно, чем в четко выраженных стадиях. Непосредственные ранние гены транскрибируются сразу после заражения, а их генные продукты активируют транскрипцию ранних генов. Ранние генные продукты помогают реплицировать вирусную ДНК. Репликация вирусной ДНК , в свою очередь, стимулирует экспрессию поздних генов, кодирующих структурные белки. [26]
Транскрипция генов немедленной ранней стадии (IE) начинается сразу после того, как ДНК вируса попадает в ядро. Все гены вируса транскрибируются РНК-полимеразой II хозяина . Хотя белков-хозяев достаточно для транскрипции вируса, вирусные белки необходимы для транскрипции определенных генов. [26] Например, VP16 играет важную роль в транскрипции IE, и вирусная частица, по-видимому, переносит его в клетку-хозяина, поэтому его не нужно сначала производить. Аналогично, белки IE RS1 (ICP4), UL54 (ICP27) и ICP0 способствуют транскрипции ранних (E) генов. Подобно генам IE, промоторы ранних генов содержат сайты связывания клеточных факторов транскрипции. Один ранний белок, ICP8, необходим как для транскрипции поздних генов, так и для репликации ДНК. [26]
На более поздних стадиях жизненного цикла ВПГ экспрессия ближайших ранних и ранних генов прекращается. Это опосредовано специфическими вирусными белками, например ICP4, который подавляет себя путем связывания с элементами своего собственного промотора. Как следствие, снижение уровня ICP4 приводит к снижению ранней и поздней экспрессии генов, поскольку ICP4 важен для обоих. [26]
Важно отметить, что ВПГ отключает синтез РНК, ДНК и белка клетки-хозяина, чтобы направить клеточные ресурсы на производство вируса. Во-первых, вирусный белок vhs индуцирует деградацию существующих мРНК на ранних стадиях инфекции. Другие вирусные гены препятствуют клеточной транскрипции и трансляции. Например, ICP27 ингибирует сплайсинг РНК , так что мРНК вируса (которые обычно не подвергаются сплайсингу) получают преимущество над мРНК хозяина. Наконец, вирусные белки дестабилизируют определенные клеточные белки, участвующие в цикле клетки -хозяина , так что как деление клетки, так и репликация ДНК клетки-хозяина нарушаются в пользу репликации вируса. [26]
Геномы простого герпеса 1 можно разделить на шесть клад . [57] Четыре из них встречаются в Восточной Африке , один в Восточной Азии и один в Европе и Северной Америке . Это говорит о том, что вирус мог возникнуть в Восточной Африке. Самый недавний общий предок евразийских штаммов, по-видимому, появился примерно 60 000 лет назад. [58] Восточноазиатские изоляты ВПГ-1 имеют необычную структуру, которая в настоящее время лучше всего объясняется двумя волнами миграции, ответственными за заселение Японии . [58]
Геномы простого герпеса 2 можно разделить на две группы: одна распространена по всему миру, а другая в основном ограничена странами Африки к югу от Сахары . [59] Глобально распространенный генотип претерпел четыре древних рекомбинации с простым герпесом 1. Также сообщалось, что HSV-1 и HSV-2 могут иметь современные и стабильные события рекомбинации у хозяев, одновременно инфицированных обоими патогенами. Во всех случаях ВПГ-2 приобретает части генома ВПГ-1, иногда при этом меняя части своего антигенного эпитопа. [60]
По оценкам, частота мутаций составляет ~ 1,38×10 -7 замен/сайт/год. [57] В клинических условиях мутации либо в гене тимидинкиназы, либо в гене ДНК-полимеразы вызвали устойчивость к ацикловиру . Однако большинство мутаций происходит в гене тимидинкиназы, а не в гене ДНК-полимеразы. [61]
Другой анализ показал, что частота мутаций в геноме простого герпеса 1 составляет 1,82×10 -8 замен нуклеотидов на сайт в год. Этот анализ установил, что самый последний общий предок этого вируса произошел примерно 710 000 лет назад. [62]
Herpes simplex 1 и 2 разошлись около 6 миллионов лет назад . [60]
Подобно другим герпесвирусам , вирусы простого герпеса вызывают латентную пожизненную инфекцию и, следовательно, не могут быть уничтожены из организма с помощью современных методов лечения. [63]
Лечение обычно включает противовирусные препараты общего назначения , которые препятствуют репликации вируса, уменьшают физическую тяжесть поражений, связанных со вспышкой, и снижают вероятность передачи инфекции другим людям. Исследования уязвимых групп пациентов показали, что ежедневное использование противовирусных препаратов, таких как ацикловир [64] и валацикловир, может снизить частоту реактивации. [ 15 ] Широкое использование противогерпетических препаратов привело к развитию некоторой лекарственной устойчивости , что, в свою очередь , может привести к неэффективности лечения. Поэтому для решения этой проблемы широко исследуются новые источники наркотиков. В январе 2020 года была опубликована обширная обзорная статья, продемонстрировавшая эффективность натуральных продуктов в качестве перспективных препаратов против ВПГ. [65] Пиритион , ионофор цинка , продемонстрировал противовирусную активность против простого герпеса. [66]
В 1979 году сообщалось, что существует возможная связь между ВПГ-1 и болезнью Альцгеймера у людей с аллелем эпсилон4 гена APOE . [67] ВПГ-1 особенно вреден для нервной системы и увеличивает риск развития болезни Альцгеймера. Вирус взаимодействует с компонентами и рецепторами липопротеинов , что может привести к развитию болезни Альцгеймера. [68] Это исследование идентифицирует ВПГ как патоген, наиболее явно связанный с возникновением болезни Альцгеймера. [69] Согласно исследованию, проведенному в 1997 году, без присутствия аллеля гена ВПГ -1, по-видимому, не вызывает никаких неврологических повреждений и не увеличивает риск болезни Альцгеймера. [70] Однако более позднее проспективное исследование, опубликованное в 2008 году с участием 591 человека, показало статистически значимую разницу между пациентами с антителами, указывающими на недавнюю реактивацию ВПГ, и пациентами без этих антител в заболеваемости болезнью Альцгеймера, без прямой корреляции с Аллель APOE-эпсилон4. [71]
В исследовании участвовала небольшая выборка пациентов, у которых на исходном уровне не было антител, поэтому результаты следует рассматривать как весьма неопределенные . В 2011 году ученые Манчестерского университета показали, что обработка инфицированных ВПГ1 клеток противовирусными средствами снижает накопление β-амилоида и тау-белка , а также снижает репликацию ВПГ-1. [72]
Ретроспективное исследование, проведенное в Тайване в 2018 году на 33 000 пациентах, показало, что инфицирование вирусом простого герпеса увеличивает риск деменции в 2,56 раза (95% ДИ: 2,3–2,8) у пациентов, не получающих противогерпетические препараты (в 2,6 раза для инфекций ВПГ-1 и в 2,0 раза для инфекций ВПГ-2). Однако у пациентов, инфицированных ВПГ, которые получали противогерпетические препараты (например, ацикловир , фамцикловир , ганцикловир , идоксуридин , пенцикловир , тромантадин , валацикловир или валганцикловир ), не наблюдалось повышенного риска развития деменции по сравнению с пациентами, не инфицированными ВПГ. [73]
Реактивация множественности (MR) — это процесс, посредством которого вирусные геномы, содержащие инактивирующие повреждения, взаимодействуют внутри инфицированной клетки с образованием жизнеспособного вирусного генома. Первоначально MR был обнаружен у бактериального вируса-бактериофага Т4, но впоследствии был также обнаружен у патогенных вирусов, включая вирус гриппа, ВИЧ-1, аденовирус обезьяньего вируса 40, вирус коровьей оспы, реовирус, полиовирус и вирус простого герпеса. [74]
Когда частицы HSV подвергаются воздействию доз агента, повреждающего ДНК, который был бы смертельным при единичных инфекциях, но затем подвергается множественному заражению (т.е. двум или более вирусам на клетку-хозяина), наблюдается MR. Повышенная выживаемость ВПГ-1 из-за MR происходит при воздействии различных агентов, повреждающих ДНК, включая метилметансульфонат , [75] триметилпсорален (который вызывает поперечные связи между цепями ДНК), [76] [77] и УФ-свет. [78] После лечения генетически маркированного простого герпеса триметилпсораленом рекомбинация между мечеными вирусами увеличивается, что позволяет предположить, что повреждение триметилпсораленом стимулирует рекомбинацию. [76] MR HSV, по-видимому, частично зависит от механизма рекомбинационной репарации клеток-хозяев, поскольку клетки фибробластов кожи, дефектные в компоненте этого механизма (т.е. клетки пациентов с синдромом Блума), испытывают дефицит MR. [78]
Эти наблюдения позволяют предположить, что MR при инфекциях простого герпеса включает генетическую рекомбинацию поврежденных вирусных геномов, приводящую к образованию жизнеспособного потомства вирусов. ВПГ-1 при заражении клеток-хозяев вызывает воспаление и окислительный стресс. [79] Таким образом, оказывается, что геном ВПГ может подвергаться окислительному повреждению ДНК во время инфекции, и что MR может повысить выживаемость и вирулентность вируса в этих условиях. [ нужна цитата ]
Модифицированный вирус простого герпеса рассматривается в качестве потенциального средства лечения рака и прошел обширные клинические испытания для оценки его онколитической (убивающей рак) способности. [80] Промежуточные данные об общей выживаемости 3-й фазы исследования Amgen генетически ослабленного вируса герпеса свидетельствуют об эффективности против меланомы . [81]
Вирус простого герпеса также используется в качестве транснейронального индикатора, определяющего связи между нейронами посредством пересечения синапсов. [82]
ВПГ-2 — наиболее частая причина менингита Молларе . [83] ВПГ-1 может привести к потенциально смертельным случаям герпетического энцефалита . [84] Вирусы простого герпеса также изучались при заболеваниях центральной нервной системы, таких как рассеянный склероз , но исследования были противоречивыми и неубедительными. [85]
После постановки диагноза инфекции простого генитального герпеса у пациентов может развиться эпизод глубокой депрессии . Помимо предложения противовирусных препаратов для облегчения симптомов и сокращения их продолжительности, врачи также должны учитывать влияние нового диагноза на психическое здоровье. Предоставление информации об очень высокой распространенности этих инфекций, их эффективном лечении и будущих методах лечения, находящихся в стадии разработки, может дать надежду пациентам, которые в противном случае деморализованы. [ нужна цитата ]
Существуют широко используемые вакцины против некоторых герпевирусов, такие как ветеринарная вакцина HVT/LT (вакцина против векторного ларинготрахеита индейки). Однако он предотвращает атеросклероз (который гистологически отражает атеросклероз у людей) у вакцинированных целевых животных. [86] [87] Единственные человеческие вакцины, доступные против герпесвирусов, — это вакцина против вируса ветряной оспы , которую вводят детям в возрасте около первого дня рождения для предотвращения ветряной оспы (ветряной оспы) или взрослым для предотвращения вспышки опоясывающего лишая (опоясывающего герпеса). Однако человеческой вакцины против вирусов простого герпеса не существует. По состоянию на 2022 год проводятся активные доклинические и клинические исследования простого герпеса на людях; разрабатываются вакцины как для лечения, так и для профилактики. [ нужна цитата ]