Гистоновые ацетилтрансферазы ( HAT ) представляют собой ферменты , которые ацетилируют консервативные аминокислоты лизина на гистоновых белках путем переноса ацетильной группы от ацетил-КоА с образованием ε- N -ацетиллизина. ДНК обернута вокруг гистонов, и путем переноса ацетильной группы на гистоны гены можно включать и выключать. В целом ацетилирование гистонов увеличивает экспрессию генов.
В общем, ацетилирование гистонов связано с активацией транскрипции и связано с эухроматином . Эухроматин, который менее плотен, позволяет факторам транскрипции легче связываться с регуляторными сайтами ДНК, вызывая активацию транскрипции. Когда это было впервые обнаружено, считалось, что ацетилирование лизина нейтрализует обычно присутствующий положительный заряд , тем самым уменьшая сродство между гистоном и (отрицательно заряженной) ДНК, что делает ДНК более доступной для факторов транскрипции . С тех пор появились исследования, показавшие, что ацетилирование лизина и другие посттрансляционные модификации гистонов создают сайты связывания для специфических доменов межбелкового взаимодействия, таких как ацетиллизин-связывающий бромодомен . Гистоновые ацетилтрансферазы могут также ацетилировать негистоновые белки, такие как ядерные рецепторы и другие факторы транскрипции, чтобы облегчить экспрессию генов.
HAT традиционно делят на два разных класса в зависимости от их субклеточной локализации. [2] HAT типа А расположены в ядре и участвуют в регуляции экспрессии генов посредством ацетилирования нуклеосомных гистонов в контексте хроматина. [3] Они содержат бромодомен , который помогает им распознавать и связываться с остатками ацетилированного лизина на гистоновых субстратах. Gcn5, p300/CBP и TAF II 250 являются примерами HAT типа A, которые взаимодействуют с активаторами для усиления транскрипции. HAT типа B расположены в цитоплазме и отвечают за ацетилирование вновь синтезированных гистонов перед их сборкой в нуклеосомы . В этих HAT отсутствует бромодомен, поскольку их мишени неацетилированы. Ацетильные группы, добавленные HAT типа B к гистонам, удаляются HDAC , как только они попадают в ядро и включаются в хроматин . Hat1 — один из немногих известных примеров HAT типа B. [4] Несмотря на эту историческую классификацию HAT, некоторые белки HAT функционируют в нескольких комплексах или местах и, таким образом, их нелегко отнести к определенному классу. [5]

HAT можно сгруппировать в несколько различных семейств на основе гомологии последовательностей, а также общих структурных особенностей и функциональных ролей. Семейство N- ацетилтрансфераз (GNAT), родственное Gcn5, включает Gcn5, PCAF , Hat1, Elp3 , Hpa2, Hpa3, ATF-2 и Nut1. Эти HAT обычно характеризуются наличием бромодомена, и обнаружено, что они ацетилируют остатки лизина на гистонах H2B , H3 , [6] и H4 . [2] Все члены семейства GNAT характеризуются наличием до четырех консервативных мотивов (AD), обнаруженных в каталитическом домене HAT. Сюда входит наиболее консервативный мотив А, который содержит последовательность Arg/Gln-XX-Gly-X-Gly/Ala, которая важна для распознавания и связывания ацетил-КоА . [4] Мотив C встречается в большинстве GNAT, но отсутствует в большинстве других известных HAT. [5] Дрожжевой HAT Gcn5 (общий контроль, недерепрессируемый-5) является одним из наиболее изученных членов этого семейства. Он имеет четыре функциональных домена, включая N-концевой домен, высококонсервативный каталитический (HAT) домен, домен взаимодействия Ada2 и C-концевой бромодомен. PCAF (p300/CBP-ассоциированный фактор) и GCN5 представляют собой GNAT млекопитающих, которые имеют высокую степень гомологии во всех своих последовательностях. Эти белки имеют N-концевую область из 400 остатков, которая отсутствует у дрожжевого Gcn5, но их функции HAT эволюционно консервативны по отношению к последнему. Hat1 был первым идентифицированным белком HAT. Он отвечает за большую часть цитоплазматической активности HAT у дрожжей и прочно связывается с гистоном H4 благодаря его ассоциации с дополнительной субъединицей Hat2. Elp3 является примером HAT типа А, обнаруженного у дрожжей. Он является частью голофермента РНК-полимеразы II и играет роль в элонгации транскрипции.
Семейство HAT MYST названо в честь четырех его основателей MOZ , Ybf2 (Sas3), Sas2 и Tip60 . [2] Другие важные члены включают Esa1 , MOF , MORF и HBO1 . Эти HAT обычно характеризуются наличием цинковых пальцев и хромодоменов , и обнаружено, что они ацетилируют остатки лизина на гистонах H2A , H3 и H4. Некоторые белки семейства MYST содержат цинковые пальцы, а также высококонсервативный мотив А, обнаруженный среди GNAT, который облегчает связывание ацетил-КоА. [4] Богатая цистеином область, расположенная на N-конце домена HAT белков MYST, участвует в связывании цинка, что важно для активности HAT. [7] Tip60 (Tat-интерактивный белок, 60 кДа) был первым человеческим членом семейства MYST, проявившим активность HAT. Sas3, обнаруженный в дрожжах, является гомологом MOZ (белок цинковых пальцев моноцитарного лейкоза), который является онкогеном , обнаруженным у людей. Esa1 был первой незаменимой HAT, обнаруженной у дрожжей, а MOF является его гомологом у плодовых мух. HAT-активность последнего необходима для двукратного увеличения транскрипции Х-хромосомы самца ( дозовая компенсация ) у мух. Человеческий HBO1 (HAT, связанный с ORC1) был первым HAT, который, как было показано, связывается с компонентами комплекса начала репликации . MORF (фактор, связанный с MOZ) демонстрирует очень близкую гомологию с MOZ на всей своей длине. [5] Он содержит N-концевую область репрессии, которая снижает активность HAT in vitro , а также C-концевой домен активации, который функционален в отсутствие домена HAT.
Помимо тех, которые являются членами семейств GNAT и MYST, существует несколько других белков, обычно обнаруживаемых у высших эукариот, которые проявляют HAT-активность. К ним относятся p300/CBP, коактиваторы ядерных рецепторов (например, ACTR/SRC-1), TAF II 250, TFIIIC, Rtt109 и CLOCK . p300/CBP специфичны для многоклеточных животных [8] и содержат несколько областей цинковых пальцев, бромодомен, каталитический (HAT) домен и области, которые взаимодействуют с другими факторами транскрипции. [4] Важно отметить, что домен HAT не имеет гомологии последовательности с другими известными HAT, [9] и необходим для функционирования p300/CBP в активации транскрипции. [4] Кроме того, эти белки содержат несколько мотивов домена HAT (A, B и D), которые аналогичны мотивам GNAT. Они также обладают новым мотивом E, который гомологичен последовательностям HAT-доменов GNAT. TFIIIC является одним из основных факторов транскрипции, участвующих в транскрипции, опосредованной РНК-полимеразой III . Было показано, что три компонента человеческого белка обладают независимой активностью HAT ( hTFIIIC220 , hTFIIIC110 и hTFIIIC90 ). [10] Rtt109 представляет собой специфичную для грибов HAT, для активности которой требуется ассоциация с белками-шаперонами гистонов. [8] HAT-активность коактиваторов TAF II 250 и CLOCK человека не изучалась столь широко. TAF II 250 является одной из субъединиц фактора, связанного с TBP, TFIID , и он имеет общий паттерн Gly-X-Gly с Gcn5, который важен для активности HAT. [5] CLOCK — это главный регулятор циркадных ритмов, который взаимодействует с BMAL1 для выполнения своей HAT-активности. [11]
Тремя важными коактиваторами ядерных рецепторов, которые проявляют активность HAT, являются SRC-1 , ACTR и TIF-2 . Известно, что SRC-1 человека (коактиватор стероидных рецепторов-1) взаимодействует с p300/CBP и PCAF, а его домен HAT расположен в его C-концевой области. ACTR (также известный как RAC3, AIB1 и TRAM-1 у людей) имеет значительную гомологию последовательностей с SRC-1, в частности, в N-концевых и C-концевых (HAT) областях, а также в доменах взаимодействия рецептора и коактиватора. . [5] ACTR также взаимодействует с p300/CBP и PCAF. Первый может препятствовать связыванию ACTR и активации его рецептора путем ацетилирования его в домене взаимодействия с рецептором. TIF-2 (транскрипционный промежуточный фактор 2; также известный как GRIP1) является еще одним коактиватором ядерного рецептора с активностью HAT, и он также взаимодействует с p300/CBP.
Ниже представлена таблица, в которой суммированы различные семейства HAT, а также связанные с ними члены, родительские организмы, мультисубъединичные комплексы, гистоновые субстраты и структурные особенности. [2] [5] [8] [10] [12] [13] [14] [15] [16] [17]

В целом HAT характеризуются структурно консервативной основной областью, состоящей из трехцепочечного β-листа , за которым следует длинная α-спираль, параллельная ему и охватывающая одну его сторону. [7] [8] Коровая область, соответствующая мотивам A, B и D белков GNAT, [4] фланкирована с противоположных сторон N- и C-концевыми α/β-сегментами, которые структурно уникальны для данное семейство HAT. [7] [8] Центральное ядро и фланкирующие сегменты вместе образуют щель над первым, где субстраты гистонов могут связываться перед катализом. [8] В то время как центральный ядерный домен (мотив A в GNAT) участвует в связывании и катализе ацетил-КоА, N- и C-концевые сегменты помогают связывать субстраты гистонов. [7] Уникальные особенности, связанные с последовательностью и/или структурой N- и C-концевых областей для разных семейств HAT, могут помочь объяснить некоторые наблюдаемые различия между HAT в специфичности субстрата гистонов. Было обнаружено, что связывание CoA расширяет канавку для связывания гистонов в центральном ядре за счет перемещения C-концевого сегмента Gcn5 наружу. Кроме того, поскольку контакты между КоА и белком способствуют образованию благоприятных контактов гистон-белок, вполне вероятно, что связывание КоА предшествует связыванию гистонов in vivo .
HAT в семействе GNAT в первую очередь характеризуются доменом HAT, состоящим примерно из 160 остатков, и C-концевым бромодоменом, который связывается с ацетилированными остатками лизина. [7] Члены семейства MYST имеют домены HAT длиной около 250 остатков. Многие белки MYST также содержат богатый цистеином цинк-связывающий домен в области HAT в дополнение к N-концевому хромодомену, который связывается с метилированными остатками лизина .
В более широком масштабе структуры каталитических доменов белков GNAT (Gcn5, PCAF) демонстрируют смешанную глобулярную α/β-складку с пятью α-спиралями и шестью β-нитями. [4] Общая топология напоминает тиски , с центральным ядром белка в основании и N- и C-концевыми сегментами по бокам.
HAT p300/CBP имеют более крупные домены HAT (около 500 остатков), чем те, которые присутствуют в семействах GNAT и MYST. [7] Они также содержат бромодомен, а также три домена, богатых цистеином/гистидином, которые, как полагают, опосредуют взаимодействие с другими белками. Структура p300/CBP характеризуется удлиненным глобулярным доменом, содержащим в центре семицепочечный β-лист, окруженный девятью α-спиралями и несколькими петлями. [9] Структура центральной области ядра, связанной со связыванием ацетил-КоА, консервативна по отношению к GNAT и MYST HAT, но существует множество структурных различий в областях, фланкирующих это центральное ядро. В целом структурные данные согласуются с тем фактом, что HAT p300/CBP более беспорядочны, чем HAT GNAT и MYST, в отношении связывания субстрата.
Структура Rtt109 очень похожа на структуру p300, несмотря на то, что идентичность последовательностей между двумя белками составляет всего 7%. [9] Существует семицепочечный β-лист, окруженный α-спиралями, а также петля, которая участвует в связывании субстрата ацетил-КоА. Несмотря на консервативную структуру, Rtt109 и p300/CBP функционально уникальны. Например, сайт связывания субстрата первого больше похож на сайт GNAT и MYST HAT. Кроме того, остатки в активном центре каждого фермента различны, что позволяет предположить, что они используют разные каталитические механизмы переноса ацетильной группы.
Основной механизм, катализируемый HAT, включает перенос ацетильной группы от ацетил-КоА к ε-аминогруппе целевой боковой цепи лизина внутри гистона. [8] Различные семейства HAT используют уникальные стратегии для осуществления такой трансформации.

Члены семейства GNAT имеют консервативный остаток глутамата, который действует как общее основание для катализа нуклеофильной атаки лизинамина на тиоэфирную связь ацетил-КоА. [8] Эти HAT используют упорядоченный последовательный механизм bi-bi, при котором оба субстрата (ацетил-КоА и гистон) должны связываться с образованием тройного комплекса с ферментом, прежде чем может произойти катализ. Первым связывается ацетил-КоА, а затем гистоновый субстрат. Консервативный остаток глутамата (Glu173 в дрожжевом Gcn5) активирует молекулу воды для удаления протона из аминогруппы лизина, что активирует ее для прямой нуклеофильной атаки на карбонильный углерод связанного с ферментом ацетил-КоА. После реакции сначала высвобождается ацетилированный гистон, а затем КоА. [4] [8]
Исследования дрожжевого Esa1 из семейства HAT MYST выявили механизм пинг-понга, включающий консервативные остатки глутамата и цистеина. [18] Первая часть реакции включает образование ковалентного промежуточного продукта, в котором остаток цистеина ацетилируется в результате нуклеофильной атаки этого остатка на карбонильный углерод ацетил-КоА. Затем остаток глутамата действует как общее основание, облегчая перенос ацетильной группы от цистеина к субстрату гистона способом, аналогичным механизму, используемому GNAT. Когда Esa1 собирается в комплекс пикколо NuA4 , он теряет свою зависимость от остатка цистеина для катализа, что позволяет предположить, что реакция может протекать по тройному механизму bi-bi, когда фермент является частью физиологически значимого мультибелкового комплекса.
В p300 человека Tyr1467 действует как обычная кислота, а Trp1436 помогает ориентировать целевой остаток лизина субстрата гистона в активный центр. [8] Эти два остатка высококонсервативны в семействе p300/CBP HAT и, в отличие от ферментов семейств GNAT и MYST, p300 не использует общую основу для катализа. Скорее всего, члены семейства p300/CBP используют механизм переноса ацетила Теорелла-Чанса (т.е. «ударил и беги»).
Rtt109, вероятно, использует механизм, отличный от механизма других HAT. [9] Дрожжевой фермент обладает очень низкой каталитической активностью в отсутствие белков-шаперонов гистонов Asf1 и Vps75, которые могут участвовать в доставке субстратов гистонов к ферменту для ацетилирования. [8] Более того, общая кислота или основание для этой HAT еще не идентифицированы.
Структуры нескольких HAT-доменов, связанных с ацетил-КоА и пептидами-субстратами гистонов, показывают, что последние связываются через бороздку на белке, который образован центральной сердцевинной областью в основании и с противоположных сторон окружен переменными N- и C. -концевые сегменты, которые опосредуют большинство взаимодействий с пептидом-субстратом. [8] Вполне вероятно, что эти вариабельные области, по крайней мере частично, ответственны за наблюдаемую специфичность различных HAT к различным субстратам гистонов.
Члены семейств GNAT и MYST, а также Rtt109 проявляют большую селективность в отношении субстрата, чем p300/CBP, что довольно беспорядочно в отношении связывания субстрата. [8] Хотя оказывается, что только три-пять остатков с каждой стороны ацетилируемого лизина необходимы для эффективного связывания субстрата и катализа членами семейств GNAT и p300/CBP, более дистальные области субстрата могут быть важны для эффективное ацетилирование HAT семейства MYST. [19]
Было показано, что различные HAT, обычно в контексте мультисубъединичных комплексов, ацетилируют определенные остатки лизина в гистонах.
Gcn5 не может ацетилировать нуклеосомные гистоны в отсутствие других белковых факторов. [5] Однако в контексте таких комплексов, как SAGA и ADA, Gcn5 способен ацетилировать H3K14 среди других сайтов внутри гистонов H2B, H3 и H4 (например, H3K9, H3K36, H4K8, H4K16). [3] [4] [7] [19] И Gcn5, и PCAF имеют самое сильное предпочтение сайта для H3K14, либо в виде свободного гистона, либо внутри нуклеосомы. [4] [7] Hat1 ацетилирует H4K5 и H4K12, а Hpa2 ацетилирует H3K14 in vitro . [4] [5]
У мух ацетилирование H4K16 на Х-хромосоме самца с помощью MOF в контексте комплекса MSL коррелирует с усилением транскрипции как механизмом дозовой компенсации у этих организмов. [2] У человека комплекс MSL осуществляет большую часть полногеномного ацетилирования H4K16. В контексте родственных им комплексов Sas2 (SAS) и Esa1 (NuA4) также осуществляют ацетилирование H4K16, в частности, в теломерных областях хромосом. Также обнаружено, что Sas2 ацетилирует H3K14 in vitro на свободных гистонах. [12] Esa1 также может ацетилировать H3K14 in vitro на свободных гистонах, а также H2AK5, H4K5, H4K8 и H4K12 in vitro или in vivo на нуклеосомных гистонах. H2AK7 и H2BK16 также ацетилируются Esa1 in vivo . Примечательно, что ни Sas2, ни Esa1 не могут ацетилировать нуклеосомные гистоны in vitro в качестве свободного фермента. То же самое относится и к Sas3, который, как наблюдают, ацетилирует H3K9 и H3K14 in vivo , а также остатки лизина на H2A и H4. MOZ также может ацетилировать H3K14. [19]
p300/CBP одинаково хорошо ацетилирует все четыре ядра нуклеосомных гистонов. [4] In vitro было обнаружено, что они ацетилируют H2AK5, H2BK12, H2BK15, H3K14, H3K18, H4K5 и H4K8. [5] SRC-1 ацетилирует H3K9 и H3K14, TAF II 230 (дрозофиловый гомолог человеческого TAF II 250) ацетилирует H3K14, а Rtt109 ацетилирует H3K9, H3K23, [19] и H3K56 в присутствии Asf1 или Vps75. [9]
Помимо основных гистонов, некоторые HAT ацетилируют ряд других клеточных белков, включая активаторы транскрипции , базальные факторы транскрипции , структурные белки, полиамины и белки, участвующие в импорте ядра. [4] Ацетилирование этих белков может изменить их способность взаимодействовать с родственной им ДНК и/или белковыми субстратами. Идея о том, что ацетилирование может влиять на функцию белка таким образом, привела к исследованию роли ацетилтрансфераз в путях передачи сигнала и можно ли провести в этом отношении подходящую аналогию с киназами и событиями фосфорилирования.
PCAF и p300/CBP являются основными HAT, которые, как было замечено, ацетилируют ряд негистоновых белков. Для PCAF к ним относятся негистоновые белки хроматина ( группа высокой подвижности (HMG) ) HMG-N2/HMG17 и HMG-I(Y) , активаторы транскрипции p53 , MyoD , E2F(1-3) и ВИЧ Tat. и общие факторы транскрипции TFIIE и TFIIF . [5] Другие белки включают CIITA , Brm (ремоделер хроматина), NF-κB (p65), TAL1/SCL , Beta2/NeuroD , C/EBPβ , IRF2 , IRF7 , YY1 , KLF13 , EVI1 , AME, ER81 и андроген . рецептор (АР) . [20] Также было обнаружено, что PCAF ацетилирует белки аденовируса c-MYC , GATA-2 , ретинобластомы (Rb) , Ku70 и E1A . [21] Он также может аутоацетилироваться, что облегчает внутримолекулярные взаимодействия с его бромодоменом, который может участвовать в регуляции его активности HAT. [4]
p300/CBP имеет множество негистоновых субстратов, включая негистоновые белки хроматина HMG1 , HMG-N1/HMG14 и HMG-I(Y), активаторы транскрипции p53, c-Myb , GATA-1 , EKLF , TCF , и Tat ВИЧ, коактиваторы ядерных рецепторов ACTR, SRC-1 и TIF-2, а также общие факторы транскрипции TFIIE и TFIIF. [5] Другие субстраты включают факторы транскрипции Sp1, KLF5 , FOXO1 , MEF2C , SRY , GATA-4 и HNF-6 , [12] HMG-B2 , [21] STAT3 , рецепторы андрогенов и эстрогенов (α) , GATA. -2, GATA-3 , MyoD, E2F(1-3), p73 α, ретинобластома (Rb), NF-κB (p50, p65), Smad7 , импортин-α , Ku70, YAP1 , [22] белок аденовируса E1A, и S-HDAg ( малый дельта-антиген вируса гепатита дельта ). [21] p300/CBP также ацетилирует β-катенин , RIP140 , PCNA , эндонуклеазу-1 метаболических ферментов ДНК , тиминовую ДНК-гликозилазу и ДНК-хеликазу синдрома Вернера , STAT6 , Runx1 (AML1) , UBF, Beta2/ NeuroD, CREB , c-Jun , C/EBPβ, NF-E2 , SREBP , IRF2, Sp3 , YY1, KLF13, EVI1, BCL6 , HNF-4 , ER81 и FOXO4 (AFX) . [20]
Было обнаружено, что образование мультисубъединичных комплексов модулирует субстратную специфичность HAT. [12] В целом, хотя рекомбинантные HAT способны ацетилировать свободные гистоны, HAT могут ацетилировать нуклеосомные гистоны только тогда, когда они находятся в соответствующих комплексах HAT in vivo . [5] Некоторые из белков, которые связываются с HAT в этих комплексах, действуют путем нацеливания комплекса HAT на нуклеосомы в определенных областях генома . [2] [12] Например, было замечено, что комплексы HAT (например, SAGA, NuA3) часто используют метилированные гистоны в качестве сайтов стыковки, так что каталитическая субъединица HAT может более эффективно осуществлять ацетилирование гистонов. [2]
Кроме того, образование мультисубъединичных комплексов HAT влияет на лизиновую специфичность HAT. [12] Конкретные остатки лизина, которые ацетилирует данная HAT, могут стать либо более широкими, либо более ограниченными в объеме после ассоциации с соответствующим комплексом. Например, лизиновая специфичность HAT семейства MYST по отношению к их гистоновым субстратам становится более ограниченной, когда они связываются со своими комплексами. Напротив, Gcn5 приобретает способность ацетилировать несколько сайтов как в гистонах H2B, так и в H3, когда он присоединяется к другим субъединицам с образованием комплексов SAGA и ADA. [4] Более того, специфичность сайта ацетилирования Rtt109 определяется его ассоциацией либо с Vps75, либо с Asf1. [19] В комплексе с первым Rtt109 ацетилирует H3K9 и H3K27, но в комплексе со вторым он преимущественно ацетилирует H3K56. [8]
Каталитическая активность HAT регулируется двумя типами механизмов: (1) взаимодействием с регуляторными субъединицами белка и (2) аутоацетилированием. [8] Один и тот же HAT может регулироваться разными способами, и один и тот же эффектор может фактически приводить к разным результатам в разных условиях. [4] Хотя очевидно, что ассоциация HAT с мультибелковыми комплексами обеспечивает механизм регуляции как активности HAT, так и субстратной специфичности in vivo , молекулярная основа того, как это происходит на самом деле, до сих пор в значительной степени неизвестна. [8] Однако данные свидетельствуют о том, что ассоциированные субъединицы могут способствовать катализу, по крайней мере частично, способствуя продуктивному связыванию комплекса HAT с его нативными гистоновыми субстратами.
Было показано, что семейство HAT MYST, p300/CBP и Rtt109 регулируется посредством аутоацетилирования. [8] Человеческий MOF, а также дрожжевые Esa1 и Sas2 аутоацетилируются по консервативному остатку лизина в активном центре, и эта модификация необходима для их функционирования in vivo . Человеческий p300 содержит высокоосновную петлю, встроенную в середину домена HAT, которая гиперацетилирована в активной форме фермента. [8] [9] Было высказано предположение, что при аутоацетилировании эта петля высвобождается из электроотрицательного сайта связывания субстрата, где она находится в неактивной HAT. [23] Ацетилирование дрожжевого Rtt109 по Lys290 также необходимо для проявления полной каталитической активности. [24] Некоторые HAT также ингибируются ацетилированием. Например, активность HAT коактиватора ядерного рецептора ACTR ингибируется при ацетилировании p300/CBP. [4]
Гистон-ацетилтрансферазы (HAT) и гистон-деацетилазы (HDAC) рекрутируются на свои целевые промоторы посредством физических взаимодействий со специфичными для последовательности факторами транскрипции. Обычно они функционируют в составе мультисубъединичного комплекса, в котором другие субъединицы необходимы для модификации остатков гистонов вокруг сайта связывания. Эти ферменты также могут модифицировать негистоновые белки.
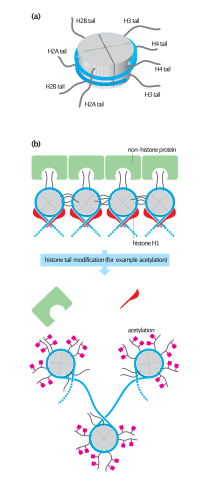
Гистоновые ацетилтрансферазы выполняют множество биологических ролей внутри клетки. Хроматин представляет собой комбинацию белков и ДНК , обнаруженную в ядре , и он претерпевает множество структурных изменений по мере того, как происходят различные клеточные события, такие как репликация ДНК , репарация ДНК и транскрипция . [25] Хроматин в клетке может находиться в двух состояниях: конденсированном и несконденсированном. Последний, известный как эухроматин , транскрипционно активен, тогда как первый, известный как гетерохроматин , транскрипционно неактивен. [25] [26] Гистоны составляют белковую часть хроматина. Существует пять различных белков -гистонов : H1, H2A, H2B, H3 и H4. Коровый гистон образуется, когда два гистона каждого подтипа, за исключением H1, образуют четверичный комплекс. Этот октамерный комплекс в сочетании со 147 парами оснований ДНК, скрученными вокруг него, образует нуклеосому . [4] Гистон H1 соединяет нуклеосомный комплекс вместе, и это последний белок, который связывается в комплексе.
Гистоны, как правило, представляют собой положительно заряженные белки с N-концевыми хвостами, отходящими от ядра. Фосфодиэфирный остов ДНК отрицательный, что обеспечивает сильные ионные взаимодействия между белками-гистонами и ДНК. Гистон-ацетилтрансферазы переносят ацетильную группу на определенные остатки лизина на гистонах, что нейтрализует их положительный заряд и, таким образом, уменьшает сильные взаимодействия между гистонами и ДНК. [25] Также считается, что ацетилирование нарушает взаимодействия между отдельными нуклеосомами и действует как сайты взаимодействия для других белков, связанных с ДНК. [4]
Могут существовать разные уровни ацетилирования гистонов, а также другие типы модификаций, позволяющие клетке контролировать уровень упаковки хроматина во время различных клеточных событий, таких как репликация, транскрипция, рекомбинация и репарация. Ацетилирование — не единственная регуляторная посттрансляционная модификация гистонов, которая определяет структуру хроматина; Также сообщалось о метилировании, фосфорилировании, АДФ-рибозилировании и убиквитинировании. [4] [25] Эти комбинации различных ковалентных модификаций на N-концевых хвостах гистонов называются кодом гистонов , и считается, что этот код может передаваться по наследству и сохраняться в следующем поколении клеток. [26]
Белки-гистоны H3 и H4 являются основными мишенями HAT, но H2A и H2B также ацетилируются in vivo . Лизины 9, 14, 18 и 23 H3 и лизины 5, 8, 12 и 16 H4 нацелены на ацетилирование. [4] [25] Лизины 5, 12, 15 и 20 ацетилируются по гистону H2B, в то время как только лизины 5 и 9 ацетилируются по гистону H2A. [4] [25] [26] При таком большом количестве различных сайтов ацетилирования можно достичь высокого уровня специфичности в запуске специфических ответов. Примером этой специфичности является ацетилирование гистона H4 по лизинам 5 и 12. Этот паттерн ацетилирования наблюдался во время синтеза гистонов. Другим примером является ацетилирование H4K16, которое связано с дозовой компенсацией мужской Х-хромосомы у Drosophila melanogaster . [2] [4]

Модификации гистонов модулируют упаковку хроматина. Уровень упаковки ДНК важен для транскрипции гена, поскольку для осуществления транскрипции транскрипционный аппарат должен иметь доступ к промотору. [4] Нейтрализация заряженных остатков лизина с помощью HAT позволяет хроматину деконденсироваться, так что этот механизм получает доступ к гену, подлежащему транскрипции. Однако ацетилирование не всегда связано с повышенной транскрипционной активностью. Например, ацетилирование H4K12 связано с конденсированным и транскрипционно неактивным хроматином. [27] Кроме того, некоторые модификации гистонов связаны как с повышенной, так и с подавленной активностью в зависимости от контекста. [28]
HAT действуют как коактиваторы транскрипции или сайленсеры генов и чаще всего обнаруживаются в больших комплексах, состоящих из 10–20 субъединиц, некоторые из которых являются общими для разных комплексов HAT. [25] Эти комплексы включают SAGA (Spt/Ada/Gcn5L ацетилтрансфераза), PCAF, ADA (адаптер транскрипции), TFIID (фактор транскрипции II D), TFTC (TAF-содержащий комплекс без TBP) и NuA3/NuA4 (нуклеосомные ацетилтрансферазы). H3 и H4). [2] [25] Эти комплексы модулируют специфичность HAT, доставляя HAT к генам-мишеням, где они затем могут ацетилировать нуклеосомные гистоны. [25] Некоторые коактиваторы транскрипции HAT содержат бромодомен , модуль из 110 аминокислот, который распознает ацетилированные остатки лизина и функционально связан с коактиваторами в регуляции транскрипции. [29]
Способность гистон-ацетилтрансфераз манипулировать структурой хроматина и закладывать эпигенетический каркас делает их незаменимыми для поддержания и выживания клеток. В процессе ремоделирования хроматина участвуют несколько ферментов, в том числе HAT, которые помогают в реформировании нуклеосом и необходимы для функционирования систем восстановления повреждений ДНК. [30] HAT участвуют в прогрессировании заболеваний, особенно нейродегенеративных расстройств. Например, болезнь Хантингтона — это заболевание, которое влияет на моторику и умственные способности. Единственная известная мутация, связанная с заболеванием, находится в N-концевой области белка хантингтина (htt) . [31] Сообщалось, что htt напрямую взаимодействует с HAT и подавляет каталитическую активность p300/CBP и PCAF in vitro .
Синдром преждевременного старения человека, прогерия Хатчинсона-Гилфорда , вызван мутационным дефектом в обработке ламина А , белка ядерного матрикса . В мышиной модели этого состояния задерживается рекрутирование репарирующих белков в места повреждения ДНК . Молекулярный механизм, лежащий в основе этой реакции отсроченного восстановления, включает дефект ацетилирования гистонов. [32] В частности, гистон H4 гипоацетилируется по остатку лизина 16 (H4K16), и этот дефект обусловлен снижением ассоциации гистон-ацетилтрансферазы Mof с ядерным матриксом [32]
Спиноцеребеллярная атаксия 1 типа — нейродегенеративное заболевание, возникающее в результате дефектного мутантного белка атаксина-1 . Мутантный атаксин-1 снижает ацетилирование гистонов, что приводит к подавлению транскрипции, опосредованной гистон-ацетилтрансферазой . [33]
HAT также связаны с контролем функций обучения и памяти. Исследования показали, что у мышей без PCAF или CBP наблюдаются признаки нейродегенерации . [31] Мыши с делецией PCAF неспособны к обучению, а мыши с делецией CBP, по-видимому, страдают от долговременной потери памяти. [34]
Нарушение баланса между ацетилированием и деацетилированием также связано с проявлением некоторых видов рака. Если гистон-ацетилтрансферазы ингибируются, поврежденная ДНК не может быть восстановлена, что в конечном итоге приводит к гибели клеток. Контроль процесса ремоделирования хроматина в раковых клетках может стать новой лекарственной мишенью для исследований рака. [35] Атака этих ферментов в раковых клетках может привести к усилению апоптоза из-за большого количества повреждений ДНК. Один из таких ингибиторов гистон-ацетилтрансфераз называется гарцинол. Это соединение содержится в кожуре плодов гарцинии индийской , также известной как мангустин . Чтобы изучить влияние гарцинола на ацетилтрансферазы гистонов, исследователи использовали клетки HeLa . Клетки подверглись облучению, создавшему двухцепочечные разрывы в ДНК, и в клетки вводили гарцинол, чтобы проверить, влияет ли он на реакцию повреждения ДНК. Если гарцинол успешно ингибирует процесс соединения негомологичных концов (механизм репарации ДНК, который отдает предпочтение фиксации двухцепочечных разрывов), [36] тогда он может служить радиосенсибилизатором — молекулой, повышающей чувствительность клеток к радиации. повреждать. Повышение радиочувствительности может повысить эффективность лучевой терапии. [35]