Карбеновый комплекс переходного металла представляет собой металлоорганическое соединение с двухвалентным углеродным лигандом , который сам по себе также называется карбеном . [1] Карбеновые комплексы были синтезированы из большинства переходных металлов и металлов с f-блоком , [2] с использованием множества различных синтетических путей, таких как нуклеофильное присоединение и абстракция альфа-водорода. [1] Термин «карбеновый лиганд» является формализмом, поскольку многие из них не происходят напрямую из карбенов и большинство из них гораздо менее реакционноспособны, чем одиночные карбены. [2] Часто описываемые как =CR 2 , карбеновые лиганды занимают промежуточное положение между алкилами (-CR 3 ) и карбинами (≡CR) . В синтезе используется множество различных реагентов на основе карбена, таких как реагент Теббе . Они также участвуют в каталитических реакциях, особенно в метатезисе алкенов , и представляют ценность как в промышленном гетерогенном, так и в гомогенном катализе для приготовления тонких химикатов в лабораторных и промышленных масштабах. [1] [3] [4]
Карбеновые комплексы металлов часто делят на два типа. Карбены Фишера, названные в честь Эрнста Отто Фишера , имеют сильные π-акцепторы у металла и электрофильны по атому углерода карбена. Карбены Шрока , названные в честь Ричарда Р. Шрока , характеризуются более нуклеофильными карбеновыми углеродными центрами; эти виды обычно содержат металлы с более высокой степенью окисления (валентностью). N -Гетероциклические карбены (NHC) стали популяризироваться после того, как Ардуэнго в 1991 году выделил стабильный свободный карбен. [5] В связи с ростом этой области в настоящее время известны карбеновые комплексы с широким диапазоном различной реакционной способности и разнообразными заместителями. Часто невозможно классифицировать карбеновый комплекс исключительно по его электрофильности или нуклеофильности. [1]

Общими чертами карбенов Фишера являются: [6]
Примеры включают (CO) 5 W=COMePh и (OC) 5 Cr=C(NR 2 )Ph .

Карбеновые комплексы Фишера относятся к синглетной форме карбенов, где оба электрона занимают одну и ту же sp 2 -орбиталь у углерода. Эта неподеленная пара отдает предпочтение пустой d-орбитали на основе металла, образуя σ-связь. Возможно π-связывание заполненной d-орбитали металла с пустой p-орбиталью атома углерода. Однако это взаимодействие обычно слабое, поскольку атомы альфа-донора также вносят вклад в эту орбиталь. По существу, карбены Фишера характеризуются наличием частичной двойной связи. Основные резонансные структуры карбенов Фишера передают отрицательный заряд металлическому центру, а положительный - атому углерода, что делает его электрофильным. [6]

Карбены Фишера можно сравнить с кетонами, причем атом углерода карбена является электрофильным, как и карбонильный атом углерода кетона. Это видно по резонансным структурам , где существенный вклад вносит структура, несущая положительный углеродный центр. [6] Как и кетоны, карбены Фишера могут подвергаться альдольным реакциям. Атомы водорода, присоединенные к атому углерода α к атому углерода карбена, являются кислотными и могут быть депротонированы основанием, таким как н -бутиллитий , с образованием нуклеофила, который может подвергаться дальнейшей реакции. [7]

Карбены Шрока не имеют π-принимающих лигандов на металлическом центре. Их часто называют алкилиденовыми комплексами . Обычно это подмножество карбеновых комплексов встречается с: [6]
Примеры включают ((CH 3 ) 3 CCH 2 )Ta=CHC(CH 3 ) 3 [9] и Os(PPh 3 ) 2 (NO)Cl(=CH 2 ) . [10]

Связывание в таких комплексах можно рассматривать как соединение металла в триплетном состоянии и триплетного карбена, образующее настоящую двойную связь. И металл, и атом углерода отдают по два электрона, по одному на каждую связь. Поскольку нет донорства атому карбена от соседних групп, степень обратной связи пи намного больше, образуя прочную двойную связь. Эти связи слабо поляризованы по отношению к углероду, поэтому атом карбена является нуклеофилом. Более того, основные резонансные структуры карбена Шрока передают отрицательный заряд атому углерода, делая его нуклеофильным. [6] Комплексы с метилиденовым лигандом ( =CH 2 ) являются простейшими карбенами типа Шрока.

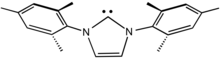
N -Гетероциклические карбены (NHC) являются особенно распространенными карбеновыми лигандами. [11] Они популярны, потому что их легче приготовить, чем карбены Шрока и Фишера. Фактически, многие NHC выделяются в виде свободных лигандов, поскольку они представляют собой стойкие карбены . [12] [13] Будучи сильно стабилизированными π-донорными заместителями, NHC являются мощными σ-донорами, но π-связь с металлом слабая. [14] По этой причине связь между углеродом и металлическим центром часто изображается в виде одинарной дативной связи, тогда как карбены Фишера и Шрока обычно изображаются с двойными связями с металлом. Продолжая эту аналогию, NHC часто сравнивают с триалкилфосфиновыми лигандами . Подобно фосфинам, NHC служат лигандами-наблюдателями , которые влияют на катализ посредством комбинации электронных и стерических эффектов, но они не связывают субстраты напрямую. [15] [16]
Ранним примером этого способа связывания был [C 5 Me 5 Mn(CO) 2 ] 2 (μ-CO), полученный из диазометана :
Another example of this family of compounds is Tebbe's reagent. It features a methylene bridge joining titanium and aluminum.[17]
Metal carbene complexes have applications in hetereogeneous and homogeneous catalysis, and as reagents for organic reactions.

The dominant application of metal carbenes involves none of the above classes of compounds, but rather heterogeneous catalysts used for alkene metathesis for the synthesis of higher alkenes. A variety of related reactions are used to interconvert light alkenes, e.g. butenes, propylene, and ethylene.[18] Carbene complexes are invoked as intermediates in the Fischer–Tropsch route to hydrocarbons.[3]
A variety of homogeneous carbene catalysts, especially the Grubbs' ruthenium and Schrock molybdenum-imido catalysts have been used for olefin metathesis in laboratory-scale synthesis of natural products and materials science.[4]
Homogeneous Schrock-type carbene complexes such as Tebbe's reagent can be used for the olefination of carbonyls, replacing the oxygen atom with a methylidene group. The nucleophilic carbon atom behaves similarly to the carbon atom of the phosphorus ylide in the Wittig reaction, attacking the electrophilic carbonyl atom of a ketone, followed by elimination of a metal oxide.[1]

In the nucleophilic abstraction reaction, a methyl group can be abstracted from the donating group of a Fischer carbene, making it a strong nucleophile for further reaction.[6]

Diazo compounds like methyl phenyldiazoacetate can be used for cyclopropanation or to insert into C-H bonds of organic substrates. These reactions are catalyzed by dirhodium tetraacetate or related chiral derivatives. Such catalysis is assumed to proceed via the intermediacy of carbene complexes.[19]

Fischer carbenes are used with alkynes as the starting reagents for the Wulff–Dötz reaction, forming phenols.[20]


The first metal carbene complex to have been reported was Chugaev's red salt, first synthesized as early as 1925, although it was never identified to be a carbene complex.[21] The characterization of (CO)5W(COCH3(Ph)) in the 1960s is often cited as the starting point of the area and Ernst Otto Fischer, for this and other achievements in organometallic chemistry, was awarded the 1973 Nobel Prize in Chemistry.[22] In 1968, Hans-Werner Wanzlick and Karl Öfele separately reported metal-bonded N-heterocyclic carbenes.[6][23][24] The synthesis and characterization of ((CH3)3CCH2)Ta=CHC(CH3)3 by Richard R. Schrock in 1974 marked the first metal alkylidene complex.[9] In 1991, Anthony J. Arduengo synthesized and crystallized the first persistent carbene, an NHC with large adamantane alkyl groups, accelerating the field of N-heterocarbene ligands to its current use.[5][6]