
Кристаллизация белка — это процесс образования регулярного массива отдельных белковых молекул, стабилизированных кристаллическими контактами. Если кристалл достаточно упорядочен, он будет дифрагировать . Некоторые белки естественным образом образуют кристаллические массивы, например аквапорин в хрусталике глаза. [1] [2]
В процессе кристаллизации белков белки растворяются в водной среде и растворе пробы до достижения пересыщенного состояния . [3] Для достижения этого состояния используются различные методы, такие как диффузия паров, микропартия, микродиализ и диффузия со свободным интерфейсом. Образование кристаллов белка — сложный процесс, на который влияют многие факторы, включая pH, температуру, ионную силу кристаллизационного раствора и даже гравитацию. [3] После формирования эти кристаллы можно использовать в структурной биологии для изучения молекулярной структуры белка, особенно для различных промышленных или медицинских целей. [4] [5]
Уже более 150 лет учёным всего мира известно о кристаллизации белковых молекул. [6]
В 1840 году Фридрих Людвиг Хюнефельд случайно обнаружил образование кристаллического материала в образцах крови дождевых червей, хранившихся под двумя предметными стеклами, и иногда наблюдал небольшие пластинчатые кристаллы в высушенных образцах свиной или человеческой крови. Эти кристаллы были названы Феликсом Хоппе-Зейлером в 1864 году «гемоглобином». Основополагающие открытия Хюнефельда вдохновили многих ученых в будущем. [7]
В 1851 году Отто Функе описал процесс получения кристаллов человеческого гемоглобина путем разбавления эритроцитов растворителями, например чистой водой, спиртом или эфиром, с последующим медленным испарением растворителя из белкового раствора. В 1871 году Уильям Т. Прейер, профессор Йенского университета, опубликовал книгу под названием Die Blutkrystalle («Кристаллы крови»), в которой были рассмотрены особенности кристаллов гемоглобина примерно 50 видов млекопитающих, птиц, рептилий и рыб. [7]
В 1909 году физиолог Эдвард Т. Райхерт вместе с минералогом Амосом П. Брауном опубликовали трактат о получении, физиологии и геометрических характеристиках кристаллов гемоглобина нескольких сотен животных, включая вымершие виды, такие как тасманийский волк. [7] Было обнаружено увеличение количества кристаллов белка.
В 1934 году Джон Десмонд Бернал и его студентка Дороти Ходжкин обнаружили, что кристаллы белка, окруженные маточным раствором, дают лучшие дифракционные картины, чем высушенные кристаллы. Используя пепсин , они первыми различили дифракционную картину влажного глобулярного белка. До Бернала и Ходжкина кристаллография белков проводилась только в сухих условиях с противоречивыми и ненадежными результатами. Это первая рентгенограмма кристалла белка. [8]
В 1958 году Джон Кендрю впервые сообщил о структуре миоглобина (красного белка, содержащего гем), определенной методом рентгеновской кристаллографии . [9] За это открытие Кендрю разделил Нобелевскую премию по химии 1962 года с Максом Перуцем . [4]
Теперь, на основе белковых кристаллов, их структуры играют значительную роль в биохимии и трансляционной медицине.

Кристаллизация белка регулируется той же физикой, которая управляет образованием неорганических кристаллов. Чтобы кристаллизация происходила самопроизвольно, кристаллическое состояние должно быть термодинамически благоприятным. Это описывается свободной энергией Гибба (∆G), определяемой как ∆G = ∆H-T∆S, которая отражает, как энергетика процесса ∆H согласуется с соответствующим изменением энтропии ∆S. [10] Энтропия, грубо говоря, описывает беспорядок системы. Высокоупорядоченные состояния, такие как кристаллы белков, термодинамически невыгодны по сравнению с более неупорядоченными состояниями, такими как растворы белков в растворителе, поскольку переход в более упорядоченное состояние уменьшит общую энтропию системы (положительное ∆S). Для самопроизвольного образования кристаллов ∆G кристаллообразования должна быть отрицательной. Другими словами, энтропийный штраф должен быть оплачен соответствующим уменьшением полной энергии системы (∆H). Знакомые неорганические кристаллы, такие как хлорид натрия, самопроизвольно образуются в условиях окружающей среды, поскольку кристаллическое состояние уменьшает общую энергию системы. Однако кристаллизация некоторых белков в условиях окружающей среды приведет как к уменьшению энтропии (положительное ∆S), так и к увеличению полной энергии (положительное ∆H) системы и, следовательно, не происходит спонтанно. Для достижения кристаллизации таких белков условия модифицируются, чтобы сделать образование кристаллов энергетически выгодным. Это часто достигается путем создания пересыщенного раствора образца. [3]
Формирование кристаллов состоит из двух этапов: зарождения и роста. [3] Нуклеация — это начальный этап кристаллизации. [3] На этапе нуклеации молекулы белка в растворе объединяются в агрегаты, образуя стабильное твердое ядро. [3] По мере формирования ядра кристалл становится все больше и больше за счет молекул, прикрепляющихся к этому стабильному ядру. [3] Этап зародышеобразования имеет решающее значение для образования кристаллов, поскольку это фазовый переход первого рода образцов, переходящих от высокой степени свободы к получению упорядоченного состояния (водного состояния в твердое). [3] Для успешного этапа нуклеации необходимо манипулирование параметрами кристаллизации. Подход к кристаллизации белка заключается в обеспечении более низкой растворимости целевого белка в растворе. [3] Как только предел растворимости превышен и присутствуют кристаллы, кристаллизация завершается. [3]
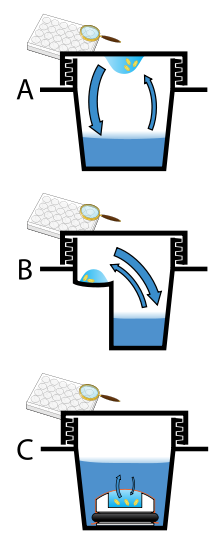
Диффузия паров является наиболее часто используемым методом кристаллизации белков. В этом методе каплям, содержащим очищенный белок, буфер и осадитель, позволяют прийти в равновесие с резервуаром большего размера, содержащим аналогичные буферы и осадители в более высоких концентрациях. Первоначально капля белкового раствора содержит сравнительно низкие концентрации осадителя и белка, но по мере уравновешивания капли и резервуара концентрации осадителя и белка в капле увеличиваются. Если для данного белка используются соответствующие растворы для кристаллизации, рост кристаллов происходит в капле. [11] [12] Этот метод используется потому, что он позволяет плавно и постепенно изменять концентрацию белка и концентрацию осадителя, что способствует росту крупных и хорошо упорядоченных кристаллов.
Диффузия пара может осуществляться как в виде висячей капли, так и в форме сидячей капли. В аппарате с висячими каплями каплю белкового раствора помещают на перевернутое покровное стекло, которое затем подвешивают над резервуаром. В аппарате для кристаллизации сидячей капли каплю помещают на подставку, отделенную от резервуара. Оба эти метода требуют герметизации окружающей среды, чтобы могло произойти равновесие между каплей и резервуаром. [11] [13]
Микропартия обычно предполагает погружение очень небольшого объема капель белка в масло (всего 1 мкл). Причина, по которой требуется масло, заключается в том, что используется такой малый объем белкового раствора, и поэтому для проведения эксперимента в водной среде необходимо препятствовать испарению. Хотя можно использовать различные масла, двумя наиболее распространенными герметиками являются парафиновые масла (описанные Чайеном и др.) и силиконовые масла (описанные Д'Арси). Существуют также другие методы микродозирования, в которых не используется жидкий герметик, а вместо этого требуется, чтобы ученый быстро поместил пленку или ленту на планшет с прорезями после помещения капли в лунку.
Помимо очень ограниченного количества необходимых образцов, этот метод также имеет еще одно преимущество: образцы защищены от загрязнения, передающегося по воздуху, поскольку они никогда не подвергаются воздействию воздуха во время эксперимента.
В микродиализе используется полупроницаемая мембрана, через которую могут проходить небольшие молекулы и ионы, в то время как белки и крупные полимеры не могут пересекаться. Устанавливая градиент концентрации растворенных веществ на мембране и позволяя системе приближаться к равновесию, система может медленно двигаться к перенасыщению, после чего могут образовываться кристаллы белка.
Микродиализ может производить кристаллы путем высаливания с использованием высоких концентраций соли или других небольших проницаемых через мембрану соединений, которые снижают растворимость белка. В очень редких случаях некоторые белки можно кристаллизовать путем диализного высаливания, диализа против чистой воды, удаления растворенных веществ, стимулирования самоассоциации и кристаллизации.
Этот метод объединяет растворы белка и осадков, не смешивая их предварительно, а вместо этого впрыскивая их через обе стороны канала, обеспечивая равновесие посредством диффузии. Два раствора вступают в контакт в камере для реагентов, оба при максимальных концентрациях, инициируя спонтанное зародышеобразование. По мере того как система приходит в равновесие, уровень пересыщения снижается, что способствует росту кристаллов. [14]
Основной движущей силой кристаллизации белка является оптимизация количества связей, которые можно образовать с другим белком посредством межмолекулярных взаимодействий. [3] Эти взаимодействия зависят от электронной плотности молекул и боковых цепей белка, которые изменяются в зависимости от pH. [10] Третичная и четвертичная структура белков определяются межмолекулярными взаимодействиями между боковыми группами аминокислот, в которых гидрофильные группы обычно обращены наружу, к раствору, образуя гидратную оболочку растворителя (воды). [10] По мере изменения pH заряд этих полярных боковых групп также меняется в зависимости от pH раствора и pKa белка. Следовательно, выбор pH важен либо для того, чтобы способствовать образованию кристаллов, в которых связь между молекулами друг с другом более благоприятна, чем с молекулами воды. [10] pH – одна из самых мощных манипуляций, которую можно назначить для достижения оптимальных условий кристаллизации.
Температура — еще один интересный параметр для обсуждения, поскольку растворимость белка является функцией температуры. [15] При кристаллизации белка манипуляция температурой для получения успешных кристаллов является одной из распространенных стратегий. В отличие от pH, температура различных компонентов кристаллографических экспериментов может влиять на конечные результаты, например, температура приготовления буфера, [16] температура фактического эксперимента по кристаллизации и т. д.
Химические добавки — это небольшие химические соединения, которые добавляются в процесс кристаллизации для увеличения выхода кристаллов. [17] Роль малых молекул в кристаллизации белка вначале не была хорошо продумана, поскольку в большинстве случаев их считали загрязнителями. [17] Меньшие молекулы кристаллизуются лучше, чем макромолекулы, такие как белки, поэтому до исследования Макферсона использование химических добавок было ограничено. Однако это важный аспект экспериментальных параметров кристаллизации, который важен для дальнейшего исследования и применения биохимиками и кристаллографами. [17]
Существуют высокопроизводительные методы, которые помогают оптимизировать большое количество экспериментов, необходимых для изучения различных условий, необходимых для успешного роста кристаллов. Для заказа доступно множество коммерческих наборов, в которых предварительно собранные ингредиенты применяются в системах, гарантированно обеспечивающих успешную кристаллизацию. Используя такой набор, ученый избавляется от хлопот по очистке белка и определению подходящих условий кристаллизации.
Роботы, работающие с жидкостью, могут использоваться для одновременной постановки и автоматизации большого количества экспериментов по кристаллизации. То, что в противном случае было бы медленным и потенциально подверженным ошибкам процессом, выполняемым человеком, может быть выполнено эффективно и точно с помощью автоматизированной системы. В роботизированных системах кристаллизации используются те же компоненты, что описаны выше, но каждый этап процедуры выполняется быстро и с большим количеством повторов. В каждом эксперименте используются крошечные количества раствора, и преимущество меньшего размера двойное: меньшие размеры выборки не только сокращают расход очищенного белка, но и меньшие количества раствора приводят к более быстрой кристаллизации. Каждый эксперимент контролируется камерой, которая обнаруживает рост кристаллов. [12]
Белки можно спроектировать так, чтобы повысить вероятность успешной кристаллизации белков, используя такие методы, как уменьшение поверхностной энтропии [19] или инженерию в кристаллических контактах. [20] Часто проблемные остатки цистеина можно заменить аланином, чтобы избежать дисульфид -опосредованной агрегации, а такие остатки, как лизин, глутамат и глутамин, можно заменить на аланин, чтобы уменьшить внутреннюю гибкость белка, что может препятствовать кристаллизации.
Макромолекулярные структуры можно определить из кристаллов белка с помощью различных методов, включая дифракцию рентгеновских лучей / рентгеновскую кристаллографию , криогенную электронную микроскопию (CryoEM) (включая электронную кристаллографию и дифракцию микрокристаллических электронов (MicroED) ), малоугловую рентгеновскую рентгенографию. рассеяние и дифракция нейтронов . См. также Структурную биологию .
Кристаллизация белков также может быть полезна при приготовлении белков для фармацевтических целей. [21]