Миастения гравис ( МГ ) — это хроническое заболевание нервно-мышечных соединений , которое приводит к различной степени слабости скелетных мышц . [1] Чаще всего поражаются мышцы глаз , лица и глотания. [1] [5] Это может привести к двоению в глазах , опущению век и трудностям при разговоре и ходьбе. [1] Начало может быть внезапным. [1] У больных часто наблюдается большой тимус или развивается тимома . [1]
Миастения гравис — аутоиммунное заболевание нервно-мышечного соединения, возникающее в результате действия антител , которые блокируют или разрушают никотиновые рецепторы ацетилхолина (АХР) в месте соединения нерва и мышцы . [6] [7] [1] Это препятствует тому, чтобы нервные импульсы вызывали мышечные сокращения. [1] Большинство случаев связано с антителами иммуноглобулина G1 (IgG1) и IgG3, которые атакуют AChR в постсинаптической мембране, вызывая опосредованное комплементом повреждение и мышечную слабость. [8] В редких случаях наследственный генетический дефект нервно -мышечного соединения приводит к аналогичному состоянию, известному как врожденная миастения . [9] [10] У детей, чьи матери страдают миастенией, в течение первых нескольких месяцев жизни могут наблюдаться симптомы, известные как неонатальная миастения. [1] Диагноз может быть подтвержден анализами крови на специфические антитела, тестом с эдрофонием или исследованием нервной проводимости . [1]
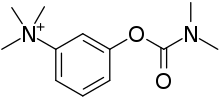
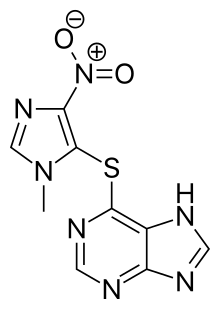
МГ обычно лечат препаратами, известными как ингибиторы ацетилхолинэстеразы , такими как неостигмин и пиридостигмин . [1] Также можно использовать иммунодепрессанты , такие как преднизолон или азатиоприн . [1] В некоторых случаях хирургическое удаление тимуса может улучшить симптомы . [1] Плазмаферез и высокие дозы внутривенного иммуноглобулина могут использоваться во время внезапных обострений заболевания. [1] Если дыхательные мышцы значительно ослабевают, может потребоваться искусственная вентиляция легких . [1] После интубации прием ингибиторов ацетилхолинэстеразы может быть временно приостановлен для уменьшения секреции в дыхательных путях. [11]
МГ поражает от 50 до 200 человек на миллион. [3] [4] Ежегодно его впервые диагностируют у 3–30 человек на миллион. [12] Диагноз стал более распространенным из-за повышения осведомленности. [12] МГ чаще всего встречается у женщин в возрасте до 40 лет и у мужчин старше 60 лет. [1] [5] [13] У детей это заболевание встречается редко. [1] При лечении большинство из них живут до средней продолжительности жизни . [1] Это слово происходит от греческого mys — «мышца», astheneia — «слабость» и латинского gravis — «серьёзный». [14]
Начальным, основным симптомом МГ является безболезненная слабость определенных мышц, а не утомляемость. [15] Мышечная слабость прогрессивно усиливается в периоды физической активности и уменьшается после периодов отдыха. Обычно слабость и утомляемость усиливаются к концу дня. [16] МГ обычно начинается со слабости глаз; затем оно может перейти в более тяжелую генерализованную форму, характеризующуюся слабостью конечностей или мышц, управляющих основными жизненными функциями. [17]
Примерно у двух третей людей начальный симптом МГ связан с мышцами вокруг глаз. [15] Опущение век ( птоз может возникнуть из-за слабости мышцы, поднимающей верхнее веко ) [18] и двоение в глазах ( диплопия , [15] из-за слабости экстраокулярных мышц ). [16] Глазные симптомы обычно ухудшаются при просмотре телевизора, чтении или вождении автомобиля, особенно при ярком освещении. [15] Следовательно, некоторые пострадавшие люди предпочитают носить солнцезащитные очки. [15] Термин «глазная миастения» описывает подтип МГ, при котором мышечная слабость ограничивается глазами, т.е. экстраокулярными мышцами, m. levator palpebrae Superioris и m. Круговая мышца глаза . [18] Обычно этот подтип развивается в генерализованную МГ, обычно через несколько лет. [18]
Слабость мышц, участвующих в глотании, может привести к затруднению глотания ( дисфагии ). Как правило, это означает, что часть пищи может остаться во рту после попытки глотания [19] или пища и жидкости могут срыгивать в нос, а не в глотку ( небно-глоточная недостаточность ). [16] Слабость мышц, которые двигают челюсть ( жевательные мышцы ), может вызвать затруднения при жевании. У людей с МГ жевание становится более утомительным при пережевывании жесткой, волокнистой пищи. [15] Трудности с глотанием, жеванием и речью являются первым симптомом примерно у одной шестой части людей. [15]
Слабость мышц, участвующих в разговоре, может привести к дизартрии и гипофонии . [15] Речь может быть медленной и невнятной, [20] или иметь гнусавый характер . [16] В некоторых случаях от певческого хобби или профессии приходится отказаться. [19]
Из-за слабости мимики и жевательных мышц мимическая слабость может проявляться в виде неспособности держать рот закрытым [15] («признак отвисшей челюсти») и рычащего выражения лица при попытке улыбнуться. [16] При опущенных веках и слабости лица человек может выглядеть сонным или грустным. [15] Могут возникнуть трудности с удержанием головы в вертикальном положении. [20]
Также могут поражаться мышцы, контролирующие дыхание и движения конечностей ; они редко проявляются как первые симптомы МГ, но развиваются в течение месяцев или лет. [21] При миастеническом кризе возникает паралич дыхательных мышц, что требует искусственной вентиляции легких для поддержания жизни. [22] Кризы могут быть вызваны различными биологическими стрессорами, такими как инфекция, лихорадка, побочная реакция на лекарства или эмоциональный стресс. [22]
МГ — аутоиммунная синаптопатия . Заболевание возникает, когда иммунная система дает сбой и вырабатывает антитела, атакующие ткани организма. Антитела в MG атакуют нормальный человеческий белок, никотиновый рецептор ацетилхолина или родственный ему белок под названием MuSK , специфическую для мышц киназу. [23] [24] Другие, менее частые антитела обнаруживаются против белков LRP4 , агрина и тайтина . [8] [25]
Гаплотипы лейкоцитарного антигена человека связаны с повышенной восприимчивостью к миастении и другим аутоиммунным заболеваниям. У родственников людей с миастенией наблюдается более высокий процент других иммунных нарушений. [26] [27]
Клетки вилочковой железы являются частью иммунной системы организма. У пациентов с миастенией вилочковая железа имеет большие размеры и имеет аномальную форму. Иногда он содержит скопления иммунных клеток, что указывает на лимфоидную гиперплазию, а вилочковая железа может давать неверные инструкции иммунным клеткам. [28]
Известно, что у беременных женщин, уже имеющих МГ, в трети случаев наблюдается обострение симптомов, и в этих случаях это обычно происходит в первом триместре беременности. [29] Признаки и симптомы у беременных имеют тенденцию к улучшению во втором и третьем триместрах . У некоторых матерей может наблюдаться полная ремиссия . [30] Иммуносупрессивную терапию следует продолжать на протяжении всей беременности, поскольку это снижает вероятность мышечной слабости новорожденных и контролирует миастению у матери. [31]
Около 10–20% младенцев, матери которых страдают этим заболеванием, рождаются с преходящей неонатальной миастенией (ТНМ), которая обычно вызывает трудности с кормлением и дыханием , которые развиваются примерно от 12 часов до нескольких дней после рождения. [29] [31] Ребенок с TNM обычно очень хорошо реагирует на ингибиторы ацетилхолинэстеразы, и состояние обычно проходит в течение трех недель по мере уменьшения количества антител и обычно не приводит к каким-либо осложнениям. [29] Очень редко ребенок может родиться с множественным врожденным артрогрипозом , возникающим вследствие глубокой внутриутробной слабости. Это связано с материнскими антителами , которые нацелены на рецепторы ацетилхолина ребенка. В некоторых случаях мать остается бессимптомной . [31]
МГ может быть трудно диагностировать, поскольку симптомы могут быть едва заметными и их трудно отличить как от нормальных вариантов, так и от других неврологических расстройств. [19]
У детей можно выделить три типа миастенических симптомов: [32]
Врожденные миастении вызывают мышечную слабость и утомляемость, сходные с таковыми при МГ. [33] Признаки врожденной миастении обычно присутствуют в первые годы детства, хотя их можно не распознать до взрослой жизни. [34]
При диагнозе МГ у человека оценивают его неврологический статус и устанавливают уровень заболевания. Обычно это делается с использованием принятой шкалы клинической классификации Американского фонда миастении Гравис. [ нужна цитата ]
Во время медицинского осмотра на наличие МГ врач может попросить человека выполнить повторяющиеся движения. Например, врач может попросить человека смотреть в фиксированную точку в течение 30 секунд и расслабить мышцы лба, поскольку человек с МГ и птозом глаз может непроизвольно задействовать мышцы лба для компенсации слабости глаз. веки. [19] Клинический эксперт также может попытаться вызвать у человека «признак занавеса», удерживая один глаз человека открытым, что в случае МГ приведет к закрытию другого глаза. [19]
При подозрении на диагноз можно провести серологическое исследование :


Мышечные волокна людей с МГ легко утомляются, что может помочь диагностировать повторяющийся тест на стимуляцию нервов . При одноволоконной электромиографии , которая считается наиболее чувствительным (хотя и не самым специфичным) тестом на МГ, [19] тонкий игольчатый электрод вводится в разные области конкретной мышцы для регистрации потенциалов действия из нескольких проб. различные отдельные мышечные волокна. Идентифицируются два мышечных волокна, принадлежащие к одной и той же двигательной единице, и измеряется временная изменчивость их паттернов активности. Частота и доля определенных аномальных паттернов потенциала действия, называемых «дрожанием» и «блокировкой», являются диагностическими. Джиттер – это аномальное изменение временного интервала между потенциалами действия соседних мышечных волокон в одной и той же двигательной единице. Блокировка означает неспособность нервных импульсов вызвать потенциалы действия в соседних мышечных волокнах одной и той же двигательной единицы. [38]
Сообщается, что приложение льда к мышцам на 2–5 минут имеет чувствительность и специфичность 76,9% и 98,3% соответственно для идентификации МГ. Считается, что ацетилхолинэстераза ингибируется при более низкой температуре, что является основой для этого диагностического теста. Обычно это делается на веках при наличии птоза и считается положительным, если после удаления льда происходит подъем века на ≥2 мм. [39]
Этот тест требует внутривенного введения хлорида эдрофония или неостигмина — препаратов, которые блокируют расщепление ацетилхолина холинэстеразой ( ингибиторы ацетилхолинэстеразы). [40] Этот тест обычно больше не проводится, так как его использование может привести к опасной для жизни брадикардии (замедлению сердечного ритма), которая требует немедленной неотложной помощи. [41] Производство эдрофония было прекращено в 2008 году. [22]
Рентгенография грудной клетки может выявить расширение средостения, указывающее на тимому, но компьютерная томография или магнитно-резонансная томография (МРТ) являются более чувствительными способами выявления тимом и обычно проводятся по этой причине. [42] МРТ черепа и орбит также может быть выполнена для исключения компрессионных и воспалительных поражений черепных нервов и глазных мышц. [43]
Форсированную жизненную емкость можно контролировать через определенные промежутки времени, чтобы обнаружить нарастающую мышечную слабость. В остром периоде для определения адекватности вентиляции можно использовать отрицательную силу вдоха ; его проводят людям с MG. [44] [45]
Мышечная слабость, которая усиливается при физической активности (аномальная мышечная утомляемость ) при миастении [46], является симптомом, характерным для других нервно-мышечных заболеваний. Большинство метаболических миопатий , таких как болезнь МакАрдла (GSD-V), характеризуются аномальной мышечной утомляемостью, а не фиксированной мышечной слабостью. [47] [48] Кроме того, как и при миастении, [46] непереносимость физических упражнений при болезни МакАрдла улучшается при регулярной физической активности (выполняемой безопасно с использованием адаптаций к активности, таких как открытие второго дыхания , «правило 30 из 80» и «правило шести секунд»). правило»). [49] [50] У небольшого меньшинства пациентов с болезнью МакАрдла также имеется сопутствующее заболевание — птоз (опущение верхнего века). [51] GSD-II с поздним началом ( болезнь Помпе ) и GSD-XV также имеют мышечную слабость или утомляемость с сопутствующими заболеваниями в виде птоза и офтальмоплегии; как и многие митохондриальные миопатии . [52]
Другие заболевания, сопровождающиеся аномальной мышечной усталостью (которую можно охарактеризовать как мышечную слабость, вызванную физической нагрузкой, обратимую мышечную слабость или мышечную слабость, которая проходит после отдыха), включают: эндокринные миопатии (например, синдром Хоффмана ), тубулярную агрегатную миопатию (ТАМ), ишемию. (такие как перемежающаяся хромота , синдром ущемления подколенной артерии и хроническая венозная недостаточность ), а также неправильное питание или заболевания мальабсорбции, которые приводят к дефициту витамина D (остеомальная миопатия). Хотя поясно- конечностные мышечные дистрофии (LGMD) сопровождаются фиксированной мышечной слабостью, LGMDR8 также предполагает мышечную утомляемость; [53] , а также некоторые мышечные дистрофии-дистрогликанопатии конечностей, такие как MDDGC3 (ранее известные как LGMDR15 и LGMD2O). [52] [54] Миофибриллярная миопатия 10, [55] дефицит диметилглициндегидрогеназы, [56] дефект переносчика лактата эритроцитов, [57] и миопатия с миалгией, повышением уровня креатинкиназы в сыворотке, с эпизодическим рабдомиолизом (MMCKR) или без него [58] также включают мышечную усталость.
Х-сцепленная эпизодическая мышечная слабость (ЭМСС) включает общую мышечную слабость, птоз и колебания силы. У некоторых людей была заметна утомляемость, фенотип имел черты, сравнимые с врожденными миастеническими синдромами и каналопатиями . [59]
Признаки и симптомы миастении, проявляющиеся с младенчества или детства, могут быть одним из врожденных миастенических синдромов , которые могут наследоваться как по аутосомно-доминантному, так и по рецессивному типу. В настоящее время известно более двух десятков типов врожденных миастенических синдромов. [60]
Лечение заключается в приеме лекарств и/или хирургическом вмешательстве. Лекарства состоят в основном из ингибиторов ацетилхолинэстеразы для непосредственного улучшения мышечной функции и иммунодепрессантов для уменьшения аутоиммунного процесса. [5] [61] Тимэктомия — хирургический метод лечения МГ. [62]
Ухудшение может произойти при приеме таких лекарств, как фторхинолоны , аминогликозиды и магний. [63] Около 10% людей с генерализованной МГ считаются невосприимчивыми к лечению . [64] Аутологичная трансплантация гемопоэтических стволовых клеток (ТГСК) иногда используется при тяжелой, резистентной к лечению МГ. Имеющиеся данные предоставляют предварительные доказательства того, что ТГСК может быть эффективным терапевтическим вариантом в тщательно отобранных случаях. [65]
Эфгартигимод альфа (Вивгарт) был одобрен для медицинского применения в США в декабре 2021 года. [66] [67] [68]
Эфгартигимод альфа/гиалуронидаза (Vyvgart Hytrulo) был одобрен для медицинского применения в США в июне 2023 года. [69] [70]
Розаноликизумаб (Ристигго) был одобрен для медицинского применения в США в июне 2023 года. [71] [72]
Ингибиторы ацетилхолинэстеразы могут принести симптоматическую пользу, но не могут полностью устранить слабость человека от MG. [73] Хотя они не могут полностью устранить все симптомы МГ, они все же могут позволить человеку выполнять нормальную повседневную деятельность. [73] Обычно ингибиторы ацетилхолинэстеразы начинают с низкой дозы и увеличивают ее до тех пор, пока не будет достигнут желаемый результат. Если принять за 30 минут до еды, симптомы будут слабыми во время еды, что полезно для тех, у кого проблемы с глотанием из-за болезни. Другой препарат, используемый при МГ, атропин , может уменьшить мускариновые побочные эффекты ингибиторов ацетилхолинэстеразы. [74] Пиридостигмин является препаратом относительно длительного действия (по сравнению с другими холинергическими агонистами), с периодом полувыведения около четырех часов и относительно небольшим количеством побочных эффектов. [75] Как правило, его прекращают у тех, кто находится на искусственной вентиляции легких, поскольку известно, что он увеличивает количество слюнных выделений. [75] В нескольких высококачественных исследованиях ингибиторы холинэстеразы напрямую сравнивались с другими методами лечения (или плацебо); их практическая польза может быть настолько значительной, что проведение исследований, в которых они были бы скрыты от некоторых людей, было бы затруднительно. [61]
Для достижения лучшего результата также можно использовать стероид преднизолон , но он может привести к ухудшению симптомов, и для достижения максимальной эффективности требуются недели. [75] Исследования показывают, что до 15% пациентов не реагируют положительно на иммуносупрессанты. [76] [77] [5] Из-за множества симптомов, которые может вызвать стероидное лечение, это не предпочтительный метод лечения. [75] Также можно использовать другие иммуносупрессивные препараты, включая ритуксимаб [78] или азатиоприн . [1]
Если миастения серьезная (миастенический криз), можно использовать плазмаферез для удаления предполагаемых антител из кровообращения. Кроме того, для связывания циркулирующих антител можно использовать внутривенные иммуноглобулины (ВВИГ). Оба этих метода лечения имеют относительно кратковременный эффект, обычно измеряемый неделями, и часто связаны с высокими затратами, что делает их непомерно высокими; они обычно предназначены для случаев, когда MG требует госпитализации. [75] [79]
Поскольку тимомы наблюдаются у 10% всех людей с МГ, им часто делают рентгенографию грудной клетки и компьютерную томографию, чтобы оценить необходимость хирургического удаления вилочковой железы и любой раковой ткани, которая может присутствовать. [22] [41] Даже если операция по удалению тимомы проводится, она обычно не приводит к ремиссии МГ. [75] Хирургическое вмешательство в случае МГ включает удаление тимуса, хотя в 2013 году не было выявлено явных преимуществ, за исключением наличия тимомы. [80] Однако рандомизированное контролируемое исследование 2016 года выявило некоторые преимущества. [81]
Людей с МГ следует информировать о меняющемся характере их симптомов, включая слабость и утомляемость, вызванную физической нагрузкой. Участие в упражнениях следует поощрять частым отдыхом. [17] Некоторые данные указывают на то, что у людей с генерализованной МГ частичная домашняя программа, включающая обучение диафрагмальному дыханию , дыханию через поджатые губы и интервальную мышечную терапию, может улучшить силу дыхательных мышц, подвижность грудной клетки, характер дыхания и дыхательную выносливость. [82]
У людей с миастенией более старые формы йодсодержащего контраста , используемые для медицинской визуализации, вызывали повышенный риск обострения заболевания, но современные формы не имеют немедленного повышения риска. [83]
Прогноз для людей с МГ, как правило, хороший, как и качество жизни при очень хорошем лечении. [84] Мониторинг человека с МГ очень важен, поскольку по крайней мере у 20% людей с диагнозом МГ в течение двух лет после постановки диагноза возникает миастенический криз, требующий быстрого медицинского вмешательства. [75] Как правило, наиболее инвалидизирующий период МГ может длиться годы после первоначального диагноза. [73] Для облегчения передвижения могут потребоваться вспомогательные устройства. [1] В начале 1900-х годов 70% выявленных случаев умирали от проблем с легкими; теперь это число оценивается примерно в 3–5%, и это улучшение связано с повышением осведомленности и приемом лекарств для лечения симптомов. [75]
МГ встречается во всех этнических группах и обоих полах. Чаще всего от него страдают женщины до 40 лет и люди от 50 до 70 лет любого пола, но известно, что оно возникает в любом возрасте. У молодых людей тимома встречается редко. Распространенность в Соединенных Штатах оценивается от 0,5 до 20,4 случаев на 100 000, при этом, по оценкам, пострадало 60 000 американцев. [22] [85] В Соединенном Королевстве, по оценкам, 15 случаев МГ встречаются на 100 000 человек. [41]
Первыми о MG написали Томас Уиллис , Сэмюэл Уилкс , Эрб и Голдфлам. [18] Термин «псевдопаралитическая миастения гравис» был предложен в 1895 году немецким врачом Жолли. [18] Мэри Уокер лечила человека с МГ физостигмином в 1934 году. [18] Симпсон и Настук подробно описали аутоиммунную природу заболевания. [18] В 1973 году Патрик и Линдстром на кроликах показали, что иммунизация очищенными мышечными рецепторами ацетилхолина вызывает развитие MG-подобных симптомов. [18]
В настоящее время исследуются иммуномодулирующие вещества, такие как препараты, которые предотвращают модуляцию рецептора ацетилхолина иммунной системой. [86] Недавно были проведены некоторые исследования ингибиторов анти-c5 для изучения лечения, поскольку они безопасны и используются при лечении других заболеваний. [13] Эфедрин, похоже, приносит некоторым людям больше пользы, чем другие лекарства, но по состоянию на 2014 год он не был должным образом изучен. [10] [87] В лаборатории МГ в основном изучается на модельных организмах, таких как грызуны. Кроме того, в 2015 году ученые разработали in vitro функциональный анализ нервно-мышечных соединений in vitro на основе эмбриональных стволовых клеток человека и стволовых клеток сомато-мышечных клеток. После добавления патогенных антител против рецептора ацетилхолина и активации системы комплемента нервно-мышечная совместная культура проявляет такие симптомы, как ослабление мышечных сокращений. [88]