
Иммуносупрессивные препараты , также известные как иммунодепрессанты , иммунодепрессанты и препараты против отторжения , представляют собой препараты , которые ингибируют или предотвращают активность иммунной системы .
Иммунодепрессанты можно разделить на пять групп :
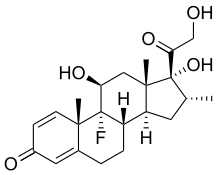
В фармакологических (супрафизиологических) дозах глюкокортикоиды, такие как преднизолон , дексаметазон и гидрокортизон , используются для подавления различных аллергических , воспалительных и аутоиммунных нарушений. Их также применяют в качестве посттрансплантарных иммунодепрессантов для предотвращения острого отторжения трансплантата и реакции «трансплантат против хозяина» . Тем не менее, они не предотвращают инфекцию, а также тормозят последующие репаративные процессы.
Глюкокортикоиды подавляют клеточный иммунитет . Они действуют путем ингибирования экспрессии генов цитокинов, включая интерлейкин 1 (IL-1), IL-2 , IL-3 , IL-4 , IL-5 , IL-6 , IL-8 и TNF-альфа, связываясь с кортикостероидной реакцией . элементы ДНК. [1] Это снижение выработки цитокинов снижает пролиферацию Т-клеток . При снижении пролиферации Т-клеток снижается выработка IL-2. Это еще больше снижает пролиферацию Т-клеток. [2] [3]
Глюкокортикоиды также подавляют гуморальный иммунитет , заставляя В-клетки экспрессировать меньшее количество рецепторов IL-2 и IL-2 . Это уменьшает как экспансию клонов В-клеток, так и синтез антител .
Глюкокортикоиды влияют на все типы воспалительных явлений, независимо от их причины. Они индуцируют синтез липокортина-1 (аннексина-1), который затем связывается с клеточными мембранами , предотвращая контакт фосфолипазы А2 с ее субстратом арахидоновой кислотой . Это приводит к уменьшению выработки эйкозаноидов . Экспрессия циклооксигеназы (как ЦОГ-1 , так и ЦОГ-2) также подавляется, что усиливает эффект.
Глюкокортикоиды также стимулируют выход липокортина-1 во внеклеточное пространство, где он связывается с рецепторами мембран лейкоцитов и ингибирует различные воспалительные процессы: эпителиальную адгезию , эмиграцию , хемотаксис , фагоцитоз , дыхательный взрыв и высвобождение различных медиаторов воспаления (лизосомальных ферментов, цитокины, тканевой активатор плазминогена , хемокины и др.) из нейтрофилов , макрофагов и мастоцитов .
Цитостатики подавляют деление клеток . В иммунотерапии их применяют в меньших дозах, чем при лечении злокачественных заболеваний. Они влияют на пролиферацию как Т-клеток, так и В-клеток. Из-за своей высочайшей эффективности наиболее часто назначают аналоги пурина .
Алкилирующими средствами , применяемыми в иммунотерапии, являются азотистые иприты ( циклофосфамид ), нитрозомочевины , соединения платины и другие. Циклофосфамид (цитоксан Бакстера), вероятно, является наиболее мощным иммунодепрессантом. В малых дозах весьма эффективен при терапии системной красной волчанки , аутоиммунных гемолитических анемий , гранулематоза с полиангиитом и других иммунных заболеваний. Высокие дозы вызывают панцитопению и геморрагический цистит .
Антиметаболиты препятствуют синтезу нуклеиновых кислот. К ним относятся:
Метотрексат – аналог фолиевой кислоты . Он связывает дигидрофолатредуктазу и предотвращает синтез тетрагидрофолата . Он используется при лечении аутоиммунных заболеваний (например, ревматоидного артрита или болезни Бехчета) и при трансплантации.
Азатиоприн (Имуран Прометея) является основным иммунодепрессивным цитотоксическим веществом. Он широко используется для контроля реакций отторжения трансплантата. Он неферментативно расщепляется до меркаптопурина , который действует как аналог пурина и ингибитор синтеза ДНК. Сам меркаптопурин также можно вводить напрямую.
Предотвращая клональную экспансию лимфоцитов в фазе индукции иммунного ответа, он влияет как на клеточный , так и на гуморальный иммунитет . Он также эффективен при лечении аутоиммунных заболеваний.
Среди них дактиномицин является наиболее важным. Его используют при трансплантации почек . Другими цитотоксическими антибиотиками являются антрациклины , митомицин С , блеомицин , митрамицин .
Антитела иногда используются в качестве быстрой и мощной иммуносупрессивной терапии для предотвращения острых реакций отторжения, а также для таргетного лечения лимфопролиферативных или аутоиммунных заболеваний (например, моноклональные анти- CD20 ).
Гетерологичные поликлональные антитела получают из сыворотки животных (например, кролика , лошади ) и вводят в тимоциты или лимфоциты пациента . Используются антилимфоцитарный ( АЛГ ) и антитимоцитарный антигены ( АТГ ). Они являются частью стероидорезистентной острой реакции отторжения и лечения тяжелой апластической анемии . Однако их добавляют в первую очередь к другим иммунодепрессантам, чтобы уменьшить их дозировку и токсичность. Они также позволяют перейти на терапию циклоспорином.
Поликлональные антитела ингибируют Т-лимфоциты и вызывают их лизис , который представляет собой как цитолиз, опосредованный комплементом , так и клеточную опсонизацию с последующим удалением ретикулоэндотелиальных клеток из кровообращения в селезенке и печени . Таким образом, поликлональные антитела ингибируют клеточно-опосредованные иммунные реакции, включая отторжение трансплантата, гиперчувствительность замедленного типа (т.е. туберкулиновую кожную реакцию) и реакцию «трансплантат против хозяина» (РТПХ), но влияют на продукцию тимус -зависимых антител.
По состоянию на март 2005 года на рынке доступны два препарата: Атгам , полученный из лошадиной сыворотки, и Тимоглобулин , полученный из кроличьей сыворотки. Поликлональные антитела поражают все лимфоциты и вызывают общую иммуносупрессию, что может привести к посттрансплантационным лимфопролиферативным расстройствам (ПТЛП) или серьезным инфекциям, особенно цитомегаловирусом . Чтобы снизить эти риски, лечение проводится в больнице, где обеспечена адекватная изоляция от инфекции. Обычно их вводят в течение пяти дней внутривенно в соответствующем количестве. Пациенты остаются в больнице до трех недель, чтобы дать иммунной системе время восстановиться до точки, когда больше нет риска сывороточной болезни .
Из-за высокой иммуногенности поликлональных антител практически у всех пациентов возникает острая реакция на лечение. Для него характерны лихорадка , приступы озноба и даже анафилаксия . В дальнейшем в ходе лечения у некоторых пациентов развивается сывороточная болезнь или иммунокомплексный гломерулонефрит. Сывороточная болезнь возникает через семь-четырнадцать дней после начала терапии. У пациента наблюдается лихорадка, боли в суставах и эритема , которые можно снять с помощью стероидов и анальгетиков . Также может присутствовать крапивница (крапивница). Уменьшить их токсичность можно путем использования высокоочищенных фракций сыворотки и внутривенного введения в сочетании с другими иммунодепрессантами, например ингибиторами кальциневрина, цитостатиками и кортикостероидами . Наиболее частой комбинацией является одновременное использование антител и циклоспорина, чтобы предотвратить постепенное развитие у пациентов сильного иммунного ответа на эти препараты, снижая или устраняя их эффективность.
Моноклональные антитела направлены на точно определенные антигены. Поэтому они вызывают меньше побочных эффектов. Особенно значимыми являются антитела, направленные на рецептор IL-2 (CD25-) и CD3. Их используют для предотвращения отторжения пересаженных органов, а также для отслеживания изменений в субпопуляциях лимфоцитов. Разумно ожидать появления подобных новых лекарств в будущем.
Муромонаб-CD3 представляет собой мышиное моноклональное антитело против CD3 типа IgG2a, которое ранее использовалось для предотвращения активации и пролиферации Т-клеток путем связывания рецепторного комплекса Т-клеток, присутствующего на всех дифференцированных Т-клетках. По существу, это было одно из первых сильнодействующих иммунодепрессивных веществ, которое применялось для контроля эпизодов острого отторжения, резистентных к стероидным и/или поликлональным антителам. Поскольку он действует более специфично, чем поликлональные антитела, его также использовали профилактически при трансплантации. Однако муромонаб-CD3 больше не производится [4] и это мышиное моноклональное антитело было заменено в клинике химерными, гуманизированными или человеческими моноклональными антителами.
Механизм действия муромонаба понятен лишь частично. Известно, что молекула связывает комплекс TCR/CD3-рецептор. При первых нескольких введениях это связывание неспецифически активирует Т-клетки, что приводит к серьезному синдрому через 30–60 минут. Для него характерны лихорадка, миалгия , головная боль и артралгия . Иногда развивается опасная для жизни реакция сердечно-сосудистой системы и центральной нервной системы, требующая длительной терапии. По истечении этого периода CD3 блокирует связывание TCR-антиген и вызывает конформационные изменения или удаление всего комплекса TCR3/CD3 с поверхности Т-клеток. Это снижает количество доступных Т-клеток, возможно, за счет повышения их чувствительности к поглощению эпителиальными ретикулярными клетками . Перекрестное связывание молекул CD3 также активирует внутриклеточный сигнал, вызывающий анергию или апоптоз Т-клеток, если только клетки не получают другой сигнал через костимулирующую молекулу . Антитела к CD3 смещают баланс с клеток Th1 на клетки Th2, поскольку CD3 стимулирует активацию Th1. [5]
У пациента могут вырабатываться нейтрализующие антитела, снижающие эффективность муромонаба-CD3. Муромонаб-CD3 может вызывать чрезмерную иммуносупрессию. Хотя антитела к CD3 действуют более специфично, чем поликлональные антитела, они значительно снижают клеточный иммунитет, предрасполагая пациента к оппортунистическим инфекциям и злокачественным новообразованиям. [6]
Интерлейкин-2 является важным регулятором иммунной системы, необходимым для экспансии клонов и выживания активированных лимфоцитов Т. Его эффекты опосредуются тримерным рецептором клеточной поверхности IL-2a , состоящим из α-, β- и γ-цепей. IL-2a (CD25, антиген активации Т-клеток, TAC) экспрессируется только уже активированными Т-лимфоцитами. Поэтому селективная иммуносупрессивная терапия имеет особое значение, и исследования были сосредоточены на разработке эффективных и безопасных антител против IL-2. С помощью технологии рекомбинантных генов мышиные антитела против Tac были модифицированы, что привело к представлению в 1998 году двух химерных мышиных/человеческих антител против Tac: базиликсимаба (Симулект) и даклизумаба (Зенапакс). Эти препараты действуют путем связывания α-цепи рецептора IL-2a, предотвращая индуцированную IL-2 клональную экспансию активированных лимфоцитов и сокращая их выживаемость. Они используются для профилактики острого отторжения органов после двусторонней трансплантации почек , оба они одинаково эффективны и имеют лишь небольшое количество побочных эффектов. [ нужна цитата ]
Как и такролимус , циклоспорин (Sandimmune компании Novartis) является ингибитором кальциневрина (CNI). Он используется с 1983 года и является одним из наиболее широко используемых иммунодепрессантов. Это циклический грибной пептид, состоящий из 11 аминокислот.
Считается, что циклоспорин связывается с цитозольным белком циклофилином ( иммунофилином ) иммунокомпетентных лимфоцитов, особенно Т-лимфоцитов . Этот комплекс циклоспорина и циклофилина ингибирует фосфатазу кальцинейрин , которая в норме индуцирует транскрипцию интерлейкина-2 . Препарат также ингибирует выработку лимфокинов и высвобождение интерлейкинов , что приводит к снижению функции эффекторных Т-клеток.
Циклоспорин используется для лечения острых реакций отторжения, но его все чаще заменяют более новыми и менее нефротоксичными [ 7] иммунодепрессантами.
Ингибиторы кальциневрина и азатиоприн связаны с возникновением посттрансплантационных злокачественных новообразований и рака кожи у реципиентов трансплантированных органов. Немеланомный рак кожи (НМРК) после трансплантации почки встречается часто и может приводить к значительной заболеваемости и смертности. Результаты ряда исследований позволяют предположить, что ингибиторы кальциневрина обладают онкогенными свойствами, главным образом связанными с выработкой цитокинов, способствующих росту опухоли, метастазированию и ангиогенезу.
Сообщалось, что этот препарат снижает частоту регуляторных Т-клеток (T-Reg), и после перехода от монотерапии CNI к монотерапии микофенолатом у пациентов наблюдалось увеличение успеха трансплантации и частоты T-Reg. [8]
Такролимус (торговые названия Програф, Астаграф XL, Энварсус XR) является продуктом бактерии Streptomyces tsukubensis . Это макролид-лактон , который действует путем ингибирования кальциневрина .
Препарат применяют преимущественно при трансплантации печени и почек, хотя в некоторых клиниках его применяют при трансплантации сердца, легких и сердце/легких. Он связывается с иммунофилином FKBP1A с последующим связыванием комплекса с кальциневрином и ингибированием его фосфатазной активности. Таким образом, он предотвращает переход клетки из фазы G0 в фазу G1 клеточного цикла . Такролимус более эффективен, чем циклоспорин, и имеет менее выраженные побочные эффекты.
Сиролимус (рапамицин, торговое название Рапамун) представляет собой макролид-лактон, продуцируемый актиномицетной бактерией Streptomyces hygroscopeus . Используется для предотвращения реакций отторжения. Хотя это структурный аналог такролимуса, он действует несколько иначе и имеет другие побочные эффекты.
В отличие от циклоспорина и такролимуса, препаратов, влияющих на первую фазу активации Т-лимфоцитов, сиролимус влияет на вторую фазу, а именно на передачу сигнала и клональную пролиферацию лимфоцитов. Он связывается с FKBP1A, как такролимус, однако комплекс ингибирует не кальциневрин, а другой белок, mTOR . Таким образом, сиролимус действует синергично с циклоспорином и в сочетании с другими иммунодепрессантами имеет мало побочных эффектов. Кроме того, он косвенно ингибирует некоторые киназы и фосфатазы, специфичные для Т-лимфоцитов, тем самым предотвращая их переход из фазы G1 в фазу S клеточного цикла. Аналогичным образом сиролимус предотвращает дифференцировку В-клеток в плазматические клетки, снижая выработку антител IgM, IgG и IgA.
Он также активен в отношении опухолей , PI3K/AKT/mTOR-зависимых.
Эверолимус является аналогом сиролимуса, а также ингибитором mTOR.
Зотаролимус — полусинтетическое производное сиролимуса, используемое в стентах с лекарственным покрытием .
ИФН-β подавляет продукцию цитокинов Th1 и активацию моноцитов. Его применяют для замедления прогрессирования рассеянного склероза . IFN-γ способен запускать апоптоз лимфоцитов .
Длительное употребление опиоидов может вызвать иммуносупрессию как врожденного, так и адаптивного иммунитета. [9] Снижение пролиферации, а также иммунной функции наблюдалось как в макрофагах, так и в лимфоцитах. Считается, что эти эффекты опосредуются опиоидными рецепторами, экспрессируемыми на поверхности этих иммунных клеток. [9]
Белок, связывающий TNF -α (фактор некроза опухоли-альфа), представляет собой моноклональное антитело или циркулирующий рецептор , такой как инфликсимаб (Remicade), этанерцепт (Enbrel) или адалимумаб (Humira), который связывается с TNF-α, предотвращая индуцирование им синтез IL-1 и IL-6 и адгезия молекул, активирующих лимфоциты. Их применяют при лечении ревматоидного артрита , болезни Бехтерева , болезни Крона и псориаза .
Эти препараты могут повысить риск заражения туберкулезом или активизации латентной инфекции. Инфликсимаб и адалимумаб имеют предупреждения на этикетках, в которых говорится, что пациентов следует обследовать на предмет латентной туберкулезной инфекции и начинать лечение до начала их терапии.
TNF или эффекты TNF также подавляются различными природными соединениями, включая куркумин (ингредиент куркумы ) и катехины (в зеленом чае ).
Микофеноловая кислота действует как неконкурентный, селективный и обратимый ингибитор инозин-5'-монофосфатдегидрогеназы (IMPDH), которая является ключевым ферментом в синтезе гуанозиновых нуклеотидов de novo . В отличие от других типов клеток человека, лимфоциты В и Т очень зависят от этого процесса. Микофенолата мофетил применяют в сочетании с циклоспорином или такролимусом у пациентов, перенесших трансплантацию.
Финголимод – синтетический иммунодепрессант. Он увеличивает экспрессию или изменяет функцию определенных молекул адгезии ( интегрин α4/β7 ) в лимфоцитах, поэтому они накапливаются в лимфатической ткани (лимфатических узлах), а их количество в кровообращении уменьшается. В этом отношении он отличается от всех других известных иммунодепрессантов.
Сообщалось, что мириоцин в 10–100 раз более эффективен, чем циклоспорин .
Иммуносупрессивные препараты используются в иммуносупрессивной терапии для:
Распространенным побочным эффектом многих иммунодепрессантов является иммунодефицит , поскольку большинство из них действуют неселективно, что приводит к повышению восприимчивости к инфекциям , снижению иммунонадзора за раком и снижению способности вырабатывать антитела после вакцинации . [10] [11] Тем не менее, перед началом любого лечения следует проверить вакцинационный статус пациентов, принимающих иммунодепрессанты от хронических заболеваний, таких как ревматоидный артрит или воспалительные заболевания кишечника , и в конечном итоге пациенты должны быть вакцинированы против болезней, предупреждаемых с помощью вакцин . [12] Некоторые исследования показали низкий уровень вакцинации против некоторых заболеваний, предупреждаемых с помощью вакцин, среди пациентов, принимающих иммунодепрессанты, несмотря на в целом положительное отношение к вакцинации. [13]
Существуют и другие побочные эффекты, такие как гипертония , дислипидемия , гипергликемия , язвенная болезнь , липодистрофия , лунообразное лицо , поражение печени и почек . Иммуносупрессивные препараты также взаимодействуют с другими лекарствами и влияют на их метаболизм и действие. Действующие или предполагаемые иммунодепрессанты можно оценить с точки зрения их воздействия на субпопуляции лимфоцитов в тканях с помощью иммуногистохимии . [14]