Реакция Стилле — это химическая реакция, широко используемая в органическом синтезе . Реакция включает в себя соединение двух органических групп, одна из которых переносится как оловоорганическое соединение (также известное как органостаннаны ). Различные органические электрофилы обеспечивают другого партнера по соединению . Реакция Стилле — одна из многих реакций соединения, катализируемых палладием . [1] [2] [3]
Группа R 1 , присоединенная к триалкилолово, обычно sp 2 -гибридизована, включая винильные и арильные группы.
Эти органостаннаны также устойчивы как к воздуху, так и к влаге, и многие из этих реагентов либо коммерчески доступны, либо могут быть синтезированы из литературных прецедентов. Однако эти оловянные реагенты, как правило, очень токсичны. X, как правило, представляет собой галогенид , такой как Cl , Br или I , однако псевдогалогениды, такие как трифлаты , сульфонаты и фосфаты , также могут быть использованы. [4] [5] Было опубликовано несколько обзоров. [6] [2] [7] [8] [9] [10] [11] [12] [13] [14] [15] [ чрезмерное цитирование ]
Первый пример катализируемого палладием связывания арилгалогенидов с оловоорганическими реагентами был описан Колином Иборном в 1976 году. [16] Эта реакция дала от 7% до 53% диарильного продукта. Этот процесс был расширен до связывания ацилхлоридов с алкилоловоорганическими реагентами в 1977 году Тошихико Мигитой, что дало от 53% до 87% кетонного продукта. [17]

В 1977 году Мигита опубликовал дальнейшую работу по связыванию реагентов аллил -олова как с арил ( C ), так и с ацил ( D ) галогенидами. Большая способность аллильных групп мигрировать к палладиевому катализатору позволила проводить реакции при более низких температурах. Выходы для арилгалогенидов составляли от 4% до 100%, а для ацилгалогенидов — от 27% до 86%. [18] [19] Отражая ранние вклады Мигиты и Косуги, реакцию Стилле иногда называют сочетанием Мигиты–Косуги–Стилле .

Джон Кеннет Стилл впоследствии сообщил в 1978 году о связывании различных реагентов алкилолова с многочисленными арил- и ацилгалогенидами в мягких условиях реакции с гораздо лучшими выходами (76%–99%). [18] [20] Стилл продолжил свою работу в 1980-х годах по синтезу множества кетонов с использованием этого широкого и мягкого процесса и выяснил механизм этого превращения. [21] [22]

К середине 1980-х годов было опубликовано более 65 статей по теме реакций сочетания с участием олова, продолжая изучать субстратный охват этой реакции. В то время как первоначальные исследования в этой области были сосредоточены на сочетании алкильных групп, большинство последующих работ включали гораздо более синтетически полезное сочетание винильных , алкенильных , арильных и аллильных органостаннанов с галогенидами. Благодаря стабильности этих оловоорганических реагентов на воздухе и простоте их синтеза, реакция Стилла стала распространенной в органическом синтезе. [8]
Механизм реакции Стилле был тщательно изучен. [11] [23] Каталитический цикл включает окислительное присоединение галогенида или псевдогалогенида ( 2 ) к палладиевому катализатору ( 1 ) , трансметаллирование 3 с оловоорганическим реагентом ( 4 ) и восстановительное устранение 5 с получением связанного продукта ( 7 ) и регенерированного палладиевого катализатора ( 1 ). [24]

Однако детальный механизм связывания Стилле чрезвычайно сложен и может происходить через многочисленные пути реакции. Как и в других реакциях связывания, катализируемых палладием , активным палладиевым катализатором считается 14-электронный комплекс Pd(0), который может быть получен различными способами. При использовании 18- или 16-электронного источника Pd(0) Pd(PPh 3 ) 4 , Pd(dba) 2 может подвергаться диссоциации лиганда с образованием активных видов. Во-вторых, фосфины могут быть добавлены к безлигандному палладию(0). Наконец, как показано на рисунке, восстановление источника Pd(II) ( 8) (Pd(OAc)2, PdCl2(MeCN)2 , PdCl2 ( PPh3 ) 2 , BnPdCl ( PPh3 ) 2 и т . д . ) путем добавления фосфиновых лигандов или оловоорганических реагентов также является обычным явлением [ 6]
Предлагается окислительное присоединение к 14-электронному комплексу Pd(0). Этот процесс дает 16-электронные виды Pd(II). Было высказано предположение, что анионные лиганды , такие как OAc , ускоряют этот шаг за счет образования [Pd(OAc)(PR 3 ) n ] − , делая виды палладия более нуклеофильными. [11] [25] В некоторых случаях, особенно при использовании sp 3 -гибридизованного органогалогенида , механизм типа S N 2 имеет тенденцию преобладать, однако это не так часто встречается в литературе. [11] [25] Однако, несмотря на обычное образование цис -промежуточного продукта после согласованного окислительного присоединения , этот продукт находится в быстром равновесии со своим транс -изомером. [26] [27]

Существует несколько причин, по которым здесь благоприятствует изомеризация . Во-первых, в этих процессах обычно используется громоздкий набор лигандов , такой как фосфины , и для них крайне невыгодно принимать цис -ориентацию относительно друг друга, что приводит к изомеризации в более благоприятный транс-продукт. [26] [27] Альтернативное объяснение этого явления, получившее название антисимбиоз или трансфобия, заключается в привлечении модели sd n . [24] [28] Согласно этой теории, палладий является гипервалентным видом . Следовательно, R 1 и транс-лиганд, будучи транс-друг к другу, будут конкурировать с одной палладиевой орбиталью за связывание. Эта 4-электронная 3-центровая связь является наиболее слабой, когда присутствуют две сильные донорные группы, которые сильно конкурируют за палладиевую орбиталь. По сравнению с любым обычно используемым лигандом , лиганд C-донора R 1 имеет гораздо более высокий транс-эффект . Это транс-влияние является мерой того, как конкурентные лиганды, транс-друг к другу, будут конкурировать за орбиталь палладия. Обычный набор лигандов, фосфины и доноры C (R 1 ) являются мягкими лигандами, что означает, что они будут образовывать прочные связи с палладием и сильно конкурировать друг с другом за связывание. [29] [30] Поскольку галогениды или псевдогалогениды значительно более электроотрицательны , их связь с палладием будет сильно поляризованной , причем большая часть электронной плотности будет на группе X, что делает их лигандами с низким транс-эффектом . Следовательно, для R 1 будет весьма выгодно находиться в транс-положении к X, поскольку группа R 1 сможет образовывать более прочную связь с палладием. [24] [28] [30]

Считается, что трансметаллирование транс - промежуточного соединения со стадии окислительного присоединения происходит посредством различных механизмов в зависимости от субстратов и условий. Наиболее распространенный тип трансметаллирования для сопряжения Стилле включает ассоциативный механизм . Этот путь подразумевает, что органостаннан , обычно атом олова , связанный с аллильной, алкенильной или арильной группой, может координироваться с палладием через одну из этих двойных связей. Это дает мимолетный пятивалентный, 18-электронный вид , который затем может подвергнуться отсоединению лиганда, чтобы снова образовать квадратный плоский комплекс. Несмотря на то, что органостаннан координируется с палладием через группу R 2 , R 2 должен быть формально перенесен на палладий (связь R 2 -Sn должна быть разорвана), а группа X должна уйти с оловом, завершая трансметаллирование. Считается, что это происходит посредством двух механизмов. [31]
Во-первых, когда органостаннан изначально присоединяется к транс-металлическому комплексу, группа X может координироваться с оловом , в дополнение к палладию, создавая циклическое переходное состояние . Распад этого аддукта приводит к потере R 3 Sn-X и трехвалентного палладиевого комплекса с R 1 и R 2, присутствующими в цис -отношении. Другой часто встречающийся механизм включает то же начальное добавление органостаннана к транс -палладиевому комплексу, что и выше; однако в этом случае группа X не координируется с оловом, создавая открытое переходное состояние . После того, как α-углерод относительно олова атакует палладий, комплекс олова уйдет с чистым положительным зарядом. На схеме ниже, пожалуйста, обратите внимание, что двойная связь, координирующаяся с оловом, обозначает R 2 , поэтому любая алкенильная , аллильная или арильная группа. Кроме того, группа X может диссоциировать в любой момент в течение механизма и связываться с комплексом Sn + в конце. Расчеты теории функционала плотности предсказывают, что открытый механизм будет преобладать, если 2 лиганда остаются прикрепленными к палладию, а группа X уходит, в то время как циклический механизм более вероятен, если лиганд диссоциирует до трансметаллирования . Следовательно, хорошие уходящие группы, такие как трифлаты в полярных растворителях, благоприятствуют циклическому переходному состоянию, в то время как объемные фосфиновые лиганды будут благоприятствовать открытому переходному состоянию. [31]

Менее распространенный путь трансметаллирования — через диссоциативный или растворяющий механизм. Здесь лиганд из четырехвалентных видов палладия диссоциирует, и координирующий растворитель может присоединиться к палладию. Когда растворитель отсоединяется , образуя 14-электронный трехвалентный промежуточный продукт, органостаннан может присоединиться к палладию , подвергаясь открытому или циклическому процессу, как указано выше. [31]
Для того, чтобы R 1 -R 2 восстанавливающе элиминировал , эти группы должны занимать взаимно цис- координационные сайты. Поэтому любые транс -аддукты должны изомеризоваться в цис- промежуточный продукт, иначе соединение будет нарушено. Существует множество механизмов восстановительного элиминирования, и обычно их считают согласованными. [11] [32] [33]
Во-первых, 16-электронный четырехвалентный интермедиат из стадии трансметаллирования может подвергаться необслуживаемому восстановительному элиминированию из квадратного плоского комплекса. Эта реакция происходит в два этапа: во-первых, восстановительное элиминирование сопровождается координацией вновь образованной сигма-связи между R 1 и R 2 с металлом, с окончательной диссоциацией, дающей связанный продукт. [11] [32] [33]

Однако предыдущий процесс иногда протекает медленно и может быть значительно ускорен путем диссоциации лиганда с образованием 14-электронного промежуточного соединения в форме T. Затем это промежуточное соединение может перестраиваться с образованием Y-образного аддукта, который может подвергаться более быстрому восстановительному элиминированию. [11] [32] [33]

Наконец, дополнительный лиганд может ассоциироваться с палладием, образуя 18-электронную тригональную бипирамидальную структуру с R 1 и R 2 цис друг к другу в экваториальных положениях. Геометрия этого промежуточного соединения делает его похожим на Y-образное соединение, представленное выше. [11] [32] [33]

Присутствие объемных лигандов также может увеличить скорость элиминации. Лиганды, такие как фосфины с большими углами укуса , вызывают стерическое отталкивание между L и R 1 и R 2 , что приводит к увеличению угла между группами L и R и, следовательно, уменьшению угла между R 1 и R 2 , что позволяет ускорить восстановительную элиминацию . [11] [24]

Скорость, с которой органостаннаны трансметаллируются с палладиевыми катализаторами, показана ниже. Sp 2 -гибридизованные углеродные группы, присоединенные к олову, являются наиболее часто используемыми партнерами сочетания, а sp 3 -гибридизованные углероды требуют более жестких условий, а терминальные алкины могут быть связаны через связь CH посредством реакции Соногаширы .

В качестве органического соединения олова обычно используют триметилстаннил или трибутилстаннил. Хотя триметилстанниловые соединения показывают более высокую реакционную способность по сравнению с трибутилстанниловыми соединениями и имеют гораздо более простые спектры 1 H-ЯМР, токсичность первых намного выше. [34]
Оптимизация того, какие лиганды лучше всего подходят для проведения реакции с высоким выходом и скоростью оборота, может быть сложной. Это связано с тем, что окислительное присоединение требует металла, богатого электронами, следовательно, благоприятствует лигандам, отдающим электроны. Однако металл с дефицитом электронов более благоприятен для стадий трансметаллирования и восстановительного элиминирования , что делает лиганды, отдающие электроны, лучшими здесь. Поэтому оптимальный набор лигандов в значительной степени зависит от индивидуальных субстратов и используемых условий. Они могут изменить стадию определения скорости, а также механизм стадии трансметаллирования . [35]
Обычно используются лиганды промежуточной донорности, такие как фосфины. Повышение скорости можно наблюдать при использовании умеренно бедных электронами лигандов, таких как три-2-фурилфосфин или трифениларсенин. Аналогично, лиганды с большим числом доноров могут замедлять или ингибировать реакции связывания. [35] [36]
Эти наблюдения подразумевают, что обычно определяющим скорость этапом реакции Стилле является трансметаллирование . [36]
Наиболее распространенной добавкой к реакции Стилла является стехиометрическая или сокаталитическая медь(I) , в частности, иодид меди , который может увеличить скорость более чем в 10 3 раз. Было высказано предположение, что в полярных растворителях медь трансметаллируется с органостаннаном . Полученный органокупратный реагент затем может трансметаллироваться с палладиевым катализатором. Кроме того, в эфирных растворителях медь также может способствовать удалению фосфинового лиганда , активируя центр Pd. [9] [37] [38] [39] [40]
Было обнаружено, что хлорид лития является мощным ускорителем скорости в случаях, когда группа X диссоциирует от палладия (т. е. открытый механизм). Считается, что ион хлорида либо вытесняет группу X на палладии, делая катализатор более активным для трансметаллирования , либо путем координации с аддуктом Pd(0) ускоряет окислительное присоединение . Кроме того, соль LiCl усиливает полярность растворителя, облегчая уход этого обычно анионного лиганда (– Cl , – Br , – OTf и т. д.). Эта добавка необходима, когда используется такой растворитель, как ТГФ ; однако использование более полярного растворителя, такого как NMP , может заменить необходимость в этой солевой добавке. Однако, когда этап трансметаллирования сопряжения протекает через циклический механизм, добавление хлорида лития может фактически снизить скорость. Как и в циклическом механизме, нейтральный лиганд, такой как фосфин, должен диссоциировать вместо анионной группы X. [10] [41]
Наконец, источники фторид-ионов , такие как фторид цезия , также влияют на каталитический цикл . Во-первых, фторид может увеличить скорость реакций органотрифлатов , возможно, тем же эффектом, что и хлорид лития . Кроме того, фторид-ионы могут действовать как поглотители побочных продуктов олова , облегчая их удаление с помощью фильтрации . [39]
Наиболее распространенной побочной реакцией, связанной с реакцией Стилла, является гомосочетание реагентов станнана с образованием димера R 2 -R 2 . Считается, что оно протекает по двум возможным механизмам. Во-первых, реакция двух эквивалентов органостаннана с предкатализатором Pd(II) даст гомосоединенный продукт после восстановительного элиминирования . Во-вторых, катализатор Pd(0) может подвергаться радикальному процессу с получением димера. Используемый реагент органостаннана традиционно является четырехвалентным по олову, обычно состоящим из sp 2 -гибридизованной группы, которая должна быть перенесена, и трех «непереносимых» алкильных групп. Как показано выше, алкильные группы обычно медленнее всего мигрируют на палладиевый катализатор. [10]

Также было обнаружено, что при температурах до 50 °C арильные группы как на палладии , так и на координированном фосфине могут обмениваться. Хотя обычно они не обнаруживаются, во многих случаях они могут быть потенциальным второстепенным продуктом. [10]

Наконец, довольно редкая и экзотическая побочная реакция известна как замещение кин . Здесь, после начального окислительного добавления арилгалогенида , этот вид Pd-Ar может вставляться через двойную связь винилолова. После элиминирования β-гидрида , миграционной вставки и протодестаннилирования может быть синтезирован 1,2 - дизамещенный олефин. [10]

Могут происходить многочисленные другие побочные реакции, и они включают E/Z изомеризацию , которая может быть потенциально проблемой при использовании алкенилстаннана. Механизм этого превращения в настоящее время неизвестен. Обычно органостаннаны довольно устойчивы к гидролизу , однако, когда используются очень богатые электронами арилстаннаны, это может стать значительной побочной реакцией. [10]
Винилгалогениды являются обычными партнерами по сочетанию в реакции Стилла, и реакции этого типа встречаются в многочисленных полных синтезах природных продуктов . Обычно используются винилиодиды и бромиды. Винилхлориды недостаточно реакционноспособны по отношению к окислительному присоединению к Pd(0). Обычно предпочтительны иодиды : они обычно реагируют быстрее и в более мягких условиях, чем бромиды . Это различие продемонстрировано ниже с помощью селективного сочетания винилиодида в присутствии винилбромида. [10]

Обычно стереохимия алкена сохраняется на протяжении всей реакции, за исключением жестких условий реакции. Могут использоваться различные алкены, и они включают как α-, так и β-галоген-α,β ненасыщенные кетоны , сложные эфиры и сульфоксиды (которые обычно требуют добавки меди (I) для протекания реакции) и многое другое (см. пример ниже). [42] Иногда также используются винилтрифлаты. Некоторые реакции требуют добавления LiCl , а другие замедляются, что подразумевает наличие двух механистических путей. [10]

Другой класс распространенных электрофилов — арильные и гетероциклические галогениды. Что касается винильных субстратов, то бромиды и иодиды более распространены, несмотря на их большую стоимость. Можно выбрать множество арильных групп, включая кольца, замещенные электронно-донорными заместителями, биарильные кольца и т. д. Галогензамещенные гетероциклы также использовались в качестве партнеров по связыванию, включая пиридины , фураны , тиофены , тиазолы , индолы , имидазолы , пурины , урацил , цитозины , пиримидины и т. д. (См. ниже таблицу гетероциклов; галогены могут быть замещены в различных положениях на каждом из них). [10]

Ниже приведен пример использования связи Стилла для создания сложности на гетероциклах нуклеозидов , таких как пурины . [43]

Арильные трифлаты и сульфонаты также сочетаются с широким спектром реагентов органостаннана. Трифлаты имеют тенденцию реагировать сравнимо с бромидами в реакции Стилла. [10]
Ацилхлориды также используются в качестве партнеров по связыванию и могут использоваться с большим диапазоном органостаннанов, даже с алкилоловосодержащими реагентами, для получения кетонов (см. пример ниже). [44] Однако иногда бывает трудно ввести функциональные группы ацилхлорида в большие молекулы с чувствительными функциональными группами. Альтернативой, разработанной для этого процесса, является реакция перекрестного связывания Стилле-карбонилирования, которая вводит карбонильную группу посредством введения оксида углерода . [10]

Аллиловые , бензиловые и пропаргиловые галогениды также могут быть связаны. Хотя обычно используются, аллиловые галогениды протекают через η 3 переходное состояние, что позволяет связываться с органостаннаном либо в α, либо в γ положении, преимущественно при наименее замещенном углероде (см. пример ниже). [45] Алкенилэпоксиды (соседние эпоксиды и алкены ) также могут подвергаться этой же связи через η 3 переходное состояние , как, открывая эпоксид в спирт . В то время как аллиловые и бензиловые ацетаты обычно используются, пропаргиловые ацетаты не реагируют с органостаннанами. [10]

Реагенты станнана распространены. Некоторые из них коммерчески доступны. [46] Реагенты станнана могут быть синтезированы реакцией реактива Гриньяра или литийорганического реагента с хлоридами триалкилолова. Например, винилтрибутилолово получают реакцией бромида винилмагния с хлоридом трибутилолова . [47] Гидростаннилирование алкинов или алкенов дает множество производных. Реагенты оловоорганические стабильны на воздухе и во влаге. Некоторые реакции могут даже происходить в воде. [48] Их можно очищать с помощью хроматографии . Они толерантны к большинству функциональных групп. Некоторые оловоорганические соединения сильно токсичны , особенно производные триметилстаннила. [10]
Широко распространено использование винилстаннановых или алкенилстаннановых реагентов. [10] Что касается ограничений, то как очень громоздкие станнановые реагенты, так и станнаны с замещением на α-углероде , как правило, реагируют вяло или требуют оптимизации. Например, в приведенном ниже случае α-замещенный винилстаннан реагирует только с терминальным иодидом из-за стерических препятствий . [49]

Арилстаннановые реагенты также распространены, и как электронодонорные , так и электроноакцепторные группы фактически увеличивают скорость трансметаллирования. Это снова подразумевает, что могут иметь место два механизма трансметаллирования . Единственным ограничением для этих реагентов являются заместители в орто-положении, поскольку метильные группы могут снижать скорость реакции. Широкий спектр гетероциклов (см. раздел Электрофилы) также может использоваться в качестве партнеров по связыванию (см. пример с тиазольным кольцом ниже). [10] [50]


Алкинилстаннаны, наиболее реакционноспособные из станнанов, также использовались в реакциях Стилле. Обычно они не нужны, поскольку терминальные алкины могут напрямую связываться с палладиевыми катализаторами через их связь CH посредством реакции Соногаширы . Сообщалось, что аллилстаннаны работали, однако возникают трудности, как и с аллильными галогенидами, с трудностью контроля региоселективности для α- и γ-присоединения. Дистаннановые и ацилстаннановые реагенты также использовались в реакциях Стилле. [10]
Реакция Стилле использовалась в синтезе различных полимеров. [51] [52] [53] Однако наиболее распространенным применением реакции Стилле является ее использование в органических синтезах , и в частности, в синтезе природных продуктов .
19-шаговый энантиоселективный полный синтез квадригемина С Ларри Овермана включает двойную реакцию перекрестного метатезиса Стилле . [6] [54] Сложный органостаннан соединяется с двумя арильными иодидными группами. После двойной циклизации Хека получается продукт.

32-шаговый энантиоселективный полный синтез антибиотика ансамицина ( +)-микотриенола Панека использует макроциклическую связь типа Стилле на поздней стадии тандема. Здесь органостаннан имеет две терминальные трибутилоловогруппы, атакованные алкеном. Этот органостаннан «сшивает» два конца линейного исходного материала в макроцикл, добавляя в процессе недостающие две метиленовые единицы. После окисления ароматического ядра нитратом аммония церия (CAN) и снятия защиты плавиковой кислотой получается натуральный продукт с выходом 54% за 3 шага. [6] [55]

21-шаговый энантиоселективный полный синтез противоопухолевого алкалоида манзамина Ирцинала А Стивена Ф. Мартина и его коллег использует тандемную однореакторную реакцию Стилле/Дильса-Альдера. Алкеновая группа добавляется к винилбромиду, после чего следует циклоприсоединение Дильса-Альдера in situ между добавленным алкеном и алкеном в пирролидиновом кольце. [6] [56]

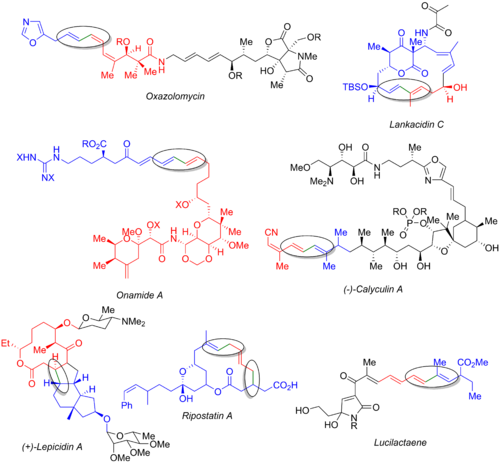
Многочисленные другие полные синтезы используют реакцию Стилле, включая синтезы оксазоломицина, [57] ланкацидина С, [58] онамида А, [59] каликулина А, [60] лепицидина А, [61] рипостатина А, [62] и люцилактаена. [6] [63] На изображении ниже показан конечный природный продукт , органогалогенид (синий), органостаннан (красный) и образующаяся связь (зеленая и обведенная кружком). Из этих примеров ясно, что реакцию Стилле можно использовать как на ранних стадиях синтеза (оксазоломицин и каликулин А), так и в конце конвергентного маршрута (онамид А, ланкацидин С, рипостатин А) или в середине (лепицидин А и люцилактаен). Синтез рипостатина А включает два параллельных связывания Стилле с последующим метатезисом с замыканием кольца . Синтез люцилактаена характеризуется наличием средней субъединицы, содержащей боран с одной стороны и станнан с другой, что позволяет осуществить реакцию Стилле с последующим сочетанием Сузуки.
Помимо проведения реакции в различных органических растворителях, были разработаны условия, которые позволяют проводить широкий спектр реакций Стилла в водном растворителе. [14]
В присутствии солей Cu(I) палладий на углероде показал себя эффективным катализатором. [64] [65]
В области зеленой химии сообщается о реакции Стилла, происходящей в низкоплавкой и высокополярной смеси сахара, такого как маннит , мочевины, такой как диметилмочевина, и соли, такой как хлорид аммония [66] . [67] Каталитической системой является трис(дибензилиденацетон)дипалладий(0) с трифениларсином :

Распространенным изменением в сочетании Стилле является включение карбонильной группы между R 1 и R 2 , служащее эффективным методом для образования кетонов . Этот процесс чрезвычайно похож на первоначальное исследование Мигиты и Стилле (см. Историю) связывания органостаннана с ацилхлоридами . Однако эти фрагменты не всегда легко доступны и могут быть труднообразуемы, особенно в присутствии чувствительных функциональных групп . Кроме того, контроль их высокой реакционной способности может быть сложным. Карбонилирующее перекрестное сочетание Стилле использует те же условия, что и сочетание Стилле, за исключением того, что используется атмосфера оксида углерода (CO). CO может координироваться с палладиевым катализатором ( 9 ) после начального окислительного добавления, за которым следует вставка CO в связь Pd-R 1 ( 10 ), что приводит к последующему восстановительному элиминированию в кетон ( 12 ). Стадия трансметаллирования обычно является стадией, определяющей скорость . [6]

Ларри Оверман и его коллеги используют карбонилирующее перекрестное сочетание Стилле в своем 20-шаговом энантиоселективном общем синтезе стрихнина . Добавленный карбонил позже преобразуется в терминальный алкен через реакцию Виттига , что позволяет сформировать ключевой третичный азот и пентациклическое ядро через аза -реакцию Копа - Манниха . [6] [68]
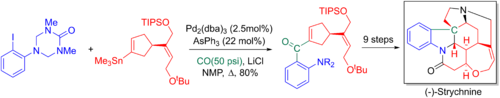
Джорджио Ортар и др. исследовали, как можно использовать карбонилирующее перекрестное сочетание Стилле для синтеза фосфоров бензофенона . Они были встроены в пептиды 4-бензоил-L-фенилаланина и использовались для их свойств фотоаффинной маркировки для исследования различных взаимодействий пептид-белок. [6] [69]

16-шаговый рацемический полный синтез Ятрафона Луи Хегедуса включал карбонилирующее перекрестное сочетание Стилле в качестве последнего шага для формирования 11-членного макроцикла . Вместо галогенида в качестве партнера по связыванию там используется винилтрифлат. [6] [70]

Используя основополагающую публикацию Иборна 1976 года, которая образует арилстаннаны из арилгалогенидов и дистаннанов, Т. Росс Келли применил этот процесс к внутримолекулярному связыванию арилгалогенидов. Это тандемное связывание станнилирования/арилгалогенида использовалось для синтеза различных дигидрофенантренов. Большинство образующихся внутренних колец ограничены 5 или 6 членами, однако сообщалось о некоторых случаях макроциклизации. В отличие от обычного связывания Стилле, хлор не работает как галоген, возможно, из-за его более низкой реакционной способности в последовательности галогенов (его более короткая длина связи и более сильная энергия диссоциации связи затрудняют его разрыв посредством окислительного присоединения ). Начиная с середины схемы ниже и двигаясь по часовой стрелке, палладиевый катализатор ( 1 ) окислительно присоединяется к наиболее реакционноспособной связи CX ( 13 ) с образованием 14 , за которым следует трансметаллирование с дистаннаном ( 15 ) с образованием 16 и восстановительное элиминирование с образованием арилстаннана ( 18 ). Регенерированный палладиевый катализатор ( 1 ) может окислительно присоединяться ко второй связи CX 18 с образованием 19 , за которым следует внутримолекулярное трансметаллирование с образованием 20 , за которым следует восстановительное элиминирование с образованием связанного продукта ( 22 ). [6]

Jie Jack Lie и др. использовали связь Стилла-Келли в своем синтезе различных кольцевых систем бензо[4,5]фуропиридинов. Они используют трехступенчатый процесс, включающий аминирование Бухвальда-Хартвига , еще одну реакцию сочетания, катализируемую палладием , за которой следует внутримолекулярная связь Стилла-Келли. Обратите внимание, что арилиодидная связь будет окислительно присоединяться к палладию быстрее, чем любая из арилбромидных связей. [6] [71]
![Синтез бензо[4,5]фуропиридинов](http://upload.wikimedia.org/wikipedia/commons/thumb/2/25/Benzofuropyridines.png/500px-Benzofuropyridines.png)