Эпотилоны представляют собой класс потенциальных лекарств от рака. Как и таксаны , они предотвращают деление раковых клеток, вмешиваясь в работу тубулина , но в ранних исследованиях эпотилоны имели лучшую эффективность и более мягкие побочные эффекты, чем таксаны. [1] [2]
Эпотилоны первоначально были идентифицированы как метаболиты, продуцируемые почвенной миксобактерией Sorangium cellulosum . [3] По состоянию на сентябрь 2008 г. [update]эпотилоны от A до F были идентифицированы и охарактеризованы. [4]
Ранние исследования на линиях раковых клеток и больных раком людей указывают на превосходную эффективность таксанов . Их механизм действия аналогичен, но химическая структура проще. Кремофоры (солюбилизирующие агенты, используемые для паклитаксела , которые могут влиять на функцию сердца и вызывать тяжелую гиперчувствительность) из-за их лучшей растворимости в воде не требуются. [5] Эндотоксиноподобные свойства, известные у паклитаксела, такие как активация макрофагов, синтезирующих воспалительные цитокины и оксид азота, не наблюдаются у эпотилона Б. [6]
Структура эпотилона А была определена в 1996 году с помощью рентгеновской кристаллографии . [7]
Основным механизмом действия класса эпотилонов является ингибирование функции микротрубочек . [8] Микротрубочки необходимы для деления клеток, а эпотилоны, следовательно, препятствуют правильному делению клеток. Эпотилон В обладает теми же биологическими эффектами, что и паклитаксел, как in vitro, так и в культивируемых клетках. Это связано с тем, что они имеют один и тот же сайт связывания, а также аффинность связывания с микротрубочками. Как и паклитаксел, эпотилон B связывается с субъединицей гетеродимера αβ-тубулина. После связывания скорость диссоциации αβ-тубулина снижается, тем самым стабилизируя микротрубочки. Кроме того, было показано, что эпотилон B индуцирует полимеризацию тубулина в микротрубочки без присутствия GTP. Это вызвано образованием пучков микротрубочек по всей цитоплазме. Наконец, эпотилон B также вызывает остановку клеточного цикла в фазе перехода G2-M, что приводит к цитотоксичности и, в конечном итоге, к апоптозу клеток. [9] Способность эпотилона ингибировать функцию веретена обычно объясняется его подавлением динамики микротрубочек; [10] , но недавние исследования показали, что подавление динамики происходит при концентрациях ниже тех, которые необходимы для блокирования митоза. При более высоких антимитотических концентрациях паклитаксел, по-видимому, действует путем подавления отслоения микротрубочек от центросом - процесса, который обычно активируется во время митоза. Вполне возможно, что эпотилон также может действовать по аналогичному механизму. [11]
Эпотилон D под общим названием утиделон был одобрен в Китае в 2021 году для лечения метастатического рака молочной железы . [12] [13] Утиделон продемонстрировал преимущества в III фазе исследования рака молочной железы при добавлении к капецитабину . [14]
Один синтетический аналог, иксабепилон , был одобрен в октябре 2007 года Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для использования в лечении агрессивного метастатического или местно-распространенного рака молочной железы , который больше не реагирует на доступные в настоящее время химиотерапии. [15] В ноябре 2008 года EMEA отказало в выдаче регистрационного удостоверения на иксабепилон. [16]
На нескольких моделях ксенотрансплантатов человека было доказано, что эпотилон B с непатентованным названием патупилон обладает мощной противораковой активностью in vivo при переносимых уровнях доз. [17] В результате патупилон и различные аналоги прошли различные клинические фазы.
Патупилон и полностью синтетический сагопилон были протестированы в исследованиях фазы II, а BMS-310705 - в исследованиях фазы I). Патупилон провалил исследование III фазы по лечению рака яичников в 2010 году. [18]
Были объявлены результаты исследования III фазы иксабепилона (BMS-247550) в сочетании с капецитабином при метастатическом раке молочной железы (2007 г. – привело к одобрению FDA). [19]
Из-за высокой эффективности и клинической необходимости в лечении рака эпотилоны стали целью многих тотальных синтезов . [20] Первой группой, опубликовавшей полный синтез эпотилонов, была SJ Danishefsky et al. в 1996 году. [9] [21] Этот полный синтез эпотилона А был достигнут посредством внутримолекулярной конденсации енолат-альдегида сложного эфира. Другие синтезы эпотилонов были опубликованы Николау , [22] Шинцером, [23] Мульцером , [24] и Каррейрой . [25] В этом подходе ключевые строительные блоки альдегид , глицидолы и кетокислота были построены и соединены с предшественником метатезиса олефина посредством альдольной реакции , а затем этерификационного сочетания. Катализатор Граббса использовали для замыкания бис-концевого олефина соединения-предшественника. Полученные соединения представляли собой цис- и транс-макроциклические изомеры с различными стереоцентрами . Эпоксидирование цис- и транс-олефинов дает эпотилон А и его аналоги.
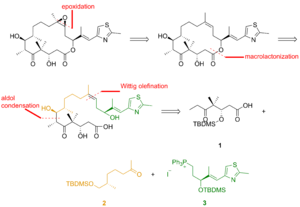
Один из полных синтезов эпотилона В описан ниже и описан лабораторией К.С. Николау . [26] Ретросинтетический анализ показал, что 1 , 2 и 3 являются строительными блоками (рис. 1).
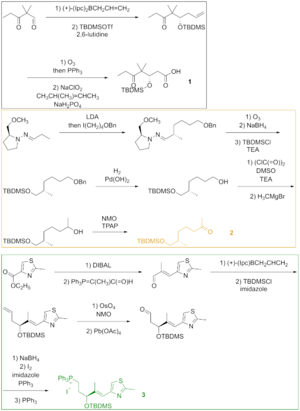
Как видно на рисунке 2, кетокислота 1 образовалась из кетоальдегида, который был преобразован в силиловый эфир посредством асимметричного аллилборирования и силилирования полученного спирта. Озонолиз силилового эфира и окисление альдегида по Линдгрену - Пиннику дали кетокислоту. Кетон 2 был создан путем алкилирования по Эндерсу, исходя из гидразона. Озонолиз, последняя стадия алкилирования по Эндерсу, сопровождался восстановлением альдегида и силилированием полученного спирта. Гидрогенолиз бензилового эфира дал спирт, который окислили в условиях Сверна и алкилировали реактивом Гриньяра с получением вторичного спирта. Окисление этого спирта реагентом Лея-Гриффита дало искомый кетон. Тиазол 3 синтезировали из сложного эфира, который восстанавливали диизобутилалюминийгидридом , а альдегид вводили в реакцию со стабилизированным илидом по реакции Виттига . Асимметрическое аллилборирование α,β-ненасыщенного альдегида и защита гидроксигруппы дали силиловый эфир, концевой олефин которого подвергался реакции с тетроксидом осмия с образованием диола, который расщеплялся тетраацетатом свинца с образованием альдегида. Восстановление, йодирование и обработка трифенилфосфином привели к образованию фосфониевой соли.
Фрагменты 1 , 2 и 3 подвергали взаимодействию друг с другом для доставки эпотилона B, используя подход, включающий реакцию Виттига , альдольную реакцию и этерификацию Ямагути (рис. 3). Для разделения диастереомеров использовали препаративную тонкослойную хроматографию .

Эпотилон Б представляет собой 16-членный поликетид макролактон с метилтиазольной группой , связанной с макроциклом олефиновой связью. Поликетидный остов был синтезирован поликетидсинтазой I типа (PKS), а тиазольное кольцо было получено из цистеина , включенного нерибосомальной пептидсинтетазой (NRPS). В этом биосинтезе и PKS, и NRPS используют белки-носители , которые были посттрансляционно модифицированы фосфопантетеиновыми группами, чтобы присоединиться к растущей цепи. PKS использует тиоэфир коэнзима-A для катализа реакции и модификации субстратов путем избирательного восстановления β-карбонила до гидроксила (кеторедуктаза, KR), алкена (дегидратаза, DH) и алкана (еноилредуктаза, ER). ПКС-I также может метилировать α-углерод субстрата. С другой стороны, NRPS использует аминокислоты, активированные ферментом, в виде аминоациладенилатов. В отличие от PKS, в ферменте NRPS происходит эпимеризация , N-метилирование и образование гетероцикла. [27]


Эпотилон B начинается со стартовой единицы 2-метил-4-карбокситиазола, которая образуется в результате трансляционного взаимодействия между PKS, модулем EPOS A (epoA) и NRPS, модулем EPOS P(epoP). EPOS A содержит модифицированную β-кетоацилсинтазу (малонил-ACP-декарбоксилазу, KSQ), ацилтрансферазу (AT), еноилредуктазу (ER) и домен белка-переносчика ацила (ACP). Однако EPOS P содержит домен гетероцилизации, аденилирования, оксидазы и тиолирования. Эти домены важны, поскольку они участвуют в образовании пятичленного гетероциклического кольца тиазола. Как видно на фигуре 4 , EPOS P активирует цистеин и связывает активированный цистеин в виде аминоацил-S-PCP. После связывания цистеина EPOS A загружает ацетатную единицу в комплекс EPOS P, тем самым инициируя образование тиазолинового кольца путем внутримолекулярной циклодегидратации. [27]
После образования 2-метилтиазольного кольца его переносят в ПКС EPOS B (epoB), EPOS C (epoC), EPOS D (epoD), EPOS E (epoE) и EPOS F (epoF) для последующей элонгации. и модификацию для образования олефиновой связи, 16-членного кольца и эпоксида, как показано на Фигуре 5 . Важно отметить синтез гем-диметильного звена в модуле 7. Эти два диметила не были синтезированы путем двух последовательных C-метилирований. Вместо этого одна из метильных групп была получена из единицы пропионатного удлинителя, а вторая метильная группа была интегрирована с помощью домена C-метилтрансферазы. [27]