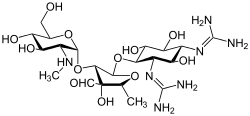
Аминогликозиды — это медицинская и бактериологическая категория традиционных грамотрицательных антибактериальных препаратов , которые ингибируют синтез белка и содержат в качестве части молекулы аминомодифицированный гликозид ( сахар ). [1] [2] Термин может также относиться в более общем смысле к любой органической молекуле, которая содержит субструктуры аминосахаров . Аминогликозидные антибиотики проявляют бактерицидную активность против грамотрицательных аэробов и некоторых анаэробных бацилл , когда резистентность еще не возникла, но, как правило, не против грамположительных и анаэробных грамотрицательных бактерий. [3]
Стрептомицин — первый в своем классе антибиотик из группы аминогликозидов . Он получен из Streptomyces griseus и является самым ранним современным средством, используемым против туберкулеза . У стрептомицина отсутствует общая группа 2-дезоксистрептамина (изображение справа, ниже), присутствующая у большинства других членов этого класса. Другие примеры аминогликозидов включают в себя дезоксистрептаминсодержащие агенты канамицин , тобрамицин , гентамицин и неомицин (см. ниже).

Аминогликозиды, полученные из бактерий рода Streptomyces , называются с суффиксом -мицин , тогда как те, которые получены из Micromonospora [4], называются с суффиксом -мицин . [5] Однако эта система номенклатуры не является специфичной для аминогликозидов, и поэтому появление этого набора суффиксов не подразумевает общий механизм действия. (Например, ванкомицин , гликопептидный антибиотик , [6] и эритромицин , [7] макролидный антибиотик , продуцируемый Saccharopolyspora erythraea , вместе с его синтетическими производными кларитромицином и азитромицином , все имеют общие суффиксы, но имеют заметно разные механизмы действия.)
В следующей галерее канамицин А и нетилмицин являются примерами подкласса аминогликозидов 4,6-дизамещенных дезоксистрептаминов, неомицины являются примерами подкласса 4,5 - дизамещенных, а стрептомицин является примером недезоксистрептаминовых аминогликозидов. [2]
Аминогликозиды проявляют зависящую от концентрации бактерицидную активность против «большинства грамотрицательных аэробных и факультативно анаэробных бацилл», но не против грамотрицательных анаэробов и большинства грамположительных бактерий. [3] Им требуется лишь короткое время контакта, и они наиболее эффективны против восприимчивых популяций бактерий, которые быстро размножаются. [8] Эти действия приписываются основному способу действия в качестве ингибиторов синтеза белка , хотя для некоторых конкретных агентов предполагаются дополнительные механизмы, и/или подробные механистические описания пока отсутствуют. [2] [3] [8]
Ингибирование синтеза белка опосредовано энергозависимым, иногда необратимым связыванием аминогликозидов с цитозольной , связанной с мембраной бактериальной рибосомой (изображение справа). [2] (Аминогликозиды сначала пересекают стенки бактериальных клеток — липополисахарид у грамотрицательных бактерий — и клеточные мембраны, куда они активно транспортируются . [8] ) Хотя конкретные этапы синтеза белка, на которые оказывается воздействие, могут несколько различаться между конкретными аминогликозидными агентами, как и их сродство и степень связывания, [8] присутствие аминогликозидов в цитозоле обычно нарушает удлинение пептида в 30S рибосомальной субъединице, что приводит к неточной трансляции мРНК и, следовательно, биосинтезу белков, которые укорочены или имеют измененный аминокислотный состав в определенных точках. [2] В частности, связывание ухудшает трансляционную корректуру, что приводит к неправильному прочтению сообщения РНК, преждевременному завершению или и тому, и другому, и, таким образом, к неточности транслируемого белкового продукта. Подмножество аберрантных белков, которые включены в бактериальную клеточную мембрану, может затем привести к изменениям в ее проницаемости, а затем к «дальнейшей стимуляции транспорта аминогликозидов». [2] Аминосахаридная часть этого класса молекул (например, 2- дезоксистрептамин в канамицинах, гентамицинах и тобрамицине, см. выше) участвует в ассоциации малой молекулы с рибосомальными структурами, что приводит к неточностям в трансляции (там же). Также было предложено ингибирование рибосомальной транслокации — т. е. перемещения пептидил-тРНК из A- в P-сайт — [ необходима цитата ] . Недавние эксперименты по отслеживанию одиночных молекул в живых E. coli показали продолжающийся, но более медленный синтез белка при лечении различными аминогликозидными препаратами. [9] ( Спектиномицин , родственный, но отличающийся по химической структуре класс, часто обсуждаемый с аминогликозидами, не вызывает неправильного считывания мРНК и, как правило, не обладает бактерицидным действием.) [8]
Было высказано предположение, что аминогликозидные антибиотики вызывают окисление гуаниновых нуклеотидов в бактериальном нуклеотидном пуле, и что это способствует цитотоксичности этих антибиотиков. [10] Включение окисленных гуаниновых нуклеотидов в ДНК может быть бактерицидным, поскольку неполное восстановление близко расположенных 8-оксо-2'-дезоксигуанозинов в ДНК может привести к летальным двухцепочечным разрывам. [10]
Наконец, еще один «клеточно-мембранный эффект» также возникает с аминогликозидами; «функциональная целостность бактериальной клеточной мембраны» может быть утрачена позднее в ходе воздействия и транспортировки аминогликозидов. [11]
Существует значительная изменчивость в соотношении между введенной дозой и полученным уровнем в плазме крови. [ необходима цитата ] Терапевтический лекарственный мониторинг (TDM) необходим для получения правильной дозы. Эти агенты проявляют постантибиотический эффект , при котором уровень препарата в крови не обнаруживается или очень мал, но все еще наблюдается ингибирование повторного роста бактерий. Это происходит из-за сильного, необратимого связывания с рибосомой и остается внутриклеточным в течение длительного времени после падения уровня в плазме, что позволяет увеличить интервал дозировки. [ необходима цитата ] В зависимости от их концентрации они действуют как бактериостатические или бактерицидные агенты. [12]
Аминогликозиды полезны в первую очередь при инфекциях, связанных с аэробными , грамотрицательными бактериями, такими как Pseudomonas , Acinetobacter и Enterobacter . Кроме того, некоторые микобактерии , включая бактерии, вызывающие туберкулез , восприимчивы к аминогликозидам. Стрептомицин был первым эффективным препаратом для лечения туберкулеза, хотя роль аминогликозидов, таких как стрептомицин и амикацин, затмилась (из-за их токсичности и неудобного пути введения), за исключением штаммов с множественной лекарственной устойчивостью. [ необходима цитата ] Наиболее часто аминогликозиды используются в эмпирической терапии серьезных инфекций, таких как сепсис , осложненные интраабдоминальные инфекции, осложненные инфекции мочевыводящих путей и нозокомиальные инфекции дыхательных путей. Обычно, как только культуры возбудителя выращены и их восприимчивость проверена, аминогликозиды прекращают принимать в пользу менее токсичных антибиотиков. [ необходима цитата ]
Как уже отмечалось, аминогликозиды в основном неэффективны против анаэробных бактерий, грибков и вирусов. [2] Инфекции, вызванные грамположительными бактериями, также можно лечить аминогликозидами, но другие типы антибиотиков более эффективны и менее опасны для хозяина. В прошлом аминогликозиды использовались в сочетании с бета-лактамными антибиотиками при стрептококковых инфекциях из-за их синергического эффекта, в частности при эндокардите . Одной из наиболее частых комбинаций является ампициллин ( бета-лактамный или пенициллин-родственный антибиотик) и гентамицин. Часто персонал больницы называет эту комбинацию «amp and gent» или в последнее время ее называют «pen and gent» для пенициллина и гентамицина. [ необходима цитата ]
Вмешательство в корректуру мРНК использовалось для лечения генетических заболеваний, возникающих из-за преждевременных стоп-кодонов (что приводит к раннему прекращению синтеза белка и укорочению белков). Аминогликозиды могут заставить клетку преодолеть стоп-кодоны, вставить случайную аминокислоту и экспрессировать полноразмерный белок. [13] Аминогликозид гентамицин использовался для лечения клеток кистозного фиброза (CF) в лабораторных условиях, чтобы побудить их выращивать полноразмерные белки. CF вызывается мутацией в гене, кодирующем белок регулятора трансмембранной проводимости кистозного фиброза ( CFTR ). Примерно в 10% случаев CF мутация в этом гене вызывает его раннее прекращение во время трансляции , что приводит к образованию укороченного и нефункционального белка CFTR. Считается, что гентамицин искажает структуру комплекса рибосома-РНК, что приводит к неправильному считыванию терминирующего кодона , заставляя рибосому «перескакивать» через стоп-последовательность и продолжать нормальное удлинение и производство белка CFTR. [14]
Поскольку они не всасываются из кишечника, их вводят внутривенно и внутримышечно . Некоторые из них используются в местных препаратах для ран. Пероральное введение может использоваться для деконтаминации кишечника (например, при печеночной энцефалопатии). Тобрамицин может вводиться в распыленной форме. [15]
Недавнее появление инфекций, вызванных грамотрицательными бактериальными штаммами с развитой резистентностью к противомикробным препаратам, побудило врачей пересмотреть использование этих антибактериальных средств. [16] Этот возрожденный интерес к использованию аминогликозидов вновь высветил дебаты по двум основным вопросам, связанным с этими соединениями, а именно спектру чувствительности к противомикробным препаратам и токсичности. Текущие данные показывают, что аминогликозиды сохраняют активность против большинства грамотрицательных клинических бактериальных изолятов во многих частях мира. Тем не менее, относительно частое возникновение нефротоксичности и ототоксичности во время лечения аминогликозидами заставляет врачей неохотно использовать эти соединения в повседневной практике. Недавние достижения в понимании влияния различных схем дозировки аминогликозидов на токсичность предоставили частичное решение этой проблемы, хотя все еще необходимо провести больше исследований, чтобы полностью преодолеть эту проблему. [17]
Аминогликозиды относятся к категории D применительно к беременности [18] , то есть имеются положительные доказательства риска для плода человека, основанные на данных о побочных реакциях, полученных в ходе исследований или маркетинговых исследований, или исследований на людях, но потенциальная польза может оправдать использование препарата у беременных женщин, несмотря на потенциальные риски.
Аминогликозиды могут вызывать токсичность внутреннего уха, которая может привести к сенсоневральной потере слуха . [19] Частота токсичности внутреннего уха варьируется от 7 до 90% в зависимости от типов используемых антибиотиков, восприимчивости пациента к таким антибиотикам и продолжительности приема антибиотиков. [20]
Другим серьезным и инвалидизирующим побочным эффектом использования аминогликозидов является вестибулярная ототоксичность. [19] Это приводит к осциллопсии (нестабильности взгляда) и нарушениям равновесия, которые влияют на все аспекты антигравитационной функции человека. Эта потеря постоянна и может произойти при любой дозе. [21] [22] [23] [24]
Частое использование аминогликозидов может привести к повреждению почек (острое повреждение почек), что может привести к хроническому заболеванию почек . [25]
Аминогликозиды могут усугубить слабость у пациентов с миастенией , поэтому их применение у таких пациентов следует избегать. [26]
Аминогликозиды противопоказаны пациентам с митохондриальными заболеваниями, поскольку они могут привести к нарушению трансляции мтДНК, что может привести к необратимой потере слуха, шуму в ушах, сердечной токсичности и почечной токсичности. Однако потеря слуха и шум в ушах также наблюдались у некоторых пациентов без митохондриальных заболеваний. [27]