Ацетилен ( систематическое название : этин ) — химическое соединение с формулой C 2 H 2 и структурой H−C≡C−H . Это углеводород и простейший алкин . [7] Этот бесцветный газ широко используется в качестве топлива и химического строительного материала. В чистом виде он нестабилен, поэтому с ним обычно обращаются как с раствором. [8] Чистый ацетилен не имеет запаха, но коммерческие сорта обычно имеют выраженный запах из-за примесей, таких как дивинилсульфид и фосфин . [8] [9]
Как алкин, ацетилен ненасыщен , поскольку два его атома углерода связаны тройной связью . Тройная связь углерод-углерод помещает все четыре атома на одну прямую линию с валентным углом CCH 180 °. [10]
Ацетилен был открыт в 1836 году Эдмундом Дэви , который определил его как «новый карбюратор водорода». [11] [12] Это было случайное открытие при попытке изолировать металлический калий . Нагревая карбонат калия с углеродом при очень высоких температурах, он получил остаток того, что сейчас известно как карбид калия (K 2 C 2 ), который прореагировал с водой с выделением нового газа. Он был вновь открыт в 1860 году французским химиком Марселленом Бертло , который придумал название ацетилен . [13] Эмпирическая формула Бертло для ацетилена (C 4 H 2 ), а также альтернативное название « квадрикарбюр д'гидроген » (квадрикарбид водорода) были неверными, поскольку многие химики того времени использовали неправильную атомную массу углерода (6 вместо из 12). [14] Бертло смог получить этот газ, пропуская пары органических соединений (метанол, этанол и т. д.) через раскаленную трубку и собирая выходящие потоки . Он также обнаружил, что ацетилен образуется в результате искрообразования в смеси газов циана и водорода . Позднее Бертло получил ацетилен непосредственно путем пропускания водорода между полюсами угольной дуги . [15] [16]
За исключением Китая , в производстве ацетилена преобладает частичное сжигание природного газа. [17]
С 1950- х годов ацетилен в основном производят путем частичного сжигания метана . [18] [19] [20] Это побочный продукт, получаемый при производстве этилена путем крекинга углеводородов . В 1983 году этим методом было произведено около 400 000 тонн. [18] Его присутствие в этилене обычно нежелательно из-за его взрывчатого характера и способности отравлять катализаторы Циглера-Натта . Его селективно гидрируют в этилен , обычно с использованием катализаторов Pd - Ag . [21]
3 СН 4 + 3 О 2 → С 2 Н 2 + СО + 5 Н 2 О.
При частичном сгорании метана также образуется ацетилен:
Самые тяжелые алканы нефти и природного газа расщепляются на более легкие молекулы, которые дегидрируются при высокой температуре:
Эта последняя реакция реализуется в процессе анаэробного разложения метана микроволновой плазмой. Преимуществом этой технологии является отсутствие выбросов CO2 и совместное производство водорода как побочного продукта. [22] Это делает производство низкоуглеродным и электрифицированным. На 32 т преобразованного метана получается 26 т ацетилена и 6 т водорода (по стехиометрии).
Производство ацетилена из карбида кальция является традиционным и до сих пор доминирующим способом:
Условия производства карбида кальция экологически неприемлемы в большинстве развитых стран, кроме Китая. [ нужна цитата ]
До 1950-х годов, когда нефть вытеснила уголь в качестве основного источника восстановленного углерода, ацетилен (и ароматическая фракция каменноугольной смолы ) был основным источником органических химикатов в химической промышленности. Его получали гидролизом карбида кальция — реакции, открытой Фридрихом Вёлером в 1862 году [23] и до сих пор знакомой студентам:
Производство карбида кальция требует высоких температур, ~ 2000 ° C, что требует использования электродуговой печи . В США этот процесс был важной частью химической революции конца XIX века, ставшей возможным благодаря масштабному проекту гидроэлектростанции на Ниагарском водопаде . [24]
При использовании карбид реагирует с водой с образованием ацетилена: из 1 кг карбида в сочетании с 562,5 г воды выделяется 350 л ацетилена.
С точки зрения теории валентных связей , в каждом атоме углерода 2s- орбиталь гибридизуется с одной 2p-орбиталью, образуя sp-гибрид. Две другие 2p-орбитали остаются негибридизованными. Два конца двух sp-гибридной орбитали перекрываются , образуя прочную валентную связь между атомами углерода, в то время как на каждом из двух других концов атомы водорода также присоединяются посредством σ-связей. Две неизмененные 2p-орбитали образуют пару более слабых π-связей . [25]
Поскольку ацетилен является линейной симметричной молекулой , он обладает точечной группой D∞h . [26]
При атмосферном давлении ацетилен не может существовать в жидком виде и не имеет температуры плавления. Тройная точка на фазовой диаграмме соответствует температуре плавления (-80,8 ° C) при минимальном давлении, при котором может существовать жидкий ацетилен (1,27 атм). При температурах ниже тройной точки твердый ацетилен может превращаться непосредственно в пар (газ) путем сублимации . Точка сублимации при атмосферном давлении составляет -84,0 °C. [27]
При комнатной температуре растворимость ацетилена в ацетоне составляет 27,9 г на кг. Для того же количества диметилформамида (ДМФ) растворимость составляет 51 г. При 20,26 бар растворимость увеличивается до 689,0 и 628,0 г для ацетона и ДМФ соответственно. Эти растворители используются в газовых баллонах под давлением. [28]
Около 20% ацетилена поставляется промышленностью промышленных газов для газогенной сварки и резки из-за высокой температуры пламени. Сгорание ацетилена с кислородом дает пламя с температурой более 3600 К (3330 ° C; 6020 ° F), выделяя 11,8 кДж / г. Кислород с ацетиленом — самая горячая горючая газовая смесь. [29] Ацетилен является третьим по температуре природным химическим пламенем после дицианоацетилена с температурой 5260 К (4990 °C; 9010 °F) и цианогена с температурой 4798 К (4525 °C; 8177 °F). Кислородно-ацетиленовая сварка была популярным процессом сварки в предыдущие десятилетия. Развитие и преимущества процессов дуговой сварки привели к тому, что кислородно-топливная сварка практически исчезла для многих применений. Использование ацетилена для сварки значительно сократилось. С другой стороны, оборудование для ацетиленовой сварки весьма универсально – не только потому, что горелка предпочтительна для некоторых видов сварки железа или стали (например, в некоторых художественных применениях), но и потому, что она легко поддается пайке, сварке твердым припоем. , нагрев металла (для отжига или отпуска, гибки или формовки), ослабление проржавевших гаек и болтов и другие применения. Специалисты по ремонту кабелей Bell Canada до сих пор используют портативные комплекты горелок, работающих на ацетилене, в качестве паяльного инструмента для герметизации соединений выводных гильз в люках и в некоторых местах над землей. Газогенно-ацетиленовая сварка также может использоваться в местах, где электричество недоступно. Газокислородная резка применяется во многих цехах металлообработки. Для использования при сварке и резке рабочее давление должно контролироваться регулятором, поскольку при давлении выше 15 фунтов на квадратный дюйм (100 кПа) при воздействии ударной волны (вызванной, например, вспышкой ) ацетилен взрывоопасно разлагается на водород и углерод . [30]

Ацетилен, несмотря на свою простоту, не используется во многих промышленных процессах.
Одним из основных химических применений является этинилирование формальдегида. [8] Ацетилен присоединяется к альдегидам и кетонам с образованием α-этиниловых спиртов:
Реакция дает бутиндиол с пропаргиловым спиртом в качестве побочного продукта. В качестве катализатора используется ацетилид меди . [31] [32]
Помимо этинилирования, ацетилен реагирует с окисью углерода , ацетилен реагирует с образованием акриловой кислоты или акриловых эфиров. Требуются металлические катализаторы. Эти производные образуют такие продукты, как акриловые волокна , стекла , краски , смолы и полимеры . За исключением Китая, использование ацетилена в качестве химического сырья сократилось на 70% с 1965 по 2007 год из-за затрат и экологических соображений. [33]
До широкого распространения нефтехимии ацетилен, полученный из угля, был строительным блоком для некоторых промышленных химикатов. Таким образом, ацетилен может гидратироваться с образованием ацетальдегида , который, в свою очередь, может окисляться до уксусной кислоты. Процессы получения акрилатов также были коммерциализированы. Почти все эти процессы устарели с появлением этилена и пропилена, получаемых из нефти. [34]
В 1881 году русский химик Михаил Кучеров [35] описал гидратацию ацетилена в ацетальдегид с использованием такого катализатора, как бромид ртути(II) . До появления процесса Вакера эта реакция проводилась в промышленных масштабах. [36]
Полимеризация ацетилена с катализаторами Циглера-Натта приводит к образованию полиацетиленовых пленок. Полиацетилен — цепочка центров CH с чередующимися одинарными и двойными связями — был одним из первых открытых органических полупроводников . Его реакция с йодом приводит к образованию материала с высокой электропроводностью. Хотя такие материалы бесполезны, эти открытия привели к развитию органических полупроводников , что было признано Нобелевской премией по химии в 2000 году Алану Дж. Хигеру , Алану Дж. МакДиармиду и Хидеки Сиракаве . [8]
В 1920-х годах чистый ацетилен экспериментально использовался в качестве ингаляционного анестетика . [37]
Ацетилен иногда используется для цементации (то есть закалки) стали, когда объект слишком велик, чтобы поместиться в печи. [38]
Ацетилен используется для улетучивания углерода при радиоуглеродном датировании . Углеродистый материал археологического образца обрабатывается металлическим литием в небольшой специализированной исследовательской печи с образованием карбида лития (также известного как ацетилид лития). Затем карбид может быть подвергнут реакции с водой, как обычно, с образованием газообразного ацетилена, который подается в масс-спектрометр для измерения изотопного соотношения углерода-14 и углерода-12. [39]
Сгорание ацетилена дает сильный и яркий свет, а повсеместное распространение карбидных ламп способствовало значительной коммерциализации ацетилена в начале 20 века. Общие области применения включали прибрежные маяки , [40] уличные фонари , [41] и автомобильные [42] и фары для горнодобывающей промышленности . [43] В большинстве этих применений прямое горение представляет опасность возгорания , поэтому ацетилен был заменен сначала лампами накаливания , а много лет спустя светодиодами малой мощности и высокой светосилы. Тем не менее, ацетиленовые лампы по-прежнему используются ограниченно в отдаленных или иным образом недоступных районах, а также в странах со слабой или ненадежной центральной электросетью . [43]
Энергетическое богатство тройной связи C≡C и довольно высокая растворимость ацетилена в воде делают его подходящим субстратом для бактерий при наличии адекватного источника. [44] Был идентифицирован ряд бактерий, живущих на ацетилене. Фермент ацетиленгидратаза катализирует гидратацию ацетилена с образованием ацетальдегида : [ 45]
Ацетилен — довольно распространенное химическое вещество во Вселенной, часто связанное с атмосферами газовых гигантов . [46] Одно любопытное открытие ацетилена произошло на Энцеладе , спутнике Сатурна . Считается, что природный ацетилен образуется в результате каталитического разложения длинноцепочечных углеводородов при температуре 1700 К (1430 ° C; 2600 ° F) и выше. Поскольку такие температуры крайне маловероятны на таком маленьком отдалённом теле, это открытие потенциально наводит на мысль о каталитических реакциях на этой луне, что делает её многообещающим местом для поиска пребиотической химии. [47] [48]
В реакциях винилирования соединения H-X присоединяются по тройной связи. Спирты и фенолы присоединяются к ацетилену с образованием виниловых эфиров . Тиолы дают винилтиоэфиры. Аналогичным образом винилпирролидон и винилкарбазол производятся в промышленности путем винилирования 2-пирролидона и карбазола . [28] [8]
Гидратация ацетилена представляет собой реакцию винилирования, но образующийся виниловый спирт изомеризуется в ацетальдегид . Реакцию катализируют соли ртути. Эта реакция когда-то была доминирующей технологией производства ацетальдегида, но ее заменил процесс Вакера , который дает ацетальдегид путем окисления этилена , более дешевого сырья. Аналогичная ситуация применима к превращению ацетилена в ценный винилхлорид путем гидрохлорирования , а не оксихлорирования этилена.
Винилацетат используется вместо ацетилена для некоторых винилирований, которые более точно описываются как трансвинилирования . [49] Высшие эфиры винилацетата использовались в синтезе винилформиата .
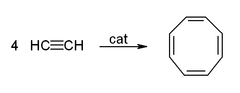
Ацетилен и его производные (2-бутин, дифенилацетилен и др.) образуют комплексы с переходными металлами . Его связь с металлом в чем-то аналогична связи этиленовых комплексов. Эти комплексы являются промежуточными продуктами во многих каталитических реакциях, таких как тримеризация алкина в бензол , тетрамеризация в циклооктатетраен [8] и карбонилирование в гидрохинон : [50]

Также распространены ацетилиды металлов , разновидности формулы L n M-C 2 R . Ацетилид меди(I) и ацетилид серебра могут легко образовываться в водных растворах благодаря благоприятному равновесию растворимости . [51]
Ацетилен имеет p K a 25, ацетилен может быть депротонирован супероснованием с образованием ацетилида : [51]
Эффективны различные металлоорганические [52] и неорганические [53] реагенты.
Ацетилен можно полугидрировать до этилена , обеспечивая сырье для различных полиэтиленовых пластиков. Галогены присоединяются к тройной связи.
Ацетилен не особенно токсичен, но, будучи получен из карбида кальция , он может содержать токсичные примеси, такие как следы фосфина и арсина , которые придают ему отчетливый чесночный запах. Он также легко воспламеняется, как и большинство легких углеводородов, поэтому его используют при сварке. Его самая особенная опасность связана с его внутренней нестабильностью, особенно когда он находится под давлением: при определенных условиях ацетилен может вступать в экзотермическую реакцию присоединения с образованием ряда продуктов, обычно бензола и/или винилацетилена , возможно, в дополнение к углероду и водород . [ нужна цитата ] Следовательно, ацетилен, если он инициируется сильным нагревом или ударной волной, может разложиться со взрывом, если абсолютное давление газа превышает примерно 200 килопаскалей (29 фунтов на квадратный дюйм). Большинство регуляторов и манометров на оборудовании показывают манометрическое давление , поэтому безопасный предел для ацетилена составляет 101 кПа ( манометрическое давление) или 15 фунтов на квадратный дюйм. [54] [55] Поэтому он поставляется и хранится растворенным в ацетоне или диметилформамиде (ДМФ), [55] [56] [57] содержится в газовом баллоне с пористым наполнением ( Агамассан ), что делает его безопасным при транспортировке и хранении. использования при условии надлежащего обращения. Баллоны с ацетиленом следует использовать в вертикальном положении, чтобы избежать вытекания ацетона во время использования. [58]
Информация о безопасном хранении ацетилена в вертикальных баллонах предоставлена OSHA, [59] [60] Ассоциацией по сжатому газу, [55] Управлением по безопасности и гигиене труда в шахтах США (MSHA), [61] EIGA, [58] и другими агентствами. .
Медь катализирует разложение ацетилена, поэтому ацетилен не следует транспортировать в медных трубах. [62]
Баллоны следует хранить в помещении, изолированном от окислителей, чтобы избежать обострения реакции в случае возгорания/протечки. [55] [60] Баллоны с ацетиленом не следует хранить в замкнутых пространствах, закрытых транспортных средствах, гаражах и зданиях, чтобы избежать непреднамеренной утечки, приводящей к взрывоопасной атмосфере. [55] [60] В США Национальный электротехнический кодекс (NEC) требует учитывать опасные зоны, в том числе те, где ацетилен может выделяться во время аварий или утечек. [63] Рассмотрение может включать электрическую классификацию и использование электрических компонентов группы А, включенных в список в США. [63] Дополнительную информацию об определении зон, требующих особого внимания, можно найти в NFPA 497. [64] В Европе ATEX также требует учитывать опасные зоны, где во время аварий или утечек могут выделяться легковоспламеняющиеся газы. [58]
Название ацетилен сохранено за соединением HC≡CH. Это предпочтительное имя IUPAC, но его замена любого рода не допускается; однако в общей номенклатуре допускается замещение, например, фторацетиленом [фторэтином (ПИН)], но не алкильными группами или какой-либо другой группой, удлиняющей углеродную цепь, а также характерными группами, выраженными суффиксами.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) CS1 maint: другие ( ссылка )Для углерода использовались атомные веса 6 и 12.
{{cite encyclopedia}}: CS1 maint: числовые имена: список авторов ( ссылка )