Генная дупликация (или хромосомная дупликация или амплификация гена ) является основным механизмом, посредством которого генерируется новый генетический материал в ходе молекулярной эволюции . Ее можно определить как любую дупликацию области ДНК , содержащей ген . Генные дупликации могут возникать как продукты нескольких типов ошибок в репликации ДНК и механизмах восстановления , а также в результате случайного захвата эгоистичными генетическими элементами. Распространенными источниками генных дупликаций являются эктопическая рекомбинация , ретротранспозиция , анеуплоидия , полиплоидия и проскальзывание репликации . [1]
Дупликации возникают из-за события, называемого неравным кроссинговером , которое происходит во время мейоза между невыровненными гомологичными хромосомами. Вероятность того, что это произойдет, зависит от степени совместного использования повторяющихся элементов между двумя хромосомами. Продуктами этой рекомбинации являются дупликация в месте обмена и взаимная делеция. Эктопическая рекомбинация обычно опосредуется сходством последовательностей в точках разрыва дубликатов, которые образуют прямые повторы. Повторяющиеся генетические элементы, такие как транспонируемые элементы, предлагают один из источников повторяющейся ДНК, которая может способствовать рекомбинации, и они часто встречаются в точках разрыва дупликации у растений и млекопитающих. [2]
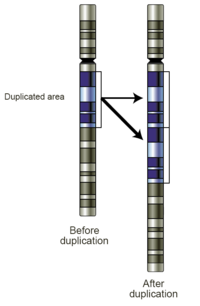
Проскальзывание репликации — это ошибка в репликации ДНК, которая может приводить к дупликациям коротких генетических последовательностей. Во время репликации ДНК-полимераза начинает копировать ДНК. В какой-то момент процесса репликации полимераза отделяется от ДНК, и репликация останавливается. Когда полимераза снова присоединяется к цепи ДНК, она выравнивает реплицирующую цепь в неправильном положении и случайно копирует один и тот же участок более одного раза. Проскальзывание репликации также часто облегчается повторяющимися последовательностями, но требует всего нескольких оснований сходства. [ необходима цитата ]
Ретротранспозоны , в основном L1 , могут иногда воздействовать на клеточную мРНК. Транскрипты подвергаются обратной транскрипции в ДНК и вставляются в случайное место генома, создавая ретрогены. Полученная последовательность обычно не содержит интронов и часто содержит поли(А)-последовательности, которые также интегрированы в геном. Многие ретрогены демонстрируют изменения в регуляции генов по сравнению с их родительскими генными последовательностями, что иногда приводит к новым функциям. Ретрогены могут перемещаться между различными хромосомами, формируя хромосомную эволюцию. [3]
Анеуплоидия происходит, когда нерасхождение в одной хромосоме приводит к аномальному числу хромосом. Анеуплоидия часто вредна и у млекопитающих регулярно приводит к спонтанным абортам (выкидышам). Некоторые анеуплоидные особи жизнеспособны, например, трисомия 21 у людей, которая приводит к синдрому Дауна . Анеуплоидия часто изменяет дозировку генов способами, которые пагубны для организма; поэтому маловероятно, что она распространится в популяции.
Полиплоидия , или дупликация всего генома, является продуктом нерасхождения во время мейоза, что приводит к появлению дополнительных копий всего генома. Полиплоидия распространена среди растений, но она также наблюдалась у животных, с двумя раундами дупликации всего генома ( событие 2R ) в линии позвоночных, ведущей к человеку. [4] Она также наблюдалась у дрожжей-гемиаскомицетов ~100 млн лет назад. [5] [6]
После дупликации целого генома наступает относительно короткий период нестабильности генома, обширной потери генов, повышенных уровней замены нуклеотидов и перестройки регуляторной сети. [7] [8] Кроме того, значительную роль играют эффекты дозировки генов. [9] Таким образом, большинство дубликатов теряются в течение короткого периода, однако значительная часть дубликатов выживает. [10] Интересно, что гены, участвующие в регуляции, преимущественно сохраняются. [11] [12] Более того, сохранение регуляторных генов, в первую очередь генов Hox , привело к адаптивным инновациям.
Быстрая эволюция и функциональная дивергенция наблюдались на уровне транскрипции дублированных генов, обычно за счет точечных мутаций в коротких мотивах связывания факторов транскрипции. [13] [14] Кроме того, быстрая эволюция мотивов фосфорилирования белков, обычно встроенных в быстро развивающиеся внутренне неупорядоченные области, является еще одним фактором, способствующим выживанию и быстрой адаптации/неофункционализации дублированных генов. [15] Таким образом, по-видимому, существует связь между регуляцией генов (по крайней мере на посттрансляционном уровне) и эволюцией генома. [15]
Полиплоидия также является хорошо известным источником видообразования, поскольку потомство, имеющее разное количество хромосом по сравнению с родительскими видами, часто неспособно скрещиваться с неполиплоидными организмами. Считается, что дупликации всего генома менее пагубны, чем анеуплоидия, поскольку относительная дозировка отдельных генов должна быть одинаковой.

Сравнение геномов показывает, что дупликации генов распространены у большинства исследованных видов. На это указывают переменные числа копий ( вариации числа копий ) в геноме людей [16] [17] или плодовых мушек. [18] Однако было трудно измерить скорость, с которой происходят такие дупликации. Недавние исследования дали первую прямую оценку скорости дупликации генов по всему геному у C. elegans , первого многоклеточного эукариота, для которого такая оценка стала доступна. Скорость дупликации генов у C. elegans составляет порядка 10−7 дупликаций /ген/поколение, то есть в популяции из 10 миллионов червей у одного будет дупликация гена на поколение. Эта скорость на два порядка больше, чем спонтанная скорость точечной мутации на нуклеотидный участок у этого вида. [19] Более ранние (косвенные) исследования сообщали о локус-специфических показателях дупликации у бактерий, дрозофилы и людей в диапазоне от 10−3 до 10−7 / ген/поколение. [20] [21] [22]
Генные дупликации являются важным источником генетической новизны, которая может привести к эволюционным инновациям. Дупликация создает генетическую избыточность, где вторая копия гена часто свободна от селективного давления — то есть ее мутации не оказывают пагубного воздействия на организм-хозяин. Если одна копия гена испытывает мутацию, которая влияет на ее первоначальную функцию, вторая копия может служить «запасной частью» и продолжать правильно функционировать. Таким образом, дублированные гены накапливают мутации быстрее, чем функциональный ген с одной копией, на протяжении поколений организмов, и возможно, что одна из двух копий разовьет новую и иную функцию. Некоторые примеры такой неофункционализации — это очевидная мутация дублированного пищеварительного гена в семействе ледяных рыб в ген антифриза и дупликация, приводящая к новому гену змеиного яда [23] и синтез 1 бета-гидрокситестостерона у свиней. [24]
Считается, что дупликация генов играет важную роль в эволюции ; эта позиция поддерживается членами научного сообщества уже более 100 лет. [25] Сусуму Оно был одним из самых известных разработчиков этой теории в своей классической книге «Эволюция путем дупликации генов» (1970). [26] Оно утверждал, что дупликация генов является самой важной эволюционной силой с момента появления универсального общего предка . [27] Крупные события дупликации генома могут быть довольно распространенными. Считается, что весь геном дрожжей подвергся дупликации около 100 миллионов лет назад. [28] Растения являются самыми плодовитыми дупликаторами генома. Например, пшеница является гексаплоидом (разновидностью полиплоида ), что означает, что у нее есть шесть копий ее генома.
Другая возможная судьба для дублирующихся генов заключается в том, что обе копии одинаково свободны накапливать дегенеративные мутации, пока любые дефекты дополняются другой копией. Это приводит к нейтральной « субфункционализации » (процесс конструктивной нейтральной эволюции ) или модели DDC (дублирование-дегенерация-комплементация), [29] [30] , в которой функциональность исходного гена распределяется между двумя копиями. Ни один из генов не может быть потерян, поскольку оба теперь выполняют важные не избыточные функции, но в конечном итоге ни один из них не может достичь новой функциональности.
Субфункционализация может происходить посредством нейтральных процессов, в которых мутации накапливаются без каких-либо вредных или полезных эффектов. Однако в некоторых случаях субфункционализация может происходить с явными адаптивными преимуществами. Если ген предка является плейотропным и выполняет две функции, часто ни одна из этих двух функций не может быть изменена без воздействия на другую функцию. Таким образом, разделение функций предка на два отдельных гена может обеспечить адаптивную специализацию подфункций, тем самым обеспечивая адаптивное преимущество. [31]
Часто возникающая геномная вариация приводит к неврологическим расстройствам, зависящим от дозы гена, таким как синдром Ретта и болезнь Пелицеуса-Мерцбахера . [32] Такие вредные мутации, скорее всего, будут утрачены из популяции и не сохранятся или не разовьют новые функции. Однако многие дупликации на самом деле не являются вредными или полезными, и эти нейтральные последовательности могут быть утрачены или могут распространяться в популяции посредством случайных колебаний посредством генетического дрейфа .
Два гена, которые существуют после события дупликации гена, называются паралогами и обычно кодируют белки со схожей функцией и/или структурой. Напротив, ортологичные гены, присутствующие в разных видах, каждый из которых изначально произошел от одной и той же предковой последовательности. (См. Гомология последовательностей в генетике ).
Важно (но часто трудно) различать паралоги и ортологи в биологических исследованиях. Эксперименты по функции генов человека часто можно проводить на других видах , если гомолог гена человека может быть найден в геноме этого вида, но только если гомолог является ортологичным. Если они являются паралогами и возникли в результате дупликации гена, их функции, вероятно, будут слишком разными. Одна или несколько копий дуплицированных генов, составляющих семейство генов, могут быть затронуты вставкой транспонируемых элементов , что вызывает значительные различия между ними в их последовательности и в конечном итоге может стать причиной дивергентной эволюции . Это также может сделать шансы и скорость генной конверсии между гомологами дубликатов генов из-за меньшего или отсутствующего сходства в их последовательностях.
Паралоги могут быть идентифицированы в отдельных геномах посредством сравнения последовательностей всех аннотированных моделей генов друг с другом. Такое сравнение может быть выполнено на транслируемых аминокислотных последовательностях (например, BLASTp, tBLASTx) для идентификации древних дупликаций или на последовательностях нуклеотидов ДНК (например, BLASTn, megablast) для идентификации более поздних дупликаций. Большинство исследований для идентификации дупликаций генов требуют взаимных лучших совпадений или нечетких взаимных лучших совпадений, где каждый паралог должен быть единственным лучшим совпадением другого в сравнении последовательностей. [33]
Большинство генных дупликаций существуют в виде низкокопийных повторов (LCR), довольно высокоповторяющихся последовательностей, таких как мобильные элементы. Они в основном встречаются в перицентрономных , субтеломерных и интерстициальных областях хромосомы. Многие LCR из-за своего размера (>1 Кб), сходства и ориентации очень восприимчивы к дупликациям и делециям.
Такие технологии, как геномные микрочипы , также называемые массивом сравнительной геномной гибридизации (массив CGH), используются для обнаружения хромосомных аномалий, таких как микродупликации, в высокопроизводительном режиме из образцов геномной ДНК. В частности, технология ДНК- микрочипов может одновременно контролировать уровни экспрессии тысяч генов во многих обработках или экспериментальных условиях, что значительно облегчает эволюционные исследования регуляции генов после дупликации генов или видообразования . [34] [35]
Генные дупликации также могут быть идентифицированы с помощью платформ секвенирования следующего поколения. Самый простой способ идентифицировать дупликации в данных геномного ресеквенирования — это использование прочтений парного конца. Тандемные дупликации определяются парами прочтений секвенирования, которые отображаются в аномальных ориентациях. Благодаря сочетанию увеличенного покрытия последовательностей и аномальной ориентации картирования можно идентифицировать дупликации в данных геномного секвенирования.
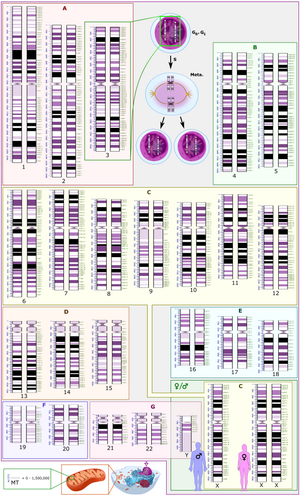
Международная система цитогеномной номенклатуры человека (ISCN) — это международный стандарт номенклатуры хромосом человека , который включает в себя названия полос, символы и сокращенные термины, используемые при описании хромосом человека и аномалий хромосом. Сокращения включают dup для дупликации частей хромосомы. [36] Например, dup(17p12) вызывает болезнь Шарко-Мари-Тута типа 1A. [37]
Генная дупликация не обязательно представляет собой долгосрочное изменение в геноме вида. Фактически, такие изменения часто не сохраняются после первоначального организма-хозяина. С точки зрения молекулярной генетики , амплификация гена является одним из многих способов, с помощью которых ген может быть сверхэкспрессирован . Генетическая амплификация может происходить искусственно, как при использовании метода полимеразной цепной реакции для амплификации коротких цепей ДНК in vitro с использованием ферментов , или она может происходить естественным образом, как описано выше. Если это естественная дупликация, она все равно может происходить в соматической клетке , а не в клетке зародышевой линии (что было бы необходимо для долгосрочного эволюционного изменения).
Дупликации онкогенов являются распространенной причиной многих типов рака . В таких случаях генетическая дупликация происходит в соматической клетке и влияет только на геном самих раковых клеток, а не на весь организм, не говоря уже о каком-либо последующем потомстве. Недавняя комплексная классификация на уровне пациента и количественная оценка драйверных событий в когортах TCGA показали, что в среднем на опухоль приходится 12 драйверных событий, из которых 1,5 являются амплификациями онкогенов. [38]
Полногеномные дупликации также часто встречаются при раке, обнаруживаясь в 30–36 % опухолей наиболее распространенных типов рака. [40] [41] Их точная роль в канцерогенезе неясна, но в некоторых случаях они приводят к потере сегрегации хроматина, что приводит к изменениям конформации хроматина, которые в свою очередь приводят к онкогенным эпигенетическим и транскрипционным модификациям. [42]