Кислородная токсичность — это состояние, возникающее в результате вредного воздействия дыхания молекулярным кислородом ( O
2) при повышенных парциальных давлениях . Тяжелые случаи могут привести к повреждению и гибели клеток , причем последствия чаще всего наблюдаются в центральной нервной системе, легких и глазах. Исторически состояние центральной нервной системы называлось эффектом Пола Берта , а состояние легких — эффектом Лоррейна Смита , в честь исследователей, которые были пионерами открытий и описаний в конце 19 века. Кислородная токсичность является проблемой для подводных дайверов , тех, кто получает высокие концентрации дополнительного кислорода, а также тех, кто проходит гипербарическую кислородную терапию .
Результатом дыхания при увеличении парциального давления кислорода является гипероксия — избыток кислорода в тканях организма. На организм воздействуют по-разному в зависимости от типа воздействия. Токсичность центральной нервной системы вызвана кратковременным воздействием высокого парциального давления кислорода при давлении, превышающем атмосферное. Легочная и глазная токсичность возникает в результате длительного воздействия повышенного уровня кислорода при нормальном давлении. Симптомы могут включать дезориентацию, проблемы с дыханием и изменения зрения, такие как близорукость . Длительное воздействие парциального давления кислорода выше нормального или более короткое воздействие очень высокого парциального давления может вызвать окислительное повреждение клеточных мембран , коллапс альвеол в легких, отслоение сетчатки и судороги . Кислородную токсичность можно контролировать путем снижения воздействия повышенного уровня кислорода. Исследования показывают, что в долгосрочной перспективе возможно надежное восстановление после большинства видов кислородной токсичности.
Протоколы предотвращения последствий гипероксии существуют в областях, где кислород вдыхается при более высоких, чем обычно, парциальных давлениях, включая подводное плавание с использованием сжатых дыхательных газов , гипербарическую медицину, уход за новорожденными и полеты человека в космос . Эти протоколы привели к увеличению редкости судорог из-за кислородного отравления, при этом повреждение легких и глаз в значительной степени ограничивается проблемами ведения недоношенных детей.
В последние годы кислород стал доступен для рекреационного использования в кислородных барах . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предупредило тех, у кого есть такие заболевания, как болезни сердца или легких, не использовать кислородные бары. Аквалангисты используют дыхательные газы, содержащие до 100% кислорода, и должны пройти специальную подготовку по использованию таких газов.
Последствия кислородной токсичности можно классифицировать по пораженным органам, выделяя три основные формы: [2] [3] [4]
Кислородное отравление центральной нервной системы может вызывать судороги, короткие периоды ригидности, за которыми следуют судороги и потеря сознания, и это вызывает беспокойство у дайверов, которые сталкиваются с давлением, превышающим атмосферное. Легочная кислородная токсичность приводит к повреждению легких, вызывая боль и затруднение дыхания. [2] Окислительное повреждение глаз может привести к близорукости или частичной отслойке сетчатки . Повреждения легких и глаз чаще всего возникают при введении дополнительного кислорода в рамках лечения, особенно у новорожденных, но также могут вызывать беспокойство во время гипербарической оксигенотерапии. [5] [6]
Окислительное повреждение может произойти в любой клетке организма, но первоочередной проблемой будет воздействие на три наиболее восприимчивых органа. Это также может быть связано с повреждением эритроцитов ( гемолиз ), [7] [8] печени , [ 9] сердца , [10] эндокринных желез ( надпочечников , половых желез и щитовидной железы ), [11] [12] [13] или почки , [14] и общее повреждение клеток . [2] [15]
В необычных обстоятельствах может наблюдаться воздействие на другие ткани: предполагается, что во время космического полета высокие концентрации кислорода могут способствовать повреждению костей. [16] Гипероксия также может косвенно вызывать наркоз углекислого газа у пациентов с заболеваниями легких, такими как хроническая обструктивная болезнь легких или с угнетением центрального дыхания. [16] Гипервентиляция атмосферного воздуха при атмосферном давлении не вызывает кислородной токсичности, поскольку воздух на уровне моря имеет парциальное давление кислорода 0,21 бар (21 кПа), тогда как токсичность не возникает ниже 0,3 бар (30 кПа). [17]
Кислородная токсичность центральной нервной системы проявляется в виде таких симптомов, как изменения зрения (особенно туннельное зрение ), звон в ушах ( шум в ушах ), тошнота , подергивание (особенно лица), изменения поведения (раздражительность, беспокойство , спутанность сознания) и головокружение . За этим может последовать тонико-клонический припадок, состоящий из двух фаз: происходит интенсивное сокращение мышц в течение нескольких секунд (тоническая фаза); с последующими быстрыми спазмами с попеременным расслаблением и сокращением мышц, вызывающими судорожные подергивания ( клоническая фаза). Приступ заканчивается периодом потери сознания ( постиктальное состояние ). [18] [19] Начало приступа зависит от парциального давления кислорода в дыхательном газе и продолжительности воздействия. Однако время воздействия до начала заболевания непредсказуемо, поскольку тесты показали большие различия как среди отдельных людей, так и у одного и того же человека изо дня в день. [18] [20] [21] Кроме того, многие внешние факторы, такие как погружение под воду, воздействие холода и физические упражнения, сокращают время появления симптомов со стороны центральной нервной системы. [1] Снижение толерантности тесно связано с задержкой углекислого газа . [22] [23] [24] Другие факторы, такие как темнота и кофеин , повышают толерантность у подопытных животных, но эти эффекты не были доказаны на людях. [25] [26]
Воздействие кислорода под давлением более 0,5 бар, например, во время дайвинга, предварительного дыхания кислородом перед полетом или гипербарической терапии, связано с появлением симптомов легочной токсичности. [27] Симптомы легочной токсичности возникают в результате воспаления, которое начинается в дыхательных путях, ведущих к легким, а затем распространяется в легкие ( трахеобронхиальное дерево ). Симптомы появляются в верхней части грудной клетки ( подгрудинной и каринальной областях). [28] [29] [30] Это начинается с легкого щекотания при вдохе и переходит в частый кашель. [28] Если дыхание с повышенным парциальным давлением кислорода продолжается, субъекты испытывают легкое жжение при вдохе, а также неконтролируемый кашель и периодическую одышку ( одышку ). [28] Физикальные данные, связанные с легочной токсичностью, включали пузырящиеся звуки, слышимые через стетоскоп (пузырящиеся хрипы ), лихорадку и увеличение притока крови к слизистой оболочке носа ( гиперемия слизистой оболочки носа ). [30] Первоначально наблюдается экссудативная фаза, приводящая к отеку легких. При гистологическом исследовании можно увидеть увеличение ширины интерстициального пространства. [27] Рентгенограммы легких показывают незначительные изменения в краткосрочной перспективе, но длительное воздействие приводит к увеличению диффузного затемнения в обоих легких. [28] Показатели функции легких снижаются, о чем свидетельствует уменьшение количества воздуха, которое могут удерживать легкие ( жизненная емкость ), а также изменения функции выдоха и эластичности легких. [30] [31] Диффузионная способность легких снижается, что в конечном итоге приводит к гипоксемии. [27] Испытания на животных показали различия в толерантности, аналогичные тем, которые наблюдаются при токсичности для центральной нервной системы, а также значительные различия между видами. Когда воздействие кислорода при давлении выше 0,5 бар (50 кПа) носит прерывистый характер, это позволяет легким восстановиться и задерживает наступление токсичности. [32] Подобная прогрессия характерна для всех видов млекопитающих. [27] Если смерть от гипоксемии не наступила после воздействия в течение нескольких дней, наступает пролиферативная фаза, развивающаяся хроническое утолщение альвеолярной мембраны и снижение диффузионной способности легких. Эти изменения в основном обратимы при возвращении к нормоксии, но время, необходимое для полного выздоровления, неизвестно. [27]
У недоношенных детей признаки поражения глаз ( ретинопатия недоношенных , или РН) наблюдаются с помощью офтальмоскопа в виде разграничения васкуляризированных и неваскуляризированных областей сетчатки младенца. Степень этого разграничения используется для обозначения четырех стадий: (I) разграничение представляет собой линию; (II) демаркация становится гребнем; (III) вокруг гребня происходит рост новых кровеносных сосудов; (IV) сетчатка начинает отслаиваться от внутренней стенки глаза ( сосудистой оболочки ). [5]
Кислородная токсичность вызвана гипероксией, воздействием кислорода при парциальном давлении, превышающем то, которому обычно подвергается организм. Это происходит в трех основных ситуациях: подводное плавание, [33] гипербарическая кислородная терапия, [34] и предоставление дополнительного кислорода в отделениях интенсивной терапии, [35] и при длительном лечении хронических заболеваний, особенно у недоношенных детей. [36] В каждом случае факторы риска заметно различаются. [33] [34] [36]
При нормальном или пониженном давлении окружающей среды эффекты гипероксии первоначально ограничиваются легкими, которые подвергаются непосредственному воздействию, но после длительного воздействия или при гипербарическом давлении другие органы могут подвергаться риску. При нормальном парциальном давлении вдыхаемого кислорода большая часть кислорода, переносимого кровью, переносится гемоглобином, но количество растворенного кислорода увеличивается при парциальном давлении артериального кислорода, превышающем 100 миллиметров ртутного столба (0,13 бар), когда насыщение оксигемоглобина почти полный. При более высоких концентрациях эффекты гипероксии более распространены в тканях организма за пределами легких. [37]
Воздействие в течение от нескольких минут до нескольких часов парциального давления кислорода выше примерно 1,6 бар (160 кПа ) — примерно в восемь раз превышающего нормальное атмосферное парциальное давление — обычно связано с кислородным отравлением центральной нервной системы и чаще всего встречается у пациентов, перенесших гипербарическую терапию. кислородная терапия и водолазы. Поскольку атмосферное давление на уровне моря составляет около 1 бар (100 кПа), токсичность для центральной нервной системы может возникнуть только в гипербарических условиях, когда давление окружающей среды превышает нормальное. [34] [38] Дайверы, дышащие воздухом на глубине более 60 м (200 футов), сталкиваются с возрастающим риском «удара» кислородной токсичности (припадка). Дайверы, вдыхающие газовую смесь, обогащенную кислородом, такую как найтрокс , также увеличивают риск приступа на меньшей глубине, если они опускаются ниже максимальной рабочей глубины, принятой для смеси. [39] Токсичность ЦНС усугубляется высоким парциальным давлением углекислого газа, стрессом, усталостью и холодом, которые гораздо более вероятны при дайвинге, чем при гипербарической терапии. [40]
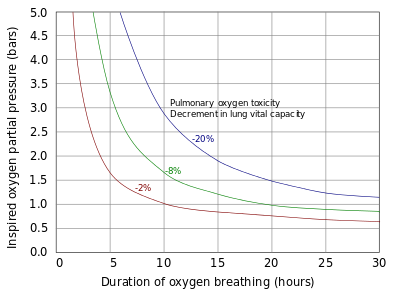
Легкие и остальная часть дыхательных путей подвергаются воздействию самой высокой концентрации кислорода в организме человека и поэтому являются первыми органами, проявляющими токсичность. Легочная токсичность возникает только при воздействии парциального давления кислорода более 0,5 бар (50 кПа), что соответствует доле кислорода 50% при нормальном атмосферном давлении. Самые ранние признаки легочной токсичности начинаются с признаков трахеобронхита или воспаления верхних дыхательных путей после бессимптомного периода от 4 до 22 часов при содержании кислорода более 95% [41] , при этом некоторые исследования показывают, что симптомы обычно начинаются примерно через 14 часов при этот уровень кислорода. [42]
При парциальном давлении кислорода от 2 до 3 бар (от 200 до 300 кПа) — 100% кислорода при давлении, в 2–3 раза превышающем атмосферное — эти симптомы могут начаться уже через 3 часа после воздействия кислорода. [41] Эксперименты на крысах, вдыхающих кислород при давлении от 1 до 3 бар (от 100 до 300 кПа), позволяют предположить, что легочные проявления кислородной токсичности могут быть не такими же в нормобарических условиях, как и в гипербарических условиях. [43] Признаки снижения функции легких, измеренные с помощью функционального тестирования легких, могут возникнуть уже через 24 часа непрерывного воздействия 100% кислорода, [42] с признаками диффузного альвеолярного повреждения и началом острого респираторного дистресс-синдрома, обычно возникающего после 48 часов на 100% кислороде. [41] Вдыхание 100% кислорода также в конечном итоге приводит к коллапсу альвеол ( ателектазу ) , в то время как — при том же парциальном давлении кислорода — присутствие значительного парциального давления инертных газов, обычно азота, предотвратит этот эффект. [44]
Известно, что недоношенные новорожденные подвергаются более высокому риску развития бронхолегочной дисплазии при длительном воздействии высоких концентраций кислорода. [45] К другим группам повышенного риска кислородной токсичности относятся пациенты, находящиеся на искусственной вентиляции легких с уровнем воздействия кислорода более 50%, а также пациенты, подвергшиеся воздействию химических веществ, повышающих риск кислородной токсичности, таких как химиотерапевтический агент блеомицин . [42] Таким образом, действующие рекомендации для пациентов на искусственной вентиляции легких в отделениях интенсивной терапии рекомендуют поддерживать концентрацию кислорода менее 60%. [41] Аналогичным образом, дайверы, проходящие лечение от декомпрессионной болезни, подвергаются повышенному риску кислородной токсичности, поскольку лечение влечет за собой длительные периоды дыхания кислородом в гипербарических условиях в дополнение к любому воздействию кислорода во время погружения. [34]
Длительное воздействие высоких вдыхаемых фракций кислорода вызывает повреждение сетчатки . [46] [47] [48] Повреждение развивающегося глаза у младенцев, подвергшихся воздействию высокой фракции кислорода при нормальном давлении, имеет другой механизм и эффект, чем повреждение глаз, которое испытывают взрослые дайверы в гипербарических условиях. [49] [50] Гипероксия может быть фактором, способствующим развитию заболевания, называемого ретролентальной фиброплазией или ретинопатией недоношенных (РН) у младенцев. [49] [51] У недоношенных детей сетчатка часто не полностью васкуляризирована. Ретинопатия недоношенных возникает, когда развитие сосудистой сети сетчатки задерживается, а затем протекает аномально. С ростом этих новых сосудов связана фиброзная ткань (рубцовая ткань), которая может сокращаться, вызывая отслоение сетчатки. Дополнительное воздействие кислорода, хотя и является фактором риска , не является основным фактором риска развития этого заболевания. Ограничение использования дополнительного кислорода не обязательно снижает частоту ретинопатии недоношенных и может повысить риск системных осложнений, связанных с гипоксией. [49]
Гипероксическая близорукость наблюдалась у дайверов с кислородным ребризером замкнутого цикла при длительном воздействии. [50] [52] [53] Это также часто встречается у тех, кто проходит повторную гипербарическую оксигенотерапию. [47] [54] Это происходит из-за увеличения преломляющей силы хрусталика , поскольку показания осевой длины и кератометрии не выявляют роговичную или продольную основу миопического сдвига. [54] [55] Обычно со временем это обратимо. [47] [54]
Возможным побочным эффектом гипербарической оксигенотерапии является начальное или дальнейшее развитие катаракты , которая представляет собой увеличение помутнения хрусталика глаза, что снижает остроту зрения и может в конечном итоге привести к слепоте. Это редкое явление, связанное с воздействием повышенной концентрации кислорода на протяжении всей жизни, и о нем может быть занижено, поскольку оно развивается очень медленно. Причина не до конца ясна, но данные свидетельствуют о том, что повышенный уровень кислорода может вызвать ускоренное ухудшение состояния стекловидного тела из-за разрушения кристаллинов хрусталика за счет поперечных связей, образующих агрегаты, способные рассеивать свет. Это может быть конечным развитием более часто наблюдаемого миопического сдвига, связанного с гипербарическим лечением. [6]

Биохимической основой токсичности кислорода является частичное восстановление кислорода одним или двумя электронами с образованием активных форм кислорода, [56] которые являются естественными побочными продуктами нормального метаболизма кислорода и играют важную роль в передаче сигналов в клетках . [57] Один вид, вырабатываемый организмом, супероксид- анион ( O−
2), [58], возможно, участвует в приобретении железа. [59] Более высокие, чем обычно, концентрации кислорода приводят к повышению уровня активных форм кислорода. [60] Кислород необходим для клеточного метаболизма, и кровь доставляет его ко всем частям тела. Когда кислород вдыхается при высоком парциальном давлении, гипероксическое состояние быстро распространяется, при этом наиболее васкуляризированные ткани становятся наиболее уязвимыми. Во время экологического стресса уровни активных форм кислорода могут резко возрасти, что может повредить клеточные структуры и вызвать окислительный стресс . [21] [61]
Хотя все механизмы реакции этих видов в организме еще полностью не изучены, [62] одним из наиболее реактивных продуктов окислительного стресса является гидроксильный радикал ( ·OH ), который может инициировать повреждающую цепную реакцию перекисного окисления липидов в организме. ненасыщенные липиды клеточных мембран . [63] Высокие концентрации кислорода также увеличивают образование других свободных радикалов , таких как оксид азота , пероксинитрит и триоксидан , которые повреждают ДНК и другие биомолекулы. [21] [64] Хотя в организме имеется множество антиоксидантных систем, таких как глутатион , которые защищают от окислительного стресса, эти системы в конечном итоге перегружаются при очень высоких концентрациях свободного кислорода, и скорость повреждения клеток превышает возможности систем, которые предотвращают или восстановить его. [65] [66] [67] В результате происходит повреждение клеток и их гибель. [68]
Диагностика кислородного отравления центральной нервной системы у дайверов до припадка затруднена, поскольку симптомы нарушения зрения, проблем с ушами, головокружения, спутанности сознания и тошноты могут быть вызваны многими факторами, общими для подводной среды, такими как наркоз , заложенность носа и холод. Однако эти симптомы могут быть полезны при диагностике первых стадий кислородной токсичности у пациентов, подвергающихся гипербарической оксигенотерапии. В любом случае, если в анамнезе нет эпилепсии или тесты не указывают на гипогликемию , приступ, возникающий в условиях дыхания кислородом при парциальном давлении более 1,4 бар (140 кПа), предполагает диагноз кислородной токсичности. [69]
Диагностика бронхолегочной дисплазии у новорожденных с затрудненным дыханием в первые несколько недель затруднена. Однако если за это время дыхание ребенка не улучшится, для подтверждения бронхолегочной дисплазии можно использовать анализы крови и рентгенологическое исследование . Кроме того, эхокардиограмма может помочь исключить другие возможные причины, такие как врожденные пороки сердца или легочная артериальная гипертензия . [70]
Диагноз ретинопатии недоношенных у новорожденных обычно предполагает клиническая ситуация. Недоношенность, низкий вес при рождении и воздействие кислорода в анамнезе являются основными показателями, хотя наследственные факторы не выявили закономерности. [71]
Клинический диагноз может быть подтвержден уровнем кислорода в артериальной крови. [40] Ряд других состояний можно спутать с кислородным отравлением, в том числе: [40]

Предотвращение кислородной токсичности полностью зависит от условий. Как под водой, так и в космосе, надлежащие меры предосторожности могут устранить самые пагубные последствия. Недоношенным детям обычно требуется дополнительный кислород для лечения осложнений преждевременных родов. В этом случае профилактику бронхолегочной дисплазии и ретинопатии недоношенных необходимо проводить без ущерба для обеспечения кислородом, достаточного для сохранения жизни ребенка. [72]
Токсичность кислорода представляет собой катастрофическую опасность при подводном плавании с аквалангом , поскольку припадок приводит к высокому риску смерти в результате утопления. [39] [73] Приступ может возникнуть внезапно и без каких-либо предупреждающих симптомов. [19] Последствиями являются внезапные судороги и потеря сознания, во время которых жертвы могут потерять регулятор и утонуть. [74] [75] Одним из преимуществ полнолицевой маски для дайвинга является предотвращение потери регулятора в случае приступа. Ремни, удерживающие мундштук, — относительно недорогая альтернатива с аналогичной, но менее эффективной функцией. [73] Поскольку существует повышенный риск кислородной токсичности центральной нервной системы при глубоких, длительных погружениях и погружениях с использованием богатых кислородом дыхательных газов, дайверов учат рассчитывать максимальную рабочую глубину для дыхательных газов , богатых кислородом , и баллонов. содержащие такие смеси, должна быть четко обозначена такая глубина. [24] [76]
Риск судорог, по-видимому, зависит от дозы – кумулятивной комбинации парциального давления и продолжительности. Порог парциального давления кислорода, ниже которого никогда не возникают судороги, не установлен и может зависеть от многих переменных, некоторые из которых являются личными. Риск для конкретного человека может значительно варьироваться в зависимости от индивидуальной чувствительности, уровня физических упражнений и задержки углекислого газа, на которую влияет работа дыхания. [73]
На некоторых курсах подготовки дайверов по режимам дайвинга, при которых воздействие может достигать уровней со значительным риском, дайверов учат планировать и контролировать так называемые «кислородные часы» своих погружений. [76] Это условный будильник, который тикает быстрее при повышенном давлении кислорода и настроен на активацию при максимальном пределе однократного воздействия, рекомендованном в Руководстве по дайвингу Национального управления океанических и атмосферных исследований . [24] [76] Для следующих парциальных давлений кислорода предельные значения составляют: 45 минут при 1,6 бар (160 кПа), 120 минут при 1,5 бар (150 кПа), 150 минут при 1,4 бар (140 кПа), 180 минут при 1,3 бар (130 кПа) и 210 минут при 1,2 бар (120 кПа), но невозможно с какой-либо достоверностью предсказать, возникнут ли симптомы токсичности и когда они возникнут. [77] [78] Многие дайв-компьютеры с поддержкой найтрокса рассчитывают кислородную нагрузку и могут отслеживать ее во время нескольких погружений. Цель состоит в том, чтобы избежать активации сигнала тревоги за счет снижения парциального давления кислорода в дыхательном газе или за счет сокращения времени, затрачиваемого на дыхание газом с более высоким парциальным давлением кислорода. Поскольку парциальное давление кислорода увеличивается с увеличением доли кислорода в дыхательном газе и глубины погружения, дайвер получает больше времени на кислородных часах, погружаясь на меньшую глубину, вдыхая менее богатый кислородом газ или сокращение продолжительности воздействия газов, богатых кислородом. [79] [80] Эту функцию обеспечивают некоторые декомпрессионные компьютеры для технического дайвинга, а также оборудование для управления и мониторинга ребризеров. [81] [82]
Погружение на глубину ниже 56 м (184 футов) на воздухе подвергает дайвера возрастающей опасности кислородного отравления, поскольку парциальное давление кислорода превышает 1,4 бар (140 кПа), поэтому следует использовать газовую смесь, содержащую менее 21% кислорода (так называемый гипоксическая смесь). Увеличивать долю азота нецелесообразно, так как это приведет к образованию сильнонаркотической смеси . Однако гелий не является наркотическим средством, и пригодную к использованию смесь можно смешивать либо путем полной замены азота гелием (полученная смесь называется гелиоксом ), либо путем замены части азота гелием, получая тримикс . [83]
Легочную кислородную токсичность можно полностью предотвратить во время дайвинга. Ограниченная продолжительность и естественный прерывистый характер большинства погружений делают это относительно редким (и даже в этом случае обратимым) осложнением для дайверов. [84] Установленные рекомендации позволяют дайверам рассчитать, когда они подвергаются риску легочной токсичности. [85] [86] [87] При погружениях с насыщением этого можно избежать, ограничив содержание кислорода в газе в жилых помещениях до уровня ниже 0,4 бар. [88]
Целью скрининга с использованием теста на толерантность к кислороду является выявление дайверов с низкой толерантностью к высокому парциальному давлению гипербарического кислорода, которые могут быть более склонны к кислородным судорогам во время водолазных операций или во время гипербарического лечения декомпрессионной болезни. Ценность этого теста была поставлена под сомнение, и статистические исследования показали низкую частоту судорог во время стандартных схем гипербарического лечения, поэтому некоторые военно-морские силы прекратили его использование, хотя другие продолжают требовать прохождения теста для всех кандидатов в дайверы. [89]
Изменчивость толерантности и другие переменные факторы, такие как рабочая нагрузка, привели к тому, что ВМС США отказались от проверки толерантности к кислороду. Из 6250 тестов на толерантность к кислороду, проведенных в период с 1976 по 1997 год, наблюдалось только 6 эпизодов кислородной токсичности (0,1%). [90] [91]
Тест на толерантность к кислороду, используемый ВМС Индии и соответствующий рекомендациям ВМС США и Национального управления океанических и атмосферных исследований США, заключается в вдыхании 100% кислорода, подаваемого через маску BIBS, при атмосферном давлении 2,8 бар абсолютного давления (18 мсв) в течение 30 минут. , в покое в сухой барокамере. Дежурный не может наблюдать никаких симптомов кислородного отравления ЦНС. [89]
Наличие лихорадки или судорог в анамнезе является относительным противопоказанием к лечению гипербарическим кислородом. [92] Схемы лечения декомпрессионной болезни предусматривают периоды дыхания воздухом, а не 100% кислородом (воздушные перерывы), чтобы снизить вероятность судорог или повреждения легких. ВМС США используют таблицы лечения, основанные на периодах чередования 100% кислорода и воздуха. Например, таблица USN 6 требует 75 минут (три периода по 20 минут кислорода/5 минут воздуха) при атмосферном давлении 2,8 стандартных атмосфер (280 кПа), что эквивалентно глубине 18 метров (60 футов). За этим следует медленное снижение давления до 1,9 атм (190 кПа) в течение 30 минут на кислороде. Затем пациент остается под этим давлением еще 150 минут, состоящих из двух периодов по 15 минут воздуха и 60 минут кислорода, прежде чем давление снизится до атмосферного в течение 30 минут на кислороде. [93]
Витамин Е и селен были предложены, но позже отвергнуты как потенциальный метод защиты от токсичности кислорода в легких. [94] [95] [96] Однако есть некоторые экспериментальные данные на крысах о том, что витамин Е и селен помогают предотвратить перекисное окисление липидов и повреждение свободными радикалами in vivo и, следовательно, предотвращают изменения сетчатки после повторяющегося воздействия гипербарического кислорода. [97]
Бронхолегочная дисплазия обратима на ранних стадиях за счет использования периодов перерывов при более низком давлении кислорода, но в конечном итоге она может привести к необратимому повреждению легких, если ей позволить прогрессировать до серьезного повреждения. Чтобы вызвать такое повреждение, необходимы один или два дня воздействия без кислородных перерывов. [16]
Ретинопатию недоношенных в значительной степени можно предотвратить с помощью скрининга. Действующие рекомендации требуют, чтобы все дети с гестационным возрастом менее 32 недель или с массой тела при рождении менее 1,5 кг (3,3 фунта) проходили обследование на ретинопатию недоношенных не реже одного раза в две недели. [98] Национальное совместное исследование, проведенное в 1954 году, показало причинную связь между дополнительным кислородом и ретинопатией недоношенных, но последующее ограничение дополнительного кислорода привело к увеличению младенческой смертности. Чтобы сбалансировать риски гипоксии и ретинопатии недоношенных, современные протоколы теперь требуют мониторинга уровня кислорода в крови у недоношенных детей, получающих кислород. [99]
Тщательное титрование дозировки для минимизации доставляемой концентрации при достижении желаемого уровня оксигенации сведет к минимуму риск кислородного токсичного повреждения и количество кислорода, используемого для долгосрочной терапии. [37] Типичный целевой уровень сатурации кислорода при кислородной терапии находится в диапазоне 91–95% как у доношенных, так и у недоношенных детей. [72]
В средах с низким давлением кислородной токсичности можно избежать, поскольку токсичность вызвана высоким парциальным давлением кислорода, а не высокой долей кислорода. Это иллюстрируется использованием чистого кислорода в скафандрах, которые должны работать при низком давлении, а также высокой долей кислорода и давлением в кабине ниже нормального атмосферного давления в ранних космических кораблях, например, кораблях « Джемини » и «Аполлон» . [100] В таких применениях, как работа вне транспортных средств , кислород с высокой фракцией не токсичен даже при доле дыхательной смеси, приближающейся к 100%, поскольку парциальное давление кислорода не может хронически превышать 0,3 бар (4,4 фунта на квадратный дюйм). [100]


Во время гипербарической оксигенотерапии пациент обычно дышит 100% кислородом через маску, находясь внутри гипербарической камеры с давлением воздуха около 2,8 бар (280 кПа). Приступы во время терапии купируются путем снятия маски с пациента, тем самым снижая парциальное давление вдыхаемого кислорода ниже 0,6 бар (60 кПа). [19]
Припадок под водой требует, чтобы дайвер был поднят на поверхность как можно скорее. Хотя в течение многих лет дайверу рекомендовалось не поднимать дайвера во время самого припадка из-за опасности артериальной газовой эмболии (AGE), [101] есть некоторые свидетельства того, что голосовая щель не полностью перекрывает дыхательные пути. [102] Это привело к тому, что Комитет по дайвингу Общества подводной и гипербарической медицины в настоящее время рекомендует поднимать дайвера во время клонической (судорожной) фазы припадка, если регулятор не находится во рту дайвера, поскольку существует опасность утопления. тогда больше, чем у AGE, но в противном случае подъем следует отложить до конца клонической фазы. [74] Спасатели следят за тем, чтобы их собственная безопасность не подвергалась риску во время судорожной фазы. Затем они проверяют, поддерживается ли подача воздуха к пострадавшему, и выполняют контролируемый плавучий подъем . Большинство агентств по обучению дайверов- любителей преподают подъем бессознательного тела как продвинутый навык, а для профессиональных дайверов это базовый навык, поскольку это одна из основных функций дежурного дайвера . При достижении поверхности всегда вызываются службы экстренной помощи, поскольку существует вероятность дальнейших осложнений, требующих медицинской помощи. [103] Если под водой развиваются симптомы, отличные от судорог, дайвер должен немедленно переключиться на газ с более низкой долей кислорода или подняться на меньшую глубину, если это позволяют обязательства по декомпрессии. Если на поверхности имеется камера, рекомендуется использовать поверхностную декомпрессию. ВМС США опубликовали процедуры выполнения декомпрессионных остановок в тех случаях, когда рекомпрессионная камера недоступна немедленно. [104] Некоторые подводные компьютеры пересчитывают требования к декомпрессии для альтернативных смесей при условии, что активирована фактическая настройка газа. [81]
Возникновение симптомов бронхолегочной дисплазии или острого респираторного дистресс-синдрома лечат снижением доли вводимого кислорода, сокращением периодов воздействия и увеличением перерывов в подаче нормального воздуха. Если для лечения другого заболевания требуется дополнительный кислород (особенно у младенцев), может потребоваться аппарат искусственной вентиляции легких , чтобы гарантировать, что легочная ткань остается раздутой. Снижение давления и воздействия будет производиться постепенно, и могут использоваться такие лекарства, как бронхолитики и легочные сурфактанты . [105]
Дайверы контролируют риск повреждения легких, ограничивая воздействие до уровней, которые, как показывают экспериментальные данные, в целом приемлемы, используя систему единиц накопленной токсичности кислорода , которая основана на времени воздействия при определенных парциальных давлениях. В случае неотложной помощи при декомпрессионной болезни может потребоваться превышение нормальных пределов воздействия, чтобы справиться с более серьезными симптомами. [33]
Ретинопатия недоношенных может регрессировать спонтанно, но если заболевание прогрессирует сверх порогового значения (определяемого как пять последовательных или восемь совокупных часов ретинопатии недоношенных 3 стадии ), как было показано, как криохирургия , так и лазерная хирургия снижают риск слепоты в качестве исхода. Если заболевание прогрессирует дальше, такие методы, как пломбирование склеры и витрэктомия , могут помочь повторно прикрепить сетчатку. [106]
Повторяющееся воздействие потенциально токсичных концентраций кислорода в дыхательном газе довольно распространено при гипербарической активности, особенно в гипербарической медицине , погружениях с насыщением , подводных средах обитания и повторяющихся декомпрессионных погружениях . Исследования Национального управления океанических и атмосферных исследований (НОАА), проведенные Р. У. Гамильтоном и другими, определили приемлемые уровни воздействия для однократного и многократного воздействия. Делается различие между допустимым воздействием острой и хронической токсичности, но на самом деле это крайности возможного непрерывного диапазона воздействия. Можно провести дальнейшее различие между обычным воздействием и воздействием, необходимым для неотложной помощи, когда более высокий риск кислородной токсичности может быть оправдан для снижения более серьезных травм, особенно в относительно безопасной контролируемой и контролируемой среде. [33] [93]
Метод Repex (повторяющееся воздействие), разработанный в 1988 году, позволяет рассчитывать дозу токсичности кислорода с использованием значения разовой дозы, эквивалентной 1 минуте воздействия 100% кислорода при атмосферном давлении, называемого единицей толерантности к кислороду (OTU), и используется для предотвращения токсичного воздействия. эффекты в течение нескольких дней оперативного воздействия. Некоторые дайв-компьютеры автоматически отслеживают дозировку на основе измеренной глубины и выбранной газовой смеси. Пределы допускают большее облучение, если человек в последнее время не подвергался облучению, а суточная допустимая доза уменьшается с увеличением числа последовательных дней воздействия. [33] Эти значения могут не полностью поддерживаться текущими данными. [107]
В более позднем предложении используется простое уравнение мощности: индекс токсичности (TI) = t 2 × P O 2 c , где t — время, а c — степенной член. Это значение было получено на основе химических реакций с образованием активных форм кислорода или азота и, как было показано, дает хорошие прогнозы токсичности для ЦНС при c = 6,8 и легочной токсичности при c = 4,57. [107]
Для легочной токсичности время указывается в часах, а P O 2 в абсолютной атмосфере, TI должен быть ограничен 250.
Для токсичности ЦНС время указано в минутах, P O 2 в абсолютной атмосфере, а TI 26,108 указывает на риск 1%.
Хотя судороги, вызванные кислородным отравлением центральной нервной системы, могут привести к случайным травмам жертвы, в течение многих лет оставалось неясным, может ли произойти повреждение нервной системы после припадка, и в нескольких исследованиях был проведен поиск доказательств такого повреждения. Обзор этих исследований, проведенный Биттерманом в 2004 году, пришел к выводу, что после удаления дыхательного газа, содержащего высокие доли кислорода, долгосрочных неврологических повреждений от приступа не остается. [21] [108]
У большинства младенцев, выживших после перенесенной бронхолегочной дисплазии, в конечном итоге восстанавливается почти нормальная функция легких, поскольку легкие продолжают расти в течение первых 5–7 лет, а повреждения, вызванные бронхолегочной дисплазией, в некоторой степени обратимы (даже у взрослых). ). Однако они, вероятно, будут более восприимчивы к респираторным инфекциям на всю оставшуюся жизнь, и тяжесть последующих инфекций часто выше, чем у их сверстников. [109] [110]
Ретинопатия недоношенных (РН) у младенцев часто регрессирует без вмешательства, и в последующие годы зрение может нормализоваться. Если заболевание достигло стадий, требующих хирургического вмешательства, результаты лечения РН 3-й стадии обычно хорошие, но гораздо хуже — на более поздних стадиях. Хотя хирургическое вмешательство обычно успешно восстанавливает анатомию глаза, повреждение нервной системы при прогрессировании заболевания приводит к сравнительно плохим результатам восстановления зрения. Наличие других осложняющих заболеваний также снижает вероятность благоприятного исхода. [111]
Обеспечение дополнительного кислорода по-прежнему имеет жизненно важное значение в условиях интенсивной терапии и может увеличить выживаемость при некоторых хронических состояниях, но гипероксия и образование активных форм кислорода участвуют в патогенезе некоторых опасных для жизни заболеваний. Токсические эффекты гипероксии особенно распространены в легочном отделе, а при возникновении сосудистых изменений подвергаются риску мозговое и коронарное кровообращение. Длительная гипероксия вредит иммунным реакциям, повышается восприимчивость к инфекционным осложнениям и повреждению тканей. [37]
Частота токсичности центральной нервной системы среди дайверов снизилась со времен Второй мировой войны, поскольку были разработаны протоколы, ограничивающие воздействие и парциальное давление вдыхаемого кислорода. В 1947 году Дональд рекомендовал ограничить глубину дыхания чистым кислородом до 7,6 м (25 футов), что соответствует парциальному давлению кислорода 1,8 бар (180 кПа). [112] Со временем этот предел был снижен, и сегодня обычно рекомендуется предел в 1,4 бар (140 кПа) во время рекреационных погружений и 1,6 бар (160 кПа) во время неглубоких декомпрессионных остановок, [113] хотя военные дайверы используют кислородные ребризеры. могут работать на большей глубине в течение ограниченного периода времени, подвергаясь большему риску. [114] Токсичность кислорода в настоящее время стала редким явлением, за исключением тех случаев, когда она вызвана неисправностью оборудования или человеческой ошибкой. Исторически сложилось так, что ВМС США усовершенствовали таблицы по воздуху и газовым смесям в Руководстве по дайвингу ВМФ, чтобы уменьшить количество случаев отравления кислородом. Согласно отчетам, в период с 1995 по 1999 год было совершено 405 погружений с надводной поддержкой с использованием гелий-кислородных таблиц; из них симптомы кислородного отравления наблюдались при 6 погружениях (1,5%). В результате ВМС США в 2000 году изменили графики и провели полевые испытания 150 погружений, ни одно из которых не выявило симптомов кислородного отравления. Пересмотренные таблицы были опубликованы в 2001 году. [115]
Изменчивость толерантности и другие переменные факторы, такие как рабочая нагрузка, привели к тому, что ВМС США отказались от проверки толерантности к кислороду. Из 6250 тестов на толерантность к кислороду, проведенных в период с 1976 по 1997 год, наблюдалось только 6 эпизодов кислородной токсичности (0,1%). [90] [91]
Кислородная токсичность со стороны ЦНС у пациентов, подвергающихся гипербарической оксигенотерапии, встречается редко и зависит от ряда факторов: индивидуальной чувствительности и протокола лечения; и, возможно, показания к терапии и используемое оборудование. В исследовании Вельслау, проведенном в 1996 году, сообщалось о 16 случаях из 107 264 пациентов (0,015%), тогда как Хэмпсон и Атик в 2003 году обнаружили показатель 0,03%. [116] [117] Йылдыз, Ай и Кырдеди, подведя итоги лечения 36 500 пациентов в период с 1996 по 2003 год, сообщили только о 3 случаях кислородного отравления, что дает показатель 0,008%. [116] Более поздний обзор более 80 000 пациентов, прошедших лечение, выявил еще более низкий показатель: 0,0024%. Снижение заболеваемости может быть частично связано с использованием маски, а не капюшона для подачи кислорода, поскольку в маске меньше мертвого пространства . [118]
Общий риск токсичности ЦНС может достигать 1 на 2000–3000 процедур. но оно варьируется в зависимости от давления и может достигать 1 на 200 при схемах лечения с более высоким давлением от 2,8 до 3,0 ATA или всего 1 на 10 000 для схем лечения с 2 ATA или меньше. [40]
Бронхолегочная дисплазия является одним из наиболее частых осложнений у недоношенных детей, и заболеваемость ею растет по мере увеличения выживаемости глубоко недоношенных детей. Тем не менее, тяжесть заболевания снизилась, поскольку улучшение управления дополнительным кислородом привело к тому, что заболевание теперь связано главным образом с факторами, отличными от гипероксии. [45]
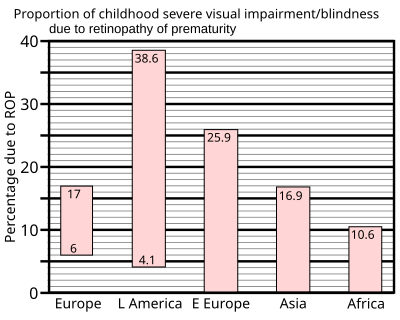
В 1997 г. сводка исследований отделений интенсивной терапии новорожденных в промышленно развитых странах показала, что до 60% детей с низкой массой тела при рождении развивалась ретинопатия недоношенных, которая выросла до 72% у детей с чрезвычайно низкой массой тела при рождении, определенной как менее 1 кг (2,2). фунт) при рождении. Однако тяжелые исходы встречаются гораздо реже: для детей с очень низкой массой тела при рождении (менее 1,5 кг (3,3 фунта) при рождении) частота слепоты составила не более 8%. [36]
Введение дополнительного кислорода широко и эффективно используется в неотложной и интенсивной терапии, но активные формы кислорода, вызванные чрезмерной оксигенацией, имеют тенденцию вызывать порочный круг повреждения тканей, характеризующийся повреждением клеток, гибелью клеток и воспалением, главным образом в легких. , что может усугубить проблемы оксигенации тканей, для лечения которых был предназначен дополнительный кислород. Подобные проблемы могут возникнуть при кислородной терапии хронических состояний, связанных с гипоксией. Тщательное титрование подачи кислорода для сведения к минимуму превышения физиологической потребности также снижает легочную гипероксическую экспозицию до практически осуществимого минимума. [37] Частота легочных симптомов кислородной токсичности составляет около 5%, и некоторые лекарства могут увеличивать риск, например, химиотерапевтический агент блеомицин. [40]

Токсичность центральной нервной системы была впервые описана Полом Бертом в 1878 году. [119] [120] Он показал, что кислород токсичен для насекомых, паукообразных , многоножек , моллюсков, дождевых червей, грибов, прорастающих семян, птиц и других животных. Токсичность центральной нервной системы можно назвать «эффектом Пола Берта». [16]
Легочная кислородная токсичность была впервые описана Дж. Лоррейном Смитом в 1899 году, когда он отметил токсичность центральной нервной системы и обнаружил в экспериментах на мышах и птицах, что давление 0,43 бар (43 кПа) не оказывает никакого эффекта, а давление кислорода 0,75 бар (75 кПа) вызывает легочную токсичность. раздражитель. [32] Легочную токсичность можно назвать «эффектом Лоррена Смита». [16] Первое зарегистрированное воздействие на человека было предпринято в 1910 году Борнштейном, когда двое мужчин дышали кислородом при давлении 2,8 бар (280 кПа) в течение 30 минут, а он продолжал 48 минут без каких-либо симптомов. В 1912 году у Борнштейна начались судороги в руках и ногах, когда он дышал кислородом под давлением 2,8 бар (280 кПа) в течение 51 минуты. [3] Затем Смит показал, что периодическое воздействие дыхательного газа с меньшим содержанием кислорода позволяет легким восстановиться и задерживает наступление легочной токсичности. [32]
Альберт Р. Бенке и др. в 1935 году первыми наблюдали сужение поля зрения ( туннельное зрение ) при погружениях с давлением от 1,0 бар (100 кПа) до 4,1 бар (410 кПа). [121] [122] Во время Второй мировой войны Дональд и Ярбро и др. провел более 2000 экспериментов по изучению токсичности кислорода для обоснования первоначального использования кислородных ребризеров с замкнутым контуром . [46] [123] Военно-морские водолазы в первые годы дайвинга с кислородным ребризером разработали мифологию о монстре по имени «Кислородный Пит», который скрывался на дне «мокрого горшка» (наполненной водой гипербарической камеры) Адмиралтейского экспериментального водолазного подразделения. ), чтобы поймать неосторожных дайверов. Они назвали приступ кислородного отравления «добрением Пита». [124] [125]
В течение десятилетия после Второй мировой войны Ламбертсен и др. сделали дальнейшие открытия о влиянии дыхания кислородом под давлением и методах профилактики. [126] [127] Их работа по прерывистому воздействию для расширения толерантности к кислороду и по модели прогнозирования легочной кислородной токсичности на основе функции легких являются ключевыми документами в разработке стандартных операционных процедур при дыхании под повышенным давлением кислорода. [128] Работа Ламбертсена, показывающая влияние углекислого газа на сокращение времени до появления симптомов со стороны центральной нервной системы, повлияла на работу от текущих рекомендаций по воздействию до будущих конструкций дыхательных аппаратов . [23] [24] [129]
Ретинопатия недоношенных не наблюдалась до Второй мировой войны, но с появлением дополнительного кислорода в последующее десятилетие она быстро стала одной из основных причин детской слепоты в развитых странах. К 1960 году использование кислорода было признано фактором риска, и его применение было ограничено. Результирующее снижение заболеваемости ретинопатией недоношенных сопровождалось ростом детской смертности и осложнений, связанных с гипоксией . С тех пор более сложный мониторинг и диагностика позволили разработать протоколы использования кислорода, которые направлены на баланс между гипоксическими состояниями и проблемами ретинопатии недоношенных. [36]
Бронхолегочная дисплазия была впервые описана Нортвеем в 1967 году, который описал состояния, при которых может быть поставлен диагноз. [130] Позже это мнение было расширено Банкалари, а в 1988 году Шеннаном, который предположил, что необходимость в дополнительном кислороде на 36 неделе может предсказать долгосрочные результаты. [131] Тем не менее, Палта и др. в 1998 году пришли к выводу, что рентгенологические данные являются наиболее точным предиктором долгосрочных последствий. [132]

Биттерман и др. в 1986 и 1995 годах показали, что темнота и кофеин задерживают наступление изменений электрической активности мозга у крыс. [25] [26] В последующие годы исследования токсичности центральной нервной системы были сосредоточены на методах профилактики и безопасного расширения толерантности. [133] Было показано, что на чувствительность к кислородному отравлению центральной нервной системы влияют такие факторы, как циркадный ритм , лекарства, возраст и пол. [134] [135] [136] [137] В 1988 году Hamilton et al. написал процедуры для Национального управления океанических и атмосферных исследований по установлению пределов воздействия кислорода для операций в среде обитания . [85] [86] [87] Даже сегодня модели прогнозирования легочной кислородной токсичности не объясняют всех результатов воздействия высокого парциального давления кислорода. [138]
Дайверы-любители обычно дышат найтроксом , содержащим до 40% кислорода, тогда как технические дайверы используют чистый кислород или найтрокс, содержащий до 80% кислорода, для ускорения декомпрессии. Дайверы, которые вдыхают больше кислорода, чем воздух (21%), должны быть осведомлены об опасностях кислородного отравления и о том, как управлять этим риском. [76] Чтобы купить найтрокс, дайверу может потребоваться предъявить свидетельство о соответствующей квалификации. [139]
С конца 1990-х годов использование кислорода в рекреационных целях пропагандируется кислородными барами, где клиенты вдыхают кислород через носовую канюлю . Утверждалось, что это снижает стресс, увеличивает энергию и уменьшает последствия похмелья и головных болей, несмотря на отсутствие каких-либо научных доказательств, подтверждающих это. [140] В продаже также есть устройства, которые предлагают «кислородный массаж» и «кислородную детоксикацию» с целью удаления токсинов из организма и уменьшения жировых отложений. [141] Американская ассоциация легких заявила, что «нет никаких доказательств того, что кислород при низких уровнях потока, используемый в барах, может быть опасен для здоровья нормального человека», но Центр оценки и исследования лекарств США предупреждает, что люди с заболеваниями сердца или легких при заболевании необходимо тщательно регулировать дополнительный кислород, и им не следует использовать кислородные бары. [140]
Викторианское общество увлекалось быстро расширяющейся областью науки. В рассказе Жюля Верна « Эксперимент доктора Окса », написанном в 1872 году, одноименный доктор использует электролиз воды для разделения кислорода и водорода. Затем он накачивает чистый кислород по всему городу Кикендоне, в результате чего обычно спокойные жители и их животные становятся агрессивными, а растения быстро растут. Взрыв водорода и кислорода на фабрике доктора Окса завершает его эксперимент. Верн резюмировал свой рассказ, объяснив, что описанные в сказке эффекты кислорода были его собственным изобретением (они никоим образом не подтверждаются эмпирическими данными). [142] В его « С Земли на Луну » есть и краткий эпизод кислородного отравления . [143]
{{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка )(требуется подписка){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite book}}: CS1 maint: неподходящий URL ( ссылка )Следующие внешние сайты содержат ресурсы, посвященные конкретным темам: