Терапия стволовыми клетками использует стволовые клетки для лечения или профилактики заболеваний или состояний. [1] По состоянию на 2024 год [обновлять]единственной одобренной FDA терапией с использованием стволовых клеток является трансплантация гемопоэтических стволовых клеток . [2] [3] Обычно это принимает форму трансплантации стволовых клеток костного мозга или периферической крови , но клетки также могут быть получены из пуповинной крови . Ведутся исследования по разработке различных источников стволовых клеток, а также по применению методов лечения стволовыми клетками нейродегенеративных заболеваний [4] и таких состояний, как диабет и болезни сердца .
Терапия стволовыми клетками стала предметом споров после таких разработок, как способность ученых изолировать и культивировать эмбриональные стволовые клетки , создавать стволовые клетки с помощью переноса ядер соматических клеток и использование ими методов создания индуцированных плюрипотентных стволовых клеток . Эти споры часто связаны с политикой абортов и клонированием человека . Кроме того, попытки вывести на рынок методы лечения, основанные на трансплантации сохраненной пуповинной крови, были спорными.
На протяжении более 90 лет трансплантация гемопоэтических стволовых клеток (ТГСК) использовалась для лечения людей с такими заболеваниями, как лейкемия и лимфома ; это единственная широко практикуемая форма терапии стволовыми клетками. [5] [6] [7] Во время химиотерапии большинство растущих клеток погибают под воздействием цитотоксических агентов. Однако эти агенты не могут отличить лейкемические или неопластические клетки от гемопоэтических стволовых клеток в костном мозге. Это побочный эффект традиционных стратегий химиотерапии, который трансплантация стволовых клеток пытается обратить вспять; здоровый костный мозг донора повторно вводит функциональные стволовые клетки для замены клеток, утраченных в организме хозяина во время лечения. Трансплантированные клетки также генерируют иммунный ответ, который помогает уничтожить раковые клетки; однако этот процесс может зайти слишком далеко, что приведет к реакции «трансплантат против хозяина» — самому серьезному побочному эффекту этого лечения. [8]
Другая терапия стволовыми клетками, называемая Prococvhymal, была условно одобрена в Канаде в 2012 году для лечения острого заболевания «трансплантат против хозяина» у детей, которые не реагируют на стероиды. [9] Это аллогенная стволовая терапия, основанная на мезенхимальных стволовых клетках (МСК), полученных из костного мозга взрослых доноров. МСК очищаются от костного мозга, культивируются и упаковываются, при этом от одного донора получают до 10 000 доз. Дозы хранятся в замороженном виде до тех пор, пока они не понадобятся. [10]
FDA одобрило пять продуктов гемопоэтических стволовых клеток, полученных из пуповинной крови, для лечения заболеваний крови и иммунологических заболеваний. [11]
В 2014 году Европейское агентство по лекарственным средствам рекомендовало одобрить лимбальные стволовые клетки для людей с тяжелым дефицитом лимбальных стволовых клеток из-за ожогов глаз. [12]
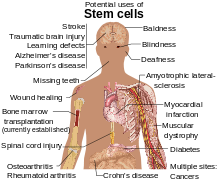
Стволовые клетки изучаются по нескольким причинам. Молекулы и экзосомы, высвобождаемые из стволовых клеток, также изучаются в попытке создания лекарств. [13] В дополнение к функциям самих клеток, было обнаружено, что паракринные растворимые факторы, вырабатываемые стволовыми клетками, известные как секретом стволовых клеток , являются еще одним механизмом, посредством которого терапии на основе стволовых клеток опосредуют свои эффекты при дегенеративных , аутоиммунных и воспалительных заболеваниях. [14]
Большинство стволовых клеток, предназначенных для регенеративной терапии, обычно выделяют либо из костного мозга пациента , либо из жировой ткани . [15] [16] Мезенхимальные стволовые клетки могут дифференцироваться в клетки, из которых состоят кости, хрящи, сухожилия и связки, а также мышечные, нервные и другие ткани-предшественники. Они были основным типом стволовых клеток, изученных при лечении заболеваний, поражающих эти ткани. [17] [18] Количество стволовых клеток, трансплантированных в поврежденную ткань, может изменить эффективность лечения. Соответственно, стволовые клетки, полученные из аспиратов костного мозга, например, культивируются в специализированных лабораториях для расширения до миллионов клеток. [15] [16] Хотя жировая ткань также требует обработки перед использованием, методология культивирования стволовых клеток, полученных из жировой ткани, не такая обширная, как для клеток, полученных из костного мозга. [19] Хотя считается, что стволовые клетки, полученные из костного мозга, предпочтительны для восстановления костей, хрящей, связок и сухожилий, другие полагают, что менее сложные методы сбора и многоклеточная микросреда, уже присутствующая во фракциях стволовых клеток, полученных из жировой ткани, делают последние предпочтительным источником для аутологичной трансплантации. [20]
Изучаются новые источники мезенхимальных стволовых клеток , включая стволовые клетки, присутствующие в коже и дерме, которые представляют интерес из-за простоты, с которой их можно собрать с минимальным риском для животного. [21] Также было обнаружено, что гемопоэтические стволовые клетки перемещаются в кровотоке и обладают такой же способностью к дифференциации, как и другие мезенхимальные стволовые клетки , опять же с помощью очень неинвазивной техники сбора. [22]
В последнее время появился интерес к использованию внеэмбриональных мезенхимальных стволовых клеток . Ведутся исследования по изучению дифференцирующих способностей стволовых клеток, обнаруженных в пуповине, желточном мешке и плаценте различных животных. Считается, что эти стволовые клетки обладают большей дифференцирующей способностью, чем их взрослые аналоги, включая способность более легко формировать ткани энтодермального и эктодермального происхождения. [23]
По состоянию на 2010 год широко разгорелись споры по поводу использования человеческих эмбриональных стволовых клеток . Эти споры в первую очередь направлены на методы, используемые для получения новых линий эмбриональных стволовых клеток , что часто требует разрушения бластоцисты . Противодействие использованию человеческих эмбриональных стволовых клеток в исследованиях часто основано на философских, моральных или религиозных возражениях. [24] Существуют и другие исследования стволовых клеток, которые не предполагают разрушения человеческого эмбриона, и такие исследования включают взрослые стволовые клетки, амниотические стволовые клетки и индуцированные плюрипотентные стволовые клетки.
В январе 2009 года Управление по контролю за продуктами и лекарствами США дало разрешение Geron Corporation на первое клиническое испытание терапии на основе эмбриональных стволовых клеток на людях. Испытание было направлено на оценку препарата GRNOPC1, олигодендроцитных прогениторных клеток, полученных из эмбриональных стволовых клеток , на людях с острой травмой спинного мозга . Испытание было прекращено в ноябре 2011 года, чтобы компания могла сосредоточиться на терапии в «текущих условиях дефицита капитала и неопределенных экономических условий». [25] В 2013 году компания по биотехнологиям и регенеративной медицине BioTime ( AMEX : BTX) приобрела активы Geron по производству стволовых клеток в рамках биржевой сделки с целью возобновления клинического испытания. [26]
Ученые сообщили в 2012 году, что МСК при переливании немедленно в течение нескольких часов после размораживания могут демонстрировать сниженную функцию или демонстрировать сниженную эффективность в лечении заболеваний по сравнению с МСК, которые находятся в логарифмической фазе роста клеток (свежие), поэтому криоконсервированные МСК следует вернуть в логарифмическую фазу роста клеток в культуре in vitro перед введением. Повторное культивирование МСК поможет восстановиться после шока, который клетки получают во время замораживания и размораживания. Различные клинические испытания МСК, в которых использовался криоконсервированный продукт сразу после размораживания, потерпели неудачу по сравнению с теми клиническими испытаниями, в которых использовались свежие МСК. [27]
Возможность выращивать функциональные взрослые ткани неограниченно долго в культуре посредством направленной дифференциации создает новые возможности для исследования лекарственных средств. Исследователи могут выращивать дифференцированные клеточные линии, а затем тестировать новые препараты на каждом типе клеток, чтобы изучить возможные взаимодействия in vitro перед проведением исследований in vivo . Это имеет решающее значение при разработке препаратов для использования в ветеринарных исследованиях из-за возможностей видоспецифических взаимодействий. Есть надежда, что наличие этих клеточных линий, доступных для использования в исследованиях, снизит потребность в использовании подопытных животных, поскольку воздействие на ткани человека in vitro даст понимание, которое обычно не известно до фазы испытаний на животных. [28]
Для использования в исследовательских или лечебных целях необходимо большое количество высококачественных стволовых клеток. Таким образом, необходимо разработать системы культивирования, которые производят чистые популяции тканеспецифичных стволовых клеток in vitro без потери потенциала стволовых клеток. Для этой цели используются два основных подхода: двумерная и трехмерная клеточная культура. [29]
Клеточная культура в двух измерениях регулярно проводилась в тысячах лабораторий по всему миру в течение последних четырех десятилетий. В двухмерных платформах клетки обычно подвергаются воздействию твердой, жесткой плоской поверхности на базальной стороне и жидкости на апикальной поверхности. Заселение такого двухмерного жесткого субстрата требует от выживших клеток резкой адаптации, поскольку у них отсутствует внеклеточный матрикс, который является уникальным для каждого типа клеток, что может изменить метаболизм клетки и снизить ее функциональность. [29]
Трехмерные системы клеточных культур могут создавать биомимикрирующую микросреду для стволовых клеток, напоминающую их родной трехмерный внеклеточный матрикс (ECM). Современные биоматериалы внесли значительный вклад в трехмерные системы клеточных культур в последние десятилетия, и были предложены более уникальные и сложные биоматериалы для улучшения пролиферации стволовых клеток и контролируемой дифференциации. Среди них наноструктурированные биоматериалы представляют особый интерес, поскольку они имеют преимущество высокого отношения поверхности к объему, и они имитируют физические и биологические особенности естественного ECM в наномасштабе. [29]
Считается, что стволовые клетки опосредуют восстановление посредством пяти основных механизмов: 1) оказывают противовоспалительное действие, 2) направляются к поврежденным тканям и привлекают другие клетки, такие как эндотелиальные клетки-предшественники , которые необходимы для роста тканей, 3) поддерживают ремоделирование тканей при образовании рубцов, 4) ингибируют апоптоз и 5) дифференцируются в костную, хрящевую, сухожильную и связочную ткань. [30] [31]
Для дальнейшего улучшения кровоснабжения поврежденных участков и, следовательно, стимулирования регенерации тканей, обогащенная тромбоцитами плазма может использоваться в сочетании с трансплантацией стволовых клеток. [20] [15] Эффективность некоторых популяций стволовых клеток также может зависеть от способа доставки; например, для регенерации кости стволовые клетки часто вводятся в каркас, где они вырабатывают минералы, необходимые для формирования функциональной кости. [20] [15] [32] [16]
Было показано, что стволовые клетки имеют низкую иммуногенность из-за относительно небольшого количества молекул MHC, обнаруженных на их поверхности. Кроме того, было обнаружено, что они секретируют хемокины, которые изменяют иммунный ответ и способствуют толерантности новой ткани. Это позволяет проводить аллогенное лечение без высокого риска отторжения. [23]
Были проведены исследования влияния стволовых клеток на животных моделях дегенерации мозга , таких как болезнь Паркинсона , боковой амиотрофический склероз и болезнь Альцгеймера . [33] [34] [35] Были проведены предварительные исследования, связанные с рассеянным склерозом , [36] [37] [38] и исследование фазы 2 2020 года показало значительное улучшение результатов у пациентов, получавших лечение мезенхимальными стволовыми клетками , по сравнению с теми, кто получал фиктивное лечение. [39] В январе 2021 года FDA одобрило первое клиническое исследование экспериментальной терапии стволовыми клетками для восстановления утраченных клеток мозга у людей с прогрессирующей болезнью Паркинсона. [40]
Здоровый взрослый мозг содержит нейральные стволовые клетки , которые делятся для поддержания общего числа стволовых клеток или становятся клетками-предшественниками . У здоровых взрослых лабораторных животных клетки-предшественники мигрируют в мозге и функционируют в первую очередь для поддержания популяций нейронов для обоняния (чувства запаха). Сообщалось , что фармакологическая активация эндогенных нейральных стволовых клеток вызывает нейропротекцию и поведенческое восстановление в моделях неврологических расстройств у взрослых крыс. [41] [42] [43]
Инсульт и травматическое повреждение мозга приводят к гибели клеток , характеризующейся потерей нейронов и олигодендроцитов в мозге. Были проведены клинические и животные исследования по экспериментальному использованию стволовых клеток в случаях повреждения спинного мозга . [44] [45] [46] [38]
В 2017 году небольшое исследование на людях в возрасте 60 лет и старше с возрастной дряхлостью показало, что после внутривенного лечения мезенхимальными стволовыми клетками (МСК) от здоровых молодых доноров наблюдалось значительное улучшение показателей физической работоспособности. МСК помогают блокировать воспаление, уменьшая его, что приводит к устранению эффектов дряхлости. [47]
В 2012 году стволовые клетки изучались у людей с тяжелыми заболеваниями сердца . [48] Работа Бодо-Эккехарда Штрауера [49] была дискредитирована из-за выявления сотен фактических противоречий. [50] Среди нескольких клинических испытаний, сообщающих о том, что терапия взрослыми стволовыми клетками безопасна и эффективна, фактические доказательства пользы были получены только в нескольких исследованиях. [51] Некоторые предварительные клинические испытания достигли лишь скромных улучшений функции сердца после использования терапии стволовыми клетками костного мозга . [52] [53]
Терапия стволовыми клетками для лечения инфаркта миокарда обычно предполагает использование аутологичных стволовых клеток костного мозга, но могут использоваться и другие типы взрослых стволовых клеток, например, стволовые клетки, полученные из жировой ткани. [54]
Возможные механизмы восстановления включают в себя: [33] генерацию клеток сердечной мышцы, стимуляцию роста новых кровеносных сосудов для заселения поврежденной ткани сердца и секрецию факторов роста .
Специфичность репертуара иммунных клеток человека позволяет человеческому организму защищать себя от быстро адаптирующихся антигенов. Однако иммунная система уязвима к деградации при патогенезе заболевания, и из-за критической роли, которую она играет в общей защите, ее деградация часто оказывается фатальной для организма в целом. Заболевания кроветворных клеток диагностируются и классифицируются с помощью узкой специализации патологии, известной как гематопатология . Специфичность иммунных клеток позволяет распознавать чужеродные антигены, что вызывает дополнительные проблемы в лечении иммунных заболеваний. Идентичные совпадения между донором и реципиентом больше не требуются для успешной трансплантации. Напротив, гаплоидентичные совпадения способствовали многочисленным трансплантациям, учитывая улучшения в посттрансплантационных иммуносупрессивных режимах. [55] Исследования с использованием как кроветворных взрослых стволовых клеток, так и эмбриональных стволовых клеток дали представление о возможных механизмах и методах лечения многих из этих заболеваний. [56]
Полностью зрелые человеческие эритроциты могут быть получены ex vivo гемопоэтическими стволовыми клетками (ГСК), которые являются предшественниками эритроцитов. В этом процессе ГСК выращиваются вместе со стромальными клетками , создавая среду, которая имитирует условия костного мозга, естественного места роста эритроцитов. Добавляется эритропоэтин , фактор роста , побуждающий стволовые клетки завершить терминальную дифференциацию в эритроциты. [57] Дальнейшие исследования этой техники должны иметь потенциальные преимущества для генной терапии, переливания крови и местной медицины.
В 2004 году ученые из Королевского колледжа Лондона открыли способ выращивания целого зуба у мышей [58] и смогли вырастить биоинженерные зубы отдельно в лабораторных условиях. Исследователи уверены, что технология регенерации зубов может быть использована для выращивания живых зубов у людей.
Теоретически, стволовые клетки, взятые у пациента, можно было бы заставить в лаборатории превратиться в зубной зачаток, который при имплантации в десны даст начало новому зубу и, как ожидается, вырастет за время более трех недель. [59] Он срастется с челюстной костью и выделит химические вещества, которые стимулируют нервы и кровеносные сосуды соединяться с ним. Процесс похож на то, что происходит, когда у людей вырастают их собственные взрослые зубы. Однако еще предстоит решить много проблем, прежде чем стволовые клетки смогут стать выбором для замены отсутствующих зубов в будущем. [60] [61]
Хеллер сообщил об успешном выращивании волосковых клеток улитки с использованием эмбриональных стволовых клеток . [62]
В обзоре 2019 года, посвященном регенерации слуха и регенеративной медицине, было установлено, что стволовые клетки-предшественники слуховых рецепторов обладают потенциалом для значительного улучшения слуха. [63]
С 2003 года исследователи успешно пересаживали стволовые клетки роговицы в поврежденные глаза для восстановления зрения. «Листы клеток сетчатки, используемые командой, собираются из абортированных плодов, что некоторые люди считают нежелательным». Когда эти листы пересаживаются на поврежденную роговицу , стволовые клетки стимулируют возобновление восстановления, в конечном итоге восстанавливая зрение. [64] Последнее подобное развитие событий произошло в июне 2005 года, когда исследователи из больницы королевы Виктории в Сассексе , Англия, смогли восстановить зрение сорока человек, используя ту же технику. Группа под руководством Шераза Дайи смогла успешно использовать взрослые стволовые клетки, полученные от пациента, родственника или даже трупа . Продолжаются дальнейшие раунды испытаний. [65]
Люди с диабетом 1 типа теряют функцию бета-клеток, вырабатывающих инсулин , в поджелудочной железе. В публикации экспериментов 2007 года ученые смогли заставить эмбриональные стволовые клетки превратиться в бета-клетки в лабораторных условиях. Теоретически, если бета-клетки будут успешно пересажены, они смогут заменить неисправные клетки у пациента с диабетом. [66] Однако существуют неблагоприятные эффекты высоких концентраций глюкозы на терапию стволовыми клетками. [67]

По состоянию на 2017 год использование мезенхимальных стволовых клеток (МСК), полученных из взрослых стволовых клеток, находилось на стадии предварительного исследования для потенциального ортопедического применения при травмах костей и мышц, восстановлении хрящей , остеоартрите , хирургии межпозвоночных дисков , хирургии вращательной манжеты плеча и заболеваниях опорно-двигательного аппарата и т. д. [68] Другие области ортопедических исследований для использования МСК включают тканевую инженерию и регенеративную медицину . [68]
Стволовые клетки также могут использоваться для стимуляции роста тканей человека. У взрослого человека раненая ткань чаще всего заменяется рубцовой тканью , которая в коже характеризуется дезорганизованной структурой коллагена, потерей волосяных фолликулов и нерегулярной сосудистой структурой. Однако в случае раненой ткани плода раненая ткань заменяется нормальной тканью посредством активности стволовых клеток. [69] Возможный метод регенерации тканей у взрослых заключается в помещении «семян» взрослых стволовых клеток в тканевую «почву» в раневом ложе и позволении стволовым клеткам стимулировать дифференциацию в клетках тканевого ложа. Этот метод вызывает регенеративный ответ, более похожий на заживление ран плода, чем на образование рубцовой ткани взрослого человека. [69] По состоянию на 2018 год исследователи все еще изучали различные аспекты «почвенной» ткани, которые способствуют регенерации. [69] Из-за общих целебных свойств стволовых клеток они приобрели интерес для лечения кожных ран, таких как рак кожи . [70]
В 2013 году ученые исследовали альтернативный подход к лечению ВИЧ-1/СПИДа, основанный на создании устойчивой к заболеванию иммунной системы путем трансплантации аутологичных, генно-модифицированных (устойчивых к ВИЧ-1) гемопоэтических стволовых и прогениторных клеток (GM-HSPC). [71]
В 2013 году было обнаружено, что исследования аутологичных стволовых клеток костного мозга на желудочковой функции содержат «сотни» несоответствий. [50] Критики сообщают, что из 48 отчетов, по-видимому, использовались только пять основных испытаний, и что во многих случаях, были ли они рандомизированными или просто наблюдательными акцептор-против-отвергателя, были противоречивы между отчетами об одном и том же исследовании. Одна пара отчетов с идентичными исходными характеристиками и окончательными результатами была представлена в двух публикациях как, соответственно, рандомизированное исследование с 578 пациентами и как наблюдательное исследование с 391 субъектом. Другие отчеты требовали (невозможных) отрицательных стандартных отклонений в подгруппах людей или содержали дробные субъекты, отрицательные классы NYHA. В целом, было сообщено о гораздо большем количестве людей, получивших стволовые клетки в испытаниях, чем количество стволовых клеток, обработанных в лаборатории больницы за это время. Университетское расследование, закрытое в 2012 году без отчета, было возобновлено в июле 2013 года. [72]
В 2014 году метаанализ терапии стволовыми клетками с использованием стволовых клеток костного мозга для лечения заболеваний сердца выявил расхождения в опубликованных отчетах клинических испытаний, при этом исследования с большим числом расхождений показали увеличение размеров эффекта. [73] Другой метаанализ, основанный на внутрисубъектных данных 12 рандомизированных испытаний, не смог обнаружить никаких существенных преимуществ терапии стволовыми клетками по первичным конечным точкам, таким как серьезные нежелательные явления или увеличение показателей функции сердца, и пришел к выводу об отсутствии пользы. [74]
Результаты исследования TIME 2018 года, в котором использовался рандомизированный, двойной слепой, плацебо-контролируемый дизайн исследования, пришли к выводу, что «введение мононуклеарных клеток костного мозга не улучшило восстановление функции ЛЖ в течение 2 лет» у людей, перенесших инфаркт миокарда. [75] Соответственно, исследование BOOST-2, проведенное в 10 медицинских центрах Германии и Норвегии, сообщило, что результат исследования «не поддерживает использование ядросодержащих BMC у пациентов с STEMI и умеренно сниженной фракцией выброса ЛЖ». [76] Кроме того, исследование также не достигло никаких других вторичных конечных точек МРТ, [77] что привело к выводу, что внутрикоронарная терапия стволовыми клетками костного мозга не обеспечивает функциональной или клинической пользы. [78]
В 2021 году инъекции стволовых клеток в США стали причиной серьезных инфекций по меньшей мере у 20 пациентов, которым были назначены препараты, полученные из пуповинной крови, продаваемые как «лечение стволовыми клетками». [79] В 2023 году был опубликован случай женщины, которая была инфицирована Mycobacterium abscessus и перенесла менингит после лечения стволовыми клетками рассеянного склероза в коммерческой клинике в Нижней Калифорнии, Мексика. [80]
Исследования, проведенные на лошадях, собаках и кошках, привели к разработке методов лечения стволовыми клетками в ветеринарной медицине, которые могут быть направлены на широкий спектр травм и заболеваний, таких как инфаркт миокарда , инсульт, повреждение сухожилий и связок , остеоартрит , остеохондроз и мышечная дистрофия , как у крупных животных, так и у людей. [81] [82] [83] [84] Хотя исследования клеточной терапии в целом отражают медицинские потребности человека, высокая степень частоты и тяжести определенных травм у скаковых лошадей вывела ветеринарную медицину на передний план этого нового регенеративного подхода. [85] Домашние животные могут служить клинически значимыми моделями, которые точно имитируют человеческие заболевания. [86] [87]
Ветеринарные применения терапии стволовыми клетками как средства регенерации тканей были в значительной степени сформированы исследованиями, которые начались с использования мезенхимальных стволовых клеток, полученных от взрослых, для лечения животных с травмами или дефектами, затрагивающими кости, хрящи, связки и/или сухожилия. [88] [17] [89] Существует две основные категории стволовых клеток, используемых для лечения: аллогенные стволовые клетки, полученные от генетически отличающегося донора в пределах того же вида, [16] [90] и аутологичные мезенхимальные стволовые клетки , полученные от пациента перед использованием в различных методах лечения. [20] Третья категория, ксеногенные стволовые клетки или стволовые клетки, полученные от разных видов, используются в основном в исследовательских целях, особенно для лечения людей. [28]
Кость имеет уникальный и хорошо документированный естественный процесс заживления, которого обычно достаточно для восстановления переломов и других распространенных травм. Неправильно расположенные переломы из-за тяжелой травмы, а также такие методы лечения, как резекция опухоли при раке кости, склонны к неправильному заживлению, если их оставить на самотек. Каркасы, состоящие из натуральных и искусственных компонентов, засеваются мезенхимальными стволовыми клетками и помещаются в дефект. В течение четырех недель после размещения каркаса новообразованная кость начинает интегрироваться со старой костью, и в течение 32 недель достигается полное сращение. [91] Необходимы дальнейшие исследования, чтобы полностью охарактеризовать использование клеточной терапии для лечения переломов костей.
Стволовые клетки использовались для лечения дегенеративных заболеваний костей у собак. Обычно рекомендуемым лечением для собак с болезнью Легга-Кальве-Пертеса является удаление головки бедренной кости после прогрессирования дегенерации. Недавно мезенхимальные стволовые клетки вводили непосредственно в головку бедренной кости, что привело не только к успешной регенерации костей, но и к уменьшению боли. [91]
Лечение травм связок , сухожилий , остеоартрита , остеохондроза и субхондральных костных кист на основе аутологичных стволовых клеток стало коммерчески доступным для практикующих ветеринаров для лечения лошадей с 2003 года в Соединенных Штатах и с 2006 года в Соединенном Королевстве. Лечение травм сухожилий, связок и остеоартрита у собак на основе аутологичных стволовых клеток стало доступно ветеринарам в Соединенных Штатах с 2005 года. Более 3000 лошадей и собак, находящихся в частной собственности, прошли лечение аутологичными стволовыми клетками, полученными из жировой ткани. Эффективность этих методов лечения была показана в двойных слепых клинических испытаниях для собак с остеоартритом бедра и локтя и лошадей с повреждением сухожилий. [92] [93]
Скаковые лошади особенно подвержены травмам сухожилий и связок. Традиционные методы лечения крайне неэффективны в возвращении лошади полного функционального потенциала. Естественное заживление, проводимое с помощью традиционных методов лечения, приводит к образованию фиброзной рубцовой ткани, которая снижает гибкость и полную подвижность суставов. Традиционные методы лечения не позволили большому количеству лошадей вернуться к полной активности, а также имеют высокий уровень повторных травм из-за жесткой природы рубцовых сухожилий. Введение стволовых клеток костного мозга и жировой ткани, наряду с естественным механическим стимулом, способствовало регенерации сухожильной ткани. Естественное движение способствовало выравниванию новых волокон и тендоцитов с естественным выравниванием, обнаруженным в неповрежденных сухожилиях. Лечение стволовыми клетками не только позволило большему количеству лошадей вернуться к полной нагрузке, но и значительно снизило частоту повторных травм в течение трехлетнего периода. [23]
Использование эмбриональных стволовых клеток также применялось для восстановления сухожилий. Было показано, что эмбриональные стволовые клетки имеют лучшую выживаемость в сухожилии, а также лучшую миграционную способность для достижения всех областей поврежденного сухожилия. Общее качество восстановления также было выше, с лучшей архитектурой сухожилия и образованным коллагеном. Также не было отмечено образования опухолей в течение трехмесячного экспериментального периода. Необходимо провести долгосрочные исследования для изучения долгосрочной эффективности и рисков, связанных с использованием эмбриональных стволовых клеток. [23] Аналогичные результаты были получены у мелких животных. [23]
Остеоартрит является основной причиной боли в суставах как у животных, так и у людей. Лошади и собаки чаще всего страдают артритом. Естественная регенерация хряща очень ограничена. Различные типы мезенхимальных стволовых клеток и других добавок все еще исследуются, чтобы найти лучший тип клеток и метод для долгосрочного лечения. [23]
Мезенхимальные клетки , полученные из жировой ткани , в настоящее время чаще всего используются для лечения остеоартрита стволовыми клетками из-за неинвазивного сбора. Это недавно разработанная неинвазивная техника, разработанная для более легкого клинического использования. Собаки, получавшие это лечение, показали большую гибкость суставов и меньшую боль. [94]
Стволовые клетки успешно использовались для улучшения заживления сердца после инфаркта миокарда у собак. Жировые и костномозговые стволовые клетки были извлечены и индуцированы в сердечную клетку перед инъекцией в сердце. Было обнаружено, что сердце улучшило сократимость и уменьшило поврежденную область через четыре недели после применения стволовых клеток. [95]
В 2007 году проводились испытания заплаты из пористого вещества, на которую «высеиваются» стволовые клетки, чтобы вызвать регенерацию тканей при пороках сердца. Ткань регенерировалась, и заплата хорошо встраивалась в сердечную ткань. Считается, что это отчасти связано с улучшением ангиогенеза и уменьшением воспаления. Хотя кардиомиоциты были получены из мезенхимальных стволовых клеток , они, по-видимому, не были сократительными. Другие методы лечения, которые вызывали сердечную судьбу в клетках перед трансплантацией, имели больший успех в создании сократительной сердечной ткани. [96]
Исследования 2018 года, такие как европейский исследовательский проект nTRACK, направлены на демонстрацию того, что мультимодальные наночастицы могут структурно и функционально отслеживать стволовые клетки в терапии регенерации мышц. Идея состоит в том, чтобы маркировать стволовые клетки золотыми наночастицами, которые полностью охарактеризованы на предмет усвоения, функциональности и безопасности. Маркированные стволовые клетки будут вводиться в травмированную мышцу и отслеживаться с помощью систем визуализации. [97] Однако система все еще должна быть продемонстрирована в лабораторных масштабах.
Повреждения спинного мозга являются одной из наиболее распространенных травм, с которыми сталкиваются ветеринарные больницы. [91] Повреждения позвоночника возникают двумя способами после травмы: первичное механическое повреждение и вторичные процессы, такие как воспаление и образование рубцов, в течение нескольких дней после травмы. Эти клетки, участвующие в реакции на вторичное повреждение, выделяют факторы, способствующие образованию рубцов и ингибирующие клеточную регенерацию. Мезенхимальные стволовые клетки , которые индуцируются в нейронную клеточную судьбу, загружаются на пористый каркас и затем имплантируются в место травмы. Клетки и каркас выделяют факторы, противодействующие факторам, выделяемым клетками, формирующими рубцы, и способствующие нейронной регенерации. Восемь недель спустя собаки, получавшие лечение стволовыми клетками, продемонстрировали огромное улучшение по сравнению с теми, кого лечили традиционными методами лечения. Собаки, получавшие лечение стволовыми клетками, могли иногда поддерживать собственный вес, чего не наблюдалось у собак, проходящих традиционное лечение. [98] [99] [100]
В исследовании по оценке лечения экспериментально вызванного рассеянного склероза у собак с использованием активированных лазером нерасширенных жировых стволовых клеток. Результаты показали улучшение клинических признаков с течением времени, подтвержденное разрешением предыдущих поражений на МРТ. Положительная миграция инъецированных клеток к месту поражения, повышенная ремиелинизация, обнаруженная основными белками миелина, положительная дифференциация в олигодендроциты, положительные по Olig2, предотвратили образование глиальных рубцов и восстановили аксональную архитектуру. [38]
Методы лечения также проходят клинические испытания по восстановлению и регенерации периферических нервов. Периферические нервы чаще повреждаются, но последствия повреждения не так распространены, как при травмах спинного мозга. Методы лечения в настоящее время проходят клинические испытания по восстановлению разорванных нервов, с ранним успехом. Стволовые клетки, индуцированные к нейронной судьбе, вводятся в разорванный нерв. В течение четырех недель наблюдалась регенерация ранее поврежденных стволовых клеток и полностью сформированных нервных пучков. [21]
Стволовые клетки также находятся в клинических фазах для лечения в офтальмологии. Гемопоэтические стволовые клетки использовались для лечения язв роговицы различного происхождения у нескольких лошадей. Эти язвы были устойчивы к обычным доступным методам лечения, но быстро реагировали положительно на лечение стволовыми клетками. Стволовые клетки также смогли восстановить зрение в одном глазу лошади с отслоением сетчатки, что позволило лошади вернуться к повседневной деятельности. [22]
Стволовые клетки изучаются для использования в усилиях по сохранению. Сперматогониальные стволовые клетки были собраны у крысы и помещены в хозяина-мышь, и были получены полностью зрелые сперматозоиды со способностью производить жизнеспособное потомство. В настоящее время ведутся исследования по поиску подходящих хозяев для введения донорских сперматогониальных стволовых клеток. Если это станет жизнеспособным вариантом для защитников природы, сперма может быть получена от особей с высоким генетическим качеством, которые умирают до достижения половой зрелости, сохраняя линию, которая в противном случае была бы потеряна. [101]
В конце 1990-х и начале 2000-х годов появилась первая волна компаний и клиник, предлагающих терапию стволовыми клетками, не подкрепляя при этом заявления о пользе для здоровья или не имея одобрения регулирующих органов. [102] К 2012 году появилась вторая волна компаний и клиник, обычно расположенных в развивающихся странах, где медицина менее регулируема, и предлагающих терапию стволовыми клетками по модели медицинского туризма . [ 103] [104] Как и компании и клиники первой волны, они сделали схожие сильные, но необоснованные заявления, в основном клиники в Соединенных Штатах, Мексике, Таиланде, Индии и Южной Африке . [103] [104] К 2016 году исследования показали, что только в США насчитывалось более 550 клиник стволовых клеток, которые продавали в целом непроверенные методы лечения широкого спектра заболеваний почти в каждом штате страны, [105] изменив динамику туризма стволовыми клетками . В 2018 году FDA направило предупредительное письмо в StemGenex Biologic Laboratories в Сан-Диего, которая предлагала услугу, в рамках которой она брала жир у людей, перерабатывала его в смеси, содержащие, по ее словам, различные формы стволовых клеток, и вводила их обратно человеку путем ингаляции, внутривенного введения или инфузии в спинной мозг; компания заявила, что такое лечение полезно при многих хронических и опасных для жизни состояниях. [106]
Одной из распространенных маркетинговых тактик является регистрация на ClinicalTrials.gov , базе данных правительства США для клинических испытаний. Регистрация исследования уведомляет агентство, но не доказывает, что рассмотрение имело место. Регистрация в FDA также не доказывает, что одобрение было предоставлено. [107]
Стоимость терапии стволовыми клетками сильно варьируется в зависимости от клиники, состояния и типа клеток, но чаще всего составляет от 10 000 до 20 000 долларов США. [108] Страхование не покрывает инъекции стволовых клеток в клиниках, поэтому пациенты часто прибегают к онлайн-сбору средств. [109] В 2018 году Федеральная торговая комиссия США обнаружила, что медицинские центры и отдельный врач делают необоснованные заявления о терапии стволовыми клетками и принудительно вернули около 500 000 долларов США. [110] Примерно в то же время FDA подало иск против двух фирм, занимающихся лечением стволовыми клетками, требуя постоянного запрета на маркетинг и использование ими неодобренных продуктов из жировых стволовых клеток. [111]
Хотя, по данным NIH, ни одно лечение стволовыми клетками не было одобрено для COVID-19 , и агентство не рекомендует использовать МСК для лечения этого заболевания, [112] некоторые клиники стволовых клеток начали продавать как непроверенные, так и не одобренные FDA стволовые клетки и экзосомы для COVID-19 в 2020 году. [113] FDA приняло оперативные меры, отправив письма указанным фирмам. [114] [115] FTC также предупредила фирму, занимающуюся стволовыми клетками, за вводящий в заблуждение маркетинг, связанный с COVID-19. [116] [117]
[118]