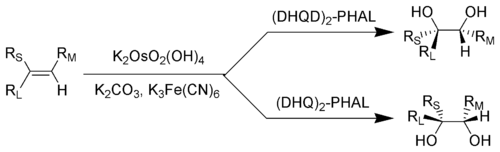
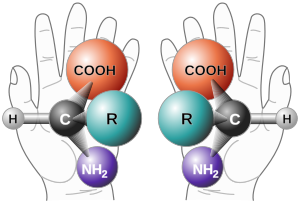
Энантиоселективный синтез , также называемый асимметричным синтезом , [1] является формой химического синтеза . ИЮПАК определяет его как « химическую реакцию (или последовательность реакций), в которой один или несколько новых элементов хиральности образуются в молекуле субстрата и которая приводит к образованию стереоизомерных ( энантиомерных или диастереомерных ) продуктов в неравных количествах ». [2]
Проще говоря: это синтез соединения методом, который способствует образованию определенного энантиомера или диастереомера. Энантиомеры — это стереоизомеры, имеющие противоположные конфигурации в каждом хиральном центре. Диастереомеры представляют собой стереоизомеры, которые различаются по одному или нескольким хиральным центрам.
Энантиоселективный синтез — ключевой процесс в современной химии и особенно важен в области фармацевтики , поскольку разные энантиомеры или диастереомеры молекулы часто обладают разной биологической активностью .
Многие строительные блоки биологических систем, такие как сахара и аминокислоты, производятся исключительно в виде одного энантиомера . В результате живые системы обладают высокой степенью химической хиральности и часто по-разному реагируют с различными энантиомерами данного соединения. Примеры такой избирательности включают в себя:
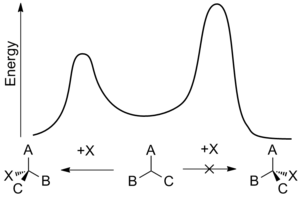
Таким образом, энантиоселективный синтез имеет большое значение, но его также может быть трудно достичь. Энантиомеры обладают одинаковой энтальпией и энтропией и, следовательно, должны производиться в равных количествах в результате ненаправленного процесса, что приводит к образованию рацемической смеси. Энантиоселективный синтез может быть достигнут путем использования хирального свойства, которое благоприятствует образованию одного энантиомера по сравнению с другим посредством взаимодействий в переходном состоянии . Это смещение известно как асимметричная индукция и может включать хиральные свойства в субстрате , реагенте , катализаторе или окружающей среде [9] и работает, делая энергию активации , необходимую для образования одного энантиомера, ниже, чем у противоположного энантиомера. [10]
Энантиоселективность обычно определяется относительными скоростями стадии энантиодифференцировки - точки, в которой один реагент может стать одним из двух энантиомерных продуктов. Константа скорости реакции k является функцией энергии активации реакции, иногда называемой энергетическим барьером , и зависит от температуры. Использование свободной энергии Гиббса энергетического барьера Δ G * означает, что относительная скорость противоположных стереохимических результатов при данной температуре T равна:
Эта температурная зависимость означает, что разница скоростей и, следовательно, энантиоселективность больше при более низких температурах. В результате даже небольшие различия в энергетических барьерах могут привести к заметному эффекту.
Энантиоселективный катализ (традиционно известный как «асимметричный катализ») осуществляется с использованием хиральных катализаторов , которые обычно представляют собой хиральные координационные комплексы . Катализ эффективен для более широкого круга превращений, чем любой другой метод энантиоселективного синтеза. Хиральные металлические катализаторы почти всегда становятся хиральными с использованием хиральных лигандов , но можно генерировать хиральные комплексы с металлом, состоящие полностью из ахиральных лигандов. [11] [12] [13] Большинство энантиоселективных катализаторов эффективны при низких соотношениях субстрат/катализатор. [14] [15] Учитывая их высокую эффективность, они часто подходят для синтеза в промышленных масштабах, даже с дорогими катализаторами. [16] Универсальным примером энантиоселективного синтеза является асимметрическое гидрирование , которое используется для восстановления широкого спектра функциональных групп .

В разработке новых катализаторов преобладает разработка новых классов лигандов . Определенные лиганды, часто называемые « привилегированными лигандами », эффективны в широком спектре реакций; примеры включают BINOL , Salen и BOX . Большинство катализаторов эффективны только для одного типа асимметричной реакции. Например, асимметричное гидрирование Нойори с использованием BINAP/Ru требует β-кетона, хотя другой катализатор, BINAP/диамин-Ru, расширяет область применения до α,β- алкенов и ароматических химических веществ .
Хиральное вспомогательное вещество представляет собой органическое соединение, которое соединяется с исходным материалом с образованием нового соединения, которое затем может подвергаться диастереоселективным реакциям посредством внутримолекулярной асимметричной индукции. [17] [18] В конце реакции вспомогательное вещество удаляют в условиях, которые не вызывают рацемизации продукта. [19] Обычно его затем восстанавливают для использования в будущем.

Хиральные вспомогательные вещества должны использоваться в стехиометрических количествах, чтобы быть эффективными, и требуют дополнительных этапов синтеза для добавления и удаления вспомогательных веществ. Однако в некоторых случаях единственная доступная стереоселективная методология основана на использовании хиральных вспомогательных веществ, и эти реакции, как правило, универсальны и очень хорошо изучены, что обеспечивает наиболее эффективный по времени доступ к энантиомерно чистым продуктам. [18] Кроме того, продукты реакций, направленных на вспомогательные вещества, представляют собой диастереомеры , что позволяет их легко разделять такими методами, как колоночная хроматография или кристаллизация.
В биокатализе для осуществления химических превращений используются биологические соединения, начиная от изолированных ферментов и заканчивая живыми клетками. [20] [21] К преимуществам этих реагентов относятся очень высокая эффективность и специфичность реагента, а также мягкие условия эксплуатации и низкое воздействие на окружающую среду . Биокатализаторы чаще используются в промышленности, чем в академических исследованиях; [22] например, при производстве статинов . [23] Однако высокая специфичность реагента может быть проблемой, поскольку часто требуется проверка широкого спектра биокатализаторов, прежде чем будет найден эффективный реагент.
Органокатализ — это форма катализа , при которой скорость химической реакции увеличивается за счет органического соединения , состоящего из углерода , водорода , серы и других неметаллических элементов. [24] [25] Когда органокатализатор является хиральным , тогда может быть достигнут энантиоселективный синтез; [26] [27] например, ряд реакций образования углерод-углеродных связей становятся энантиоселективными в присутствии пролина , ярким примером является альдольная реакция . [28] В органокатализе часто используются природные соединения и вторичные амины в качестве хиральных катализаторов; [29] они недороги и экологически безопасны , так как не содержат металлов.
Синтез хирального пула - один из самых простых и старых подходов энантиоселективного синтеза. С легкодоступным хиральным исходным материалом манипулируют посредством последовательных реакций, часто с использованием ахиральных реагентов, для получения желаемой целевой молекулы. Это может соответствовать критериям энантиоселективного синтеза, когда создается новый хиральный вид, например, в реакции S N 2 .

Синтез хирального пула особенно привлекателен для целевых молекул, имеющих хиральность, аналогичную относительно недорогому природному строительному блоку, такому как сахар или аминокислота . Однако количество возможных реакций, в которых может участвовать молекула, ограничено, и могут потребоваться извилистые пути синтеза (например, полный синтез осельтамивира ). Этот подход также требует стехиометрического количества энантиочистого исходного материала, который может быть дорогим, если он не встречается в природе.
Два энантиомера молекулы обладают многими одинаковыми физическими свойствами (например, температурой плавления , температурой кипения , полярностью и т. д.) и поэтому ведут себя идентично друг другу. В результате они будут мигрировать с одинаковым R f в тонкослойной хроматографии и иметь одинаковое время удерживания в ВЭЖХ и ГХ . Их ЯМР и ИК спектры идентичны.
Это может очень затруднить определение того, образовался ли в результате процесса один энантиомер (и, что особенно важно, какой это энантиомер), а также затруднить разделение энантиомеров в результате реакции, которая не была 100% энантиоселективной. К счастью, энантиомеры ведут себя по-другому в присутствии других хиральных материалов, и это можно использовать для их разделения и анализа.
Энантиомеры не мигрируют одинаково на хиральных хроматографических средах, таких как кварц или стандартные среды, которые были хирально модифицированы. Это составляет основу хиральной колоночной хроматографии , которую можно использовать в небольших масштабах для анализа с помощью ГХ и ВЭЖХ или в больших масштабах для разделения хирально загрязненных материалов. Однако этот процесс может потребовать большого количества хирального упаковочного материала, который может быть дорогим. Распространенной альтернативой является использование хирального дериватизирующего агента для превращения энантиомеров в диастереомеры почти так же, как и хиральные вспомогательные вещества. Они имеют разные физические свойства и, следовательно, могут быть разделены и проанализированы с использованием обычных методов. В ЯМР-спектроскопии стереоизомеров используются специальные хиральные деривитизирующие агенты, известные как «агенты хирального разделения» , они обычно включают координацию с хиральными комплексами европия, такими как Eu(fod) 3 и Eu(hfc) 3 .
Разделение и анализ компонентов энантиомеров рацемических лекарств или фармацевтических веществ называют хиральным анализом . [30] или энантиоселективный анализ . Наиболее часто используемый метод проведения хирального анализа включает процедуры разделения, в частности методы хиральной хроматографии. [31]
Энантиомерный избыток вещества можно определить и некоторыми оптическими методами. Самый старый метод сделать это — использовать поляриметр для сравнения уровня оптического вращения продукта со «стандартом» известного состава. Также возможно провести ультрафиолетово-видимую спектроскопию стереоизомеров, используя эффект Коттона .
Одним из наиболее точных способов определения хиральности соединения является определение его абсолютной конфигурации методом рентгеновской кристаллографии . Однако это трудоемкий процесс, требующий выращивания подходящего монокристалла .
В 1815 году французский физик Жан-Батист Био показал, что некоторые химические вещества могут вращать плоскость луча поляризованного света — свойство, называемое оптической активностью . [32] Природа этого свойства оставалась загадкой до 1848 года, когда Луи Пастер предположил, что оно имеет молекулярную основу, происходящую из некоторой формы диссимметрии , [33] [34] а термин хиральность был придуман лордом Кельвином год спустя. [35] Происхождение самой киральности было окончательно описано в 1874 году, когда Якобус Хенрикус ван 'т Хофф и Жозеф Ле Бель независимо друг от друга предложили тетраэдрическую геометрию углерода. [36] [37] Структурные модели до этой работы были двумерными, и Ван 'т Хофф и Ле Бель предположили, что расположение групп вокруг этого тетраэдра может определять оптическую активность полученного соединения через то, что стало известно как Правило Ле Бель-ван'т-Гоффа .

В 1894 году Герман Эмиль Фишер изложил концепцию асимметричной индукции ; [39] , в которых он правильно связывал избирательное образование D -глюкозы растениями с влиянием оптически активных веществ, входящих в состав хлорофилла. Фишер также успешно осуществил то, что сейчас будет считаться первым примером энантиоселективного синтеза, путем энантиоселективного удлинения сахаров с помощью процесса, который в конечном итоге стал синтезом Килиани-Фишера . [40]
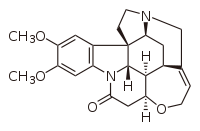
Первый энантиоселективный химический синтез чаще всего приписывают Вилли Марквальду из Берлинского университета за катализируемое бруцином энантиоселективное декарбоксилирование 2-этил-2-метилмалоновой кислоты , о котором сообщалось в 1904 году. была получена форма продукта реакции - 2-метилмасляная кислота; поскольку этот продукт также является природным продуктом — например, в виде боковой цепи ловастатина , образованной его дикетидсинтазой (LovF) во время его биосинтеза [42] — этот результат представляет собой первый зарегистрированный полный синтез с энантиоселективностью, а также другие первые (как Коскинен отмечает, первый «пример асимметричного катализа , энантиотопического отбора и органокатализа »). [38] Это наблюдение также имеет историческое значение, поскольку в то время энантиоселективный синтез можно было понять только с точки зрения витализма . В то время многие выдающиеся химики, такие как Йенс Якоб Берцелиус, утверждали, что природные и искусственные соединения фундаментально различны и что хиральность — это просто проявление «жизненной силы», которая может существовать только в природных соединениях. [43] В отличие от Фишера, Марквальд провел энантиоселективную реакцию на ахиральном, неприродном исходном материале, хотя и с хиральным органокатализатором (как мы теперь понимаем эту химию). [38] [44] [45]
Развитие энантиоселективного синтеза изначально шло медленно, во многом из-за ограниченного набора методов их разделения и анализа. Диастереомеры обладают разными физическими свойствами, что позволяет разделить их обычными способами, однако в то время энантиомеры можно было разделить только путем спонтанного разделения (когда энантиомеры разделяются при кристаллизации) или кинетического разрешения (когда один энантиомер выборочно разрушается). Единственным инструментом для анализа энантиомеров была оптическая активность с использованием поляриметра — метода, который не дает структурных данных.
Реальный прогресс начался только в 1950-х годах. Частично это было обусловлено такими химиками, как Р.Б. Вудворд и Владимир Прелог , но также и разработкой новых методов. Первым из них была рентгеновская кристаллография , которая была использована для определения абсолютной конфигурации органического соединения Йоханнесом Бийвоетом в 1951 году. [46] Хиральная хроматография была введена годом позже Дэлглишем, который использовал бумажную хроматографию для разделения хиральных аминокислот. . [47] Хотя Дэлглиш не был первым, кто наблюдал такое разделение, он правильно объяснил разделение энантиомеров дифференциальным удерживанием хиральной целлюлозы. Это было расширено в 1960 году, когда Клем и Рид впервые сообщили об использовании хирально модифицированного силикагеля для разделения хиральной ВЭЖХ . [48]

Хотя было известно, что разные энантиомеры лекарственного средства могут иметь различную активность, при этом значительная ранняя работа была проведена Артуром Робертсоном Кушни , [49] [50] это не было учтено при разработке и тестировании ранних лекарств. Однако после катастрофы с талидомидом разработка и лицензирование лекарств резко изменились.
Впервые синтезированный в 1953 году, талидомид широко прописывался при утреннем недомогании с 1957 по 1962 год, но вскоре было обнаружено, что он обладает серьезным тератогенным действием [51] и в конечном итоге вызвал врожденные дефекты у более чем 10 000 младенцев. Катастрофа побудила многие страны ввести более жесткие правила тестирования и лицензирования лекарств, такие как Поправка Кефовера-Харриса (США) и Директива 65/65/EEC1 (ЕС).
Ранние исследования тератогенного механизма с использованием мышей показали, что один энантиомер талидомида был тератогенным, в то время как другой обладал всей терапевтической активностью. Позже было показано, что эта теория неверна, и теперь она заменена множеством исследований. [52] Однако это повысило важность хиральности в разработке лекарств, что привело к увеличению количества исследований в области энантиоселективного синтеза.
Правила приоритета Кана-Ингольда-Прелога (часто сокращенно система CIP ) были впервые опубликованы в 1966 году; позволяя более легко и точно описывать энантиомеры. [53] [54] В том же году произошло первое успешное разделение энантиомеров с помощью газовой хроматографии [55], что стало важным достижением, поскольку в то время эта технология широко использовалась.
Энантиоселективный синтез, катализируемый металлами, был впервые разработан Уильямом С. Ноулзом , Рёдзи Ноёри и К. Барри Шарплессом ; за что они получат Нобелевскую премию по химии 2001 года . Ноулз и Нойори начали с разработки метода асимметричного гидрирования , который они разработали независимо в 1968 году. Ноулз заменил ахиральные трифенилфосфиновые лиганды в катализаторе Уилкинсона хиральными фосфиновыми лигандами . Этот экспериментальный катализатор использовался в асимметричном гидрировании с умеренным энантиомерным избытком 15% . Ноулз также был первым, кто применил энантиоселективный металлический катализ для синтеза в промышленных масштабах; Работая в компании Monsanto, он разработал стадию энантиоселективного гидрирования для производства L-ДОФА с использованием лиганда DIPAMP . [56] [57] [58]
Нойори разработал медный комплекс, используя хиральный лиганд основания Шиффа , который он использовал для металл-карбеноидного циклопропанирования стирола . [59] Как и результаты Ноулза, результаты Нойори по энантиомерному избытку этого лиганда первого поколения были разочаровывающе низкими: 6%. Однако продолжающиеся исследования в конечном итоге привели к разработке реакции асимметричного гидрирования Нойори .
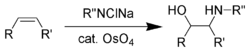
Шарплесс дополнил эти реакции восстановления, разработав ряд асимметричных окислений ( эпоксидирование Шарплесса , [60] асимметричное дигидроксилирование Шарплесса , [61] оксиаминирование Шарплесса [62] ) в 1970-х и 1980-х годах. При этом реакция асимметричного оксиаминирования с использованием тетраоксида осмия является самой ранней.
В тот же период были разработаны методы, позволяющие анализировать хиральные соединения методом ЯМР ; либо с использованием хиральных дериватизирующих агентов, таких как кислота Мошера [63] , либо сдвигающих реагентов на основе европия , из которых Eu(DPM) 3 был самым ранним. [64]
Хиральные вспомогательные вещества были представлены Э. Дж. Кори в 1978 году [65] и заняли видное место в работах Дитера Эндерса . Примерно в то же время был разработан энантиоселективный органокатализ, включающий новаторские работы, в том числе реакцию Хаджоса-Пэрриша-Эдера-Зауэра-Вихерта . Энантиоселективные реакции, катализируемые ферментами, становились все более распространенными в течение 1980-х годов, [66] , особенно в промышленности, [67] с их применением, включая асимметричный гидролиз эфиров эстеразой печени свиньи . Новые технологии генной инженерии позволили адаптировать ферменты к конкретным процессам, что позволило расширить диапазон селективных трансформаций. Например, при асимметричном гидрировании предшественников статинов . [23]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )