Окисление спиртов представляет собой совокупность реакций окисления в органической химии , которые превращают спирты в альдегиды , кетоны , карбоновые кислоты и сложные эфиры , где углерод имеет более высокую степень окисления . Реакция в основном применима к первичным и вторичным спиртам. Вторичные спирты образуют кетоны, а первичные спирты образуют альдегиды или карбоновые кислоты. [1]
Реакция может происходить с использованием различных окислителей.
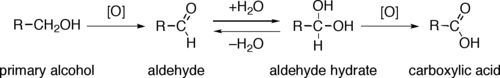
В принципе, простой способ окисления спиртов использует атом кислорода и производит воду: на практике атомы кислорода недоступны, поэтому приведенное выше уравнение является лишь концептуальным. Вместо этого в большинстве процессов окисления используются реагенты на основе оксидов, такие как оксокомплексы металлов , сульфоксиды и оксиды йода.
С помощью различных механизмов удаление гидридного эквивалента превращает первичный или вторичный спирт в альдегид или кетон соответственно. Окисление первичных спиртов до карбоновых кислот обычно протекает через соответствующий альдегид, который при реакции с водой превращается через гидрат альдегида ( гем -диол, R-CH(OH) 2 ). Таким образом, окисление первичного спирта на уровне альдегида без дальнейшего окисления до карбоновой кислоты возможно при проведении реакции в отсутствие воды, так что гидрат альдегида не может образоваться.

Многие реагенты окисляют вторичные спирты до кетонов, а первичные спирты до альдегидов. Аллиловые и бензиловые спирты представляют собой особые случаи. Альдегиды подвержены чрезмерному окислению до карбоновых кислот.

Для этих окислений обычно используются реагенты хрома (VI). В одном семействе реагентов Cr(VI) используется комплекс CrO 3 (пиридин) 2 . [2]
Второе семейство реагентов Cr(VI) представляет собой соли , содержащие катион пиридиния (C 5 H 5 NH + ).
Эти соли менее реакционноспособны, с ними легче обращаться и они более селективны, чем реагент Коллинза, при окислении спиртов.
Вышеупомянутые реагенты представляют собой усовершенствования по сравнению с более старым реагентом Джонса , раствором триоксида хрома в водной серной кислоте .
Периодинан Десса -Мартина является мягким окислителем, способствующим превращению спиртов в альдегиды или кетоны. [4] Реакцию проводят в стандартных условиях, при комнатной температуре, чаще всего в дихлорметане . Реакция длится от получаса до двух часов. Затем продукт отделяют от отработанного периодинана. [5] Разработано множество окислителей на основе йодозила, например IBX .
При окислении Сверна используются оксалилхлорид , диметилсульфоксид и органическое основание, такое как триэтиламин .
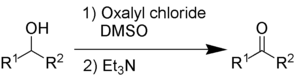
Побочными продуктами являются диметилсульфид (Me 2 S), окись углерода (CO), диоксид углерода (CO 2 ) и – когда в качестве основания используется триэтиламин – хлорид триэтиламмония (C 6 H 15 NHCl).
Этот редко используемый метод взаимно превращает спирты и карбонилы.
В окислении Лей используется NMO в качестве стехиометрического окислителя с перрутенатом тетрапропиламмония в качестве катализатора.
При окислении фетизоном , также редко используемом методе, используется карбонат серебра , нанесенный на целит. Этот реагент действует посредством одноэлектронного окисления катионами серебра.
Другой метод — окисление, катализируемое оксоаммонием .
Кроме того, сообщалось, что гипохлорит натрия (или бытовой отбеливатель) в ацетоне эффективно преобразует вторичные спирты в присутствии первичных спиртов (окисление Стивенса). [6]
растворимые комплексы переходных металлов катализируют окисление спиртов в присутствии дикислорода или другого концевого окислителя. [7]

Соединения, имеющие две гидроксильные группы, расположенные на соседних атомах углерода, то есть вицинальные диолы/1,2- диолы , подвергаются окислительному разрыву связи углерод-углерод с некоторыми окислителями, такими как периодат натрия (NaIO 4 ), (диацетоксииод)бензол (PhI( OAc) 2 ) [8] или тетраацетат свинца (Pb(OAc) 4 ), что приводит к образованию двух карбонильных групп. Реакция также известна как расщепление гликоля .

Когда первичный спирт превращается в карбоновую кислоту , концевой атом углерода увеличивает степень окисления на четыре. Прямое окисление первичных спиртов до карбоновых кислот можно проводить с использованием различных реагентов.
Альдегиды легко окисляются реагентами Cr(VI) и Mn(VII) до карбоновых кислот.
Перманганат калия (KMnO 4 ) очень эффективно окисляет первичные спирты до карбоновых кислот. Эту реакцию, впервые подробно описанную Фурнье [9] [10], обычно проводят путем добавления KMnO 4 к раствору или суспензии спирта в водном щелочном растворе. Чтобы реакция протекала эффективно, спирт должен быть хотя бы частично растворен в водном растворе. Этому можно способствовать добавлением органического сорастворителя, такого как диоксан , пиридин , ацетон или t -BuOH . KMnO 4 реагирует со многими функциональными группами , такими как вторичные спирты, 1,2-диолы, альдегиды, алкены, оксимы, сульфиды и тиолы, а также с двойными углерод-углеродными связями. Таким образом, избирательность является проблемой.

Так называемый реактив Джонса , приготовленный из триоксида хрома (CrO 3 ) и водного раствора серной кислоты , окисляет спирты до карбоновой кислоты. Протокол часто дает значительные количества эфиров . [12] Проблемы заключаются в токсичности и экологичности реагента. Описан каталитический вариант, включающий обработку избытком иодной кислоты (H 5 IO 6 ). [13]

Поскольку многие из вышеупомянутых условий окисления первичных спиртов в кислоты являются жесткими и несовместимы с обычными защитными группами, химики-органики часто используют двухстадийную процедуру окисления в кислоты. Спирт окисляется до альдегида с помощью одной из многих описанных выше процедур. Эта последовательность часто используется в синтезе натуральных продуктов, например, при синтезе платенцина. [15]
Четырехокись рутения — агрессивный, редко используемый агент, допускающий мягкие условия реакции.
Окисление Хейнса. [16]
Использование хлоритов в качестве терминальных окислителей в сочетании как с гипохлоритами, так и с ТЕМПО дает карбоновые кислоты без побочных продуктов хлорирования. [17] Реакция обычно проводится в два этапа в одном и том же котле: частичное окисление осуществляется с помощью ТЕМПО и гипохлорита, затем для завершения окисления добавляется хлорит. Наблюдается только первичное окисление спирта. В сочетании с дигидроксилированием Шарплесса этот метод можно использовать для получения энантиочистых α-гидроксикислот. [18]
При окислении по Пиннику используется хлорит натрия . [19]