Оксид цинка — неорганическое соединение формулы ZnO . Это белый порошок, нерастворимый в воде. ZnO используется в качестве добавки во многих материалах и продуктах, включая косметику, пищевые добавки , резину, пластмассу, керамику, стекло, цемент, смазочные материалы, [12] краски, солнцезащитные кремы, мази, клеи, герметики, пигменты, продукты питания, батареи, ферриты, антипирены, полупроводники [13] и ленты для оказания первой помощи. Хотя он встречается в природе в виде минерала цинкита , большая часть оксида цинка производится синтетически. [14]
Соединения цинка, вероятно, использовались древними людьми в обработанной [14] и необработанной форме в качестве краски или медицинской мази, но их состав неизвестен. Использование пушпанджана , вероятно, оксида цинка, в качестве мази для глаз и открытых ран, упоминается в индийском медицинском тексте « Чарака Самхита» , датируемом 500 годом до нашей эры или ранее. [15] Цинкоксидная мазь упоминается также греческим врачом Диоскоридом (I век нашей эры). [16] Гален предложил лечить язвенный рак оксидом цинка, [17] так же, как это сделал Авиценна в своем «Каноне медицины» . Он используется в качестве ингредиента в таких продуктах, как детская присыпка и кремы от опрелостей , крем от каламина , шампуни против перхоти и антисептические мази. [18]
Римляне производили значительные количества латуни (сплава цинка и меди ) еще в 200 г. до н.э. с помощью процесса цементации, при котором медь реагировала с оксидом цинка. [19] Считается, что оксид цинка был получен путем нагревания цинковой руды в шахтной печи. При этом выделялся металлический цинк в виде пара, который затем поднимался по дымоходу и конденсировался в виде оксида. Этот процесс был описан Диоскоридом в I веке нашей эры. [20] Оксид цинка также был обнаружен в цинковых рудниках в Заваре в Индии , датируемых второй половиной первого тысячелетия до нашей эры. [16]
С 12 по 16 века цинк и оксид цинка были признаны и произведены в Индии с использованием примитивной формы процесса прямого синтеза. Из Индии производство цинка в 17 веке переместилось в Китай. В 1743 году в Бристоле , Великобритания, был основан первый в Европе завод по выплавке цинка . [21] Около 1782 года Луи-Бернар Гайтон де Морво предложил заменить пигмент свинцовых белил оксидом цинка. [22]
Оксид цинка (цинковые белила) в основном использовался в красках и в качестве добавки к мазям. Цинковые белила были приняты в качестве пигмента в картинах маслом к 1834 году, но они плохо смешивались с маслом. Эту проблему удалось решить за счет оптимизации синтеза ZnO. В 1845 году Эдм-Жан Леклер в Париже производил масляную краску в больших масштабах, а к 1850 году цинковые белила стали производиться по всей Европе. Успех цинковых белил был обусловлен их преимуществами перед традиционными свинцовыми белилами: цинковые белила практически устойчивы на солнечном свете, не чернеют на серосодержащем воздухе, нетоксичны и более экономичны. Поскольку цинковые белила настолько «чисты», их можно использовать для создания оттенков с другими цветами, но при смешивании с другими цветами они образуют довольно хрупкую сухую пленку. Например, в конце 1890-х и начале 1900-х годов некоторые художники использовали цинковые белила в качестве основы для своих картин маслом. На всех этих картинах с годами появились трещины. [23]
В последнее время большая часть оксида цинка использовалась в резиновой промышленности для защиты от коррозии . В 1970-е годы вторым по величине применением ZnO было фотокопирование . Высококачественный ZnO, произведенный по «французскому процессу», добавляли в фотокопировальную бумагу в качестве наполнителя. Это приложение вскоре было вытеснено титаном . [24]
Чистый ZnO представляет собой белый порошок, но в природе он встречается в виде редкого минерала цинкита , который обычно содержит марганец и другие примеси, придающие цвет от желтого до красного. [25]
Кристаллический оксид цинка термохромен , меняет цвет от белого до желтого при нагревании на воздухе и становится белым при охлаждении. [26] Это изменение цвета вызвано небольшой потерей кислорода в окружающую среду при высоких температурах с образованием нестехиометрического Zn 1 +x O, где при 800 °C x = 0,00007. [26]
Оксид цинка является амфотерным оксидом . Он почти нерастворим в воде, но растворяется в большинстве кислот , таких как соляная кислота: [27]
Твердый оксид цинка также растворяется в щелочах с образованием растворимых цинкатов:
ZnO медленно реагирует с жирными кислотами в маслах с образованием соответствующих карбоксилатов , таких как олеат или стеарат . При смешивании с крепким водным раствором хлорида цинка ZnO образует цементоподобные продукты, которые лучше всего можно описать как гидроксихлориды цинка. [28] Этот цемент использовался в стоматологии. [29]

ZnO также образует цементоподобный материал при обработке фосфорной кислотой ; сопутствующие материалы используются в стоматологии. [29] Основным компонентом цинк-фосфатного цемента, полученного этой реакцией, является гопеит Zn 3 (PO 4 ) 2 ·4H 2 O. [30]
ZnO разлагается на пары цинка и кислород при температуре около 1975 °C и стандартном давлении кислорода. В карботермической реакции нагревание с углеродом превращает оксид в пары цинка при гораздо более низкой температуре (около 950 °C). [27]


Оксид цинка кристаллизуется в двух основных формах : гексагональном вюрците [31] и кубической цинковой обманке . Структура вюрцита наиболее стабильна в условиях окружающей среды и, следовательно, наиболее распространена. Форму цинковой обманки можно стабилизировать, выращивая ZnO на подложках с кубической структурой решетки. В обоих случаях центры цинка и оксида имеют тетраэдрическую форму , наиболее характерную геометрию для Zn(II). ZnO превращается в мотив каменной соли при относительно высоких давлениях около 10 ГПа. [13]
Гексагональные и цинкобманковые полиморфы не обладают инверсионной симметрией (отражение кристалла относительно любой заданной точки не превращает его в себя). Это и другие свойства симметрии решетки приводят к пьезоэлектричности гексагонального и цинковой обманки ZnO, а также пироэлектричеству гексагонального ZnO.
Шестиугольная структура имеет точечную группу 6 мм ( обозначение Германа-Могена ) или C 6v ( обозначение Шенфлиса ), а пространственную группу — P6 3 mc или C 6v 4 . Постоянные решетки a = 3,25 Å и c = 5,2 Å; их соотношение с/а ~ 1,60 близко к идеальному значению для шестиугольной ячейки с/а = 1,633. [32] Как и в большинстве материалов групп II-VI , связь в ZnO в основном ионная (Zn 2+ O 2- ) с соответствующими радиусами 0,074 нм для Zn 2+ и 0,140 нм для O 2- . Это свойство объясняет преимущественное образование вюрцита, а не структуры цинковой обманки [33] , а также сильную пьезоэлектричность ZnO. Из-за полярных связей Zn-O плоскости цинка и кислорода электрически заряжены. Чтобы сохранить электрическую нейтральность, эти плоскости реконструируются на атомном уровне в большинстве родственных материалов, но не в ZnO — его поверхности атомарно плоские, стабильные и не демонстрируют никакой реконструкции. [34] Однако исследования с использованием вюрцоидных структур объяснили возникновение плоскостности поверхности и отсутствие реконструкции на поверхностях вюрцита ZnO [35] в дополнение к возникновению зарядов на плоскостях ZnO.
ZnO — широкозонный полупроводник II-VI группы полупроводников . Самородное легирование полупроводника за счет кислородных вакансий или междоузельных элементов цинка относится к n-типу. [13]
ZnO — относительно мягкий материал с твердостью примерно 4,5 по шкале Мооса . [12] Его упругие постоянные меньше, чем у соответствующих полупроводников III-V, таких как GaN . Высокая теплоемкость и теплопроводность, низкое тепловое расширение и высокая температура плавления ZnO выгодны для керамики. [24] Оптический фонон E2 в ZnO демонстрирует необычно большое время жизни — 133 пс при 10 К. [36]
Было заявлено, что среди полупроводников с тетраэдрической связью ZnO имеет самый высокий пьезоэлектрический тензор или, по крайней мере, сравнимый с тензором GaN и AlN . [37] Это свойство делает его технологически важным материалом для многих пьезоэлектрических приложений, которые требуют большой электромеханической связи. Таким образом, ZnO в виде тонкой пленки был одним из наиболее изученных резонаторных материалов для тонкопленочных объемных акустических резонаторов .
Благоприятные свойства оксида цинка включают хорошую прозрачность, высокую подвижность электронов , широкую запрещенную зону и сильную люминесценцию при комнатной температуре . Эти свойства делают ZnO ценным для множества новых применений: прозрачные электроды в жидкокристаллических дисплеях , энергосберегающие или теплозащитные окна, а также электроника, например тонкопленочные транзисторы и светодиоды .
ZnO имеет относительно широкую прямую запрещенную зону ~3,3 эВ при комнатной температуре. Преимущества, связанные с широкой запрещенной зоной, включают более высокие напряжения пробоя , способность выдерживать большие электрические поля, более низкий электронный шум , а также работу при высоких температурах и высокой мощности. Ширина запрещенной зоны ZnO может быть дополнительно доведена до ~3–4 эВ путем его легирования оксидом магния или оксидом кадмия . [13] Из-за такой большой запрещенной зоны предпринимались попытки создать прозрачные солнечные элементы с использованием ZnO в качестве светопоглощающего слоя. Однако эти солнечные элементы до сих пор оказались крайне неэффективными. [38]
Большая часть ZnO имеет n -типный характер даже при отсутствии преднамеренного легирования . Нестехиометрия обычно является причиной возникновения характера n-типа, но этот вопрос остается спорным. [39] Было предложено альтернативное объяснение, основанное на теоретических расчетах, что за это ответственны непреднамеренные замещающие примеси водорода. [40] Контролируемое легирование n-типа легко достигается путем замены Zn элементами группы III, такими как Al, Ga, In, или путем замены кислорода элементами группы VII, хлором или йодом . [41]
Надежное легирование ZnO p-типа остается затруднительным. Эта проблема возникает из-за низкой растворимости примесей p-типа и их компенсации обильными примесями n-типа. Эта проблема наблюдается с GaN и ZnSe . Измерение p-типа в «по сути» материале n-типа затруднено неоднородностью образцов. [42]
Текущие ограничения p-легирования ограничивают электронные и оптоэлектронные применения ZnO, которые обычно требуют соединений материалов n-типа и p-типа. Известные легирующие примеси p-типа включают элементы I группы Li, Na, K; элементы V группы N, P и As; а также медь и серебро. Однако многие из них образуют глубокие акцепторы и не производят значительной проводимости p-типа при комнатной температуре. [13]
Подвижность электронов ZnO сильно меняется с температурой и имеет максимум ~2000 см 2 /(В·с) при 80 К. [43] Данные о подвижности дырок немногочисленны и имеют значения в диапазоне 5–30 см 2 /(В·с). с). [44]
Диски ZnO, действующие как варисторы , являются активным материалом в большинстве ограничителей перенапряжения . [45] [46]
Оксид цинка известен своими сильно нелинейными оптическими свойствами, особенно в объеме. Нелинейность наночастиц ZnO можно точно настроить в зависимости от их размера. [47]
Для промышленного использования ZnO производится в объеме 10 5 тонн в год [25] тремя основными процессами: [24]
При непрямом или французском процессе металлический цинк плавится в графитовом тигле и испаряется при температуре выше 907 °C (обычно около 1000 °C). Пары цинка реагируют с кислородом воздуха с образованием ZnO, что сопровождается падением его температуры и ярким свечением. Частицы оксида цинка транспортируются в охлаждающий канал и собираются в рукавном фильтре. Этот непрямой метод был популяризирован Эдмом Жаном Леклером из Парижа в 1844 году и поэтому широко известен как французский процесс. Его продукт обычно состоит из агломерированных частиц оксида цинка со средним размером от 0,1 до нескольких микрометров. По весу большая часть оксида цинка в мире производится по французскому процессу.
Прямой или американский процесс начинается с различных загрязненных цинковых композитов, таких как цинковые руды или побочные продукты плавильных заводов. Прекурсоры цинка восстанавливаются ( карботермическое восстановление ) путем нагревания с источником углерода, таким как антрацит , с образованием паров цинка, которые затем окисляются, как и в непрямом процессе. Из-за более низкой чистоты исходного материала конечный продукт при прямом процессе также имеет более низкое качество по сравнению с непрямым.
В небольшом объеме промышленного производства используются мокрые химические процессы, которые начинаются с водных растворов солей цинка, из которых осаждается карбонат или гидроксид цинка . Твердый осадок затем прокаливают при температуре около 800 °C.

Существует множество специализированных методов производства ZnO для научных исследований и нишевых приложений. Эти методы можно классифицировать по форме получаемого ZnO (объемный, тонкая пленка, нанопроволока ), температуре («низкая», то есть близкая к комнатной температуре, или «высокая», то есть Т ~ 1000 °С), типу процесса (осаждение из паровой фазы). или рост из раствора) и другие параметры.
Крупные монокристаллы (многие кубические сантиметры) можно выращивать методами газового транспорта (осаждение из паровой фазы), гидротермального синтеза , [34] [48] [49] или выращивания из расплава. [7] Однако из-за высокого давления паров ZnO рост из расплава проблематичен. Рост за счет транспорта газа трудно контролировать, поэтому предпочтение отдается гидротермальному методу. [7] Тонкие пленки могут быть получены методами химического осаждения из газовой фазы , металлоорганической эпитаксии из газовой фазы , электроосаждения , импульсного лазерного осаждения , напыления , золь-гель -синтеза, атомно-слоевого осаждения , распылительного пиролиза и т. д.
Обыкновенный белый порошкообразный оксид цинка можно получить в лаборатории электролизом раствора бикарбоната натрия с цинковым анодом. Получают гидроксид цинка и газообразный водород. Гидроксид цинка при нагревании разлагается до оксида цинка:
Наноструктуры ZnO могут быть синтезированы в различных морфологиях, включая нанопроволоки, наностержни , тетраподы, наноремни, наноцветы, наночастицы и т. д. Наноструктуры могут быть получены большинством вышеупомянутых методов при определенных условиях, а также методом пар-жидкость-твердое тело. . [34] [50] [51] Синтез обычно проводится при температуре около 90 °C в эквимолярном водном растворе нитрата цинка и уротропина , причем последний обеспечивает основную среду. Некоторые добавки, такие как полиэтиленгликоль или полиэтиленимин, могут улучшить соотношение сторон нанопроволок ZnO. [52] Легирование нанопроволок ZnO было достигнуто путем добавления нитратов других металлов в ростовой раствор. [53] Морфологию получаемых наноструктур можно регулировать, изменяя параметры, относящиеся к составу прекурсора (например, концентрация цинка и pH) или к термической обработке (например, температура и скорость нагрева). [54]
Выровненные нанопроволоки ZnO на предварительно посеянных подложках из кремния , стекла и нитрида галлия были выращены с использованием водных солей цинка, таких как нитрат цинка и ацетат цинка, в основных средах. [55] Предварительное засев подложек ZnO создает места для гомогенного зарождения кристаллов ZnO во время синтеза. Обычные методы предварительного посева включают термическое разложение кристаллитов ацетата цинка на месте , нанесение наночастиц ZnO методом центрифугирования и использование методов физического осаждения из паровой фазы для нанесения тонких пленок ZnO. [56] [57] Предварительный посев может быть выполнен в сочетании с методами формирования рисунка сверху вниз, такими как электронно-лучевая литография и наносферная литография, чтобы обозначить места зародышеобразования перед ростом. Выровненные нанопроволоки ZnO можно использовать в сенсибилизированных красителями солнечных элементах и автоэмиссионных устройствах. [58] [59]
Сферы применения порошка оксида цинка многочисленны, основные из них кратко изложены ниже. В большинстве случаев применения используется реакционная способность оксида как предшественника других соединений цинка. Для применения в материаловедении оксид цинка имеет высокий показатель преломления , высокую теплопроводность, связывающие, антибактериальные и УФ-защитные свойства. Следовательно, его добавляют в материалы и изделия, включая пластмассы, керамику, стекло, цемент, [60] резину, смазочные материалы, [12] краски, мази, клеи, герметики, производство бетона , пигменты, пищевые продукты, батареи, ферриты, антипирены, и т. д. [61]
От 50% до 60% ZnO используется в резиновой промышленности. [62] Оксид цинка вместе со стеариновой кислотой используется при серной вулканизации каучука. [24] [63] Добавки ZnO также защищают резину от грибков (см. «Медицинское применение») и ультрафиолетового излучения.
Керамическая промышленность потребляет значительное количество оксида цинка, в частности, в составах керамических глазурей и фритт. Относительно высокая теплоемкость, теплопроводность и высокая температурная стабильность ZnO в сочетании со сравнительно низким коэффициентом расширения являются желательными свойствами при производстве керамики. ZnO влияет на температуру плавления и оптические свойства глазурей, эмалей и керамических составов. Оксид цинка в качестве вторичного флюса с низким расширением улучшает эластичность глазурей за счет уменьшения изменения вязкости в зависимости от температуры и помогает предотвратить образование трещин и дрожание. При замене BaO и PbO на ZnO теплоемкость снижается, а теплопроводность увеличивается. Цинк в небольших количествах улучшает появление глянцевых и блестящих поверхностей. Однако в умеренных и высоких количествах он создает матовую и кристаллическую поверхность. Что касается цвета, цинк оказывает сложное влияние. [62]
Оксид цинка в виде смеси примерно с 0,5% оксида железа(III) (Fe 2 O 3 ) называется каламином и используется в каламиновом лосьоне. Исторически минерал каламин представляет собой смесь оксидов цинкита и гемиморфита .
Оксид цинка широко используется для лечения различных кожных заболеваний, включая атопический дерматит , контактный дерматит , зуд, вызванный экземой , опрелости и прыщи . [64] Он используется в таких продуктах, как детская присыпка и защитные кремы для лечения опрелостей , каламиновый крем, шампуни против перхоти и антисептические мази. [18] [65] Его часто комбинируют с касторовым маслом для получения смягчающего и вяжущего крема с цинком и касторовым маслом, который обычно используется для лечения младенцев. [66] [67]
Это также компонент ленты (так называемой «ленты с оксидом цинка»), используемой спортсменами в качестве повязки для предотвращения повреждения мягких тканей во время тренировок. [68]
Оксид цинка используется в средствах для полоскания рта и зубных пастах в качестве антибактериального агента, предназначенного для предотвращения образования зубного налета и зубного камня [69] , а также для контроля неприятного запаха изо рта за счет уменьшения содержания летучих газов и летучих соединений серы (ЛВС) во рту. [70] Наряду с оксидом цинка или солями цинка эти продукты также обычно содержат другие активные ингредиенты, такие как хлорид цетилпиридиния , [71] ксилит , [72] хинокитиол , [73] эфирные масла и растительные экстракты . [74] [75] Порошок оксида цинка обладает дезодорирующими и антибактериальными свойствами. [76]
ZnO добавляется в хлопчатобумажные ткани, резину, средства по уходу за полостью рта [77] [78] и упаковку пищевых продуктов. [79] [80] Повышенное антибактериальное действие мелких частиц по сравнению с сыпучим материалом характерно не только для ZnO и наблюдается и для других материалов, таких как серебро . [81] Это свойство является результатом увеличенной площади поверхности мелких частиц.
Оксид цинка используется в солнцезащитных кремах для поглощения ультрафиолетового света . [64] Это поглотитель UVA и UVB самого широкого спектра [82] [83] , который одобрен Управлением по контролю за продуктами и лекарствами США (FDA) для использования в качестве солнцезащитного крема [84] и полностью фотостабилен. [85] При использовании в качестве ингредиента солнцезащитного крема оксид цинка блокирует как UVA (320–400 нм), так и UVB (280–320 нм) лучи ультрафиолетового света . Оксид цинка и другой наиболее распространенный физический солнцезащитный крем, диоксид титана , считаются нераздражающими, неаллергенными и некомедогенными . [86] Однако цинк из оксида цинка слегка впитывается в кожу. [87]
Во многих солнцезащитных кремах используются наночастицы оксида цинка (наряду с наночастицами диоксида титана), поскольку такие мелкие частицы не рассеивают свет и поэтому не кажутся белыми. Наночастицы не впитываются в кожу в большей степени, чем частицы оксида цинка обычного размера [88] , и впитываются только в самый внешний слой кожи, но не в организм. [88]
При смешивании с эвгенолом образуется оксид цинка эвгенол , который находит применение в качестве восстановительного и ортопедического средства в стоматологии . [29] [89]
Оксид цинка добавляется во многие пищевые продукты, включая сухие завтраки , в качестве источника цинка, [90] необходимого питательного вещества . Сульфат цинка также используется с той же целью. Некоторые расфасованные продукты также содержат следовые количества ZnO, даже если он не предназначен в качестве питательного вещества.
Оксид цинка (цинковые белила) используется в качестве пигмента в красках и более непрозрачен, чем литопон , но менее непрозрачен, чем диоксид титана . [14] Он также используется в покрытиях для бумаги. Китайские белила — это особый сорт цинковых белил, используемых в пигментах художников. [91] Использование цинковых белил в качестве пигмента в масляной живописи началось в середине 18 века. [92] Он частично заменил ядовитые свинцовые белила и использовался такими художниками, как Бёклин , Ван Гог , [93] Мане , Мунк и другие. Он также является основным ингредиентом минеральной косметики (CI 77947). [94]
Микронизированный и наноразмерный оксид цинка обеспечивает надежную защиту от ультрафиолетового излучения UVA и UVB и, следовательно, используется в солнцезащитных кремах [95], а также в солнцезащитных очках с защитой от ультрафиолета для использования в космосе и для защиты при сварке , согласно исследованиям ученых из Jet. Лаборатория двигательных установок ( JPL ). [96]
Краски, содержащие порошок оксида цинка, издавна используются в качестве антикоррозионных покрытий металлов. Они особенно эффективны для оцинкованного железа. Железо трудно защитить, поскольку его реакционная способность с органическими покрытиями приводит к хрупкости и отсутствию адгезии. Краски на основе оксида цинка сохраняют гибкость и адгезию на таких поверхностях в течение многих лет. [61]
ZnO сильно n-типа, легированный алюминием , галлием или индием , является прозрачным и проводящим ( прозрачность ~90%, наименьшее удельное сопротивление ~10 -4 Ом·см [97] ). Покрытия ZnO:Al используются для энергосберегающих или теплозащитных окон. Покрытие пропускает видимую часть спектра, но либо отражает инфракрасное (ИК) излучение обратно в помещение (энергосбережение), либо не пропускает ИК-излучение в помещение (теплозащита), в зависимости от того, с какой стороны окна установлено покрытие. [25]
Пластмассы, такие как полиэтиленнафталат (ПЭН), можно защитить путем нанесения покрытия из оксида цинка. Покрытие уменьшает диффузию кислорода через PEN. [98] Слои оксида цинка также можно наносить на поликарбонат при наружном применении. Покрытие защищает поликарбонат от солнечного излучения, снижает скорость его окисления и фотопожелтения. [99]
Оксид цинка, обедненный 64 Zn ( изотоп цинка с атомной массой 64), используется для предотвращения коррозии в ядерных водо-водяных реакторах . Истощение необходимо, поскольку 64 Zn под действием реакторных нейтронов превращается в радиоактивный 65 Zn. [100]
Оксид цинка (ZnO) используется на этапе предварительной обработки для удаления сероводорода (H 2 S) из природного газа после гидрирования любых соединений серы перед установкой риформинга метана , которые могут отравить катализатор. При температуре примерно 230–430 °C (446–806 °F) H 2 S превращается в воду по следующей реакции: [101]
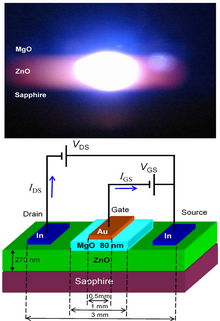

ZnO имеет широкую запрещенную зону (3,37 эВ или 375 нм при комнатной температуре). Поэтому его наиболее распространенное потенциальное применение - это лазерные диоды и светоизлучающие диоды (СИД). [104] Более того, в ZnO обнаружены сверхбыстрые нелинейности и фотопроводящие функции. [105] Некоторые оптоэлектронные применения ZnO перекрываются с применением GaN , который имеет аналогичную запрещенную зону (~ 3,4 эВ при комнатной температуре). По сравнению с GaN, ZnO имеет большую энергию связи экситонов (~ 60 мэВ, в 2,4 раза больше тепловой энергии при комнатной температуре), что приводит к яркому излучению ZnO при комнатной температуре. ZnO можно комбинировать с GaN для светодиодных применений. Например, прозрачный проводящий оксидный слой и наноструктуры ZnO обеспечивают лучшую светоотдачу. [106] Другие свойства ZnO, благоприятные для электронного применения, включают его устойчивость к высокоэнергетическому излучению и способность формировать рисунок путем влажного химического травления. [107] Радиационная стойкость [108] делает ZnO подходящим кандидатом для космического применения. ZnO является наиболее многообещающим кандидатом в области случайных лазеров для создания источника УФ-лазера с электронной накачкой.
Заостренные кончики наностержней ZnO приводят к сильному усилению электрического поля. Поэтому их можно использовать в качестве излучателей поля . [109]
Слои ZnO, легированные алюминием, используются в качестве прозрачных электродов . Компоненты Zn и Al намного дешевле и менее токсичны по сравнению с обычно используемым оксидом индия и олова (ITO). Одним из применений, которое стало коммерчески доступным, является использование ZnO в качестве переднего контакта для солнечных элементов или жидкокристаллических дисплеев . [110]
Прозрачные тонкопленочные транзисторы (TTFT) можно производить из ZnO. Как полевые транзисторы, они не нуждаются в ap-n-переходе, [111] что позволяет избежать проблемы легирования p-типа ZnO. В некоторых полевых транзисторах в качестве проводящих каналов даже используются наностержни ZnO. [112]
Оксид цинка используется в полупроводниковых газовых сенсорах для обнаружения переносимых по воздуху соединений, таких как сероводород , диоксид азота и летучие органические соединения . ZnO — это полупроводник, который становится n-легированным в результате адсорбции восстанавливающих соединений , что снижает определяемое устройством электрическое сопротивление аналогично широко используемым полупроводниковым газовым сенсорам на основе оксида олова . Из него формируются наноструктуры, такие как тонкие пленки, наночастицы , наностолбики или нанопроволоки , чтобы обеспечить большую площадь поверхности для взаимодействия с газами. Датчики изготавливаются селективными в отношении определенных газов путем легирования или прикрепления к поверхности материалов, таких как каталитические благородные металлы. [113] [114]
Было показано, что пьезоэлектричество в текстильных волокнах , покрытых ZnO, позволяет создавать «автономные наносистемы» с ежедневными механическими нагрузками от ветра или движений тела. [115] [116]
В 2008 году Центр определения характеристик наноструктур Технологического института Джорджии сообщил о создании устройства для генерации электричества (так называемого генератора гибкой зарядовой накачки), вырабатывающего переменный ток путем растяжения и высвобождения нанопроводов оксида цинка. Этот мини-генератор создает колебательное напряжение до 45 милливольт, преобразуя около семи процентов приложенной механической энергии в электричество. Исследователи использовали провода длиной 0,2–0,3 мм и диаметром от трех до пяти микрометров, но устройство можно было уменьшить до меньших размеров. [117]

В виде тонкой пленки ZnO был продемонстрирован в миниатюрных высокочастотных тонкопленочных резонаторах, датчиках и фильтрах.
ZnO является многообещающим анодным материалом для литий-ионных аккумуляторов, поскольку он дешев, биосовместим и экологичен. ZnO имеет более высокую теоретическую емкость (978 мАч г -1 ), чем многие другие оксиды переходных металлов, такие как CoO (715 мАч г -1 ), NiO (718 мАч г -1 ) и CuO (674 мАч г- 1 ). [118] ZnO также используется в качестве электрода в суперконденсаторах. [119]
В качестве пищевой добавки оксид цинка включен в список общепризнанных безопасных веществ (GRAS) Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. [120]
Оксид цинка сам по себе нетоксичен; однако опасно вдыхать высокие концентрации паров оксида цинка, образующихся, например, при плавлении и окислении цинка или цинковых сплавов при высокой температуре. Эта проблема возникает при плавке сплавов, содержащих латунь , поскольку температура плавления латуни близка к температуре кипения цинка. [121] Вдыхание оксида цинка, которое может произойти при сварке оцинкованной (оцинкованной) стали , может привести к заболеванию, называемому лихорадкой металлического дыма . [121]
В составах солнцезащитных кремов, в которых оксид цинка сочетался с низкомолекулярными поглотителями УФ-излучения, УФ-свет вызывал фотодеградацию низкомолекулярных поглотителей и токсичность в исследованиях на эмбрионах рыбок данио. [122]