Осмотерапия – применение осмотически активных веществ для уменьшения объема внутричерепного содержимого. Осмотерапия служит основным методом лечения отека мозга . Основной целью осмотерапии является повышение эластичности и уменьшение внутричерепного объема за счет удаления свободной воды, накопленной в результате отека мозга, из внеклеточного и внутриклеточного пространства мозга в сосудистое пространство путем создания осмотического градиента между кровью и мозгом. Нормальная осмоляльность сыворотки колеблется от 280 до 290 мОсм/кг, а осмоляльность сыворотки, вызывающая удаление воды из мозга без особых побочных эффектов, колеблется от 300 до 320 мОсм/кг. Обычно в своде черепа создается 90 мл пространства за счет снижения содержания воды в мозге на 1,6%. [1] Осмотерапия оказывает обезвоживающее действие на мозг. [2] Основная цель осмотерапии — снизить внутричерепное давление (ВЧД) путем выведения лишней жидкости из мозга. Это достигается путем внутривенного введения осмотических агентов, которые повышают осмоляльность сыворотки, чтобы переместить избыточную жидкость из внутриклеточного или внеклеточного пространства мозга во внутрисосудистое пространство. В результате сморщивание мозга эффективно уменьшает внутричерепной объем и снижает ВЧД. [3] [4]
В 1919 году Уид и МакКиббен, биомедицинские исследователи из Медицинской школы Джонса Хопкинса, были первыми, кто задокументировал использование и влияние осмотически активных веществ на массу мозга. Изучая перенос солевых растворов из крови в спинномозговую жидкость (СМЖ), они впервые заметили, что внутривенное (ВВ) введение концентрированного хлорида натрия приводило к коллапсу защитного мешка, что не позволяло им вывести спинномозговую жидкость из поясничной цистерны . Для дальнейшего изучения эффекта они провели лабораторные эксперименты на анестезированных кошках, которым была сделана краниотомия . Они наблюдали изменения выпуклости мозга кошки при внутривенной инъекции, в частности, они отметили, что внутривенная инъекция гипертонического физиологического раствора приводила к максимальному сжатию мозга через 15-30 минут, тогда как введение гипотонических растворов приводило к выпячиванию и разрыву ткани мозга. К 1927 году использование осмотических агентов при внутривенных родах стало официальным. [1]

Увеличение содержания воды в мозге называется отеком мозга и обычно возникает в результате черепно-мозговой травмы (ЧМТ), субарахноидального кровоизлияния (САК), внутримозгового кровоизлияния (ВМК), субдуральной гематомы , ишемического инсульта , опухолей головного мозга , инфекционных заболеваний и внутричерепных операций. Отек мозга может привести к нарушению регионального мозгового кровотока (CBF) и градиентов внутричерепного давления (ICP), что может привести к смерти пострадавшего. [1] Увеличение ВЧД приводит к увеличению внутричерепного объема. Неконтролируемое ВЧД приводит к повреждению головного мозга в результате глобального гипоксически -ишемического повреждения из-за снижения церебрального перфузионного давления (ЦПД), которое определяется путем вычитания ВЧД из среднего артериального давления (САД), церебрального кровотока и механического сжатия ткани головного мозга из-за компартментализированного ВЧД. градиенты. [2] Отек головного мозга в основном подразделяется на цитотоксический отек, вазогенный отек и интерстициальный отек. Цитотоксический отек поражает как белое, так и серое вещество и является результатом набухания клеточных элементов, таких как нейроны , глия и эндотелиальные клетки . Вазогенный отек поражает белое вещество и возникает в результате разрушения гематоэнцефалического барьера (ГЭБ). Интерстициальный отек возникает в результате недостаточного всасывания спинномозговой жидкости (СМЖ). [1]
Осмотические агенты действуют, прежде всего, воздействуя на гематоэнцефалический барьер. [1] Очень важно, чтобы осмотические агенты не могли проникнуть через гематоэнцефалический барьер, поскольку основная идея состоит в том, чтобы использовать осмотические агенты для увеличения осмолярности плазмы и создания осмотического градиента, заставляющего воду из клеток мозга течь в плазму. Как только равновесие достигнуто, и ВЧД, и внутриклеточный объем возвращаются к исходным нормальным условиям. [3] Идеальный осмотический агент должен характеризоваться своей инертностью, относительной нетоксичностью и полным исключением проникновения в мозг. Таким образом, осмотические агенты с коэффициентом отражения (σ) близким к 1 (0 = свободно проницаемые, 1 = полностью непроницаемые) являются предпочтительными, поскольку маловероятно, что они проявят какие-либо побочные эффекты, такие как отек мозга и повышение ВЧД при отмене. Обычно используемыми осмотическими агентами являются мочевина , глицерин , маннит и гипертонический солевой раствор . [1] Дозировка введения осмотического агента указывается в граммах на массу тела человека (г/кг). [3]
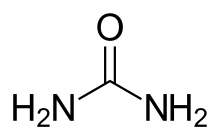
Мочевина с σ=0,59 была введена в 1956 году из-за низкой молекулярной массы и медленного проникновения ГЭБ. Однако он может вызывать эффекты рикошета и побочные эффекты, такие как внутрисосудистый гемолиз и флебит . [1] При введении мочевины доза составляет 1,5 г/кг или 0,5 г/кг (для пожилых людей). [3]

Глицерин с σ=0,48 был представлен в 1964 году, но он может проявлять рикошетный эффект и вызывать побочные эффекты, такие как гемолиз , гемоглобинурия , почечная недостаточность , гиперосмолярная кома и тошнота . [1] При использовании глицерина доза составляет 1,2 г/кг, а затем 0,5–1 г/кг в течение 3–4 часов. [3]
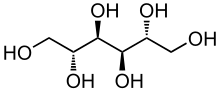
Маннитол представляет собой спиртовое производное простой сахарной маннозы, и его использование исследуется с 1962 года. Его σ = 0,9, молекулярная масса 182 дальтон, период полураспада 2–4 часа, простота приготовления, химическая стабильность и удаление свободных радикалов. Благодаря своим свойствам он считается основным осмотическим агентом для клинического использования. Однако это может вызвать диурез , почечную недостаточность, гиперкалиемию и гемолиз . [1] При назначении маннита используется 20% раствор маннита в дозе 1–1,5 г/кг с последующими дозами по 0,25–1 г/кг по мере необходимости каждые 1–6 часов в зависимости от ВЧД. [2]

Гипертонический раствор с σ=1 вызывает интерес с начала 1980-х годов. Гипертонический раствор, содержащий хлорид натрия, регулирует ВЧД, внутрисосудистый объем и сердечный выброс , не вызывая значительного диуреза, но существуют теоретические побочные эффекты, начиная от неврологических осложнений и заканчивая субдуральной гематомой . Гипертонический солевой раствор в течение последних нескольких лет использовался в качестве средства интенсивной нейрореанимации. [1] Используемый гипертонический солевой раствор варьируется и может представлять собой 3%, 7,5%, 10% или 24,3% физиологический раствор. [5] При применении гипертонического раствора доза составляет 2 г/кг. [6]
В настоящее время осмотерапия является единственным способом уменьшить отек головного мозга, и гипертонический солевой раствор оказывается лучше, чем другие осмотические агенты. По мнению некоторых исследователей, глицерин лучше всего назначать в качестве базального лечения, тогда как маннитол можно назначать для контроля внезапного повышения ВЧД. [7] По сравнению с маннитолом, есть доказательства того, что улучшение ВЧД, мозгового кровотока и ЦПД вследствие введения гипертонического физиологического раствора длится дольше. Кроме того, гипертонический солевой раствор также демонстрирует значительный эффект в улучшении реологических свойств крови, таких как гематокрит и скорость сдвига на уровне внутренней сонной артерии (ВСА). [6]
Исследования продолжаются, чтобы найти более эффективные механизмы лечения отека мозга. Сочетание осмотерапии с другими механизмами лечения имеет больший потенциал для более эффективного лечения отека мозга и его серьезных патологических последствий.
Редуктивная желудочковая омотерапия (РВОТ) может стать новым методом лечения отека мозга без использования осмотических агентов. RVOT использует катетеры, проницаемые для водяного пара, для повышения осмолярности спинномозговой жидкости. Эксперименты ex vivo были проведены для проверки эффективности RVOT. RVOT проводится локально, поэтому она более эффективна в тяжелых случаях отека мозга. Продувочный газ, любой газ, используемый для прохождения через полое волокно, проходит через катетер RVOT, состоящий из полого волокна с полупроницаемыми стенками, для удаления свободной, несвязанной воды из желудочков в виде водяного пара. [8]
Если осмотерапия с использованием осмотических агентов не помогает в лечении отека мозга, можно разработать другие методы лечения с использованием барбитуратов и кортикостероидов . Барбитураты, такие как пентобарбитал, могут действовать как поглотители свободных радикалов , а также уменьшать внутричерепной объем крови за счет снижения метаболических потребностей головного мозга. Однако применение барбитуратов сопряжено с такими рисками, как гипотония , кома и инфекция, ограничивающими их потенциальное клиническое применение. Хотя кортикостероиды не очень эффективны при лечении отека мозга, возникшего в результате ишемического инсульта и внутримозгового кровоизлияния, они очень эффективны при лечении вазогенного отека, возникшего в результате опухолей головного мозга. Идея применения как барбитуратов, так и кортикостероидов заключается в том, чтобы обеспечить пространство для отека мозга, возникающего в результате отека, поэтому это очень неспецифические методы лечения. [9]
Некоторые исследования направлены на выявление новых целей, которые предотвращают образование отека мозга. Чтобы разработать стратегии предотвращения отека мозга, важно понимать отек мозга на молекулярном уровне. Идентифицированные мишени включают: NKCC1 , канал SUR1 / TRPM4 , антагонист рецептора вазопрессина . [9]
На ранней и реперфузионной стадии ишемии происходит активация вторичного активного котранспортера NKCCl. NKCCl играют важную роль в модуляции нагрузки натрия и хлорида в нейронах, глии, эндотелиальных клетках и сосудистом сплетении . Повышение регуляции NKCCl сопровождается увеличением отложения натрия и хлорида в эндотелиальных клетках, а активность Na+K+АТФазы играет роль в вытеснении Na, а затем хлорида и воды из эндотелиальных клеток во внеклеточное пространство, что приводит к вазогенному отеку. Таким образом, предотвращение повышения регуляции NKCCl потенциально может предотвратить формирование отека мозга. Буметанид, который может доставляться через гематоэнцефалический барьер, является ингибитором NKCCl. [9] Буметанид значительно уменьшает воспаление, возникающее в результате ЧМТ. [10] Определение правильной дозы буметанида, который действует как ингибитор NKCCl, может в некоторой степени предотвратить отек мозга. Это представляет собой АТФ-зависимую стадию формирования отека мозга. [9]
Происходит активация этого неселективного катионного канала SUR1/TRPM4, что сопровождается опухолью головного мозга, ишемическим повреждением и черепно-мозговой травмой. Этот канал, который активируется при истощении АТФ, обнаруживается в нейронах, нейроглии и эндотелии . Этот канал обеспечивает пассивный транспорт воды и растворенных веществ и представляет собой независимую от АТФ стадию формирования мозга. Открытие этих каналов приводит к клеточной деполяризации и пузырению, вызывающему цитотоксический отек. Этого можно предотвратить, используя глибурид ( глибенкламид ), который ингибирует эти каналы. [9]
Рецепторы вазопрессина, активируемые вазопрессином, обнаруживаются на базолатеральной мембране клеток, выстилающих собирательные трубочки почек. Аневризматическое субарахноидальное кровоизлияние (аСАК) приводит к гипонатриемии, которая приводит к задержке воды и выбросу антидиуретического гормона, вызывая повышение внутричерепного давления и формирование отека мозга. Это можно предотвратить путем введения кониваптана , безопасного препарата, одобренного FDA, для лечения эуволемической гипонатриемии . Посредством процесса аквареза кониваптен, который является антагонистом рецепторов вазопрессина, улучшает концентрацию натрия в сыворотке крови, одновременно удаляя свободную воду, не оказывая какого-либо отрицательного влияния на систолическое артериальное давление и частоту пульса. Поскольку он может уменьшать объем головного мозга и ВЧД, он потенциально может лечить многие формы отека мозга. [9] [11]