
Открытие нейтрона и его свойств было центральным для необычайных достижений в атомной физике в первой половине 20-го века. В начале века Эрнест Резерфорд разработал грубую модель атома, [1] : 188 [2] основанную на эксперименте с золотой фольгой Ганса Гейгера и Эрнеста Марсдена . В этой модели атомы имели свою массу и положительный электрический заряд, сосредоточенные в очень маленьком ядре . [3] К 1920 году были открыты изотопы химических элементов , атомные массы были определены как (приблизительно) целые кратные массы атома водорода , [4] и атомный номер был идентифицирован как заряд ядра. [5] : §1.1.2 На протяжении 1920-х годов ядро рассматривалось как состоящее из комбинаций протонов и электронов , двух элементарных частиц, известных в то время, но эта модель представляла несколько экспериментальных и теоретических противоречий. [1] : 298
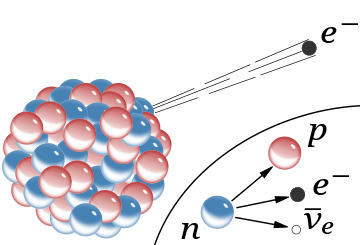
Сущность атомного ядра была установлена с открытием нейтрона Джеймсом Чедвиком в 1932 году [6] и определением того, что это новая элементарная частица, отличная от протона. [7] [8] : 55
Незаряженный нейтрон был немедленно использован в качестве нового средства исследования ядерной структуры, что привело к таким открытиям, как создание новых радиоактивных элементов путем нейтронного облучения (1934) и деление атомов урана нейтронами (1938). [9] Открытие деления привело к созданию как ядерной энергетики , так и ядерного оружия к концу Второй мировой войны. И протон, и нейтрон считались элементарными частицами до 1960-х годов, когда было установлено, что они являются составными частицами, построенными из кварков . [10]
В начале 20-го века яростные дебаты о существовании атомов еще не были разрешены. Философы, такие как Эрнст Мах и Вильгельм Оствальд, отрицали реальность атомов, рассматривая их как удобную математическую конструкцию, в то время как ученые, такие как Арнольд Зоммерфельд и Людвиг Больцман, считали, что физические теории требуют существования атомов. [9] : 13–14
Радиоактивность была открыта в 1896 году французским ученым Анри Беккерелем во время работы с фосфоресцирующими материалами. В 1898 году Эрнест Резерфорд в Кавендишской лаборатории выделил два типа радиоактивности: альфа-лучи и бета-лучи , которые различались по своей способности проникать или перемещаться в обычных объектах или газах. Два года спустя Поль Виллар открыл гамма- лучи, которые обладали еще большей проникающей способностью. [1] : 8–9 Эти излучения вскоре были идентифицированы с известными частицами: Вальтер Кауфман в 1902 году показал, что бета-лучи являются электронами ; Резерфорд и Томас Ройдс в 1907 году показали, что альфа-лучи являются ионами гелия ; и гамма-лучи были показаны как электромагнитное излучение, то есть форма света , Резерфордом и Эдвардом Андраде в 1914 году. [1] : 61–62, 87 Эти излучения также были идентифицированы как исходящие от атомов, поэтому они давали ключи к процессам, происходящим внутри атомов. Наоборот, излучения также были признаны инструментами, которые можно было использовать в экспериментах по рассеянию для исследования внутренней части атомов. [11] : 112–115
В Манчестерском университете между 1908 и 1913 годами Резерфорд руководил Гансом Гейгером и Эрнестом Марсденом в серии экспериментов, чтобы определить, что происходит, когда альфа-частицы рассеиваются на металлической фольге. Теперь называемые экспериментом Резерфорда с золотой фольгой или экспериментом Гейгера-Марсдена, эти измерения сделали необычное открытие, что хотя большинство альфа-частиц, проходящих через тонкую золотую фольгу, испытывают небольшое отклонение, несколько рассеиваются под большим углом. Рассеивание показало, что некоторые из альфа-частиц рикошетят обратно от небольшого, но плотного компонента внутри атомов. Основываясь на этих измерениях, к 1911 году Резерфорду стало очевидно, что атом состоит из небольшого массивного ядра с положительным зарядом, окруженного гораздо большим облаком отрицательно заряженных электронов . Концентрированная атомная масса была необходима для обеспечения наблюдаемого отклонения альфа-частиц, и Резерфорд разработал математическую модель, которая учитывала рассеяние. [12] : 188 [2]
Хотя в то время модель Резерфорда в значительной степени игнорировалась [12] , когда Нильс Бор присоединился к группе Резерфорда в 1913 году [13], он разработал модель Бора для электронов, вращающихся вокруг ядра , и это в конечном итоге привело к созданию атомной модели, основанной на квантовой механике, к середине 1920-х годов.
Параллельно с работой Резерфорда, Гейгера и Марсдена радиохимик Фредерик Содди в Университете Глазго изучал проблемы, связанные с химией, по радиоактивным материалам. Содди работал с Резерфордом над радиоактивностью в Университете Макгилла . [14] К 1910 году было идентифицировано около 40 различных радиоактивных элементов, называемых радиоэлементами , между ураном и свинцом, хотя периодическая таблица допускала только 11 элементов. Содди и Казимеж Фаянс независимо друг от друга обнаружили в 1913 году, что элемент, подвергающийся альфа-распаду, произведет элемент, стоящий на две позиции левее в периодической системе, а элемент, подвергающийся бета-распаду, произведет элемент, стоящий на одну позицию правее в периодической системе. Кроме того, те радиоэлементы, которые находятся в одних и тех же местах в периодической системе, химически идентичны. Содди назвал эти химически идентичные элементы изотопами . [15] : 3–5 [16] За изучение радиоактивности и открытие изотопов Содди был удостоен Нобелевской премии по химии 1921 года. [17]
.jpg/440px-Early_Mass_Spectrometer_(replica).jpg)
Основываясь на работе Дж. Дж. Томсона по отклонению положительно заряженных атомов электрическими и магнитными полями, Фрэнсис Астон построил первый масс-спектрограф в Кавендишской лаборатории в 1919 году. Затем он смог разделить два изотопа неона ,20
Не
и22
Не
. Астон открыл правило целых чисел , согласно которому массы всех частиц имеют целочисленные соотношения с кислородом-16 , [18] который, по его мнению, имеет массу ровно 16. [4] (Сегодня правило целых чисел выражается в кратных единицах атомной массы (а.е.м.) относительно углерода-12 . [19] ). Примечательно, что единственным исключением из этого правила был сам водород, который имел значение массы 1,008. Избыточная масса была небольшой, но находилась далеко за пределами экспериментальной неопределенности.
Поскольку эквивалентность массы и энергии Эйнштейна была известна с 1905 года, Астон и другие быстро поняли, что расхождение масс обусловлено энергией связи атомов. Когда содержимое нескольких атомов водорода связано в один атом, энергия одного атома должна быть меньше суммы энергий отдельных атомов водорода, и, следовательно, масса одного атома меньше суммы масс атомов водорода. [4] Работа Астона по изотопам принесла ему Нобелевскую премию по химии 1922 года за открытие изотопов в большом количестве нерадиоактивных элементов и за формулировку правила целого числа. [20] Отмечая недавнее открытие Астоном ядерной энергии связи, в 1920 году Артур Эддингтон предположил, что звезды могут получать свою энергию путем синтеза водорода (протонов) в гелий и что более тяжелые элементы могут образовываться в звездах. [21]
Резерфорд и другие отметили несоответствие между массой атома, вычисленной в атомных единицах массы, и приблизительным зарядом, необходимым для ядра, чтобы модель Резерфорда работала. Требуемый заряд атомного ядра обычно составлял около половины его атомной массы. [22] : 82 Антониус ван ден Брук смело выдвинул гипотезу, что требуемый заряд, обозначенный как Z , не был половиной атомного веса для элементов, а вместо этого был точно равен порядковому положению элемента в периодической таблице . [1] : 228 В то время не было известно, что позиции элементов в периодической таблице имеют какое-либо физическое значение. Однако, если элементы были упорядочены на основе увеличения атомной массы, то проявлялась периодичность в химических свойствах. Однако были очевидны исключения из этой периодичности, такие как кобальт и никель. [a] [23] : 180
В Манчестерском университете в 1913 году Генри Мозели обсуждал новую модель атома Бора с приезжим Бором. [22] Модель объясняла спектр электромагнитного излучения атома водорода, и Мозели и Бор задались вопросом, будут ли спектры электромагнитного излучения более тяжелых элементов, таких как кобальт и никель, следовать их упорядочению по весу или по их положению в периодической таблице. [24] : 346 В 1913–1914 годах Мозели экспериментально проверил этот вопрос, используя методы рентгеновской дифракции . Он обнаружил, что самая интенсивная коротковолновая линия в рентгеновском спектре определенного элемента, известная как линия K-альфа , была связана с положением элемента в периодической таблице, то есть с его атомным номером Z. Действительно, Мозели ввел эту номенклатуру. [5] : §1.1.2 Мозели обнаружил, что частоты излучения были связаны простым способом с атомным номером элементов для большого числа элементов. [25] [5] : 5 [23] : 181
В течение года было отмечено, что уравнение для отношения, теперь называемое законом Мозли , может быть объяснено в терминах модели Бора 1913 года с разумными дополнительными предположениями об атомной структуре других элементов. [26] : 87 Результат Мозли, по более позднему отчету Бора, не только установил атомный номер как измеримую экспериментальную величину, но и дал ему физическое значение как положительному заряду атомного ядра. Элементы могли быть упорядочены в периодической системе в порядке атомного номера, а не атомного веса. [27] : 127 Результат связал воедино организацию периодической таблицы, модель Бора для атома, [28] : 56 и модель Резерфорда для альфа-рассеяния от ядер. Резерфорд, Бор и другие цитировали его как критический шаг вперед в понимании природы атомного ядра. [29]
Дальнейшие исследования в области атомной физики были прерваны началом Первой мировой войны . Мозли погиб в 1915 году в битве при Галлиполи , [30] [23] : 182 , в то время как ученик Резерфорда Джеймс Чедвик был интернирован в Германии на время войны 1914–1918 годов. [31] В Берлине исследовательская работа Лизы Мейтнер и Отто Гана по определению цепочек радиоактивного распада радия и урана путем точного химического разделения была прервана. [9] : §4 Мейтнер провела большую часть войны, работая рентгенологом и техником по рентгенографии вблизи австрийского фронта, в то время как Ган, химик , работал над исследованиями в области отравляющих газов . [9] : 61–62, 68

В 1920 году Резерфорд прочитал лекцию Бейкера в Королевском обществе под названием «Ядерное строение атомов», резюме последних экспериментов с атомными ядрами и выводы относительно структуры атомных ядер. [32] [8] : 23 [5] : 5 К 1920 году существование электронов внутри атомного ядра было широко распространено. Предполагалось, что ядро состоит из ядер водорода в количестве, равном атомной массе. Но поскольку каждое ядро водорода имело заряд +1, ядру требовалось меньшее количество «внутренних электронов», каждый с зарядом −1, чтобы придать ядру его правильный общий заряд. Масса протонов примерно в 1800 раз больше массы электронов, поэтому масса электронов в этом вычислении несущественна. [1] : 230–231 Такая модель согласуется с рассеянием альфа-частиц тяжелыми ядрами, а также зарядом и массой многих изотопов, которые были идентифицированы. Были и другие мотивы для протонно-электронной модели. Как заметил Резерфорд в то время: «У нас есть веские основания полагать, что ядра атомов содержат электроны, а также положительно заряженные тела...», [32] : 376–377 а именно, было известно, что бета-излучение представляет собой электроны, испускаемые ядром. [8] : 21 [5] : 5–6
В этой лекции Резерфорд предположил существование новых частиц. Было известно, что альфа-частица очень стабильна, и предполагалось, что она сохраняет свою идентичность внутри ядра. Предполагалось, что альфа-частица состоит из четырех протонов и двух тесно связанных электронов, что дает ей заряд +2 и массу 4. В статье 1919 года [33] Резерфорд сообщил о кажущемся открытии новой дважды заряженной частицы с массой 3, обозначенной как X++, интерпретируемой как состоящей из трех протонов и тесно связанного электрона. Этот результат подсказал Резерфорду вероятное существование двух новых частиц: одной из двух протонов с тесно связанным электроном, а другой из одного протона и тесно связанного электрона. Позднее было определено, что частица X++ имеет массу 4 и является просто низкоэнергетической альфа-частицей. [8] : 25 Тем не менее, Резерфорд предположил существование дейтрона, частицы с зарядом +1 и массой 2, и нейтрона, нейтральной частицы с массой 1. [32] : 396 Первый является ядром дейтерия , открытым в 1931 году Гарольдом Юри . [34] Масса гипотетической нейтральной частицы будет мало отличаться от массы протона. Резерфорд определил, что такую частицу с нулевым зарядом будет трудно обнаружить имеющимися методами. [32] : 396
Примерно в то же время, когда была прочитана лекция Резерфорда, появились и другие публикации с похожими предположениями о протонно-электронном составе ядра, а в 1921 году Уильям Харкинс , американский химик, назвал незаряженную частицу нейтроном . [ 35] [36] [37] [5] : 6 Примерно в то же время слово протон было принято для обозначения ядра водорода. [38] Нейтрон, по-видимому, был образован от латинского корня, означающего «нейтральный» , и греческого окончания -он (путем имитации слов «электрон » и «протон» ). [39] [40] Однако ссылки на слово нейтрон в связи с атомом можно найти в литературе еще в 1899 году. [1] : 398 [35]
Резерфорд и Чедвик немедленно начали экспериментальную программу в Кавендишской лаборатории в Кембридже по поиску нейтрона. [8] : 27 [1] : 398 Эксперименты продолжались в течение 1920-х годов, но безуспешно. [6]
Гипотеза Резерфорда и гипотетический «нейтрон» не получили широкого признания. В своей монографии 1931 года «Состав атомного ядра и радиоактивность » Георгий Гамов , тогда работавший в Институте теоретической физики в Копенгагене, не упомянул нейтрон. [41] Во время своих измерений в Париже в 1932 году, которые привели к открытию нейтрона, Ирен Жолио-Кюри и Фредерик Жолио не знали об этой гипотезе. [42]
На протяжении 1920-х годов физики предполагали, что атомное ядро состоит из протонов и «ядерных электронов». [8] : 29–32 [43] Согласно этой гипотезе, ядро азота-14 ( 14 N) будет состоять из 14 протонов и 7 электронов, так что оно будет иметь чистый заряд +7 элементарных единиц заряда и массу 14 атомных единиц массы. Это ядро также будет вращаться вокруг еще 7 электронов, названных Резерфордом «внешними электронами», [32] : 375 , чтобы завершить атом 14 N. Однако вскоре стали очевидны проблемы с этой гипотезой.
Ральф Крониг в 1926 году указал, что наблюдаемая сверхтонкая структура атомных спектров не согласуется с протон-электронной гипотезой. Эта структура вызвана влиянием ядра на динамику орбитальных электронов. Магнитные моменты предполагаемых «ядерных электронов» должны вызывать сверхтонкие расщепления спектральных линий, подобные эффекту Зеемана , но таких эффектов не наблюдалось. [44] : 199 Казалось, что магнитный момент электрона исчезал, когда он находился внутри ядра. [1] : 299
Во время визита в Утрехтский университет в 1928 году Крониг узнал об удивительном аспекте вращательного спектра N 2 + . Прецизионное измерение, проведенное Леонардом Орнштейном , директором Физической лаборатории Утрехта, показало, что спин ядра азота должен быть равен единице. Однако, если ядро азота-14 ( 14 N) состоит из 14 протонов и 7 электронов, нечетного числа частиц со спином 1/2, то результирующий ядерный спин должен быть полуцелым. Поэтому Крониг предположил, что, возможно, «протоны и электроны не сохраняют свою идентичность в той степени, в которой они это делают вне ядра». [1] : 299–301 [45] : 117
Наблюдения вращательных уровней энергии двухатомных молекул с использованием спектроскопии Рамана, проведенные Франко Разетти в 1929 году, не соответствовали статистике, ожидаемой из протон-электронной гипотезы. Разетти получил полосатые спектры для молекул H 2 и N 2 . В то время как линии для обеих двухатомных молекул показывали чередование интенсивности между светом и темнотой, картина чередования для H 2 противоположна таковой для N 2 . После тщательного анализа этих экспериментальных результатов немецкие физики Вальтер Гайтлер и Герхард Герцберг показали, что ядра водорода подчиняются статистике Ферми, а ядра азота подчиняются статистике Бозе. Однако тогда неопубликованный результат Юджина Вигнера показал, что составная система с нечетным числом частиц со спином 1/2 должна подчиняться статистике Ферми; система с четным числом частиц со спином 1/2 подчиняется статистике Бозе. Если бы ядро азота имело 21 частицу, оно должно было бы подчиняться статистике Ферми, вопреки фактам. Таким образом, Гейтлер и Герцберг пришли к выводу: «электрон в ядре... теряет способность определять статистику ядра». [45] : 117–118
Парадокс Клейна [46] , открытый Оскаром Клейном в 1928 году, представил дальнейшие квантово-механические возражения против понятия электрона, заключенного в ядре. Выведенный из уравнения Дирака , этот ясный и точный парадокс предполагал, что электрон, приближающийся к высокому потенциальному барьеру, имеет высокую вероятность прохождения через барьер [41] посредством процесса создания пар . По-видимому, электрон не мог быть заключен в ядре никакой потенциальной ямой. Значение этого парадокса в то время было предметом интенсивных споров. [44] : 199–200
Примерно к 1930 году было общепризнано, что трудно согласовать протонно-электронную модель для ядер с соотношением неопределенностей Гейзенберга в квантовой механике. [44] : 199 [1] : 299 Это соотношение, Δ x ⋅Δ p ≥ 1 ⁄ 2 ħ , подразумевает, что электрон, ограниченный областью размером с атомное ядро, обычно имеет кинетическую энергию около 40 МэВ, [1] : 299 [b] что больше наблюдаемой энергии бета-частиц, испускаемых ядром. [1] Такая энергия также намного больше энергии связи нуклонов, [47] : 89 которая, как показали Астон и другие, составляет менее 9 МэВ на нуклон. [48] : 511
В 1927 году Чарльз Эллис и В. Вустер в Кавендишской лаборатории измерили энергии электронов β-распада. Они обнаружили, что распределение энергий от любого конкретного радиоактивного ядра было широким и непрерывным, что значительно контрастировало с различными значениями энергии, наблюдаемыми при альфа- и гамма-распаде. Кроме того, непрерывное распределение энергии, казалось, указывало на то, что энергия не сохраняется этим процессом «ядерных электронов». Действительно, в 1929 году Бор предложил изменить закон сохранения энергии, чтобы учесть непрерывное распределение энергии. Предложение получило поддержку Вернера Гейзенберга. Такие соображения были, по-видимому, разумными, поскольку законы квантовой механики совсем недавно опровергли законы классической механики.
Хотя все эти соображения не «доказывали», что электрон не может существовать в ядре, они были запутанными и сложными для интерпретации физиками . Было придумано много теорий, чтобы объяснить, как вышеприведенные аргументы могут быть неверными. [49] : 4–5 В своей монографии 1931 года Гамов суммировал все эти противоречия, пометив утверждения относительно электронов в ядре предупреждающими символами. [43] : 23
В 1930 году Вальтер Боте и его коллега Герберт Беккер в Гиссене , Германия, обнаружили, что если энергичные альфа-частицы, испускаемые полонием, попадают на некоторые легкие элементы, в частности, на бериллий (9
4Быть
), бор (11
5Б
), или литий (7
3Ли
), было получено необычайно проникающее излучение. [50] Бериллий произвел самое интенсивное излучение. Полоний очень радиоактивен, производит энергичное альфа-излучение, и в то время его обычно использовали для экспериментов по рассеянию. [41] : 99–110 Альфа-излучение может находиться под влиянием электрического поля, поскольку оно состоит из заряженных частиц. Однако наблюдаемое проникающее излучение не было подвержено влиянию электрического поля, поэтому его считали гамма-излучением . Излучение было более проникающим, чем любые известные гамма-лучи, и детали экспериментальных результатов было трудно интерпретировать. [51] [52] [41]

Два года спустя Ирен Жолио-Кюри и Фредерик Жолио в Париже показали, что если это неизвестное излучение падает на парафин или любое другое водородсодержащее соединение, оно выбрасывает протоны очень высокой энергии (5 МэВ). [53] Это наблюдение само по себе не было несовместимо с предполагаемой природой гамма-излучения нового излучения, но эта интерпретация ( рассеяние Комптона ) имела логическую проблему. Из соображений энергии и импульса гамма-луч должен был бы иметь невозможно высокую энергию (50 МэВ), чтобы рассеять массивный протон. [5] : §1.3.1 В Риме молодой физик Этторе Майорана заявил, что способ, которым новое излучение взаимодействует с протонами, требует нейтральной частицы такой же тяжелой, как протон, но отказался публиковать свой результат, несмотря на поддержку Энрико Ферми . [54]
Услышав о результатах Парижской конференции, Резерфорд и Джеймс Чедвик из Кавендишской лаборатории также не поверили в гипотезу гамма-излучения, поскольку она не сохраняла энергию . [55] С помощью Нормана Фезера [56] Чедвик быстро провел серию экспериментов, показывающих, что гипотеза гамма-излучения несостоятельна. В предыдущем году Чедвик, Дж. Э. Р. Констебль и Э. К. Поллард уже проводили эксперименты по расщеплению легких элементов с использованием альфа-излучения полония. [57] Они также разработали более точные и эффективные методы обнаружения, подсчета и регистрации выброшенных протонов. Чедвик повторил создание излучения, используя бериллий для поглощения альфа-частиц: 9 Be + 4 He (α) → 12 C + 1 n. После Парижского эксперимента он направил излучение на парафиновый воск, углеводород с высоким содержанием водорода, тем самым предлагая цель, насыщенную протонами. Как и в парижском эксперименте, излучение энергетически рассеяло некоторые из протонов. Чедвик измерил пробег этих протонов, а также измерил, как новое излучение воздействовало на атомы различных газов. [58] Измерения энергии отдачи показали, что масса частиц излучения должна быть близка к массе протона: новое излучение не могло состоять из гамма-лучей. Незаряженные частицы с примерно такой же массой, как у протона, соответствовали свойствам, описанным Резерфордом в 1920 году и позже названным нейтронами. [59] [6] [60] [61] За это открытие Чедвик получил Нобелевскую премию по физике в 1935 году. [62]
1932 год позже был назван « годом чудес » для ядерной физики в Кавендишской лаборатории [58] , в связи с открытиями нейтрона, искусственного ядерного распада с помощью ускорителя частиц Кокрофта-Уолтона и позитрона .
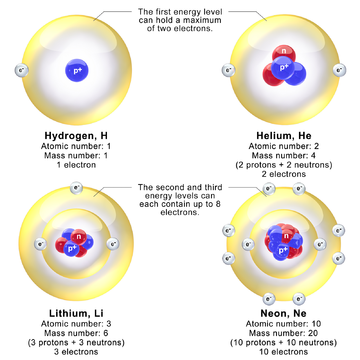
Учитывая проблемы модели протон-электрон , [43] [63] было быстро принято, что атомное ядро состоит из протонов и нейтронов, хотя точная природа нейтрона изначально была неясна. В течение нескольких месяцев после открытия нейтрона Вернер Гейзенберг [64] [65] [66] [61] и Дмитрий Иваненко [67] предложили протон-нейтронные модели для ядра. [68] В знаковых работах Гейзенберга рассматривалось описание протонов и нейтронов в ядре с помощью квантовой механики. Хотя теория Гейзенберга для протонов и нейтронов в ядре была «важным шагом к пониманию ядра как квантово-механической системы», [69] он все еще предполагал наличие ядерных электронов. В частности, Гейзенберг предполагал, что нейтрон представляет собой композит протон-электрон, для которого нет квантово-механического объяснения. У Гейзенберга не было объяснения того, как легкие электроны могут быть связаны внутри ядра. Гейзенберг ввел первую теорию ядерных обменных сил, связывающих нуклоны. Он считал протоны и нейтроны различными квантовыми состояниями одной и той же частицы, т. е. нуклонами, отличающимися значением их ядерного изоспинового квантового числа.
Протонно-нейтронная модель объяснила загадку диазота. Когда было предложено, что 14N состоит из 3 пар протонов и нейтронов, с дополнительным неспаренным нейтроном и протоном, каждый из которых вносит спин 1 ⁄ 2 ħ в том же направлении для общего спина 1 ħ, модель стала жизнеспособной. [70] [71] [72] Вскоре нейтроны стали использоваться для естественного объяснения различий спинов во многих различных нуклидах таким же образом.
Если протон-нейтронная модель ядра решила многие вопросы, она выдвинула на первый план проблему объяснения происхождения бета-излучения. Ни одна существующая теория не могла объяснить, как электроны или позитроны [73] могли исходить из ядра. [74] В 1934 году Энрико Ферми опубликовал свою классическую статью, описывающую процесс бета-распада , в котором нейтрон распадается на протон, создавая электрон и (еще не открытое) нейтрино . [75] В статье использовалась аналогия, что фотоны или электромагнитное излучение аналогичным образом создаются и уничтожаются в атомных процессах. Иваненко предложил похожую аналогию в 1932 году. [70] [76] Теория Ферми требует, чтобы нейтрон был частицей со спином 1 ⁄ 2. Теория сохранила принцип сохранения энергии, который был поставлен под сомнение непрерывным распределением энергии бета-частиц. Основная теория бета-распада, предложенная Ферми, была первой, которая показала, как частицы могут создаваться и уничтожаться. Она установила общую, базовую теорию взаимодействия частиц посредством слабых или сильных сил. [75] Хотя эта влиятельная работа выдержала испытание временем, идеи в ней были настолько новыми, что когда она была впервые представлена в журнале Nature в 1933 году, она была отклонена как слишком спекулятивная. [69]

Вопрос о том, является ли нейтрон составной частицей протона и электрона, сохранялся в течение нескольких лет после его открытия. [77] [78] В 1932 году Гарри Мэсси исследовал модель составного нейтрона, чтобы объяснить его большую проникающую способность через вещество и его электрическую нейтральность, [79] например. Проблема была наследием преобладающего взгляда 1920-х годов, что единственными элементарными частицами были протон и электрон.
Природа нейтрона была основной темой обсуждения на 7-й Сольвеевской конференции , состоявшейся в октябре 1933 года, в которой приняли участие Гейзенберг, Нильс Бор , Лиза Мейтнер , Эрнест Лоуренс , Ферми, Чедвик и другие. [69] [80] Как было поставлено Чедвиком в его Бейкерианской лекции в 1933 году, основным вопросом была масса нейтрона относительно протона. Если масса нейтрона была меньше, чем объединенные массы протона и электрона (1,0078 Да ), то нейтрон мог бы быть протонно-электронным композитом из-за дефекта массы от ядерной энергии связи . Если больше, чем объединенные массы, то нейтрон был бы элементарным, как и протон. [60] На этот вопрос было сложно ответить, поскольку масса электрона составляет всего 0,05% от массы протона, поэтому требовались исключительно точные измерения.
Сложность проведения измерений иллюстрируется широким диапазоном значений массы нейтрона, полученных с 1932 по 1934 год. Принятое сегодня значение составляет1,008 66 Да . В статье Чедвика 1932 года, посвященной открытию, он оценил массу нейтрона как равную1,005 Да и1,008 Да . [55] Бомбардируя бор альфа-частицами, Фредерик и Ирен Жолио-Кюри получили высокое значение1,012 Да , в то время как команда Эрнеста Лоуренса в Калифорнийском университете измерила небольшое значение1,0006 Да с использованием их нового циклотрона . [81]
В 1935 году Чедвик и его аспирант Морис Гольдхабер решили эту проблему, сообщив о первом точном измерении массы нейтрона. Они использовали гамма-лучи 2,6 МэВ таллия -208 ( 208 Tl) (тогда известного как торий C" ) для фоторасщепления дейтрона. [82]
В этой реакции получающиеся протон и нейтрон имеют примерно одинаковую кинетическую энергию, поскольку их массы примерно равны. Кинетическая энергия получающегося протона может быть измерена (0,24 МэВ), и, следовательно, может быть определена энергия связи дейтрона (2,6 МэВ − 2(0,24 МэВ) = 2,1 МэВ, или0,0023 Да ). Массу нейтрона можно было бы тогда определить с помощью простого баланса масс.
где m d,p,n относится к массе дейтрона, протона или нейтрона, а "be" - энергия связи. Массы дейтрона и протона были известны; Чедвик и Голдхабер использовали значения 2,0142 Да и 1,0081 Да соответственно. Они обнаружили, что масса нейтрона была немного больше массы протона1,0084 Да или1,0090 Да , в зависимости от точного значения, используемого для массы дейтрона. [7] Масса нейтрона была слишком большой, чтобы быть составной частью протона и электрона, и поэтому нейтрон был идентифицирован как элементарная частица. [55] Чедвик и Голдхабер предсказали, что свободный нейтрон сможет распадаться на протон, электрон и нейтрино ( бета-распад ).
Вскоре после открытия нейтрона косвенные доказательства предполагали, что нейтрон имеет неожиданное ненулевое значение для своего магнитного момента. Попытки измерить магнитный момент нейтрона начались с открытия Отто Штерном в 1933 году в Гамбурге того, что протон имеет аномально большой магнитный момент. [83] [84] К 1934 году группы под руководством Штерна, теперь в Питтсбурге , и II Раби в Нью-Йорке независимо друг от друга пришли к выводу, что магнитный момент нейтрона был отрицательным и неожиданно большим, измерив магнитные моменты протона и дейтрона . [78] [85] [86] [87] [88] Значения магнитного момента нейтрона были также определены Робертом Бахером [89] (1933) в Энн-Арборе и И. Я. Таммом и С. А. Альтшулером [78] [90] (1934) в Советском Союзе из исследований сверхтонкой структуры атомных спектров. К концу 1930-х годов точные значения магнитного момента нейтрона были выведены группой Раби с использованием измерений, применяющих недавно разработанные методы ядерного магнитного резонанса . [88] Большое значение магнитного момента протона и выведенное отрицательное значение магнитного момента нейтрона были неожиданными и вызвали много вопросов. [78]

Открытие нейтрона немедленно дало ученым новый инструмент для исследования свойств атомных ядер. Альфа-частицы использовались в течение предыдущих десятилетий в экспериментах по рассеянию, но такие частицы, которые являются ядрами гелия, имеют заряд +2. Этот заряд затрудняет для альфа-частиц преодоление силы отталкивания Кулона и прямое взаимодействие с ядрами атомов. Поскольку нейтроны не имеют электрического заряда, им не нужно преодолевать эту силу для взаимодействия с ядрами. Почти одновременно с их открытием нейтроны были использованы Норманом Фезером , коллегой и учеником Чедвика, в экспериментах по рассеянию с азотом. [91] Фезер смог показать, что нейтроны, взаимодействующие с ядрами азота, рассеиваются на протоны или заставляют азот распадаться с образованием бора с испусканием альфа-частицы. Таким образом, Фезер был первым, кто показал, что нейтроны вызывают ядерные распады.
В Риме Энрико Ферми и его команда бомбардировали более тяжелые элементы нейтронами и обнаружили, что продукты являются радиоактивными. К 1934 году они использовали нейтроны для индуцирования радиоактивности в 22 различных элементах, многие из которых имели высокий атомный номер. Заметив, что другие эксперименты с нейтронами в его лаборатории, казалось, лучше проходили на деревянном столе, чем на мраморном, Ферми заподозрил, что протоны дерева замедляют нейтроны и, таким образом, увеличивают вероятность взаимодействия нейтрона с ядрами. Поэтому Ферми пропускал нейтроны через парафиновый воск, чтобы замедлить их, и обнаружил, что радиоактивность некоторых бомбардируемых элементов увеличивалась в десятки и сотни раз. [92] Поперечное сечение взаимодействия с ядрами намного больше для медленных нейтронов, чем для быстрых нейтронов. В 1938 году Ферми получил Нобелевскую премию по физике «за его демонстрацию существования новых радиоактивных элементов, полученных при облучении нейтронами, и за его связанное с этим открытие ядерных реакций, вызванных медленными нейтронами» . [93] [94] Позже Ферми рассказал Чандрасекару , что изначально он планировал положить туда кусок свинца, но необъяснимое интуитивное чувство заставило его вместо этого положить на это место парафин. [95] [96]


В Берлине сотрудничество Лизы Мейтнер и Отто Гана , вместе с их помощником Фрицем Штрассманом , продвинуло исследования, начатые Ферми и его командой, когда они бомбардировали уран нейтронами. Между 1934 и 1938 годами Ган, Мейтнер и Штрассман обнаружили большое количество радиоактивных продуктов трансмутации в этих экспериментах, все из которых они считали трансурановыми . [97] Трансурановые нуклиды - это те, которые имеют атомный номер больше, чем у урана (92), образованные путем поглощения нейтронов; такие нуклиды не встречаются в природе. В июле 1938 года Мейтнер была вынуждена бежать от антисемитских преследований в нацистской Германии после аншлюса , и ей удалось получить новую должность в Швеции. Решающий эксперимент 16–17 декабря 1938 года (с использованием химического процесса, называемого « фракционированием радия–бария–мезотория ») дал озадачивающие результаты: то, что они считали тремя изотопами радия, вместо этого последовательно вело себя как барий . [9] Радий (атомный номер 88) и барий (атомный номер 56) находятся в одной химической группе . К январю 1939 года Хан пришел к выводу, что то, что они считали трансурановыми нуклидами, на самом деле было гораздо более легкими нуклидами, такими как барий, лантан , церий и легкие платиноиды . Мейтнер и ее племянник Отто Фриш немедленно и правильно интерпретировали эти наблюдения как результат ядерного деления , термина, введенного Фришем. [98]
Ган и его коллеги обнаружили расщепление ядер урана, ставших нестабильными из-за поглощения нейтронов, на более легкие элементы. Мейтнер и Фриш также показали, что деление каждого атома урана высвобождает около 200 МэВ энергии. Открытие деления электризовало мировое сообщество физиков-атомщиков и общественность. [9] В своей второй публикации о ядерном делении Ган и Штрассман предсказали существование и высвобождение дополнительных нейтронов в процессе деления. [99] Фредерик Жолио и его команда доказали, что это явление является цепной реакцией в марте 1939 года. В 1945 году Ган получил Нобелевскую премию по химии 1944 года «за открытие деления тяжелых атомных ядер». [100] [101]

Открытие ядерного деления в конце 1938 года ознаменовало собой смещение центров ядерных исследований из Европы в Соединенные Штаты. Большое количество ученых мигрировало в Соединенные Штаты, чтобы избежать проблем и антисемитизма в Европе и надвигающейся войны [102] : 407–410 (См. Еврейские ученые и Манхэттенский проект ). Новыми центрами ядерных исследований стали университеты в Соединенных Штатах, в частности Колумбийский университет в Нью-Йорке и Чикагский университет , куда переехал Энрико Ферми, [103] [104] и секретный исследовательский центр в Лос-Аламосе , штат Нью-Мексико , созданный в 1942 году, новый дом Манхэттенского проекта . [105] Этот военный проект был сосредоточен на создании ядерного оружия , используя огромную энергию, выделяемую при делении урана или плутония посредством цепных реакций на основе нейтронов.
Открытия нейтрона и позитрона в 1932 году стали началом открытий многих новых частиц. Мюоны были открыты в 1936 году. Пионы и каоны были открыты в 1947 году, а лямбда-частицы были открыты в 1950 году. На протяжении 1950-х и 1960-х годов было открыто большое количество частиц, называемых адронами . Схема классификации для организации всех этих частиц, предложенная независимо Мюрреем Гелл-Манном [106] и Джорджем Цвейгом [107] [108] в 1964 году, стала известна как модель кварков . Согласно этой модели, такие частицы, как протон и нейтрон, не были элементарными, а состояли из различных конфигураций небольшого числа других действительно элементарных частиц, называемых партонами или кварками . Модель кварков получила экспериментальное подтверждение, начиная с конца 1960-х годов, и, наконец, дала объяснение аномальному магнитному моменту нейтрона. [109] [10]
В 1920-х годах физики пришли к выводу, что материя состоит только из двух видов элементарных частиц: электронов и протонов.
В 1930 г. Боте в сотрудничестве с Х. Беккером бомбардировал бериллий с массой 9 (а также бор и литий) альфа-лучами, полученными из полония, и получил новую форму излучения ...
протон-нейтронная модель Гейзенберга.
нейтрон.
Однажды, когда я пришел в лабораторию, мне пришло в голову, что я должен изучить эффект помещения куска свинца перед падающими нейтронами. Вместо моей обычной привычки я приложил большие усилия, чтобы точно обработать кусок свинца. Я был явно чем-то недоволен; я пытался найти любой предлог, чтобы отложить установку куска свинца на место. Когда, наконец, с некоторой неохотой я собирался положить его на место, я сказал себе: «Нет, мне не нужен этот кусок свинца здесь; мне нужен кусок парафина». Это было просто так, без предварительного предупреждения, без сознательных предварительных рассуждений. Я немедленно взял какой-то странный кусок парафина и поместил его туда, где должен был быть кусок свинца.