
Температура плавления (или, реже, температура сжижения ) вещества — это температура , при которой оно меняет состояние с твердого на жидкое . В точке плавления твердая и жидкая фазы находятся в равновесии . Температура плавления вещества зависит от давления и обычно указывается при стандартном давлении, таком как 1 атмосфера или 100 кПа .
Если рассматривать ее как температуру обратного перехода из жидкого состояния в твердое, то ее называют точкой замерзания или точкой кристаллизации . Из-за способности веществ переохлаждаться , точка замерзания может легко оказаться ниже ее фактического значения. Когда определяется «характерная точка замерзания» вещества, то фактический метод почти всегда представляет собой «принцип наблюдения исчезновения, а не образования льда, то есть точки плавления». [1]

Для большинства веществ температуры плавления и замерзания примерно равны. Например, температура плавления и замерзания ртути составляет 234,32 кельвина (−38,83 °C ; −37,89 °F ). [2] Однако некоторые вещества обладают различными температурами перехода твердое тело-жидкость. Например, агар плавится при 85 °C (185 °F; 358 K) и затвердевает при 31 °C (88 °F; 304 K); такая зависимость направления известна как гистерезис . Температура плавления льда при давлении в 1 атмосферу очень близка [3] к 0 °C (32 °F; 273 K); это также известно как точка льда. В присутствии зародышеобразующих веществ температура замерзания воды не всегда совпадает с температурой плавления. При отсутствии зародышеобразователей вода может существовать как переохлажденная жидкость до температуры -48,3 °C (-54,9 °F; 224,8 K) перед замерзанием. [4]
Металл с самой высокой температурой плавления — вольфрам , при 3414 °C (6177 °F; 3687 K); [5] это свойство делает вольфрам превосходным для использования в качестве электрических нитей в лампах накаливания . Часто упоминаемый углерод не плавится при давлении окружающей среды, но сублимируется при температуре около 3700 °C (6700 °F; 4000 K); жидкая фаза существует только выше давлений 10 МПа (99 атм) и, по оценкам, 4030–4430 °C (7290–8010 °F; 4300–4700 K) (см. фазовую диаграмму углерода ). Карбонитрид гафния (HfCN) — тугоплавкое соединение с самой высокой известной температурой плавления среди всех веществ на сегодняшний день и единственное, для которого подтверждено значение температуры плавления выше 4273 К (4000 °C; 7232 °F) при давлении окружающей среды. Квантово-механическое компьютерное моделирование предсказало, что этот сплав (HfN 0,38 C 0,51 ) будет иметь температуру плавления около 4400 К. [6] Это предсказание позже было подтверждено экспериментом, хотя точное измерение его точной температуры плавления еще предстоит подтвердить. [7] С другой стороны, гелий вообще не замерзает при нормальном давлении, даже при температурах, произвольно близких к абсолютному нулю ; необходимо давление, более чем в двадцать раз превышающее нормальное атмосферное давление .

Существует множество лабораторных методов определения точек плавления. Скамья Кофлера представляет собой металлическую полоску с температурным градиентом (диапазон от комнатной температуры до 300 °C). Любое вещество можно поместить на участок полоски, показав его термическое поведение при температуре в этой точке. Дифференциальная сканирующая калориметрия дает информацию о температуре плавления вместе с ее энтальпией плавления .

Базовый аппарат для определения точки плавления для анализа кристаллических твердых тел состоит из масляной бани с прозрачным окном (самая простая конструкция: трубка Тиле ) и простой лупы. Несколько зерен твердого тела помещаются в тонкую стеклянную трубку и частично погружаются в масляную баню. Масляная баня нагревается (и перемешивается), и с помощью лупы (и внешнего источника света) можно наблюдать плавление отдельных кристаллов при определенной температуре. Вместо масляной бани можно использовать металлический блок. Некоторые современные приборы имеют автоматическое оптическое обнаружение.
Измерение также может производиться непрерывно с рабочим процессом. Например, нефтеперерабатывающие заводы измеряют точку замерзания дизельного топлива «онлайн», что означает, что образец берется из процесса и измеряется автоматически. Это позволяет проводить более частые измерения, поскольку образец не нужно вручную собирать и доставлять в удаленную лабораторию. [ необходима цитата ]
Для тугоплавких материалов (например, платины, вольфрама, тантала, некоторых карбидов и нитридов и т. д.) чрезвычайно высокая температура плавления (обычно считается, что она выше, скажем, 1800 °C) может быть определена путем нагревания материала в печи черного тела и измерения температуры черного тела с помощью оптического пирометра . Для материалов с самой высокой температурой плавления это может потребовать экстраполяции на несколько сотен градусов. Известно, что спектральное излучение раскаленного тела является функцией его температуры. Оптический пирометр сопоставляет излучение исследуемого тела с излучением источника, который был предварительно откалиброван как функция температуры. Таким образом, измерение абсолютной величины интенсивности излучения не является необходимым. Однако для определения калибровки пирометра необходимо использовать известные температуры. Для температур выше диапазона калибровки источника необходимо использовать метод экстраполяции. Эта экстраполяция выполняется с использованием закона излучения Планка . Константы в этом уравнении не известны с достаточной точностью, что приводит к увеличению ошибок в экстраполяции при более высоких температурах. Однако были разработаны стандартные методы для выполнения этой экстраполяции. [ необходима цитата ]
Рассмотрим случай использования золота в качестве источника (mp = 1063 °C). В этом методе ток через нить накала пирометра регулируется до тех пор, пока интенсивность света нити не совпадет с интенсивностью света черного тела при температуре плавления золота. Это устанавливает первичную калибровочную температуру и может быть выражено через ток через лампу пирометра. При той же настройке тока пирометр наводится на другое черное тело с более высокой температурой. Между пирометром и этим черным телом вставляется поглощающая среда с известной пропускающей способностью. Затем температура черного тела регулируется до тех пор, пока не будет достигнуто соответствие между его интенсивностью и интенсивностью нити пирометра. Затем истинная более высокая температура черного тела определяется по закону Планка. Затем поглощающая среда удаляется, а ток через нить накала регулируется так, чтобы интенсивность света нити совпадала с интенсивностью черного тела. Это устанавливает вторую точку калибровки для пирометра. Этот шаг повторяется для переноса калибровки на более высокие температуры. Теперь известны температуры и соответствующие им токи нити пирометра, и можно построить кривую зависимости температуры от тока. Затем эту кривую можно экстраполировать на очень высокие температуры.
При определении температур плавления тугоплавкого вещества этим методом необходимо либо иметь условия черного тела, либо знать излучательную способность измеряемого материала. Содержание тугоплавкого материала в жидком состоянии может привести к экспериментальным трудностям. Таким образом, температуры плавления некоторых тугоплавких металлов были измерены путем наблюдения за излучением из полости черного тела в образцах твердого металла, которые были намного длиннее своей ширины. Чтобы сформировать такую полость, в центре стержня материала просверливается отверстие перпендикулярно длинной оси. Затем эти стержни нагреваются, пропуская через них очень большой ток, и излучение, испускаемое из отверстия, наблюдается с помощью оптического пирометра. Точка плавления указывается потемнением отверстия, когда появляется жидкая фаза, разрушающая условия черного тела. Сегодня используются методы лазерного нагрева без контейнера в сочетании с быстрыми пирометрами и спектропирометрами, чтобы обеспечить точный контроль времени, в течение которого образец находится при экстремальных температурах. Подобные эксперименты продолжительностью менее секунды решают ряд проблем, связанных с более традиционными измерениями температуры плавления, проводимыми при очень высоких температурах, такими как испарение образца и реакция с контейнером.
Для того, чтобы расплавить твердое тело, требуется тепло , чтобы поднять его температуру до точки плавления. Однако для плавления необходимо дополнительное тепло: это называется теплотой плавления и является примером скрытой теплоты . [10]
С точки зрения термодинамики, в точке плавления изменение свободной энергии Гиббса (ΔG) материала равно нулю, но энтальпия ( H ) и энтропия ( S ) материала увеличиваются (ΔH, ΔS > 0). Явление плавления происходит, когда свободная энергия Гиббса жидкости становится ниже, чем твердого тела для этого материала. При различных давлениях это происходит при определенной температуре. Можно также показать, что:
Здесь T , ΔS и ΔH — соответственно температура плавления, изменение энтропии плавления и изменение энтальпии плавления.
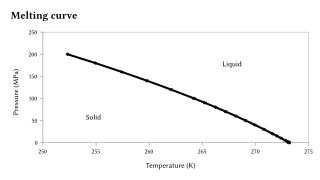
Температура плавления чувствительна к чрезвычайно большим изменениям давления , но обычно эта чувствительность на порядки меньше, чем для температуры кипения , поскольку переход твердое тело-жидкость представляет собой лишь небольшое изменение объема. [11] [12] Если, как наблюдается в большинстве случаев, вещество более плотное в твердом состоянии, чем в жидком, температура плавления будет увеличиваться с увеличением давления. В противном случае происходит обратное поведение. В частности, это касается воды, как графически показано справа, но также и Si, Ge, Ga, Bi. При чрезвычайно больших изменениях давления наблюдаются существенные изменения температуры плавления. Например, температура плавления кремния при давлении окружающей среды (0,1 МПа) составляет 1415 °C, но при давлениях, превышающих 10 ГПа, она уменьшается до 1000 °C. [13]
Температуры плавления часто используются для характеристики органических и неорганических соединений и для определения их чистоты. Температура плавления чистого вещества всегда выше и имеет меньший диапазон, чем температура плавления нечистого вещества или, в более общем смысле, смесей. Чем больше количество других компонентов, тем ниже температура плавления и тем шире будет диапазон температур плавления, часто называемый «пастообразным диапазоном». Температура, при которой начинается плавление смеси, известна как солидус, а температура, при которой плавление завершается, называется ликвидус . Эвтектики — это особые типы смесей, которые ведут себя как отдельные фазы. Они резко плавятся при постоянной температуре, образуя жидкость того же состава. Альтернативно, при охлаждении жидкость с эвтектическим составом затвердевает в виде равномерно диспергированных, мелких (мелкозернистых) смешанных кристаллов того же состава.
В отличие от кристаллических тел, стекла не имеют точки плавления; при нагревании они плавно переходят в вязкую жидкость . При дальнейшем нагревании они постепенно размягчаются, что можно охарактеризовать определенными точками размягчения .
Температура замерзания растворителя понижается при добавлении другого соединения, что означает, что раствор имеет более низкую температуру замерзания, чем чистый растворитель. Это явление используется в технических приложениях, чтобы избежать замерзания, например, путем добавления соли или этиленгликоля в воду. [ необходима цитата ]
В органической химии правило Карнелли , установленное в 1882 году Томасом Карнелли , гласит, что высокая молекулярная симметрия связана с высокой температурой плавления . [14] Карнелли основал свое правило на изучении 15 000 химических соединений. Например, для трех структурных изомеров с молекулярной формулой C5H12 температура плавления увеличивается в ряду изопентан -160 °C (113 K), н -пентан -129,8 °C (143 K) и неопентан -16,4 °C (256,8 K). [15] Аналогично в ксилолах , а также дихлорбензолах температура плавления увеличивается в порядке мета, орто и затем пара . Пиридин имеет более низкую симметрию, чем бензол, отсюда его более низкая температура плавления, но температура плавления снова увеличивается с диазином и триазинами . Многие соединения с решеточной структурой, такие как адамантан и кубан с высокой симметрией, имеют относительно высокие температуры плавления.
Высокая температура плавления является результатом высокой теплоты плавления , низкой энтропии плавления или комбинации того и другого. В высокосимметричных молекулах кристаллическая фаза плотно упакована со многими эффективными межмолекулярными взаимодействиями, что приводит к более высокому изменению энтальпии при плавлении.

Попытка предсказать температуру плавления кристаллических материалов была впервые предпринята в 1910 году Фредериком Линдеманном . [17] Идея теории заключалась в наблюдении, что средняя амплитуда тепловых колебаний увеличивается с ростом температуры. Плавление начинается, когда амплитуда колебаний становится достаточно большой для того, чтобы соседние атомы частично занимали одно и то же пространство. Критерий Линдемана гласит, что плавление ожидается, когда среднеквадратичная амплитуда колебаний превышает пороговое значение.
Предполагая, что все атомы в кристалле колеблются с одинаковой частотой ν , среднюю тепловую энергию можно оценить с помощью теоремы о равнораспределении как [18]
где m — атомная масса , ν — частота , u — средняя амплитуда колебаний, k B — постоянная Больцмана , а T — абсолютная температура . Если пороговое значение u 2 равно c 2 a 2 , где c — постоянная Линдемана , а a — атомное расстояние , то точка плавления оценивается как
Несколько других выражений для расчетной температуры плавления могут быть получены в зависимости от оценки средней тепловой энергии. Другое часто используемое выражение для критерия Линдемана — [19]
Из выражения для частоты Дебая для ν ,
где θ D — температура Дебая , а h — постоянная Планка . Значения c варьируются от 0,15 до 0,3 для большинства материалов. [20]
В феврале 2011 года Alfa Aesar опубликовала более 10 000 точек плавления соединений из своего каталога в качестве открытых данных [21] , и аналогичные данные были получены из патентов . [22] Данные Alfa Aesar и патентов были обобщены в (соответственно) случайных лесах [21] и опорных векторных машинах . [22]