В генетике промотор — это последовательность ДНК , с которой связываются белки, чтобы инициировать транскрипцию одного транскрипта РНК из ДНК ниже промотора. Транскрипт РНК может кодировать белок ( мРНК ) или может иметь функцию сам по себе, например, тРНК или рРНК . Промоторы расположены вблизи мест начала транскрипции генов, выше по течению на ДНК (по направлению к 5'-области смысловой цепи ). Промоторы могут быть длиной около 100–1000 пар оснований , последовательность которых сильно зависит от гена и продукта транскрипции, типа или класса РНК-полимеразы, привлеченной к сайту, и вида организма. [1] [2]
Промоторы контролируют экспрессию генов у бактерий и эукариот . [3] РНК-полимераза должна прикрепиться к ДНК около гена, чтобы произошла транскрипция. Последовательности ДНК промотора обеспечивают сайт связывания фермента . Последовательность -10 — это TATAAT. Последовательности -35 в среднем сохраняются, но не в большинстве промоторов.
Искусственные промоторы с сохраненными элементами -10 и -35 транскрибируются медленнее. Все ДНК имеют «близко расположенные промоторы». Возможны расходящиеся, тандемные и конвергентные ориентации. Два близко расположенных промотора, скорее всего, будут мешать. Регуляторные элементы могут находиться на расстоянии нескольких килобаз от места начала транскрипции в промоторах генов (энхансерах).
У эукариот транскрипционный комплекс может изгибать ДНК, позволяя размещать регуляторные последовательности далеко от сайта транскрипции. Дистальный промотор находится выше гена и может содержать дополнительные регуляторные элементы с более слабым влиянием. РНК-полимераза II (РНКП II), связанная с промотором сайта начала транскрипции, может запускать синтез мРНК. Он также обычно содержит CpG-островки , TATA-бокс и элементы распознавания TFIIB .
Гиперметилирование подавляет оба гена, тогда как деметилирование повышает их. Некодирующие РНК связаны с областями промотора мРНК. Субгеномные промоторы варьируются от 24 до 100 нуклеотидов (вирус некротического желтого венозного некроза свеклы). Экспрессия гена зависит от связывания промотора. Нежелательные изменения гена могут увеличить риск рака клетки.
Промоторы микроРНК часто содержат CpG-островки. Метилирование ДНК образует 5-метилцитозины на 5'-пиримидиновом кольце остатков цитозина CpG. Некоторые гены рака подавляются мутацией, но большинство подавляется метилированием ДНК. Другие являются регулируемыми промоторами. Отбор может благоприятствовать менее энергичному транскрипционному связыванию.
Изменения в промоторах или факторах транскрипции вызывают некоторые заболевания. Недоразумения могут возникнуть из-за использования канонической последовательности для описания промотора.
Для осуществления транскрипции фермент, синтезирующий РНК, известный как РНК-полимераза , должен прикрепиться к ДНК вблизи гена. Промоторы содержат определенные последовательности ДНК, такие как элементы ответа , которые обеспечивают безопасный начальный сайт связывания для РНК-полимеразы и для белков, называемых факторами транскрипции , которые рекрутируют РНК-полимеразу. Эти факторы транскрипции имеют определенные активаторные или репрессорные последовательности соответствующих нуклеотидов, которые прикрепляются к определенным промоторам и регулируют экспрессию генов. [ необходима цитата ]
Промоторы представляют собой критические элементы, которые могут работать совместно с другими регуляторными областями ( энхансерами , сайленсерами , граничными элементами/ изоляторами ) для управления уровнем транскрипции данного гена. Промотор индуцируется в ответ на изменения в избытке или конформации регуляторных белков в клетке, что позволяет активировать факторы транскрипции для привлечения РНК-полимеразы. [4] [5]
Учитывая короткие последовательности большинства элементов промотора, промоторы могут быстро эволюционировать из случайных последовательностей. Например, в E. coli ~60% случайных последовательностей могут эволюционировать до уровней экспрессии, сопоставимых с диким типом промотора lac с одной мутацией, и что ~10% случайных последовательностей могут служить активными промоторами даже без эволюции. [6]
Поскольку промоторы обычно непосредственно примыкают к рассматриваемому гену, позиции в промоторе обозначаются относительно сайта начала транскрипции , где начинается транскрипция ДНК для конкретного гена (т. е. позиции выше по течению представляют собой отрицательные числа, отсчитываемые в обратном порядке от -1, например, -100 представляет собой позицию на 100 пар оснований выше по течению). [ необходима ссылка ]
У бактерий промотор содержит два коротких элемента последовательности, расположенных примерно в 10 ( Pribnow Box ) и 35 нуклеотидах выше места начала транскрипции . [2]
Вышеуказанные промоторные последовательности распознаются только голоферментом РНК-полимеразы, содержащим сигма-70 . Холоферменты РНК-полимеразы, содержащие другие сигма-факторы, распознают различные основные промоторные последовательности.
← вверх по течению вниз по течению →5'-XXXXXXXXXPPPPPPXXXXXXPPPPPPXXXXGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGGXXXX-3' -35 -10 Ген для транскрибирования
для последовательности -10 ТАТААТ77% 76% 60% 61% 56% 82%
для последовательности -35 ТТГАСА69% 79% 61% 56% 54% 54%
Промоторы могут быть очень близко расположены в ДНК. Такие «близко расположенные промоторы» наблюдались в ДНК всех форм жизни, от людей [9] до прокариот [10] и являются высококонсервативными. [11] Следовательно, они могут обеспечивать некоторые (в настоящее время неизвестные) преимущества. Эти пары промоторов могут быть расположены в расходящихся, тандемных и сходящихся направлениях. Они также могут регулироваться факторами транскрипции и различаться по различным признакам, таким как расстояние между нуклеотидами, сила двух промоторов и т. д. Наиболее важным аспектом двух близко расположенных промоторов является то, что они, скорее всего, будут мешать друг другу. Несколько исследований изучали это с использованием как аналитических, так и стохастических моделей. [12] [13] [14] Существуют также исследования, в которых измерялась экспрессия генов в синтетических генах или от одного до нескольких генов, контролируемых двунаправленными промоторами. [15]

Совсем недавно одно исследование измерило большинство генов, контролируемых тандемными промоторами в E. coli . [16] В этом исследовании были измерены две основные формы помех. Одна из них — когда РНК-полимераза находится на нисходящем промоторе, блокируя движение РНК-полимераз, удлиняющихся от восходящего промотора. Другая — когда два промотора расположены так близко, что когда РНК-полимераза находится на одном из промоторов, она блокирует любую другую РНК-полимеразу от достижения другого промотора. Эти события возможны, поскольку РНК-полимераза занимает несколько нуклеотидов при связывании с ДНК, в том числе в точках начала транскрипции. Аналогичные события происходят, когда промоторы находятся в расходящихся и сходящихся формациях. Возможные события также зависят от расстояния между ними.
Промоторы генов обычно располагаются выше гена и могут иметь регуляторные элементы, находящиеся на расстоянии нескольких килобаз от места начала транскрипции (энхансеры). У эукариот транскрипционный комплекс может заставить ДНК согнуться, что позволяет размещать регуляторные последовательности далеко от фактического места транскрипции. Эукариотические РНК-полимераза-II-зависимые промоторы могут содержать ТАТА-бокс ( консенсусная последовательность TATAAA), который распознается общим фактором транскрипции TATA-связывающим белком (TBP); и элемент распознавания B (BRE), который распознается общим фактором транскрипции TFIIB . [17] [18] [19] Элемент TATA и BRE обычно располагаются близко к месту начала транскрипции (обычно в пределах 30–40 пар оснований).
Регуляторные последовательности эукариотических промоторов обычно связывают белки, называемые факторами транскрипции, которые участвуют в формировании транскрипционного комплекса. Примером является E-box (последовательность CACGTG), который связывает факторы транскрипции в основном семействе спираль-петля-спираль (bHLH) (например, BMAL1-Clock , cMyc ). [20] Некоторые промоторы, на которые нацелены множественные факторы транскрипции, могут достигать гиперактивного состояния, что приводит к повышению транскрипционной активности. [21]

Повышенная экспрессия генов у млекопитающих инициируется, когда сигналы передаются на промоторы, связанные с генами. Последовательности ДНК промотора могут включать различные элементы, такие как CpG-островки (присутствуют примерно в 70% промоторов), TATA-бокс (присутствуют примерно в 24% промоторов), инициатор (Inr) (присутствуют примерно в 49% промоторов), элементы распознавания TFIIB выше и ниже по течению (BREu и BREd) (присутствуют примерно в 22% промоторов) и элемент промотора ниже по течению (DPE) (присутствуют примерно в 12% промоторов). [23] Наличие нескольких метилированных сайтов CpG в CpG-островках промоторов вызывает стабильное подавление генов. [24] Однако присутствие или отсутствие других элементов оказывает относительно небольшое влияние на экспрессию генов в экспериментах. [25] Две последовательности, TATA-бокс и Inr, вызвали небольшое, но значительное увеличение экспрессии (увеличение на 45% и 28% соответственно). Элементы BREu и BREd значительно снизили экспрессию на 35% и 20% соответственно, а элемент DPE не оказал никакого обнаруженного эффекта на экспрессию. [25]
Цис-регуляторные модули , локализованные в областях ДНК, удаленных от промоторов генов, могут оказывать очень большое влияние на экспрессию генов, при этом некоторые гены подвергаются 100-кратному увеличению экспрессии из-за такого цис-регуляторного модуля. [26] Эти цис-регуляторные модули включают энхансеры , сайленсеры , инсуляторы и элементы привязки. [27] Среди этого созвездия элементов энхансеры и связанные с ними факторы транскрипции играют ведущую роль в регуляции экспрессии генов. [28]
Энхансеры — это области генома, которые являются основными элементами регуляции генов. Энхансеры контролируют программы экспрессии генов, специфичные для типа клеток, чаще всего, прокладывая петли на больших расстояниях, чтобы физически приблизиться к промоторам своих целевых генов. [29] В исследовании нейронов коры головного мозга было обнаружено 24 937 петель, которые приводят энхансеры к промоторам. [26] Несколько энхансеров, каждый из которых часто находится на расстоянии десятков или сотен тысяч нуклеотидов от своих целевых генов, прокладывают петли к своим промоторам целевых генов и координируют друг с другом, чтобы контролировать экспрессию своего общего целевого гена. [29]
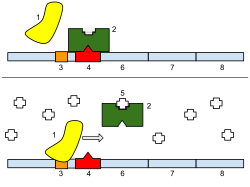
Схематическая иллюстрация в этом разделе показывает энхансер, образующий петлю, чтобы приблизиться к промотору целевого гена. Петля стабилизируется димером соединительного белка (например, димером CTCF или YY1 ), при этом один член димера прикреплен к своему связывающему мотиву на энхансере, а другой член прикреплен к своему связывающему мотиву на промоторе (представлен красными зигзагами на иллюстрации). [30] Несколько факторов транскрипции, специфичных для клеточных функций (в человеческой клетке насчитывается около 1600 факторов транскрипции [31] ), обычно связываются со специфическими мотивами на энхансере [32], и небольшая комбинация этих связанных с энхансером факторов транскрипции, когда они приближаются к промотору с помощью петли ДНК, регулируют уровень транскрипции целевого гена. Медиатор (коактиватор) (комплекс, обычно состоящий из около 26 белков во взаимодействующей структуре) передает регуляторные сигналы от факторов транскрипции, связанных с ДНК-энхансером, непосредственно ферменту РНК-полимеразе II (pol II), связанному с промотором. [33]
Активные энхансеры обычно транскрибируются с обеих цепей ДНК с помощью РНК-полимераз, действующих в двух разных направлениях, производя две эРНК, как показано на рисунке. [34] Неактивный энхансер может быть связан с неактивным фактором транскрипции. Фосфорилирование фактора транскрипции может активировать его, а активированный фактор транскрипции может затем активировать энхансер, с которым он связан (см. маленькую красную звездочку, представляющую фосфорилирование фактора транскрипции, связанного с энхансером на рисунке). [35] Активированный энхансер начинает транскрипцию своей РНК перед активацией промотора для инициирования транскрипции информационной РНК с его целевого гена. [36]
Двунаправленные промоторы — это короткие (<1 кбн) межгенные области ДНК между 5'-концами генов в двунаправленной паре генов. [37] «Двунаправленная пара генов» относится к двум соседним генам, закодированным на противоположных цепях, с их 5'-концами, ориентированными друг на друга. [38] Два гена часто функционально связаны, и модификация их общей области промотора позволяет им совместно регулироваться и, таким образом, совместно экспрессироваться. [39] Двунаправленные промоторы являются общей чертой геномов млекопитающих . [40] Около 11% человеческих генов являются двунаправленно парными. [37]
Двунаправленно спаренные гены в базе данных Gene Ontology разделяли по крайней мере одну назначенную базой данных функциональную категорию со своими партнерами в 47% случаев. [41] Анализ микрочипов показал, что двунаправленно спаренные гены коэкспрессируются в более высокой степени, чем случайные гены или соседние однонаправленные гены. [37] Хотя коэкспрессия не обязательно указывает на корегуляцию, было показано, что метилирование двунаправленных промоторных областей снижает регуляцию обоих генов, а деметилирование повышает регуляцию обоих генов. [42] Однако из этого правила есть исключения. В некоторых случаях (около 11%) экспрессируется только один ген из двунаправленной пары. [37] В этих случаях промотор участвует в подавлении неэкспрессированного гена. Механизмом, лежащим в основе этого, может быть конкуренция за те же полимеразы или модификация хроматина . Дивергентная транскрипция может смещать нуклеосомы для повышения регуляции транскрипции одного гена или удалять связанные факторы транскрипции для снижения регуляции транскрипции одного гена. [43]
Некоторые функциональные классы генов с большей вероятностью будут двунаправленно спаренными, чем другие. Гены, вовлеченные в репарацию ДНК, в пять раз чаще регулируются двунаправленными промоторами, чем однонаправленными. Шаперонные белки в три раза чаще, а митохондриальные гены — более чем в два раза чаще. Многие основные гены домашнего хозяйства и клеточного метаболизма регулируются двунаправленными промоторами. [37] Чрезмерное представительство двунаправленно спаренных генов репарации ДНК связывает эти промоторы с раком . Сорок пять процентов соматических онкогенов человека , по-видимому, регулируются двунаправленными промоторами — значительно больше, чем гены, не вызывающие рак. Гиперметилирование промоторов между парами генов WNT9A /CD558500, CTDSPL /BC040563 и KCNK15 /BF195580 было связано с опухолями. [42]
Определенные характеристики последовательности были обнаружены в двунаправленных промоторах, включая отсутствие боксов TATA , обилие CpG-островков и симметрию вокруг средней точки доминирующих Cs и As с одной стороны и Gs и Ts с другой. Недавно было показано, что мотив с консенсусной последовательностью TCTCGCGAGA, также называемый элементом CGCG, управляет двунаправленной транскрипцией, управляемой PolII, в CpG-островках. [44] Боксы CCAAT являются обычным явлением, поскольку они присутствуют во многих промоторах, в которых отсутствуют боксы TATA. Кроме того, мотивы NRF-1, GABPA , YY1 и ACTACAnnTCCC представлены в двунаправленных промоторах со значительно более высокой частотой, чем в однонаправленных промоторах. Отсутствие боксов TATA в двунаправленных промоторах предполагает, что боксы TATA играют роль в определении направленности промоторов, но контрпримеры двунаправленных промоторов действительно обладают боксами TATA, а однонаправленные промоторы без них указывают на то, что они не могут быть единственным фактором. [45]
Хотя термин «двунаправленный промотор» относится конкретно к промоторным областям генов, кодирующих мРНК , анализы люциферазы показали, что более половины человеческих генов не имеют сильного направленного смещения. Исследования показывают, что некодирующие РНК часто связаны с промоторными областями генов, кодирующих мРНК. Была выдвинута гипотеза, что набор и инициация РНК-полимеразы II обычно начинаются двунаправленно, но расходящаяся транскрипция останавливается на контрольной точке позже во время элонгации. Возможные механизмы, лежащие в основе этой регуляции, включают последовательности в промоторной области, модификацию хроматина и пространственную ориентацию ДНК. [43]
Субгеномный промотор — это промотор, добавляемый к вирусу для определенного гетерологичного гена, что приводит к образованию мРНК только для этого гена. Многие вирусы РНК с положительным смыслом производят эти субгеномные мРНК (sgRNA) в качестве одного из распространенных методов инфицирования, используемых этими вирусами, и обычно транскрибируют поздние вирусные гены. Субгеномные промоторы варьируются от 24 нуклеотидов ( вирус Синдбис ) до более 100 нуклеотидов ( вирус некротического желтого венозного некроза свеклы ) и обычно находятся выше начала транскрипции. [46]
Разработано множество алгоритмов для облегчения обнаружения промоторов в геномной последовательности, а предсказание промотора является общим элементом многих методов предсказания генов . Промоторная область расположена перед консенсусными последовательностями -35 и -10. Чем ближе промоторная область к консенсусным последовательностям, тем чаще будет происходить транскрипция этого гена. Для промоторных областей не существует установленного шаблона, как для консенсусных последовательностей.
Инициация транскрипции представляет собой многоступенчатый последовательный процесс, включающий несколько механизмов: локализацию промотора, первоначальное обратимое связывание РНК-полимеразы, конформационные изменения в РНК-полимеразе, конформационные изменения в ДНК, связывание нуклеозидтрифосфата (NTP) с функциональным комплексом РНК-полимераза-промотор и непродуктивную и продуктивную инициацию синтеза РНК. [47] [2]
Процесс связывания промотора имеет решающее значение для понимания процесса экспрессии генов. Настройка синтетических генетических систем основана на точно спроектированных синтетических промоторах с известными уровнями скоростей транскрипции. [2]
Хотя РНК-полимераза голофермента проявляет высокое сродство к неспецифическим участкам ДНК, эта характеристика не позволяет нам прояснить процесс локализации промотора. [48] Этот процесс локализации промотора был приписан структуре голофермента к ДНК и сигма 4 к ДНК комплексам. [49]
Большинство заболеваний имеют гетерогенную природу, что означает, что одно «заболевание» часто представляет собой множество различных заболеваний на молекулярном уровне, хотя проявляющиеся симптомы и реакция на лечение могут быть идентичны. То, как заболевания различного молекулярного происхождения реагируют на лечение, частично рассматривается в дисциплине фармакогеномики .
Здесь не перечислены многие виды рака, включающие аберрантную транскрипционную регуляцию из-за создания химерных генов посредством патологической хромосомной транслокации . Важно отметить, что вмешательство в количество или структуру белков, связанных с промотором, является одним из ключей к лечению заболевания без воздействия на экспрессию неродственных генов, разделяющих элементы с целевым геном. [50] Некоторые гены, изменение которых нежелательно, способны влиять на потенциал клетки стать раковой. [51]
У людей около 70% промоторов, расположенных вблизи места начала транскрипции гена (проксимальные промоторы), содержат островок CpG . [52] [53] Островки CpG обычно имеют длину от 200 до 2000 пар оснований, содержат пары оснований C: G >50% и имеют области ДНК , где за нуклеотидом цитозина следует нуклеотид гуанина , и это часто происходит в линейной последовательности оснований вдоль направления 5' → 3' .
Дистальные промоторы также часто содержат CpG-островки, такие как промотор гена репарации ДНК ERCC1 , где промотор, содержащий CpG-островок, расположен примерно на 5400 нуклеотидов выше кодирующей области гена ERCC1 . [54] CpG-островки также часто встречаются в промоторах для функциональных некодирующих РНК, таких как микроРНК .
У людей метилирование ДНК происходит в 5'-положении пиримидинового кольца остатков цитозина в CpG-сайтах с образованием 5-метилцитозинов . Наличие множественных метилированных CpG-сайтов в CpG-островках промоторов вызывает стабильное подавление генов. [24] Подавление гена может быть инициировано другими механизмами, но за этим часто следует метилирование CpG-сайтов в CpG-островке промотора, что вызывает стабильное подавление гена. [24]
Как правило, при прогрессировании рака сотни генов подавляются или активируются . Хотя подавление некоторых генов при раке происходит в результате мутации, большая часть канцерогенного подавления генов является результатом измененного метилирования ДНК (см. Метилирование ДНК при раке ). Метилирование ДНК, вызывающее подавление при раке, обычно происходит в нескольких сайтах CpG на островах CpG , которые присутствуют в промоторах генов, кодирующих белки.
Измененная экспрессия микроРНК также подавляет или активирует многие гены при прогрессировании рака (см. микроРНК при раке ). Измененная экспрессия микроРНК происходит посредством гипер/гипометилирования участков CpG в CpG-островках в промоторах, контролирующих транскрипцию микроРНК .
Подавление активности генов репарации ДНК посредством метилирования CpG-островков в их промоторах, по-видимому, особенно важно при прогрессировании рака (см. метилирование генов репарации ДНК при раке ).
Использование термина каноническая последовательность для обозначения промотора часто проблематично и может привести к недопониманию последовательностей промотора. Канонический подразумевает идеальный, в некотором смысле.
В случае сайта связывания фактора транскрипции может быть одна последовательность, которая связывает белок наиболее сильно в определенных клеточных условиях. Это можно назвать каноническим.
Однако естественный отбор может благоприятствовать менее энергичному связыванию как способу регулирования транскрипционного выхода. В этом случае мы можем назвать наиболее распространенную последовательность в популяции последовательностью дикого типа. Она может даже не быть самой выгодной последовательностью в преобладающих условиях.
Последние данные также указывают на то, что несколько генов (включая протоонкоген c-myc ) имеют мотивы G-квадруплекса в качестве потенциальных регуляторных сигналов.
Промоторы являются важными элементами регуляции генов, используемыми при настройке синтетически разработанных генетических цепей и метаболических сетей . Например, для сверхэкспрессии важного гена в сети, чтобы обеспечить более высокую выработку целевого белка, синтетические биологи разрабатывают промоторы для повышения его экспрессии . Автоматизированные алгоритмы могут использоваться для проектирования нейтральной ДНК или инсуляторов, которые не запускают экспрессию генов нижестоящих последовательностей. [55] [2]
Некоторые случаи многих генетических заболеваний связаны с изменениями в промоторах или факторах транскрипции.
Вот несколько примеров:
Некоторые промоторы называются конститутивными, поскольку они активны в любых условиях в клетке, в то время как другие регулируются , становясь активными в клетке только в ответ на определенные стимулы.
Тканеспецифический промотор — это промотор, который активен только в определенных типах клеток.
Когда некоторые авторы ссылаются на промотор, то на самом деле имеют в виду промотор + оператор ; т. е. промотор lac является индуцируемым IPTG, что означает, что помимо промотора lac присутствует также оперон lac . Если бы оператор lac отсутствовал, IPTG не имел бы индуцируемого эффекта. [ необходима цитата ] Другим примером является система Tac-промотор (Ptac). Обратите внимание, что tac записывается как промотор tac, в то время как на самом деле tac является и промотором, и оператором. [60]
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка )