Заживление ран означает замену живым организмом разрушенной или поврежденной ткани вновь образовавшейся тканью. [1]
В неповрежденной коже эпидермис (поверхностный, эпителиальный слой) и дерма (более глубокий, соединительный слой) образуют защитный барьер от внешней среды. Когда барьер разрушается, запускается регулируемая последовательность биохимических событий, направленных на устранение повреждений. [1] [2] Этот процесс разделен на предсказуемые фазы: свертывание крови ( гемостаз ), воспаление , рост тканей ( пролиферация клеток ) и ремоделирование тканей (созревание и дифференцировка клеток ). Свертывание крови можно рассматривать как часть стадии воспаления, а не как отдельную стадию. [3]

Процесс заживления ран не только сложен, но и хрупкий, и он подвержен прерываниям или неудачам, что приводит к образованию незаживающих хронических ран . Факторами, которые способствуют незаживанию хронических ран, являются диабет, заболевания вен или артерий, инфекции и метаболические нарушения в пожилом возрасте. [4]
Уход за ранами способствует и ускоряет заживление ран посредством очистки и защиты от повторного повреждения или инфекции. В зависимости от потребностей каждого пациента, она может варьироваться от простейшей первой помощи до целых сестринских услуг, таких как уход за ранами, стомой, уход за недержанием и уход за ожоговыми центрами .
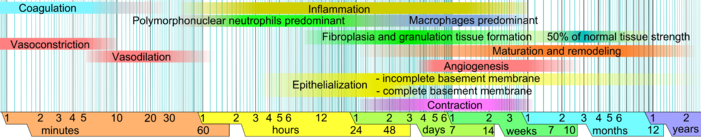
Время важно для заживления ран. Крайне важно, время реэпителизации раны может решить исход заживления. [11] Если эпителизация ткани на оголенном участке происходит медленно, рубец образуется в течение многих недель или месяцев; [12] [13] Если эпителизация раненого участка происходит быстро, заживление приведет к регенерации. [13]

Заживление ран классически разделяют на гемостаз , воспаление, пролиферацию и ремоделирование. Несмотря на то, что эта модель является полезной, она предполагает значительное перекрытие отдельных фаз. Недавно была описана дополнительная модель [1] , в которой более четко очерчены многие элементы заживления ран. Важность этой новой модели становится более очевидной благодаря ее полезности в области регенеративной медицины и тканевой инженерии (см. раздел «Исследования и разработки» ниже). В этой конструкции процесс заживления ран разделен на две основные фазы: раннюю фазу и клеточную фазу : [1]
Ранняя фаза, которая начинается сразу после повреждения кожи, включает в себя каскадные молекулярные и клеточные события, ведущие к гемостазу и формированию раннего временного внеклеточного матрикса, который обеспечивает структурную стадию клеточного прикрепления и последующей клеточной пролиферации.
В клеточной фазе участвуют несколько типов клеток, которые работают вместе, вызывая воспалительную реакцию, синтезируя грануляционную ткань и восстанавливая эпителиальный слой. [1] Подразделения клеточной фазы:
Непосредственно перед началом воспалительной фазы происходит каскад свертывания крови для достижения гемостаза или остановки кровопотери посредством сгустка фибрина. После этого высвобождаются различные растворимые факторы (включая хемокины и цитокины), которые привлекают клетки, фагоцитирующие остатки, бактерии и поврежденные ткани, а также высвобождают сигнальные молекулы, которые инициируют пролиферативную фазу заживления ран.
Когда ткань впервые повреждается, кровь вступает в контакт с коллагеном , что приводит к тому, что тромбоциты крови начинают секретировать воспалительные факторы. [15] Тромбоциты также экспрессируют липкие гликопротеины на своих клеточных мембранах , которые позволяют им агрегировать , образуя массу. [7]
Фибрин и фибронектин перекрестно сшиваются и образуют пробку, которая улавливает белки и частицы и предотвращает дальнейшую кровопотерю. [16] Эта фибрино-фибронектиновая пробка также является основной структурной опорой раны до тех пор, пока не отложится коллаген. [7] Мигрирующие клетки используют эту пробку в качестве матрицы для перемещения по ней, а тромбоциты прикрепляются к ней и секретируют факторы. [7] Сгусток в конечном итоге лизируется и заменяется грануляционной тканью , а затем коллагеном.
Тромбоциты, клетки, присутствующие в наибольшем количестве вскоре после возникновения раны, выделяют в кровь медиаторы, включая цитокины и факторы роста . [15] Факторы роста стимулируют клетки ускорять скорость их деления. Тромбоциты выделяют другие провоспалительные факторы, такие как серотонин , брадикинин , простагландины , простациклины , тромбоксан и гистамин [3] , которые служат нескольким целям, включая увеличение пролиферации клеток и их миграции в эту область, а также вызывают расширение и пористость кровеносных сосудов . Во многих отношениях экстравазативные тромбоциты при травме выполняют аналогичную функцию тканевым макрофагам и тучным клеткам , подвергшимся воздействию микробных молекулярных сигнатур при инфекции: они активируются и секретируют молекулярные медиаторы – вазоактивные амины, эйкозаноиды и цитокины – которые инициируют воспалительный процесс.
Сразу после повреждения кровеносного сосуда разорванные клеточные мембраны выделяют воспалительные факторы, такие как тромбоксаны и простагландины , которые вызывают спазм сосуда, чтобы предотвратить потерю крови и собрать воспалительные клетки и факторы в этой области. [3] Эта вазоконстрикция длится от пяти до десяти минут, за ней следует вазодилатация , расширение кровеносных сосудов, которое достигает максимума примерно через 20 минут после ранения. [3] Расширение сосудов является результатом воздействия факторов, выделяемых тромбоцитами и другими клетками. Основным фактором, участвующим в расширении сосудов, является гистамин . [3] [15] Гистамин также приводит к тому, что кровеносные сосуды становятся пористыми, что приводит к отеку тканей , поскольку белки из кровотока просачиваются во внесосудистое пространство, что увеличивает осмолярную нагрузку и втягивает воду в эту область. [3] Повышенная пористость кровеносных сосудов также облегчает проникновение воспалительных клеток, таких как лейкоциты, в место раны из кровотока . [17] [18]
В течение часа после ранения полиморфно-ядерные нейтрофилы (ПМН) прибывают к месту раны и становятся преобладающими клетками в ране в течение первых двух дней после травмы, особенно в большом количестве на вторые сутки. [19] Их привлекает к этому месту фибронектин, факторы роста и такие вещества, как кинины . Нейтрофилы фагоцитируют мусор и убивают бактерии, высвобождая свободные радикалы в результате так называемого респираторного взрыва . [20] [21] Они также очищают рану, выделяя протеазы , которые разрушают поврежденные ткани. Продолжительность жизни функциональных нейтрофилов в месте раны составляет всего около двух дней, поэтому они обычно подвергаются апоптозу после выполнения своих задач, а также поглощаются и разрушаются макрофагами . [22]
Другие лейкоциты, попадающие в эту область, включают Т-хелперы , которые секретируют цитокины , вызывающие деление большего количества Т-клеток, усиление воспаления, усиление вазодилатации и проницаемости сосудов. [17] [23] Т-клетки также повышают активность макрофагов. [17]
Одна из ролей макрофагов заключается в фагоцитировании других израсходованных фагоцитов , [24] бактерий и поврежденных тканей, [19] , а также они очищают поврежденную ткань, высвобождая протеазы. [25]
Макрофаги участвуют в регенерации [26] [27] и необходимы для заживления ран. [19] Низкое содержание кислорода в окружающей среде стимулирует их выработку факторов, которые индуцируют и ускоряют ангиогенез [20] , а также стимулируют клетки, которые реэпителизируют рану, создают грануляционную ткань и откладывают новый внеклеточный матрикс . [28] Секретируя эти факторы, макрофаги способствуют переходу процесса заживления ран на следующую фазу. Они заменяют ПМЯ как преобладающие клетки в ране через два дня после травмы. [24]
Селезенка содержит половину моноцитов организма в резерве, готовых к использованию в поврежденных тканях . [29] [30] Привлеченные к месту раны факторами роста, высвобождаемыми тромбоцитами и другими клетками, моноциты из кровотока попадают в эту область через стенки кровеносных сосудов. [31] Пик количества моноцитов в ране приходится на один-полтора дня после травмы. [23] Попадая на место раны, моноциты созревают в макрофаги. Макрофаги также секретируют ряд факторов, таких как факторы роста и другие цитокины, особенно в течение третьего и четвертого дней после ранения. Эти факторы привлекают в эту область клетки, участвующие в стадии пролиферации и заживления. [15]
При заживлении ран, приводящем к неполному заживлению, происходит сокращение рубца, что приводит к различным градациям структурных дефектов, деформаций и проблем с гибкостью. [32] Макрофаги могут сдерживать фазу сокращения. [27] Ученые сообщили, что удаление макрофагов из саламандры привело к сбою типичной реакции регенерации (регенерации конечностей), а вместо этого вызвало реакцию восстановления (рубцевания). [33] [34]
По мере угасания воспаления выделяется меньше воспалительных факторов, существующие разрушаются, а количество нейтрофилов и макрофагов в месте раны снижается. [19] Эти изменения указывают на то, что воспалительная фаза заканчивается и начинается пролиферативная фаза. [19] Данные in vitro, полученные с использованием модели дермального эквивалента , позволяют предположить, что присутствие макрофагов фактически задерживает сокращение раны и, таким образом, исчезновение макрофагов из раны может иметь важное значение для возникновения последующих фаз. [27]
Поскольку воспаление играет роль в борьбе с инфекцией, очистке от мусора и стимулировании фазы пролиферации, оно является необходимой частью заживления. Однако воспаление может привести к повреждению тканей , если оно длится слишком долго. [7] Таким образом, уменьшение воспаления часто является целью терапии. Воспаление длится до тех пор, пока в ране остаются инородные тела. Таким образом, если иммунная система человека ослаблена и не может очистить рану от остатков мусора и/или если в ране присутствует избыток детрита, нежизнеспособная ткань или микробная биопленка , эти факторы могут вызвать длительную воспалительную фазу и предотвратить развитие раны. от правильного начала фазы пролиферации исцеления. Это может привести к хронической ране .
Примерно через два-три дня после возникновения раны фибробласты начинают проникать в место раны, отмечая начало пролиферативной фазы еще до того, как фаза воспаления закончилась. [35] Как и в других фазах заживления ран, этапы пролиферативной фазы не происходят последовательно, а частично перекрываются во времени.
Процесс ангиогенеза, также называемый неоваскуляризацией, происходит одновременно с пролиферацией фибробластов, когда эндотелиальные клетки мигрируют в область раны. [36] Поскольку активность фибробластов и эпителиальных клеток требует кислорода и питательных веществ, ангиогенез необходим для других стадий заживления ран, таких как миграция эпидермиса и фибробластов. Ткань, в которой произошел ангиогенез, обычно выглядит красной (эритематозной ) из-за наличия капилляров . [36]
Ангиогенез происходит в перекрывающиеся фазы в ответ на воспаление:
Стволовые клетки эндотелия , происходящие из частей неповрежденных кровеносных сосудов, развивают псевдоподии и проникают через внеклеточный матрикс в место раны, образуя новые кровеносные сосуды. [20]
Эндотелиальные клетки притягиваются к области раны фибронектином, обнаруженным на фибриновом струпе, и хемотаксически ангиогенными факторами, высвобождаемыми другими клетками, [37] например, макрофагами и тромбоцитами в среде с низким содержанием кислорода. Рост и пролиферация эндотелия также напрямую стимулируются гипоксией и присутствием молочной кислоты в ране. [35] Например, гипоксия стимулирует фактор эндотелиальной транскрипции , фактор, индуцируемый гипоксией (HIF), для трансактивации набора пролиферативных генов, включая фактор роста эндотелия сосудов (VEGF) и транспортер глюкозы 1 (GLUT1).
Для миграции эндотелиальным клеткам необходимы коллагеназы и активатор плазминогена , чтобы разрушить сгусток и часть ЕСМ. [3] [19] Цинк -зависимые металлопротеиназы расщепляют базальную мембрану и внеклеточный матрикс, обеспечивая миграцию клеток, пролиферацию и ангиогенез. [38]
Когда макрофаги и другие клетки, продуцирующие факторы роста, больше не находятся в гипоксической среде, наполненной молочной кислотой, они перестают вырабатывать ангиогенные факторы. [20] Таким образом, когда ткань адекватно перфузируется , миграция и пролиферация эндотелиальных клеток уменьшаются. В конце концов кровеносные сосуды, которые больше не нужны, погибают в результате апоптоза . [37]
Одновременно с ангиогенезом в месте раны начинают накапливаться фибробласты . Фибробласты начинают проникать в место раны через два-пять дней после ранения, когда фаза воспаления заканчивается, а их количество достигает максимума через одну-две недели после ранения. [19] К концу первой недели фибробласты становятся основными клетками раны. [3] Фиброплазия заканчивается через две-четыре недели после ранения.
В качестве модели механизм фиброплазии можно представить как процесс, аналогичный ангиогенезу (см. выше), только задействованным типом клеток являются фибробласты, а не эндотелиальные клетки. Первоначально существует латентная фаза, когда рана подвергается экссудации плазмы, воспалительной деконтаминации и хирургической обработке. Отек увеличивает гистологическую доступность раны для последующей миграции фибропласта. Во-вторых, когда воспаление приближается к завершению, макрофаги и тучные клетки высвобождают факторы роста фибробластов и хемотаксические факторы для активации фибробластов из прилегающих тканей. Фибробласты на этом этапе отделяются от окружающих клеток и внеклеточного матрикса. Фагоциты дополнительно выделяют протеазы, которые разрушают внеклеточный матрикс соседних тканей, освобождая активированные фибробласты для пролиферации и миграции к ране. Разница между прорастанием сосудов и пролиферацией фибробластов заключается в том, что первое усиливается при гипоксии, а второе ингибируется гипоксией. Депонированная фибробластическая соединительная ткань созревает за счет секреции ЕСМ во внеклеточное пространство, образуя грануляционную ткань (см. ниже). Наконец, коллаген откладывается во внеклеточном матриксе.
В первые два-три дня после травмы фибробласты преимущественно мигрируют и пролиферируют, а в дальнейшем они являются основными клетками, откладывающими коллагеновый матрикс в месте раны. [3] Считается, что эти фибробласты происходят из прилегающей неповрежденной кожной ткани (хотя новые данные свидетельствуют о том, что некоторые из них происходят из переносимых кровью циркулирующих взрослых стволовых клеток/предшественников). [39] Первоначально фибробласты используют сшивающие фибриновые волокна (хорошо сформированные к концу воспалительной фазы) для миграции через рану, впоследствии прикрепляясь к фибронектину. [37] Фибробласты затем откладывают основное вещество в ложе раны, а затем коллаген, к которому они могут прилипать для миграции. [15]
Грануляционная ткань функционирует как рудиментарная ткань и начинает появляться в ране уже в фазе воспаления, через два-пять дней после ранения, и продолжает расти до тех пор, пока ложе раны не закроется. Грануляционная ткань состоит из новых кровеносных сосудов, фибробластов, воспалительных клеток, эндотелиальных клеток, миофибробластов и компонентов нового временного внеклеточного матрикса (ECM). Временный ЕСМ отличается по составу от ЕСМ нормальной ткани, и его компоненты происходят из фибробластов. [28] К таким компонентам относятся фибронектин, коллаген, гликозаминогликаны , эластин , гликопротеины и протеогликаны . [37] Его основными компонентами являются фибронектин и гиалуронан , которые создают очень гидратированную матрицу и облегчают миграцию клеток. [31] Позже эта временная матрица заменяется ЕСМ, который больше напоминает матрицу, обнаруженную в неповрежденной ткани.
Факторы роста ( PDGF , TGF-β ) и фибронектин стимулируют пролиферацию, миграцию к раневому ложу и выработку молекул ЕСМ фибробластами. Фибробласты также секретируют факторы роста, которые привлекают эпителиальные клетки к месту раны. Гипоксия также способствует пролиферации фибробластов и выделению факторов роста, хотя слишком мало кислорода будет подавлять их рост и отложение компонентов внеклеточного матрикса и может привести к чрезмерному фиброзному рубцеванию .
Одной из наиболее важных функций фибробластов является производство коллагена . [36]
Отложение коллагена важно, поскольку оно увеличивает прочность раны; до закладки единственное, что удерживает рану закрытой, — это фибрино-фибронектиновый сгусток, не оказывающий особой устойчивости к травматическому повреждению . [20] Кроме того, клетки, участвующие в воспалении, ангиогенезе и построении соединительной ткани, прикрепляются, растут и дифференцируются на коллагеновой матрице, отложенной фибробластами. [40]
Коллаген III типа и фибронектин обычно начинают вырабатываться в заметных количествах примерно через 10 часов [41] и 3 дня [37] , в основном в зависимости от размера раны. Пик их отложения приходится на одну-три недели. [28] Они являются преобладающими растягивающими веществами до поздней фазы созревания, на которой они заменяются более сильным коллагеном I типа .
Несмотря на то, что фибробласты производят новый коллаген, коллагеназы и другие факторы разрушают его. Вскоре после ранения синтез превышает деградацию, поэтому уровень коллагена в ране повышается, но позже производство и деградация становятся равными, поэтому чистого прироста коллагена не происходит. [20] Этот гомеостаз сигнализирует о начале более поздней фазы созревания. Грануляция постепенно прекращается, и количество фибробластов в ране уменьшается после завершения своей работы. [42] В конце фазы грануляции фибробласты начинают совершать апоптоз, превращая грануляционную ткань из среды, богатой клетками, в среду, состоящую в основном из коллагена. [3]
Формирование грануляционной ткани в открытой ране позволяет наступить фазе реэпителизации, поскольку эпителиальные клетки мигрируют через новую ткань, образуя барьер между раной и окружающей средой. [37] Базальные кератиноциты краев раны и кожных придатков , таких как волосяные фолликулы , потовые железы и сальные (масляные) железы, являются основными клетками, ответственными за фазу эпителизации при заживлении ран. [42] Они продвигаются листом через место раны и разрастаются по краям, прекращая движение, когда встречаются посередине. При заживлении, приводящем к образованию рубца, потовые железы, волосяные фолликулы [43] [44] и нервы не образуются. Из-за отсутствия волосяных фолликулов, нервов и потовых желез рана и образовавшийся в результате заживающий рубец создают проблемы для организма в плане контроля температуры. [44]
Кератиноциты мигрируют без предварительной пролиферации. [45] Миграция может начаться уже через несколько часов после ранения. Однако для миграции эпителиальным клеткам необходима жизнеспособная ткань, поэтому, если рана глубокая, ее необходимо сначала заполнить грануляционной тканью. [46] Таким образом, время начала миграции варьируется и может произойти примерно через день после ранения. [47] Клетки на краях раны пролиферируют на второй и третий день после ранения, чтобы обеспечить больше клеток для миграции. [28]
Если базальная мембрана не повреждена, эпителиальные клетки заменяются в течение трех дней путем деления и миграции клеток вверх в базальном слое таким же образом, как это происходит в неповрежденной коже. [37] Однако, если базальная мембрана повреждена в месте раны, реэпителизация должна произойти из краев раны и из придатков кожи, таких как волосяные фолликулы, потовые и сальные железы, которые проникают в дерму, выстланную жизнеспособными кератиноцитами. [28] Если рана очень глубокая, придатки кожи также могут быть разрушены, а миграция может происходить только от краев раны. [46]
Миграция кератиноцитов по месту раны стимулируется отсутствием контактного торможения и химическими веществами, такими как оксид азота . [48] Прежде чем начать мигрировать, клетки должны растворить свои десмосомы и гемидесмосомы , которые обычно прикрепляют клетки промежуточными нитями в их цитоскелете к другим клеткам и к ЕСМ. [23] Трансмембранные рецепторные белки , называемые интегринами , которые состоят из гликопротеинов и обычно прикрепляют клетку к базальной мембране ее цитоскелетом , высвобождаются из промежуточных филаментов клетки и перемещаются к актиновым нитям, чтобы служить в качестве прикрепления к внеклеточному матриксу псевдоподий во время миграции. . [23] Таким образом, кератиноциты отделяются от базальной мембраны и могут проникнуть в ложе раны. [35]
Прежде чем начать мигрировать, кератиноциты меняют форму, становясь длиннее и более плоскими, расширяя клеточные отростки, такие как ламеллиподии , и широкие отростки, похожие на рюши. [31] Формируются актиновые нити и псевдоподии . [35] Во время миграции интегрины псевдоподии прикрепляются к ЕСМ, а актиновые нити в проекции тянут клетку вперед. [23] Взаимодействие с молекулами внеклеточного матрикса через интегрины дополнительно способствует образованию актиновых нитей, ламеллиподий и филоподий . [23]
Эпителиальные клетки перелезают друг через друга, чтобы мигрировать. [42] Этот растущий лист эпителиальных клеток часто называют эпителиальным языком. [45] Первые клетки, прикрепляющиеся к базальной мембране, образуют базальный слой . Эти базальные клетки продолжают мигрировать по ложу раны, и эпителиальные клетки над ними также скользят. [45] Чем быстрее произойдет эта миграция, тем меньше останется шрама. [49]
Фибрин , коллаген и фибронектин в ЕСМ могут дополнительно сигнализировать клеткам о необходимости деления и миграции. Как и фибробласты, мигрирующие кератиноциты используют фибронектин, сшитый с фибрином, который откладывается при воспалении, в качестве места прикрепления, по которому можно ползти. [25] [31] [42]

По мере миграции кератиноциты перемещаются по грануляционной ткани, но остаются под струпом, тем самым отделяя струп от подлежащей ткани. [42] [47] Эпителиальные клетки обладают способностью фагоцитировать остатки, такие как мертвые ткани и бактериальные вещества, которые в противном случае препятствовали бы их пути. Поскольку они должны растворять образующиеся струпья, миграция кератиноцитов лучше всего усиливается во влажной среде, поскольку сухая среда приводит к образованию более крупных и жестких струпьев. [25] [37] [42] [50] Чтобы пройти по тканям, кератиноциты должны растворить сгусток, мусор и части внеклеточного матрикса, чтобы пройти. [47] [51] Они выделяют активатор плазминогена , который активирует плазминоген , превращая его в плазмин , растворяющий струп. Клетки могут мигрировать только по живой ткани, [42] поэтому они должны выделять коллагеназы и протеазы, такие как матриксные металлопротеиназы (ММП), чтобы растворять поврежденные части ЕСМ на своем пути, особенно в передней части мигрирующего листа. [47] Кератиноциты также растворяют базальную мембрану, используя вместо этого новый внеклеточный матрикс, отложенный фибробластами для перемещения по ней. [23]
Поскольку кератиноциты продолжают мигрировать, на краях раны должны образовываться новые эпителиальные клетки, чтобы заменить их и обеспечить больше клеток для продвигающегося листка. [25] Пролиферация за мигрирующими кератиноцитами обычно начинается через несколько дней после ранения [46] и происходит со скоростью, которая на этой стадии эпителизации в 17 раз выше, чем в нормальных тканях. [25] Пока вся область раны не будет обновлена, единственные эпителиальные клетки, которые пролиферируют, находятся по краям раны. [45]
Факторы роста, стимулируемые интегринами и ММП, вызывают пролиферацию клеток по краям раны. Сами кератиноциты также производят и секретируют факторы, в том числе факторы роста и белки базальной мембраны, которые способствуют как эпителизации, так и другим фазам заживления. [52] Факторы роста также важны для врожденной иммунной защиты кожных ран путем стимуляции выработки антимикробных пептидов и хемотаксических цитокинов нейтрофилов в кератиноцитах.
Кератиноциты продолжают мигрировать по ложу раны до тех пор, пока клетки с обеих сторон не встретятся посередине, после чего контактное торможение заставляет их перестать мигрировать. [31] После завершения миграции кератиноциты выделяют белки, которые образуют новую базальную мембрану. [31] Клетки обращают вспять морфологические изменения, которым они подверглись, чтобы начать миграцию; они восстанавливают десмосомы и гемидесмосомы и снова закрепляются на базальной мембране. [23] Базальные клетки начинают делиться и дифференцироваться так же, как и в нормальной коже, чтобы восстановить слои, обнаруженные в реэпителизированной коже. [31]
Сокращение является ключевым этапом заживления раны. Если сокращение продолжается слишком долго, это может привести к уродству и потере функции. [32] Таким образом, существует большой интерес к пониманию биологии сокращения ран, которую можно смоделировать in vitro с использованием анализа сокращения коллагенового геля или модели дермального эквивалента . [27] [53]
Сокращение начинается примерно через неделю после ранения, когда фибробласты дифференцируются в миофибробласты . [54] При полнослойных ранах сокращение достигает пика через 5–15 дней после ранения. [37] Сокращение может длиться несколько недель [46] и продолжается даже после полной реэпителизации раны. [3] После сокращения большая рана может уменьшиться на 40–80%. [31] [42] Раны могут сокращаться со скоростью до 0,75 мм в день, в зависимости от того, насколько рыхлы ткани в области раны. [37] Сокращение обычно не происходит симметрично; скорее, большинство ран имеют «ось сокращения», которая обеспечивает лучшую организацию и выравнивание клеток с помощью коллагена. [54]
Сначала сокращение происходит без участия миофибробластов. [55] Позже фибробласты, стимулированные факторами роста, дифференцируются в миофибробласты. За сокращение отвечают миофибробласты, похожие на гладкомышечные клетки. [55] Миофибробласты содержат тот же вид актина, что и гладкомышечные клетки. [32]
Миофибробласты привлекаются фибронектином и факторами роста и движутся вдоль фибронектина, связанного с фибрином во временном внеклеточном матриксе, чтобы достичь краев раны. [25] Они образуют связи с ЕСМ на краях раны и прикрепляются друг к другу и к краям раны с помощью десмосом . Кроме того, при спайке, называемой фибронексусом, актин в миофибробласте через клеточную мембрану связывается с молекулами внеклеточного матрикса, такими как фибронектин и коллаген. [55] Миофибробласты имеют множество таких спаек, которые позволяют им тянуть внеклеточный матрикс при их сокращении, уменьшая размер раны. [32] В этой части сокращения закрытие происходит быстрее, чем в первой, независимой от миофибробластов части. [55]
Когда актин в миофибробластах сокращается, края раны сближаются. Фибробласты откладывают коллаген, чтобы укрепить рану, когда миофибробласты сокращаются. [3] Стадия сокращения пролиферации заканчивается, когда миофибробласты перестают сокращаться и начинают апоптоз. [32] Разрушение временного матрикса приводит к снижению уровня гиалуроновой кислоты и увеличению содержания хондроитинсульфата, что постепенно приводит к прекращению миграции и пролиферации фибробластов. [19] Эти события сигнализируют о начале стадии созревания раневого процесса.
Когда уровни производства и деградации коллагена выравниваются, говорят, что началась фаза созревания восстановления тканей. [20] Во время созревания коллаген типа III , который преобладает во время пролиферации, заменяется коллагеном типа I. [17] Первоначально дезорганизованные коллагеновые волокна перестраиваются, сшиваются и выравниваются вдоль линий натяжения . [31] Начало фазы созревания может сильно различаться в зависимости от размера раны и того, была ли она изначально закрыта или оставлена открытой, [28] в диапазоне примерно от трех дней [41] до трех недель. [56] Фаза созревания может длиться год или дольше, также в зависимости от типа раны. [28]
По мере развития фазы прочность раны на растяжение увеличивается. [28] Коллаген достигнет примерно 20% своей прочности на растяжение через три недели и увеличится до 80% через 12 месяцев. Максимальная сила рубца составляет 80% от прочности неповрежденной кожи. [57] Поскольку активность в месте раны снижается, рубец теряет красный вид, поскольку кровеносные сосуды , которые больше не нужны, удаляются путем апоптоза . [20]
Фазы заживления ран обычно развиваются предсказуемо и своевременно; в противном случае заживление может прогрессировать ненадлежащим образом либо в виде хронической раны [7] , например, венозной язвы , либо в результате патологических рубцов, таких как келоидный рубец . [58] [59]
Многие факторы, контролирующие эффективность, скорость и характер заживления ран, делятся на два типа: местные и системные факторы. [2]
В 2000-х годах появились первые математические модели процесса исцеления, основанные на упрощенных предположениях и системе дифференциальных уравнений, решенных с помощью MATLAB . Модели показывают, что «скорость процесса заживления», по-видимому, «сильно зависит от активности и размера самой травмы, а также от активности заживляющего агента». [69]
Примерно до 2000 года классическая парадигма заживления ран, включающая стволовые клетки, ограниченные органоспецифическими линиями, никогда серьезно не подвергалась сомнению. С тех пор в качестве альтернативного объяснения появилось представление о том, что взрослые стволовые клетки обладают клеточной пластичностью или способностью дифференцироваться в клетки нелинейного происхождения. [1] Если быть более конкретным, гемопоэтические клетки-предшественники (которые дают начало зрелым клеткам в крови) могут обладать способностью дедифференцироваться обратно в гемопоэтические стволовые клетки и/или трансдифференцироваться в клетки нелинейного происхождения, такие как фибробласты. [39]
Мультипотентные взрослые стволовые клетки обладают способностью самообновляться и давать начало различным типам клеток. Стволовые клетки дают начало клеткам-предшественникам, которые не являются самообновляющимися, но могут генерировать несколько типов клеток. Степень участия стволовых клеток в заживлении кожных ран сложна и до конца не изучена. [ нужна цитация ] Инъекция стволовых клеток приводит к заживлению ран в первую очередь за счет стимуляции ангиогенеза. [70]
Считается, что эпидермис и дерма восстанавливаются митотически активными стволовыми клетками, которые расположены на вершинах сетчатых гребней (базальные стволовые клетки или BSC), выпуклости волосяных фолликулов (волосяные фолликулярные стволовые клетки или HFSC) и сосочковой дермы ( дермальные стволовые клетки). [1] Более того, костный мозг также может содержать стволовые клетки, которые играют важную роль в заживлении кожных ран. [39]
В редких случаях, таких как обширное повреждение кожи, самообновляющиеся субпопуляции в костном мозге участвуют в процессе заживления, в результате чего они дают начало клеткам, секретирующим коллаген, которые, по-видимому, играют роль в заживлении ран. [1] Эти две самообновляющиеся субпопуляции представляют собой (1) мезенхимальные стволовые клетки костного мозга (МСК) и (2) гемопоэтические стволовые клетки (ГСК). Костный мозг также содержит субпопуляцию предшественников ( эндотелиальные клетки-предшественники или EPC), которые в тех же условиях мобилизуются для помощи в реконструкции кровеносных сосудов. [39] Более того, считается, что обширное повреждение кожи также способствует раннему перемещению уникального подкласса лейкоцитов ( циркулирующих фиброцитов ) в поврежденную область, где они выполняют различные функции, связанные с заживлением ран. [1]
Травма – это нарушение морфологии и/или функциональности данной ткани. После травмы структурные ткани заживают с неполной или полной регенерацией. [71] [72] Ткань без нарушения морфологии почти всегда полностью регенерирует. Примером полной регенерации без нарушения морфологии является неповрежденная ткань, например кожа. [73] В неповрежденной коже происходит постоянная замена и регенерация клеток, что всегда приводит к полной регенерации. [73]
Существует тонкое различие между «восстановлением» и «регенерацией». [1] [71] [72] Ремонт означает неполную регенерацию . [71] Восстановление или неполная регенерация относится к физиологической адаптации органа после травмы с целью восстановить целостность без учета точного замещения утраченной/поврежденной ткани. [71] Истинная регенерация ткани или полная регенерация , [72] относится к замене утраченной/поврежденной ткани «точной» копией, при которой полностью восстанавливаются как морфология, так и функциональность. [72] Хотя после травмы млекопитающие могут полностью регенерировать спонтанно, обычно они не регенерируют полностью. Примером ткани, полностью регенерирующей после нарушения морфологии, является эндометрий ; эндометрий после процесса разрушения в течение менструального цикла заживает с полной регенерацией. [73]
В некоторых случаях, после разрушения тканей, например кожи, регенерация, близкая к полной, может быть вызвана использованием биоразлагаемых ( коллаген - гликоаминогликановых ) каркасов. Эти каркасы структурно аналогичны внеклеточному матриксу (ECM), обнаруженному в нормальной/неповрежденной дерме. [74] Фундаментальные условия, необходимые для регенерации тканей, часто противостоят условиям, способствующим эффективному заживлению ран, включая ингибирование (1) активации тромбоцитов, (2) воспалительной реакции и (3) сокращения раны. [1] Помимо обеспечения поддержки прикрепления фибробластов и эндотелиальных клеток, биоразлагаемые каркасы ингибируют сокращение ран, тем самым позволяя процессу заживления идти по пути более регенеративного и менее рубцового. Были исследованы фармацевтические агенты, которые могут блокировать дифференцировку миофибробластов . [75]
Новый образ мышления основан на представлении о том, что гепарансульфаты играют ключевую роль в гомеостазе тканей: процессе, который заставляет ткань заменять мертвые клетки идентичными клетками. В области ран тканевый гомеостаз теряется, поскольку гепарансульфаты разрушаются, предотвращая замену мертвых клеток идентичными клетками. Аналоги гепарансульфата не могут расщепляться всеми известными гепараназами и гликаназами и связываются со свободными пятнами связывания гепаринсульфата на внеклеточном матриксе, тем самым сохраняя нормальный гомеостаз тканей и предотвращая образование рубцов. [76] [77] [78]
Восстановление или регенерация фактора 1-альфа, индуцируемого гипоксией (HIF-1a). В нормальных условиях после травмы HIF-1a разрушается пролилгидроксилазами (PHD). Ученые обнаружили, что простая активация HIF-1a с помощью ингибиторов PHD регенерирует утраченные или поврежденные ткани у млекопитающих, у которых есть реакция восстановления; а продолжающееся снижение уровня Hif-1a приводит к заживлению с образованием рубцов у млекопитающих с предшествующей регенеративной реакцией на потерю ткани. Регуляция HIF-1a может либо отключить, либо включить ключевой процесс регенерации млекопитающих. [79] [80]
Заживление ран без рубцов — это концепция, основанная на заживлении или восстановлении кожи (или других тканей/органов) после травмы с целью заживления с субъективным и относительно меньшим количеством рубцовой ткани, чем обычно ожидается. Заживление без рубцов иногда путают с понятием заживления без рубцов , которое представляет собой заживление ран, приводящее к полному отсутствию рубцов ( без рубцов). Однако это разные понятия.
Обратной стороной заживления ран без рубцов является скарификация (заживление ран с образованием большего количества рубцов). Исторически сложилось так, что некоторые культуры считают скарификацию привлекательной; [81] , однако в современном западном обществе дело обстоит иначе, в котором многие пациенты обращаются в клиники пластической хирургии с нереалистичными ожиданиями. В зависимости от типа рубца лечение может быть инвазивным (внутриочаговые инъекции стероидов, хирургическое вмешательство) и/или консервативным ( компрессионная терапия , местный силиконовый гель , брахитерапия , фотодинамическая терапия ). [82] Клиническая оценка необходима для того, чтобы успешно сбалансировать потенциальную пользу различных доступных методов лечения с вероятностью плохого ответа и возможных осложнений в результате этих методов лечения. Многие из этих методов лечения могут иметь только эффект плацебо , а доказательная база использования многих современных методов лечения недостаточна. [83]
С 1960-х годов понимание основных биологических процессов, связанных с заживлением ран и регенерацией тканей , расширилось благодаря достижениям клеточной и молекулярной биологии . [84] В настоящее время основными целями лечения ран являются достижение быстрого закрытия раны функциональной тканью с минимальным эстетическим рубцеванием. [85] Однако конечная цель биологии заживления ран состоит в том, чтобы вызвать более совершенную реконструкцию области раны. Заживление ран без рубцов происходит только в тканях плода млекопитающих [86] , а полная регенерация ограничена низшими позвоночными, такими как саламандры и беспозвоночные . [87] У взрослых людей поврежденные ткани восстанавливаются за счет отложения коллагена , ремоделирования коллагена и возможного образования рубцов, при этом заживление ран плода считается скорее регенеративным процессом с минимальным образованием рубцов или без него. [86] Таким образом, заживление ран плода может быть использовано для создания доступной модели оптимального заживления тканей взрослого человека на млекопитающих. Ключ к пониманию того, как этого можно достичь, дают исследования заживления ран у эмбрионов, где заживление происходит быстро и эффективно и приводит к практически идеальной регенерации любой утраченной ткани.
Этимология термина «заживление ран без рубца» имеет долгую историю. [88] [89] [90] В печати устаревшая концепция исцеления без рубцов была поднята в начале 20-го века и появилась в статье, опубликованной в лондонском журнале Lancet. Этот процесс включал разрезание поверхности кожи под хирургическим наклоном, а не под прямым углом; процесс был описан в различных газетах. [88] [89] [90]
После воспаления восстановление нормальной целостности и функции тканей сохраняется за счет обратных взаимодействий между различными типами клеток, опосредованных молекулами адгезии и секретируемыми цитокинами. Нарушение нормальных механизмов обратной связи при раке угрожает целостности тканей и позволяет злокачественной опухоли ускользнуть от иммунной системы. [91] [92] Пример важности реакции заживления ран в опухолях проиллюстрирован в работе Говарда Чанга и его коллег из Стэнфордского университета, изучающих рак молочной железы. [8]
Предварительные результаты являются многообещающими для краткосрочного и долгосрочного использования пероральных добавок коллагена для заживления ран и старения кожи. Пероральные добавки с коллагеном также повышают эластичность кожи, увлажнение и плотность дермального коллагена. Добавки коллагена, как правило, безопасны, о побочных эффектах не сообщается. Необходимы дальнейшие исследования для выяснения медицинского применения при заболеваниях кожного барьера, таких как атопический дерматит, и для определения оптимальных режимов дозирования. [93]
Современные повязки для лечения ран в последние годы подверглись значительным исследованиям и разработкам. Ученые стремятся разработать раневые повязки, которые имеют следующие характеристики: [94]
Ватно-марлевые повязки были стандартом ухода, несмотря на их сухость, которая может прилипать к раневой поверхности и вызывать дискомфорт при снятии. Недавние исследования были направлены на улучшение хлопко-марлевых повязок, чтобы приблизить их к современным свойствам перевязочных материалов, путем покрытия хлопчато-марлевых повязок нанокомпозитом хитозан / Ag / ZnO . Эти обновленные повязки обеспечивают повышенную водопоглощаемость и улучшенную антибактериальную эффективность . [94]
Грязь или пыль на поверхности раны, бактерии, отмершие ткани и жидкость из раны можно очистить. Доказательства, подтверждающие наиболее эффективный метод, неясны, и недостаточно доказательств, чтобы сделать вывод о том, полезна ли очистка ран для ускорения заживления или растворы для очистки ран (полигексаметиленбигуанид, водный раствор перекиси кислорода и т. д.) лучше, чем стерильная вода или солевые растворы. помочь заживлению венозных язв на ногах. [95] Неизвестно, влияет ли выбор чистящего раствора или метода его применения на заживление венозных язв на ногах. [95]
Значительные усилия были посвящены пониманию физических взаимосвязей, регулирующих заживление ран и последующее рубцевание, с использованием математических моделей и симуляций, разработанных для выяснения этих взаимосвязей. [96] Рост ткани вокруг места раны является результатом миграции клеток и отложения коллагена этими клетками. Выравнивание коллагена описывает степень рубцевания; Корзинчатая ориентация коллагена характерна для нормальной кожи, тогда как выровненные волокна коллагена приводят к образованию значительных рубцов. [97] Было показано, что рост ткани и степень образования рубцов можно контролировать, модулируя нагрузку на место раны. [98]
Рост ткани можно моделировать, используя вышеупомянутые соотношения с биохимической и биомеханической точки зрения. Биологически активные химические вещества, которые играют важную роль в заживлении ран, моделируются с помощью диффузии Фика для создания профилей концентрации. Уравнение баланса для открытых систем при моделировании заживления ран включает рост массы за счет миграции и пролиферации клеток. Здесь используется следующее уравнение:
D т ρ 0 = Div (R) + R 0 ,
где ρ представляет собой массовую плотность, R представляет собой поток массы (в результате миграции клеток), а R 0 представляет собой источник массы (в результате пролиферации, деления или увеличения клеток). [99] Подобные отношения могут быть включены в модели на основе агентов , где можно проверить чувствительность к отдельным параметрам, таким как начальное выравнивание коллагена, свойства цитокинов и скорость пролиферации клеток. [100]
Успешное заживление ран зависит от различных типов клеток, молекулярных медиаторов и структурных элементов. [101]
Основная цель – заживление чистой раны без потери тканей. [101] В этом процессе края раны сближаются так, что они прилегают друг к другу (повторно сближаются). Закрытие раны производят швами (швами), скобами или лейкопластырем или клеем.
Первичное натяжение может быть реализовано только в том случае, если рана точная и имеется минимальное повреждение местных тканей и базальной мембраны эпителия, например, хирургические разрезы. [102]
Этот процесс происходит быстрее, чем исцеление вторичным натяжением. [101] При первичном натяжении рубцевание также меньше, поскольку нет больших потерь ткани, которые необходимо заполнить грануляционной тканью, хотя некоторое количество грануляционной ткани образуется. [101]
(Отсроченное первичное закрытие):
Если края раны не сблизились немедленно, происходит задержка первичного заживления раны. Этот тип заживления может быть желателен в случае загрязненных ран. К четвертым суткам уже полным ходом идет фагоцитоз загрязненных тканей, происходят процессы эпителизации, отложения и созревания коллагена. Инородные материалы отгораживаются макрофагами, которые могут метаморфизоваться в эпителиоидные клетки, окруженные мононуклеарными лейкоцитами, образуя гранулемы. Обычно на этом этапе рану закрывают хирургическим путем или струп разъедают, и если «очищение» раны неполное, может возникнуть хроническое воспаление, приводящее к образованию заметных рубцов.
Ниже приведены основные факторы роста , участвующие в заживлении ран:
Основных осложнений много:
Другие осложнения могут включать инфекцию и язву Маржолина .
Достижения в клиническом понимании ран и их патофизиологии привели к значительным биомедицинским инновациям в лечении острых, хронических и других типов ран. Многие биологические препараты, заменители кожи, биомембраны и каркасы были разработаны для облегчения заживления ран с помощью различных механизмов. [108] Сюда входит ряд продуктов под такими торговыми названиями, как Epicel , Laserskin , Transcyte, Dermagraft, AlloDerm/Strattice, Biobrane, Integra, Apligraf, OrCel, GraftJacket и PermaDerm. [109]
Формирование толстого струпа, медленное заживление (>1 месяца), явные рубцы,
Заживление через 2 недели – минимальное или полное отсутствие рубцов;
Заживление в течение 3 недель – минимальное или полное отсутствие рубцов, за исключением рубцов высокого риска; Заживление в течение 4 недель и более – гипертрофическое у более чем 50% пациентов.
Макрофаги присутствуют практически во всех тканях, начиная с эмбрионального развития, и, помимо их роли в защите хозяина и удалении апоптотических клеток, все чаще признаются их трофические функции и роль в регенерации.
Исследователи идентифицировали клетку, которая способствует отрастанию конечностей у саламандр.
Макрофаги — это тип восстанавливающих клеток, которые пожирают мертвые клетки и патогены и заставляют другие иммунные клетки реагировать на патогены.
Когда дерма разрушается, в рубцах не растут волосы, нервы или потовые железы, что создает дополнительные проблемы с контролем температуры тела.
Новая ткань — это не то же самое, что утраченная ткань.
После завершения процесса восстановления происходит потеря структуры или функции поврежденной ткани.
При этом типе восстановления обычно грануляционная ткань (стромальная соединительная ткань) пролиферирует, заполняя дефект, созданный некротическими клетками.
Некротические клетки затем заменяются рубцовой тканью.
(1) Полная регенерация: новая ткань такая же, как и утраченная.
После завершения процесса восстановления структура и функция поврежденной ткани полностью нормальны.
После завершения процесса восстановления структура и функция поврежденной ткани полностью нормальны.
Этот тип регенерации распространен в физиологических ситуациях.
Примерами физиологической регенерации являются постоянная замена клеток кожи и восстановление эндометрия после менструации.
Полная регенерация может произойти в патологических ситуациях в тканях, обладающих хорошей регенеративной способностью.