Молекулы рекомбинантной ДНК ( рДНК ) — это молекулы ДНК , образованные лабораторными методами генетической рекомбинации (такими как молекулярное клонирование ), которые объединяют генетический материал из нескольких источников, создавая последовательности , которые иначе не были бы обнаружены в геноме .
Рекомбинантная ДНК — это общее название участка ДНК, созданного путем объединения двух или более фрагментов из разных источников. Рекомбинантная ДНК возможна, поскольку молекулы ДНК всех организмов имеют одинаковую химическую структуру и отличаются только нуклеотидной последовательностью . Молекулы рекомбинантной ДНК иногда называют химерной ДНК, поскольку они могут состоять из материала двух разных видов, как, например, мифическая химера . Технология рДНК использует палиндромные последовательности и приводит к образованию липких и тупых концов .
Последовательности ДНК, используемые при построении молекул рекомбинантной ДНК, могут происходить от любого вида . Например, ДНК растений можно соединить с ДНК бактерий, а ДНК человека — с ДНК грибов. Кроме того, путем химического синтеза ДНК можно создать последовательности ДНК, не встречающиеся нигде в природе, и включить их в молекулы рекомбинантной ДНК. Используя технологию рекомбинантной ДНК и синтетическую ДНК, можно создать и внедрить в живые организмы любую последовательность ДНК.
Белки, которые могут возникнуть в результате экспрессии рекомбинантной ДНК в живых клетках, называются рекомбинантными белками . Когда рекомбинантную ДНК, кодирующую белок, вводят в организм хозяина, рекомбинантный белок не обязательно образуется. [1] Экспрессия чужеродных белков требует использования специализированных векторов экспрессии и часто требует значительной реструктуризации с помощью чужеродных кодирующих последовательностей. [2]
Рекомбинантная ДНК отличается от генетической рекомбинации тем, что первая возникает в результате искусственных методов, а вторая представляет собой нормальный биологический процесс, приводящий к ремиксу существующих последовательностей ДНК практически во всех организмах.

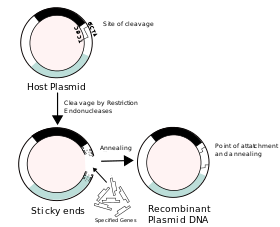
Молекулярное клонирование — это лабораторный процесс, используемый для получения рекомбинантной ДНК. [3] [4] [5] [6] Это один из двух наиболее широко используемых методов, наряду с полимеразной цепной реакцией (ПЦР), используемый для управления репликацией любой конкретной последовательности ДНК, выбранной экспериментатором. Между методами есть два принципиальных различия. Во-первых, молекулярное клонирование предполагает репликацию ДНК внутри живой клетки, тогда как ПЦР реплицирует ДНК в пробирке, свободной от живых клеток. Другое отличие состоит в том, что клонирование включает в себя вырезание и вставку последовательностей ДНК, тогда как ПЦР амплифицируется путем копирования существующей последовательности.
Для формирования рекомбинантной ДНК требуется вектор клонирования — молекула ДНК, которая реплицируется внутри живой клетки. Векторы обычно получают из плазмид или вирусов и представляют собой относительно небольшие сегменты ДНК, которые содержат необходимые генетические сигналы для репликации, а также дополнительные элементы для удобства вставки чужеродной ДНК, идентификации клеток, содержащих рекомбинантную ДНК, и, при необходимости, экспрессии чужая ДНК. Выбор вектора для молекулярного клонирования зависит от выбора организма-хозяина, размера клонируемой ДНК, а также от того, будет ли и как экспрессироваться чужеродная ДНК. [7] Сегменты ДНК можно объединять с помощью различных методов, таких как клонирование ферментов рестрикции/лигазы или сборка Гибсона . [ нужна цитата ]
В стандартных протоколах клонирования клонирование любого фрагмента ДНК по существу включает семь этапов: (1) Выбор организма-хозяина и вектора клонирования, (2) Подготовка векторной ДНК, (3) Подготовка ДНК для клонирования, (4) Создание рекомбинантной ДНК, (5) Введение рекомбинантной ДНК в организм хозяина, (6) Отбор организмов, содержащих рекомбинантную ДНК, и (7) Скрининг клонов с желаемыми вставками ДНК и биологическими свойствами. [6] Эти шаги подробно описаны в соответствующей статье ( молекулярное клонирование ).
Экспрессия ДНК требует трансфекции подходящих клеток-хозяев. Обычно в качестве клеток-хозяев используют бактериальные, дрожжевые, насекомые или клетки млекопитающих (такие как эмбриональные клетки почек человека или клетки CHO ). [8]
После трансплантации в организм хозяина чужеродная ДНК, содержащаяся в конструкции рекомбинантной ДНК, может экспрессироваться или не экспрессироваться . То есть ДНК может быть просто реплицирована без экспрессии или ее можно транскрибировать и транслировать и получать рекомбинантный белок. Вообще говоря, экспрессия чужеродного гена требует реструктуризации гена, чтобы он включал последовательности, необходимые для производства молекулы мРНК , которая может использоваться трансляционным аппаратом хозяина (например, промотор , сигнал инициации трансляции и терминатор транскрипции ). [9] В организм хозяина могут быть внесены специфические изменения для улучшения экспрессии эктопического гена. Кроме того, могут потребоваться изменения и в кодирующих последовательностях, чтобы оптимизировать трансляцию, сделать белок растворимым, направить рекомбинантный белок в нужное клеточное или внеклеточное местоположение и стабилизировать белок от деградации. [10] [11] [12]
В большинстве случаев организмы, содержащие рекомбинантную ДНК, имеют очевидно нормальный фенотип . То есть их внешний вид, поведение и метаболизм обычно не изменяются, и единственный способ продемонстрировать наличие рекомбинантных последовательностей — это изучить саму ДНК, обычно с помощью теста полимеразной цепной реакции (ПЦР). [13] Существуют существенные исключения, которые обсуждаются ниже.
Если последовательности рДНК кодируют экспрессируемый ген, то присутствие РНК и/или белковых продуктов рекомбинантного гена можно обнаружить, обычно используя методы RT-PCR или вестерн-гибридизации . [13] Грубые фенотипические изменения не являются нормой, если только рекомбинантный ген не был выбран и модифицирован таким образом, чтобы генерировать биологическую активность в организме хозяина. [14] Дополнительные встречающиеся фенотипы включают токсичность для организма-хозяина, вызванную продуктом рекомбинантного гена, особенно если он сверхэкспрессируется или экспрессируется в неподходящих клетках или тканях. [ нужна цитата ]
В некоторых случаях рекомбинантная ДНК может оказывать вредное воздействие, даже если она не экспрессируется. Одним из механизмов, с помощью которого это происходит, является инсерционная инактивация , при которой рДНК встраивается в ген клетки-хозяина. В некоторых случаях исследователи используют это явление, чтобы « выбить » гены, чтобы определить их биологическую функцию и важность. [15] Другой механизм, с помощью которого вставка рДНК в хромосомную ДНК может влиять на экспрессию генов, заключается в неадекватной активации ранее неэкспрессированных генов клетки-хозяина. Это может произойти, например, когда фрагмент рекомбинантной ДНК, содержащий активный промотор, оказывается рядом с ранее молчащим геном клетки-хозяина или когда ген клетки-хозяина, который функционирует для ограничения экспрессии гена, подвергается инсерционной инактивации рекомбинантной ДНК. [ нужна цитата ]
Рекомбинантная ДНК широко используется в биотехнологии , медицине и научных исследованиях . Сегодня рекомбинантные белки и другие продукты, полученные в результате использования технологии ДНК, можно найти практически в каждой западной аптеке, врачебном или ветеринарном кабинете, медицинской испытательной лаборатории и лаборатории биологических исследований. Кроме того, организмы, которыми манипулировали с помощью технологии рекомбинантной ДНК, а также продукты, полученные из этих организмов, попали на многие фермы, супермаркеты , домашние аптечки и даже зоомагазины, например те, которые продают GloFish и другие генетически модифицированные продукты. модифицированные животные .
Рекомбинантная ДНК чаще всего применяется в фундаментальных исследованиях, в которых эта технология важна для большинства современных работ в области биологических и биомедицинских наук. [13] Рекомбинантная ДНК используется для идентификации, картирования и секвенирования генов, а также для определения их функции. Зонды рДНК используются для анализа экспрессии генов в отдельных клетках и во всех тканях целых организмов. Рекомбинантные белки широко используются в качестве реагентов в лабораторных экспериментах и для создания зондов антител для изучения синтеза белка в клетках и организмах. [4]
Многие дополнительные практические применения рекомбинантной ДНК находят в промышленности, производстве продуктов питания, медицине и ветеринарии, сельском хозяйстве и биоинженерии. [4] Некоторые конкретные примеры приведены ниже.
Химозин , обнаруженный в сычужном ферменте , является ферментом, ответственным за гидролиз κ - казеина с образованием пара- κ -казеина и гликомакропептида , что является первым шагом в образовании сыра , а затем творога и сыворотки . [16] Это была первая генно-инженерная пищевая добавка, используемая в коммерческих целях. Традиционно переработчики получали химозин из сычужного фермента, препарата, полученного из четвертого желудка телят, вскармливаемых молоком. Ученые создали непатогенный штамм (К-12) бактерий E. coli для крупномасштабного лабораторного производства фермента. Этот рекомбинантный фермент, полученный микробиологическим путем, структурно идентичен ферменту, полученному из телят, стоит дешевле и производится в больших количествах. Сегодня около 60% твердого сыра в США производится из генно-инженерного химозина. В 1990 году FDA присвоило химозину статус « общепризнанного безопасного » (GRAS) на основании данных, показывающих, что фермент безопасен. [17]
Рекомбинантный человеческий инсулин почти полностью заменил инсулин, полученный из животных источников (например, свиней и крупного рогатого скота) для лечения диабета 1 типа . Широко используются различные препараты рекомбинантного инсулина. [18] Рекомбинантный инсулин синтезируется путем вставки гена человеческого инсулина в E. coli или дрожжи (Saccharomyces cerevisiae) [19] , которые затем производят инсулин для использования человеком. [20] Инсулин, продуцируемый E. coli, требует дальнейших посттрансляционных модификаций (например, гликозилирования), тогда как дрожжи способны выполнять эти модификации самостоятельно, поскольку являются более сложными организмами-хозяевами. Преимущество рекомбинантного человеческого инсулина заключается в том, что после его хронического применения у пациентов не вырабатывается иммунная защита против него, подобно тому, как инсулин животного происхождения стимулирует иммунную систему человека. [21]
Назначается пациентам, у которых гипофиз вырабатывает недостаточное количество препарата для поддержания нормального роста и развития. До того, как рекомбинантный гормон роста стал доступен, гормон роста для терапевтического использования получали из гипофизов трупов. Эта небезопасная практика привела к тому, что у некоторых пациентов развилась болезнь Крейтцфельдта-Якоба . Рекомбинантный гормон роста устранил эту проблему и теперь используется в терапевтических целях. [22] Спортсмены и другие люди злоупотребляли им в качестве препарата для повышения работоспособности. [23] [24]
Это рекомбинантная форма фактора VIII , белка свертывания крови, который вводится пациентам с нарушением свертываемости крови гемофилией , которые не способны вырабатывать фактор VIII в количествах, достаточных для поддержания нормального свертывания крови. [25] До разработки рекомбинантного фактора VIII белок получали путем обработки больших количеств человеческой крови от нескольких доноров, что несло очень высокий риск передачи инфекционных заболеваний, передающихся через кровь , например ВИЧ и гепатита B.
Инфекцию гепатита В можно успешно контролировать с помощью рекомбинантной субъединичной вакцины против гепатита В , которая содержит форму поверхностного антигена вируса гепатита В, вырабатываемую дрожжевыми клетками. Разработка рекомбинантной субъединичной вакцины была важным и необходимым событием, поскольку вирус гепатита В, в отличие от других распространенных вирусов, таких как вирус полиомиелита , нельзя выращивать in vitro . [26]
Рекомбинантные антитела (rAb) получают in vitro с помощью систем экспрессии на основе клеток млекопитающих. Их моноспецифическое связывание со специфическим эпитопом делает rAb пригодными не только для исследовательских целей, но и в качестве вариантов терапии против определенных типов рака, инфекций и аутоиммунных заболеваний. [27]
Каждый из трех широко используемых методов диагностики ВИЧ-инфекции разработан с использованием рекомбинантной ДНК. Тест на антитела ( ИФА или вестерн-блоттинг ) использует рекомбинантный белок ВИЧ для проверки наличия антител , которые организм вырабатывает в ответ на ВИЧ-инфекцию. ДНК-тест позволяет выявить наличие генетического материала ВИЧ с помощью полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). Разработка теста RT-PCR стала возможной благодаря молекулярному клонированию и анализу последовательности геномов ВИЧ. Страница тестирования на ВИЧ от Центров по контролю заболеваний США (CDC)
Золотой рис — это рекомбинантный сорт риса, созданный для экспрессии ферментов, ответственных за биосинтез β-каротина . [14] Этот сорт риса имеет существенные перспективы для снижения заболеваемости дефицитом витамина А среди населения мира. [28] Золотой рис в настоящее время не используется до решения вопросов регулирования и интеллектуальной собственности. [29]
Были разработаны коммерческие сорта важных сельскохозяйственных культур (включая сою, кукурузу/кукурузу, сорго, канолу, люцерну и хлопок), которые включают рекомбинантный ген, который приводит к устойчивости к гербициду глифосату (торговое название Раундап ) и упрощает борьбу с сорняками с помощью глифосата. приложение. [30] Эти культуры широко используются в коммерческих целях в нескольких странах.
Bacillus thuringiensis — это бактерия, которая естественным образом производит белок ( токсин Bt ) с инсектицидными свойствами. [28] Бактерия уже много лет применяется к сельскохозяйственным культурам в качестве стратегии борьбы с насекомыми, и эта практика получила широкое распространение в сельском хозяйстве и садоводстве. Недавно были разработаны растения, экспрессирующие рекомбинантную форму бактериального белка, которая может эффективно контролировать некоторых насекомых-хищников. Экологические проблемы, связанные с использованием этих трансгенных культур, до конца не решены. [31]
Идея рекомбинантной ДНК была впервые предложена Питером Лоббаном, аспирантом профессора Дейла Кайзера на кафедре биохимии Медицинской школы Стэнфордского университета. [32] Первые публикации, описывающие успешное производство и внутриклеточную репликацию рекомбинантной ДНК, появились в 1972 и 1973 годах в Стэнфорде и Калифорнийском университете в Сан-Франциско . [33] [34] [35] [36] В 1980 году Пол Берг , профессор кафедры биохимии в Стэнфорде и автор одной из первых статей [33], был удостоен Нобелевской премии по химии за свою работу по нуклеиновым кислотам. «с особым вниманием к рекомбинантной ДНК». Вернер Арбер , Гамильтон Смит и Дэниел Натанс получили Нобелевскую премию по физиологии и медицине 1978 года за открытие эндонуклеаз рестрикции , которые усовершенствовали методы технологии рДНК. [ нужна цитата ]
Стэнфордский университет подал заявку на патент США на рекомбинантную ДНК 4 ноября 1974 года, указав изобретателей Герберта В. Бойера (профессора Калифорнийского университета в Сан-Франциско ) и Стэнли Н. Коэна (профессора Стэнфордского университета ); этот патент, US 4,237,224A, был выдан 2 декабря 1980 года. [37] [38] Первым лицензированным препаратом, созданным с использованием технологии рекомбинантной ДНК, был человеческий инсулин, разработанный Genentech и лицензированный Eli Lilly and Company . [39]
Ученые, принимавшие участие в первоначальной разработке методов рекомбинантной ДНК, признали, что организмы, содержащие рекомбинантную ДНК, могут иметь нежелательные или опасные свойства. На Асиломарской конференции 1975 года по рекомбинантной ДНК эти проблемы обсуждались, и был инициирован добровольный мораторий на исследования рекомбинантной ДНК для экспериментов, которые считались особенно рискованными. Этот мораторий широко соблюдался до тех пор, пока Национальные институты здравоохранения (США) не разработали и не выпустили официальные рекомендации по работе с рДНК. Сегодня рекомбинантные молекулы ДНК и рекомбинантные белки обычно не считаются опасными. Однако сохраняются опасения по поводу некоторых организмов, экспрессирующих рекомбинантную ДНК, особенно когда они покидают лабораторию и попадают в окружающую среду или пищевую цепь. Эти проблемы обсуждаются в статьях о генетически модифицированных организмах и спорах о генетически модифицированных продуктах питания . Кроме того, существуют опасения по поводу побочных продуктов биофармацевтического производства, где рекомбинантная ДНК приводит к образованию специфических белковых продуктов. Основной побочный продукт, называемый белком клетки-хозяина , поступает из системы экспрессии хозяина и представляет угрозу для здоровья пациента и окружающей среды в целом. [40] [41]