
_STM.jpg/440px-Pentacene_on_Ni(111)_STM.jpg)

Молекула — это группа из двух или более атомов , удерживаемых вместе силами притяжения, известными как химические связи ; в зависимости от контекста термин может включать или не включать ионы , удовлетворяющие этому критерию. [4] [5] [6] [7] [8] В квантовой физике , органической химии и биохимии различие с ионами не учитывается, и слово «молекула» часто используется, когда речь идет о многоатомных ионах .
Молекула может быть гомоядерной , т. е. состоящей из атомов одного химического элемента , например двух атомов в молекуле кислорода (О 2 ); или это может быть гетероядерное химическое соединение , состоящее из более чем одного элемента, например воды (два атома водорода и один атом кислорода; H 2 O). В кинетической теории газов термин « молекула» часто используется для обозначения любой газообразной частицы независимо от ее состава. Это ослабляет требование о том, чтобы молекула содержала два или более атомов, поскольку благородные газы представляют собой отдельные атомы. [9] Атомы и комплексы, связанные нековалентными взаимодействиями , такими как водородные или ионные связи , обычно не считаются отдельными молекулами. [10]
Концепции, подобные молекулам, обсуждались с древних времен, но современные исследования природы молекул и их связей начались в 17 веке. Усовершенствованное со временем такими учеными, как Роберт Бойл , Амедео Авогадро , Жан Перрен и Лайнус Полинг , изучение молекул сегодня известно как молекулярная физика или молекулярная химия.
Согласно Мерриам-Вебстеру и Интернет-словарю этимологии , слово «молекула» происходит от латинского « моль » или небольшой единицы массы. Слово происходит от французского molécule (1678), от неолатинского molecula , уменьшительного от латинского moles «масса, барьер». Слово, которое до конца 18 века использовалось только в латинской форме, стало популярным после того, как его использовал в философских трудах Декарт . [11] [12]
Определение молекулы развивалось по мере увеличения знаний о структуре молекул. Более ранние определения были менее точными, определяя молекулы как мельчайшие частицы чистых химических веществ , которые все еще сохраняют свой состав и химические свойства. [13] Это определение часто не соответствует действительности, поскольку многие вещества в обычном опыте, такие как камни , соли и металлы , состоят из крупных кристаллических сетей химически связанных атомов или ионов , но не состоят из дискретных молекул.
Современная концепция молекул восходит к донаучным и греческим философам, таким как Левкипп и Демокрит , которые утверждали, что вся Вселенная состоит из атомов и пустот . Около 450 г. до н.э. Эмпедокл представил фундаментальные элементы ( огонь (![]() ), земля (
), земля (![]() ), воздух (
), воздух (![]() ) и вода (
) и вода (![]() )) и «силы» притяжения и отталкивания, позволяющие элементам взаимодействовать.
)) и «силы» притяжения и отталкивания, позволяющие элементам взаимодействовать.
Пятый элемент, нетленная квинтэссенция эфира , считался фундаментальным строительным блоком небесных тел. Точка зрения Левкиппа и Эмпедокла, наряду с эфиром, была принята Аристотелем и передана в средневековую и ренессансную Европу.
Однако в более конкретном смысле концепция агрегатов или единиц связанных атомов, то есть «молекул», берет свое начало от гипотезы Роберта Бойля 1661 года в его знаменитом трактате «Скептический химик » о том, что материя состоит из скоплений частиц. и что химические изменения происходят в результате перегруппировки кластеров. Бойль утверждал, что основные элементы материи состоят из частиц различного типа и размера, называемых «тельцами», которые способны объединяться в группы. В 1789 году Уильям Хиггинс опубликовал взгляды на то, что он назвал комбинациями «предельных» частиц, что предвосхитило концепцию валентных связей . Если бы, например, по Хиггинсу, сила между предельной частицей кислорода и предельной частицей азота была равна 6, то сила силы разделилась бы соответственно, и аналогично для других комбинаций предельных частиц.
Амедео Авогадро придумал слово «молекула». [14] В своей статье 1811 года «Очерк определения относительных масс элементарных молекул тел» он, по сути, утверждает, то есть в соответствии с « Краткой историей химии» Партингтона , что: [15]
Мельчайшие частицы газов не обязательно являются простыми атомами, а состоят из определенного числа этих атомов, объединенных притяжением в одну молекулу .
В соответствии с этими концепциями в 1833 году французский химик Марк Антуан Огюст Годен представил четкое объяснение гипотезы Авогадро [16] относительно атомных весов, используя «объемные диаграммы», которые ясно показывают как полуправильную молекулярную геометрию, так и как линейная молекула воды, и правильные молекулярные формулы, например H 2 O:

В 1917 году неизвестный американский инженер-химик по имени Лайнус Полинг изучал метод соединения крючком Дальтона , который в то время был основным описанием связей между атомами. Полинг, однако, не был удовлетворен этим методом и обратился к новой области квантовой физики в поисках нового метода. В 1926 году французский физик Жан Перрен получил Нобелевскую премию по физике за убедительное доказательство существования молекул. Он сделал это, рассчитав константу Авогадро тремя различными методами, каждый из которых включал системы жидкой фазы. Во-первых, он использовал эмульсию, похожую на мыло , во-вторых, проведя экспериментальную работу по броуновскому движению , и в-третьих, подтвердив теорию Эйнштейна о вращении частиц в жидкой фазе. [17]
В 1927 году физики Фриц Лондон и Уолтер Гейтлер применили новую квантовую механику к насыщаемым, нединамическим силам притяжения и отталкивания, то есть силам обмена, молекулы водорода. Их подход к этой проблеме в области валентных связей в их совместной статье [18] стал важной вехой в том, что она подвела химию к квантовой механике. Их работа оказала влияние на Полинга, который только что получил докторскую степень и посетил Гейтлера и Лондон в Цюрихе по стипендии Гуггенхайма .
Впоследствии, в 1931 году, основываясь на работах Гейтлера и Лондона, а также на теориях, изложенных в знаменитой статье Льюиса, Полинг опубликовал свою новаторскую статью «Природа химической связи» [19] , в которой он использовал квантовую механику для расчета свойств и структуры молекул, такие как углы между связями и вращение вокруг связей. Основываясь на этих концепциях, Полинг разработал теорию гибридизации для объяснения связей в таких молекулах, как CH 4 , в которых четыре sp³-гибридизированные орбитали перекрываются 1s - орбиталью водорода , образуя четыре сигма (σ) связи . Четыре связи имеют одинаковую длину и силу, что дает молекулярную структуру, показанную ниже:
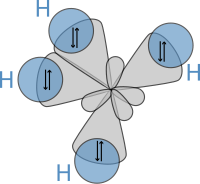
Наука о молекулах называется молекулярной химией или молекулярной физикой , в зависимости от того, на чем основное внимание уделяется химии или физике. Молекулярная химия изучает законы взаимодействия между молекулами, приводящие к образованию и разрыву химических связей, а молекулярная физика изучает законы, управляющие их структурой и свойствами. Однако на практике это различие расплывчато. В молекулярных науках молекула состоит из стабильной системы ( связанного состояния ), состоящей из двух или более атомов. Многоатомные ионы иногда можно рассматривать как электрически заряженные молекулы. Термин «нестабильная молекула» используется для обозначения очень реакционноспособных частиц, то есть кратковременных ансамблей ( резонансов ) электронов и ядер , таких как радикалы , молекулярные ионы , молекулы Ридберга , переходные состояния , комплексы Ван-дер-Ваальса или системы сталкивающихся атомов, как в Конденсат Бозе-Эйнштейна .
Молекулы как компоненты материи распространены. Они также составляют большую часть океанов и атмосферы. Большинство органических веществ представляют собой молекулы. Субстанциями жизни являются молекулы, например белки, аминокислоты, из которых они состоят, нуклеиновые кислоты (ДНК и РНК), сахара, углеводы, жиры и витамины. Питательные минералы обычно представляют собой ионные соединения, а не молекулы, как, например, сульфат железа.
Однако большинство известных твердых веществ на Земле частично или полностью состоят из кристаллов или ионных соединений, которые не состоят из молекул. К ним относятся все минералы, составляющие вещество Земли: песок, глина, галька, камни, валуны, коренная порода , расплавленные недра и ядро Земли . Все они содержат множество химических связей, но не состоят из идентифицируемых молекул.
Невозможно определить типичную молекулу ни для солей, ни для ковалентных кристаллов , хотя они часто состоят из повторяющихся элементарных ячеек , которые простираются либо в плоскости , например графен ; или трехмерно, например , алмаз , кварц , хлорид натрия . Тема повторяющейся элементарной ячеистой структуры также актуальна для большинства металлов, которые представляют собой конденсированные фазы с металлическими связями . Таким образом, твердые металлы не состоят из молекул. В стеклах , которые представляют собой твердые вещества, существующие в стекловидном неупорядоченном состоянии, атомы удерживаются вместе химическими связями без присутствия какой-либо определяемой молекулы или какой-либо регулярности повторяющейся элементарной клеточной структуры, которая характеризует соли, ковалентные кристаллы и металлы.
Молекулы обычно удерживаются вместе за счет ковалентной связи . Некоторые неметаллические элементы существуют в окружающей среде только в виде молекул либо в соединениях, либо в виде гомоядерных молекул, а не в виде свободных атомов: например, водород.
В то время как некоторые люди говорят, что металлический кристалл можно рассматривать как одну гигантскую молекулу, скрепленную металлическими связями , [20] другие отмечают, что металлы ведут себя совсем иначе, чем молекулы. [21]

Ковалентная связь — это химическая связь, которая предполагает совместное использование электронных пар между атомами. Эти электронные пары называются общими парами или связующими парами , а стабильный баланс сил притяжения и отталкивания между атомами, когда они разделяют электроны, называется ковалентной связью . [22]

Ионная связь — это тип химической связи, который включает электростатическое притяжение между противоположно заряженными ионами и является основным взаимодействием, происходящим в ионных соединениях . Ионы — это атомы, потерявшие один или несколько электронов (называемые катионами ), и атомы, получившие один или несколько электронов (называемые анионами ). [23] Этот перенос электронов называется электровалентностью в отличие от ковалентности . В простейшем случае катионом является атом металла , а анионом – атом неметалла , но эти ионы могут иметь более сложную природу, например, молекулярные ионы типа NH 4 + или SO 4 2- . При нормальных температурах и давлениях ионная связь в основном создает твердые тела (а иногда и жидкости) без отдельных идентифицируемых молекул, но испарение/сублимация таких материалов действительно приводит к образованию отдельных молекул, в которых электроны все еще передаются достаточно полно, чтобы связи можно было считать ионными, а не ковалентными. .
Большинство молекул слишком малы, чтобы их можно было увидеть невооруженным глазом, хотя молекулы многих полимеров могут достигать макроскопических размеров, включая такие биополимеры , как ДНК . Молекулы, обычно используемые в качестве строительных блоков для органического синтеза, имеют размер от нескольких ангстрем (Å) до нескольких десятков Å, или около одной миллиардной метра. Отдельные молекулы обычно невозможно наблюдать с помощью света (как отмечалось выше), но в некоторых случаях небольшие молекулы и даже контуры отдельных атомов можно проследить с помощью атомно-силового микроскопа . Некоторые из крупнейших молекул представляют собой макромолекулы или супермолекулы .
Самая маленькая молекула — двухатомный водород (H 2 ) с длиной связи 0,74 Å. [24]
Эффективный молекулярный радиус — это размер молекулы в растворе. [25] [26] Таблица селективности для различных веществ содержит примеры.
В химической формуле молекулы используется одна строка символов химических элементов, цифр, а иногда и других символов, таких как круглые скобки, тире, квадратные скобки, а также знаки плюс (+) и минус (-). Они ограничены одной типографской строкой символов, которая может включать нижние и верхние индексы.
Эмпирическая формула соединения представляет собой очень простой тип химической формулы. [27] Это простейшее целочисленное соотношение химических элементов, из которых он состоит. [28] Например, вода всегда состоит из атомов водорода и кислорода в соотношении 2:1, а этанол (этиловый спирт) всегда состоит из углерода, водорода и кислорода в соотношении 2:6:1. Однако это не определяет однозначно тип молекулы — например, диметиловый эфир имеет те же соотношения, что и этанол. Молекулы с одинаковыми атомами в разном расположении называются изомерами . Также углеводы, например, имеют одинаковое соотношение (углерод:водород:кислород = 1:2:1) (и, следовательно, одну и ту же эмпирическую формулу), но разное общее количество атомов в молекуле.
Молекулярная формула отражает точное количество атомов, составляющих молекулу, и таким образом характеризует различные молекулы. Однако разные изомеры могут иметь одинаковый атомный состав, но при этом быть разными молекулами.
Эмпирическая формула часто совпадает с молекулярной формулой, но не всегда. Например, молекула ацетилена имеет молекулярную формулу C 2 H 2 , но самое простое целочисленное соотношение элементов – CH.
Молекулярная масса может быть рассчитана по химической формуле и выражается в условных атомных единицах массы , равных 1/12 массы нейтрального атома углерода-12 ( изотопа 12 C ). Для сетчатых твердых тел термин « формульная единица» используется в стехиометрических расчетах.
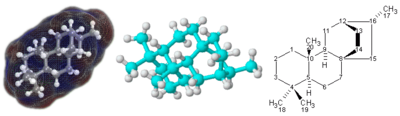
Для молекул со сложной трехмерной структурой, особенно с участием атомов, связанных с четырьмя различными заместителями, простой молекулярной формулы или даже полуструктурной химической формулы может быть недостаточно для полного описания молекулы. В этом случае может потребоваться графический тип формулы, называемый структурной формулой . Структурные формулы, в свою очередь, могут быть представлены одномерным химическим названием, но такая химическая номенклатура требует многих слов и терминов, которые не являются частью химических формул.
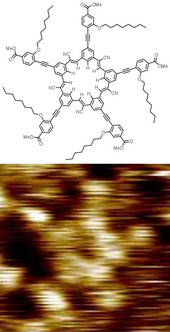
Молекулы имеют фиксированную равновесную геометрию — длины связей и углы, — вокруг которой они постоянно колеблются посредством вибрационных и вращательных движений. Чистое вещество состоит из молекул одинаковой средней геометрической структуры. Химическая формула и структура молекулы являются двумя важными факторами, определяющими ее свойства, особенно ее реакционную способность . Изомеры имеют общую химическую формулу, но обычно имеют очень разные свойства из-за разной структуры. Стереоизомеры , особый тип изомеров, могут иметь очень схожие физико-химические свойства и в то же время различную биохимическую активность.

Молекулярная спектроскопия занимается откликом ( спектром ) молекул, взаимодействующих с зондирующими сигналами известной энергии (или частоты , согласно соотношению Планка ). Молекулы имеют квантованные уровни энергии, которые можно анализировать, обнаружив энергетический обмен молекулы посредством поглощения или излучения . [31] Спектроскопия обычно не относится к дифракционным исследованиям, где частицы, такие как нейтроны , электроны или рентгеновские лучи высокой энергии , взаимодействуют с регулярным расположением молекул (как в кристалле).
Микроволновая спектроскопия обычно измеряет изменения во вращении молекул и может использоваться для идентификации молекул в космическом пространстве. Инфракрасная спектроскопия измеряет вибрацию молекул, включая движения растяжения, изгиба или скручивания. Его обычно используют для определения типов связей или функциональных групп в молекулах. Изменения в расположении электронов приводят к линиям поглощения или излучения в ультрафиолетовом, видимом или ближнем инфракрасном свете и приводят к цвету. Спектроскопия ядерного резонанса измеряет окружение определенных ядер в молекуле и может использоваться для характеристики количества атомов в разных положениях в молекуле.
Изучение молекул методами молекулярной физики и теоретической химии во многом основано на квантовой механике и имеет важное значение для понимания химической связи. Простейшей из молекул является молекула-ион водорода H 2 + , а самой простой из всех химических связей является одноэлектронная связь . H 2 + состоит из двух положительно заряженных протонов и одного отрицательно заряженного электрона , а это означает, что уравнение Шредингера для системы решается легче из-за отсутствия электрон-электронного отталкивания. С развитием быстрых цифровых компьютеров стало возможным приближенное решение более сложных молекул, что стало одним из основных аспектов вычислительной химии .
Пытаясь строго определить, является ли расположение атомов достаточно стабильным , чтобы его можно было считать молекулой, ИЮПАК предполагает, что оно «должно соответствовать углублению на поверхности потенциальной энергии , достаточно глубокому, чтобы удерживать хотя бы одно колебательное состояние». [4] Это определение не зависит от характера взаимодействия между атомами, а лишь от силы взаимодействия. Фактически, он включает в себя слабосвязанные частицы, которые традиционно не считаются молекулами, такие как димер гелия He 2 , который имеет одно колебательное связанное состояние [32] и настолько слабо связан, что его можно наблюдать только при очень низких температурах. температуры.
Является ли расположение атомов достаточно стабильным , чтобы считаться молекулой, по своей сути является оперативным определением. Следовательно, с философской точки зрения молекула не является фундаментальной сущностью (в отличие, например, от элементарной частицы ); скорее, концепция молекулы — это способ химика сделать полезное заявление о силе взаимодействий атомного масштаба в мире, который мы наблюдаем.