В химии соль или ионное соединение — это химическое соединение , состоящее из ионной сборки положительно заряженных катионов и отрицательно заряженных анионов , [1] в результате чего образуется нейтральное соединение без суммарного электрического заряда . Составляющие ионы удерживаются вместе электростатическими силами, называемыми ионными связями .
Ионы компонентов соли могут быть либо неорганическими , например хлорид (Cl- ) , либо органическими , например ацетат ( CH
3главный операционный директор−
). Каждый ион может быть либо одноатомным (называемым простым ионом ), например фторидом (F- ) , натрием (Na + ) и хлоридом (Cl- ) в хлориде натрия , либо многоатомным , например сульфатом ( SO2−
4) и аммоний ( NH+
4) и карбонат ( CO2−
3) ионы в карбонате аммония . Соль, содержащая основные ионы гидроксид (OH- ) или оксид (O 2- ), относят к основаниям , например гидроксид натрия .
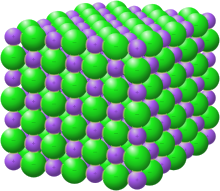
Отдельные ионы в соли обычно имеют несколько ближайших соседей, поэтому считаются не частью молекул, а частью непрерывной трехмерной сети. Соли в твердом состоянии обычно образуют кристаллические структуры .
Соли, состоящие из небольших ионов, обычно имеют высокие температуры плавления и кипения , являются твердыми и хрупкими . Будучи твердыми веществами, они почти всегда обладают электроизоляционными свойствами , но при плавлении или растворении они становятся высокопроводящими , поскольку ионы становятся подвижными. Некоторые соли содержат большие катионы, большие анионы или и то, и другое. По своим свойствам такие виды часто больше похожи на органические соединения.
.jpg/440px-X-ray_spectrometer,_1912._(9660569929).jpg)
В 1913 году структуру хлорида натрия определили Уильям Генри Брэгг и Уильям Лоуренс Брэгг . [2] [3] [4] Это показало, что у каждого атома было шесть равноудаленных ближайших соседей , демонстрируя, что составляющие были расположены не в молекулах или конечных агрегатах, а вместо этого в виде сети с дальним кристаллическим порядком. [4] Было обнаружено, что многие другие неорганические соединения имеют схожие структурные особенности. [4] Вскоре было описано, что эти соединения состоят из ионов, а не из нейтральных атомов , но доказательства этой гипотезы не были найдены до середины 1920-х годов, когда были проведены эксперименты по отражению рентгеновских лучей (которые обнаруживают плотность электронов). [4] [5]
Основной вклад в развитие теоретической трактовки ионных кристаллических структур внесли Макс Борн , Фриц Габер , Альфред Ланде , Эрвин Маделунг , Пауль Петер Эвальд и Казимеж Фаянс . [6] Борн предсказал энергию кристаллов, основываясь на предположении об ионных компонентах, которые показали хорошее соответствие термохимическим измерениям, что еще раз подтвердило это предположение. [4]

_sulfate.jpg/440px-Lead(II)_sulfate.jpg)
Многие металлы, такие как щелочные металлы, непосредственно реагируют с электроотрицательными галогенными газами, образуя соли. [7] [8]
Соли образуются при испарении их растворов . [9] Как только раствор перенасыщается и образуется зародышеобразующее вещество. [9] Этот процесс широко распространен в природе и является средством образования эвапоритовых минералов. [10]
Нерастворимые ионные соединения можно осадить путем смешивания двух растворов: одного с катионом, а другого с анионом. Поскольку все растворы электрически нейтральны, два смешанных раствора также должны содержать противоионы противоположных зарядов. Чтобы гарантировать, что они не загрязняют осажденное ионное соединение, важно убедиться, что они также не выпадают в осадок. [11] Если два раствора содержат ионы водорода и ионы гидроксида в качестве противоионов, они вступят в реакцию друг с другом в так называемой кислотно-основной реакции или реакции нейтрализации с образованием воды. [12] Альтернативно, противоионы могут быть выбраны так, чтобы даже при объединении в один раствор они оставались растворимыми в качестве ионов-наблюдателей . [11]
Если растворителем является вода при методе образования испарением или осаждением, во многих случаях образующийся ионный кристалл также включает кристаллизационную воду , поэтому продукт известен как гидрат и может иметь совершенно другие химические свойства по сравнению с безводным материалом. [13]
Расплавленные соли затвердевают при охлаждении ниже точки замерзания . [14] Иногда это используется для твердофазного синтеза сложных ионных соединений из твердых реагентов, которые сначала плавятся вместе. [15] В других случаях твердые реагенты не нужно плавить, а вместо этого они могут реагировать по твердотельному пути реакции . В этом методе реагенты многократно тонко измельчаются в пасту, а затем нагреваются до температуры, при которой ионы соседних реагентов могут диффундировать вместе в течение того времени, пока смесь реагентов остается в печи. [8] Другие способы синтеза используют твердый прекурсор с правильным стехиометрическим соотношением нелетучих ионов, который нагревают для удаления других частиц. [8]
В некоторых реакциях между высокореактивными металлами (обычно из группы 1 или группы 2 ) и высокоэлектроотрицательными галогенными газами или водой атомы могут быть ионизированы путем переноса электрона , [16] процесс, термодинамически понимаемый с использованием цикла Борна-Габера . [17]
Соли образуются в результате солеобразующих реакций.

Ионы в ионных соединениях в первую очередь удерживаются вместе электростатическими силами между распределением заряда этих тел и, в частности, ионной связью, возникающей в результате дальнодействующего кулоновского притяжения между чистым отрицательным зарядом анионов и чистым положительным зарядом катионов. . [18] Существует также небольшая дополнительная сила притяжения из-за взаимодействий Ван-дер-Ваальса , которая составляет лишь около 1–2% энергии сцепления для небольших ионов. [19] Когда пара ионов подходит достаточно близко, чтобы их внешние электронные оболочки (большинство простых ионов имеют закрытые оболочки ) перекрывались, возникает сила отталкивания ближнего действия, [20] из-за принципа Паули . [21] Баланс между этими силами приводит к потенциальной энергетической яме с минимальной энергией, когда ядра разделены определенным равновесным расстоянием. [20]
Если на электронную структуру двух взаимодействующих тел влияет присутствие друг друга, ковалентные взаимодействия (неионные) также вносят вклад в общую энергию образующегося соединения. [22] Ионные соединения редко бывают чисто ионными, то есть удерживаются вместе только электростатическими силами. Связи даже между наиболее электроотрицательными / электроположительными парами, такими как пары во фториде цезия, обладают небольшой степенью ковалентности . [23] [24] И наоборот, ковалентные связи между разнородными атомами часто демонстрируют некоторое разделение зарядов и могут рассматриваться как имеющие частичный ионный характер. [22] Обстоятельства, при которых соединение будет иметь ионный или ковалентный характер, обычно можно понять, используя правила Фаянса , которые используют только заряды и размеры каждого иона. Согласно этим правилам, соединения с наиболее ионным характером будут иметь большие положительные ионы с низким зарядом, связанные с небольшим отрицательным ионом с высоким зарядом. [25] В более общем смысле можно применить теорию HSAB , согласно которой соединения с наиболее ионным характером — это соединения, состоящие из жестких кислот и жестких оснований: небольших, сильно заряженных ионов с большой разницей в электроотрицательности между анионом и катионом. [26] [27] Эта разница в электроотрицательности означает, что разделение зарядов и возникающий в результате дипольный момент сохраняются даже при контакте ионов (лишние электроны на анионах не переносятся и не поляризуются для нейтрализации катионов). [28]
Хотя химики классифицируют идеализированные типы связей как ионные или ковалентные, существование дополнительных типов, таких как, например , водородные связи и металлические связи , побудило некоторых философов науки предположить, что необходимы альтернативные подходы к пониманию связей. Это может быть возможно путем применения квантовой механики для расчета энергий связи. [29] [30]

Энергия решетки представляет собой сумму взаимодействия всех узлов со всеми остальными узлами. Для неполяризующихся сферических ионов для определения энергии электростатического взаимодействия необходимы только заряды и расстояния. Для любой конкретной идеальной кристаллической структуры все расстояния геометрически связаны с наименьшим межъядерным расстоянием. Таким образом, для каждой возможной кристаллической структуры полная электростатическая энергия может быть связана с электростатической энергией единичных зарядов на ближайшем соседнем расстоянии с помощью мультипликативной константы, называемой константой Маделунга [20] , которую можно эффективно вычислить с помощью суммы Эвальда . [31] Когда принимается разумная форма дополнительной энергии отталкивания, полная энергия решетки может быть смоделирована с использованием уравнения Борна-Ланде , [32] уравнения Борна -Майера или, при отсутствии структурной информации, уравнения Капустинского . [33]
Используя еще более простое приближение ионов как непроницаемых твердых сфер, расположение анионов в этих системах часто связано с плотноупакованным расположением сфер, при этом катионы занимают тетраэдрические или октаэдрические междоузлия . [34] [35] В зависимости от стехиометрии ионного соединения и координации (в основном определяемой соотношением радиусов ) катионов и анионов, обычно наблюдаются различные структуры, [36] которые теоретически рационализируются правилами Полинга . [37]
В некоторых случаях анионы принимают простую кубическую упаковку, и в результате наблюдаются общие структуры:
Некоторые ионные жидкости, особенно со смесями анионов или катионов, можно охладить достаточно быстро, чтобы не хватило времени для зарождения кристаллов , поэтому образуется ионное стекло (без дальнего порядка). [53]
В любом кристалле обычно есть некоторые дефекты. Для сохранения электронейтральности кристаллов дефекты, связанные с потерей катиона, будут связаны с потерей аниона, т. е. эти дефекты возникают парами. [54] Дефекты Френкеля состоят из катионной вакансии в паре с межузельным катионом и могут образовываться в любом месте кристалла. [54] Чаще всего встречаются в соединениях с низким координационным числом и катионами, которые намного меньше анионов. [55] Дефекты Шоттки состоят из одной вакансии каждого типа и возникают на поверхности кристалла, [54] чаще всего встречаются в соединениях с высоким координационным числом и когда анионы и катионы имеют одинаковый размер. [55] Если катионы имеют несколько возможных степеней окисления , то катионные вакансии могут компенсировать дефицит электронов на катионных участках с более высокими степенями окисления, что приводит к образованию нестехиометрического соединения . [54] Другой нестехиометрической возможностью является образование F-центра , свободного электрона, занимающего анионную вакансию. [56] Когда соединение имеет три или более ионных компонента, возможно еще больше типов дефектов. [54] Все эти точечные дефекты могут быть созданы посредством тепловых колебаний и иметь равновесную концентрацию. Поскольку они энергетически затратны, но энтропийно полезны, они встречаются в большей концентрации при более высоких температурах. После создания эти пары дефектов могут диффундировать практически независимо друг от друга, прыгая между узлами решетки. Эта подвижность дефектов является источником большинства явлений переноса внутри ионного кристалла, включая диффузию и ионную проводимость в твердом состоянии . [54] Когда вакансии сталкиваются с междоузлиями (Френкель), они могут рекомбинировать и аннигилировать друг друга. Аналогичным образом удаляются вакансии, когда они достигают поверхности кристалла (Шоттки). Дефекты кристаллической структуры обычно расширяют параметры решетки , снижая общую плотность кристалла. [54] Дефекты также приводят к тому, что ионы оказываются в совершенно разных локальных средах, что приводит к тому, что они испытывают различную симметрию кристаллического поля , особенно в случае, когда разные катионы обмениваются узлами решетки. [54] Это приводит к различному расщеплению d-электронных орбиталей , так что оптическое поглощение (и, следовательно, цвет) может меняться в зависимости от концентрации дефектов. [54]
Ионные соединения, содержащие ионы водорода (H + ), относят к кислотам , а содержащие электроположительные катионы [57] и основные анионы ионы гидроксид (OH- ) или оксид (O 2- ) — к основаниям. Другие ионные соединения известны как соли и могут образовываться в результате кислотно-основных реакций . [58] Если соединение является результатом реакции между сильной кислотой и слабым основанием , в результате образуется кислая соль . Если это результат реакции между сильным основанием и слабой кислотой , то в результате образуется основная соль . Если это результат реакции между сильной кислотой и сильным основанием, то в результате образуется нейтральная соль. Слабые кислоты, реагирующие со слабыми основаниями, могут образовывать ионные соединения как с сопряженным ионом основания , так и с сопряженным ионом кислоты, такие как ацетат аммония .
Некоторые ионы классифицируются как амфотерные , способные реагировать как с кислотой, так и с основанием. [59] Это также верно в отношении некоторых соединений ионного характера, обычно оксидов или гидроксидов менее электроположительных металлов (поэтому соединение также имеет значительный ковалентный характер), таких как оксид цинка , гидроксид алюминия , оксид алюминия и оксид свинца (II). . [60]
Электростатические силы между частицами наиболее сильны, когда заряды велики, а расстояние между ядрами ионов мало. В таких случаях соединения обычно имеют очень высокие температуры плавления и кипения и низкое давление пара . [61] Тенденции температуры плавления можно еще лучше объяснить, если принять во внимание структуру и соотношение размеров ионов. [62] При температуре выше точки плавления ионные твердые вещества плавятся и превращаются в расплавленные соли (хотя некоторые ионные соединения, такие как хлорид алюминия и хлорид железа (III), демонстрируют молекулоподобные структуры в жидкой фазе). [63] Неорганические соединения с простыми ионами обычно имеют небольшие ионы и, следовательно, имеют высокие температуры плавления, как и твердые вещества при комнатной температуре. Однако некоторые вещества с более крупными ионами имеют температуру плавления ниже или близкой к комнатной температуре (часто определяемую как до 100 °C) и называются ионными жидкостями . [64] Ионы в ионных жидкостях часто имеют неравномерное распределение заряда или объемистые заместители , такие как углеводородные цепи, которые также играют роль в определении силы взаимодействий и склонности к плавлению. [65]
Даже когда локальная структура и связи ионного твердого тела разрушаются настолько, что оно расплавляется, все еще существуют сильные дальнодействующие электростатические силы притяжения, удерживающие жидкость вместе и предотвращающие кипение ионов с образованием газовой фазы. [66] Это означает, что даже ионные жидкости при комнатной температуре имеют низкое давление пара и требуют значительно более высоких температур для кипения. [66] Точки кипения демонстрируют схожие тенденции с температурами плавления с точки зрения размера ионов и силы других взаимодействий. [66] При испарении ионы все еще не освобождаются друг от друга. Например, в паровой фазе хлорид натрия существует в виде двухатомных «молекул». [67]
Большинство ионных соединений очень хрупкие . Достигнув предела своей прочности, они не могут деформироваться податливо , поскольку необходимо поддерживать строгое выравнивание положительных и отрицательных ионов. Вместо этого материал подвергается разрушению в результате расщепления . [68] При повышении температуры (обычно близкой к температуре плавления) происходит пластично-хрупкий переход , и пластическое течение становится возможным за счет движения дислокаций . [68] [69]
Сжимаемость ионного соединения во многом определяется его структурой и, в частности, координационным числом . Например, галогениды со структурой хлорида цезия (координационное число 8) менее сжимаемы, чем галогениды со структурой хлорида натрия (координационное число 6), и снова меньше, чем галогениды со структурой 4. [70]

При растворении простых солей они диссоциируют на отдельные ионы, которые сольватируются и диспергируются по всему полученному раствору. Соли в растворе не существуют. [71] Напротив, молекулярные соединения, в том числе большинство органических соединений, остаются нетронутыми в растворе.
Растворимость солей самая высокая в полярных растворителях (таких как вода ) или ионных жидкостях , но имеет тенденцию быть низкой в неполярных растворителях (таких как бензин / бензин ). [72] Этот контраст обусловлен главным образом тем, что возникающие в результате ион-дипольные взаимодействия значительно сильнее, чем ионно-индуцированные дипольные взаимодействия, поэтому теплота растворения выше. Когда противоположно заряженные ионы в твердой ионной решетке окружены противоположным полюсом полярной молекулы, твердые ионы вытягиваются из решетки в жидкость. Если энергия сольватации превышает энергию решетки , отрицательное изменение чистой энтальпии раствора обеспечивает термодинамический стимул для удаления ионов с их позиций в кристалле и растворения в жидкости. Кроме того, изменение энтропии раствора обычно положительное для большинства твердых растворенных веществ, таких как ионные соединения, а это означает, что их растворимость увеличивается с повышением температуры. [73] Существуют некоторые необычные ионные соединения, такие как сульфат церия (III) , у которых это изменение энтропии отрицательное из-за дополнительного порядка, наведенного в воде при растворении, а растворимость уменьшается с температурой. [73]
Энергия решетки , силы сцепления между этими ионами внутри твердого тела, определяет растворимость. Растворимость зависит от того, насколько хорошо каждый ион взаимодействует с растворителем, поэтому становятся очевидными определенные закономерности. Например, соли натрия , калия и аммония обычно растворимы в воде. Заметные исключения включают гексахлорплатинат аммония и кобальтинитрит калия . Большинство нитратов и многие сульфаты растворимы в воде. Исключения включают сульфат бария , сульфат кальция (плохо растворимый) и сульфат свинца (II) , где спаривание 2+/2- приводит к высоким энергиям решетки. По тем же причинам большинство карбонатов металлов не растворяются в воде. Некоторые растворимые карбонатные соли: карбонат натрия , карбонат калия и карбонат аммония .

Соли являются характерными изоляторами . Хотя они содержат заряженные атомы или кластеры, эти материалы обычно не проводят электричество в сколько-нибудь значительной степени, когда вещество твердое. Чтобы проводить электричество, заряженные частицы должны быть подвижными , а не неподвижными в кристаллической решетке . В некоторой степени это достигается при высоких температурах, когда концентрация дефектов увеличивает подвижность ионов и наблюдается твердотельная ионная проводимость . Когда ионные соединения растворяются в жидкости или расплавляются в жидкость , они могут проводить электричество, поскольку ионы становятся полностью подвижными. По этой причине в качестве электролитов можно использовать жидкие (расплавленные) соли и растворы, содержащие растворенные соли (например, хлорид натрия в воде) . [75] Увеличение проводимости при растворении или плавлении иногда используется в качестве определяющей характеристики ионных соединений. [76]
В некоторых необычных ионных соединениях: проводниках быстрых ионов и ионных стеклах [53] один или несколько ионных компонентов обладают значительной подвижностью, обеспечивающей проводимость, даже если материал в целом остается твердым. [77] Это часто сильно зависит от температуры и может быть результатом фазового перехода или высокой концентрации дефектов. [77] Эти материалы используются во всех твердотельных суперконденсаторах , батареях и топливных элементах , а также в различных типах химических датчиков . [78] [79]
Цвет ионного соединения часто отличается от цвета водного раствора , содержащего составляющие его ионы [80] или гидратированной формы того же соединения. [13]
Анионы в соединениях со связями наиболее ионного характера имеют тенденцию быть бесцветными (с полосой поглощения в ультрафиолетовой части спектра). [81] В соединениях с менее ионным характером их цвет становится глубже через желтый, оранжевый, красный и черный (поскольку полоса поглощения смещается в сторону более длинных волн в видимый спектр). [81]
Полоса поглощения простых катионов смещается в сторону более коротких длин волн, когда они участвуют в более ковалентных взаимодействиях. [81] Это происходит во время гидратации ионов металлов, поэтому бесцветные безводные ионные соединения с анионом, поглощающим инфракрасное излучение, могут становиться окрашенными в растворе. [81]
Соли существуют самых разных цветов , которые возникают из составляющих их анионов, катионов или сольватов . Например:
Некоторые минералы представляют собой соли, некоторые из которых растворимы в воде. [ сомнительно ] [ необходимо разъяснение ] Точно так же неорганические пигменты, как правило, не являются солями, потому что для устойчивости требуется нерастворимость. Некоторые органические красители представляют собой соли, но они практически нерастворимы в воде.
Соли могут вызывать все пять основных вкусов , например, соленый ( хлорид натрия ), сладкий ( диацетат свинца , который при попадании в организм вызывает отравление свинцом), кислый ( битартрат калия ), горький ( сульфат магния ) и умами или пикантный ( глутамат натрия ). .
Соли сильных кислот и сильных оснований («сильные соли») нелетучи и часто не имеют запаха, тогда как соли слабых кислот или слабых оснований («слабые соли») могут пахнуть сопряженной кислотой (например, ацетаты, подобные уксусной кислоте (например, ацетаты, подобные уксусной кислоте). уксус ) и цианиды, такие как цианистый водород ( миндаль ) или сопряженное основание (например, соли аммония, такие как аммиак ) составляющих ионов. Это медленное частичное разложение обычно ускоряется присутствием воды, поскольку гидролиз — это вторая половина уравнения обратимой реакции образования слабых солей.
Ионные соединения уже давно имеют широкое применение и применение. Многие минералы являются ионными. [82] Люди обрабатывают поваренную соль (хлорид натрия) уже более 8000 лет, используя ее сначала в качестве пищевой приправы и консерванта, а теперь также в производстве, сельском хозяйстве , водоподготовке, для борьбы с обледенением дорог и во многих других целях. [83] Многие ионные соединения настолько широко используются в обществе, что имеют общие названия, не связанные с их химической идентичностью. Примеры этого включают буру , каломель , магнезиальное молоко , соляную кислоту , купоросное масло , селитру и гашеную известь . [84]
Растворимые ионные соединения, такие как соль, можно легко растворить с получением растворов электролитов . Это простой способ контролировать концентрацию и ионную силу . Концентрация растворенных веществ влияет на многие коллигативные свойства , включая увеличение осмотического давления и снижение температуры замерзания и повышение температуры кипения . [85] Поскольку растворенные вещества представляют собой заряженные ионы, они также увеличивают электропроводность раствора. [86] Повышенная ионная сила уменьшает толщину двойного электрического слоя вокруг коллоидных частиц и, следовательно, стабильность эмульсий и суспензий . [87]
Химическая идентичность добавленных ионов также важна во многих случаях. Например, фторидсодержащие соединения растворяются, чтобы обеспечить ионы фтора для фторирования воды . [88]
Твердые ионные соединения издавна используются в качестве пигментов красок и устойчивы к органическим растворителям, но чувствительны к кислотности и щелочности. [89] С 1801 года пиротехники описали и широко использовали металлосодержащие ионные соединения в качестве источников цвета в фейерверках. [90] При сильном нагреве электроны в ионах металлов или небольших молекулах могут возбуждаться. [91] Эти электроны позже возвращаются в состояния с более низкой энергией и испускают свет с цветовым спектром, характерным для присутствующих видов. [92] [93]
В химии ионные соединения часто используются в качестве прекурсоров для высокотемпературного твердотельного синтеза. [94]
Многие металлы геологически наиболее распространены в виде ионных соединений в рудах . [95] Чтобы получить элементарные материалы, эти руды обрабатываются путем плавки или электролиза , в ходе которых происходят окислительно-восстановительные реакции (часто с восстановителем, таким как углерод), в результате чего ионы металлов приобретают электроны и становятся нейтральными атомами. [96] [97]
Согласно номенклатуре , рекомендованной ИЮПАК , ионные соединения называются по их составу, а не по структуре. [98] В самом простом случае бинарного ионного соединения без возможной двусмысленности относительно зарядов и, следовательно, стехиометрии , общее название пишется с использованием двух слов. [99] Сначала идет название катиона (немодифицированное название элемента для одноатомных катионов), а затем название аниона. [100] [101] Например, MgCl 2 называется хлоридом магния , а Na 2 SO 4 — сульфатом натрия ( SO2−
4, сульфат , является примером многоатомного иона ). Чтобы получить эмпирическую формулу из этих названий, стехиометрию можно вывести из зарядов ионов и требования общей нейтральности заряда. [102]
Если имеется несколько различных катионов и/или анионов, для обозначения относительного состава часто требуются мультипликативные префиксы ( ди- , три- , тетра- , ...), [103] и тогда катионы перечисляются в алфавитном порядке. [104] Например, KMgCl 3 назван трихлоридом магния-калия , чтобы отличить его от K 2 MgCl 4 , тетрахлорида магния дикалия [105] (обратите внимание, что и в эмпирической формуле, и в письменном названии катионы располагаются в алфавитном порядке, но порядок между ними различается, потому что символ калия — K ). [106] Если один из ионов уже имеет мультипликативный префикс в своем названии, используются альтернативные мультипликативные префиксы ( бис- , трис- , тетракис- , ...). [107] Например, Ba(BrF 4 ) 2 называют бис(тетрафтордоброматом бария). [108]
Соединения, содержащие один или несколько элементов, которые могут существовать в различных степенях заряда/окисления, будут иметь стехиометрию, которая зависит от того, какие степени окисления присутствуют, чтобы обеспечить общую нейтральность. Это можно указать в названии, указав либо степень окисления присутствующих элементов, либо заряд ионов. [108] Из-за риска двусмысленности при определении степеней окисления ИЮПАК предпочитает прямое указание чисел заряда ионов. [108] Они записываются в виде арабского целого числа, за которым следует знак (... , 2−, 1−, 1+, 2+, ...) в круглых скобках непосредственно после названия катиона (без разделяющего их пробела). ). [108] Например, FeSO 4 называется сульфатом железа(2+) (при этом заряд 2+ на ионах Fe 2+ уравновешивает заряд 2- на сульфат-ионе), тогда как Fe 2 (SO 4 ) 3 называется железом. (3+) сульфат (поскольку каждый из двух ионов железа в каждой формульной единице имеет заряд 3+, чтобы уравновесить 2- на каждом из трех сульфат-ионов). [108] Номенклатура запасов , все еще широко используемая, записывает степень окисления римскими цифрами ( ..., -II, -I, 0, I, II, ...). Таким образом, приведенные выше примеры можно было бы назвать сульфатом железа (II) и сульфатом железа (III) соответственно. [109] Для простых ионов ионный заряд и степень окисления одинаковы, но для многоатомных ионов они часто различаются. Например, ион уранила(2+) UO2+
2, имеет уран в степени окисления +6, поэтому в номенклатуре Штока он будет называться ионом диоксоурана (VI). [110] Еще более старая система наименования катионов металлов, также широко используемая, добавляла суффиксы -ous и -ic к латинскому корню названия, чтобы дать специальные названия для низких и высоких степеней окисления. [111] Например, в этой схеме используются «железо» и «железо» для железа (II) и железа (III) соответственно, [111] поэтому приведенные выше примеры классически назывались сульфатом железа и сульфатом железа . [ нужна цитата ]
К распространенным солеобразующим катионам относятся:
Обычные солеобразующие анионы (исходные кислоты в скобках, если таковые имеются) включают:
Соли с различным количеством атомов водорода, замененных катионами по сравнению с их исходной кислотой, могут называться одноосновными , двухосновными или трехосновными , что указывает на то, что заменены один, два или три атома водорода; Многоосновные соли относятся к солям, в которых заменено более одного атома водорода. Примеры включают в себя:
Соли можно классифицировать по-разному. Соли, образующие ионы гидроксида при растворении в воде , называются солями щелочных металлов , а соли, образующие ионы водорода при растворении в воде, называются солями кислот . Нейтральные соли – это те соли, которые не являются ни кислотными, ни щелочными. Цвиттер-ионы содержат анионный и катионный центры в одной молекуле , но не считаются солями. Примерами цвиттер-ионов являются аминокислоты , многие метаболиты , пептиды и белки . [112]
Сильные соли или соли сильных электролитов — это химические соли, состоящие из сильных электролитов . Эти соли полностью или почти полностью диссоциируют в воде . Они, как правило, не имеют запаха и нелетучи .
Сильные соли начинаются с Na__, K__, NH 4 __ или заканчиваются __NO 3 , __ClO 4 или __CH 3 COO. Большинство металлов 1 и 2 групп образуют сильные соли. Сильные соли особенно полезны при создании проводящих соединений, поскольку входящие в их состав ионы обеспечивают большую проводимость. [ нужна цитата ]
Слабые соли или соли со слабым электролитом состоят из слабых электролитов . Эти соли плохо диссоциируют в воде. Они, как правило, более летучи , чем сильные соли. По запаху они могут быть похожи на кислоту или основание, из которых они получены. Например, ацетат натрия CH 3 COONa по запаху похож на уксусную кислоту CH 3 COOH.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )