Тиреоидит Хашимото , также известный как хронический лимфоцитарный тиреоидит и болезнь Хашимото , является аутоиммунным заболеванием , при котором щитовидная железа постепенно разрушается. [1] [6] Немного более широкий термин — аутоиммунный тиреоидит , идентичный за исключением того, что он также используется для описания похожего состояния без зоба. [7] [8]
На ранней стадии симптомы могут быть незаметны. [1] Со временем щитовидная железа может увеличиться, образуя безболезненный зоб . [1] У некоторых людей в конечном итоге развивается гипотиреоз с сопутствующим увеличением веса , усталостью , запорами , депрессией , выпадением волос и общими болями. [1] После многих лет щитовидная железа обычно уменьшается в размерах. [1] К потенциальным осложнениям относится лимфома щитовидной железы . [2] Кроме того, поскольку у нелеченных пациентов с болезнью Хашимото часто развивается гипотиреоз, дальнейшие осложнения могут включать, помимо прочего, высокий уровень холестерина , болезни сердца , сердечную недостаточность , высокое кровяное давление , микседему и потенциальные проблемы с беременностью. [9]
Считается, что тиреоидит Хашимото возникает из-за сочетания генетических и экологических факторов . [4] Факторы риска включают семейный анамнез заболевания и наличие другого аутоиммунного заболевания. [1] Диагноз подтверждается анализами крови на ТТГ , Т4 и антитиреоидные аутоантитела . [1] Другие состояния, которые могут вызывать похожие симптомы, включают болезнь Грейвса и нетоксический узловой зоб . [5]
Тиреоидит Хашимото обычно лечат левотироксином . [1] [10] Если гипотиреоз отсутствует, некоторые могут рекомендовать не лечиться, в то время как другие могут лечить, чтобы попытаться уменьшить размер зоба. [1] [11] Больным следует избегать употребления большого количества йода ; однако, достаточное количество йода необходимо, особенно во время беременности. [1] Хирургическое вмешательство для лечения зоба требуется редко. [5]
Тиреоидит Хашимото поражает около 5% белых людей западноевропейского происхождения в какой-то момент их жизни. [4] Это самая распространенная причина гипотиреоза в регионах мира с достаточным содержанием йода. [12] Обычно он начинается в возрасте от 30 до 50 лет и гораздо чаще встречается у женщин, чем у мужчин. [1] [3] Показатели заболевания, по-видимому, растут. [5] Впервые он был описан японским врачом Хакару Хашимото в 1912 году. [13] В 1957 году он был признан аутоиммунным заболеванием. [14]
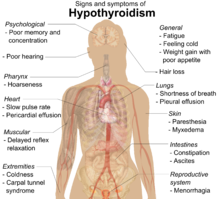

Многие симптомы связаны с развитием тиреоидита Хашимото. Наиболее распространенные симптомы включают: усталость , увеличение веса, бледное или опухшее лицо, чувство холода, боли в суставах и мышцах , запоры , сухие и истонченные волосы, обильные менструации или нерегулярные месячные , депрессию , паническое расстройство , замедленный сердечный ритм , а также проблемы с зачатием и выкидыши . [15]
У некоторых пациентов на ранней стадии заболевания могут наблюдаться симптомы гипертиреоза из-за высвобождения тиреоидных гормонов из-за периодического разрушения щитовидной железы. [16]
Болезнь Хашимото встречается примерно в семь раз чаще у женщин, чем у мужчин. Она может возникнуть у подростков и молодых женщин, но чаще всего появляется в среднем возрасте , особенно у мужчин. Люди, у которых развивается болезнь Хашимото, часто имеют членов семьи, которые имеют заболевания щитовидной железы или другие аутоиммунные заболевания, а иногда и сами имеют другие аутоиммунные заболевания. [17]
Ранние стадии аутоиммунного тиреоидита могут иметь нормальный физический осмотр с зобом или без него. [18] Зоб - это диффузное, часто симметричное, опухание щитовидной железы, видимое на передней поверхности шеи, которое может развиться. [18] Щитовидная железа может стать твердой, большой и дольчатой при тиреоидите Хашимото, но изменения в щитовидной железе также могут быть непальпируемыми. [19] Увеличение щитовидной железы происходит из-за лимфоцитарной инфильтрации и фиброза , а не гипертрофии ткани . Хотя их роль в первоначальном разрушении фолликулов неясна , антитела против тиреоидной пероксидазы или тиреоглобулина имеют значение, поскольку они служат маркерами для выявления заболевания и его тяжести. [20] Считается, что они являются вторичными продуктами разрушения железы, опосредованного Т-клетками . [21]
По мере прогрессирования лимфоцитарной инфильтрации у пациентов могут проявляться признаки гипотиреоза во многих системах организма, включая, помимо прочего, увеличение зоба, увеличение веса, непереносимость холода, утомляемость, микседему, запоры, нарушения менструального цикла, бледную или сухую кожу, сухие, ломкие волосы, депрессию, атаксию и мышечную слабость. [18] [12]
У пациентов с зобом, страдающих аутоиммунным тиреоидитом в течение многих лет, зоб может уменьшиться на поздних стадиях заболевания из-за разрушения щитовидной железы. [16]
Хотя гипотиреоз, вызванный аутоиммунным тиреоидитом, встречается редко, более серьезными осложнениями являются перикардиальный выпот , плевральный выпот , оба из которых требуют дальнейшего медицинского внимания, и микседематозная кома , которая является неотложным эндокринным состоянием. [12]
Болезнь Грейвса может возникнуть до или после развития аутоиммунного тиреоидита. [22] У пациентов также могут быть сопутствующие аутоиммунные заболевания других органов. К ним могут относиться болезнь Аддисона , диабет 1 типа , синдром Шегрена , целиакия и ревматоидный артрит . [18] [16] Аутоиммунный тиреоидит также наблюдался у пациентов с аутоиммунными полиэндокринными синдромами 1 и 2 типа. [22]
Аутоиммунитет щитовидной железы может быть семейным. [7] Многие пациенты сообщают о семейном анамнезе аутоиммунного тиреоидита или болезни Грейвса . [18] Исследования близнецов выявили конкордантность болезни Хашимото у монозиготных близнецов. [12]
Сильный генетический компонент подтверждается в исследованиях монозиготных близнецов , с конкордантностью 38–55%, с еще более высокой конкордантностью циркулирующих тиреоидных антител, не связанной с клинической картиной (до 80% у монозиготных близнецов). Ни один из результатов не был замечен в аналогичной степени у дизиготных близнецов , что дает сильное преимущество высокой генетической этиологии . [23]
Определенные лекарства или препараты связаны с изменением и вмешательством в функцию щитовидной железы. У этих лекарств есть два основных механизма вмешательства, которые они могут иметь. [24]
Одним из механизмов вмешательства является изменение препаратом белков переноса сывороточных гормонов щитовидной железы. [24] Эстроген , тамоксифен , героин , метадон , клофибрат , 5-флуороурацил , митотан и перфеназин увеличивают концентрацию тиреоидсвязывающего глобулина (ТСГ). [24] Андрогены , анаболические стероиды, такие как даназол , глюкокортикоиды и медленно высвобождающаяся никотиновая кислота снижают концентрацию ТСГ. Фуросемид , фенофленак, мефенамовая кислота , салицилаты , фенитоин , диазепам , сульфонилмочевины , свободные жирные кислоты и гепарин мешают связыванию тиреоидных гормонов с ТСГ и/или транстиретином . [24]
Другим механизмом, который могут использовать лекарства для вмешательства в функцию щитовидной железы, является изменение внетиреоидного метаболизма гормонов щитовидной железы. Пропилтиоурацил, глюкокортикоиды, пропранолол, ионизированные контрастные вещества, амиодарон и кломипрамин — все они ингибируют преобразование Т4 и Т3. [24] Фенобарбитал, рифампицин, фенитоин и карбамазепин — все они усиливают печеночный метаболизм. [24] Наконец, холестриамин, колестипол, гидроксид алюминия, сульфат железа и сукральфат — все это препараты, которые снижают абсорбцию Т4 или усиливают экскрецию. [24]
Первый локус гена, связанный с аутоиммунным заболеванием щитовидной железы, был областью главного комплекса гистосовместимости (MHC) на хромосоме 6p21. Он кодирует HLA. Определенные аллели HLA имеют более высокое сродство к аутоантигенным тиреоидным пептидам и могут способствовать развитию аутоиммунного заболевания щитовидной железы. В частности, при болезни Хашимото была продемонстрирована аберрантная экспрессия HLA II на тироцитах. Они могут представлять аутоантигены щитовидной железы и инициировать аутоиммунное заболевание щитовидной железы. [25] Аллели восприимчивости не являются постоянными при болезни Хашимото. У европеоидов, как сообщается, с заболеванием связаны различные аллели, включая DR3, DR5 и DQ7. [26] [27]
Этот ген является вторым основным иммунорегуляторным геном, связанным с аутоиммунным заболеванием щитовидной железы. Полиморфизмы гена CTLA-4 могут способствовать снижению ингибирования пролиферации Т-клеток и повышению восприимчивости к аутоиммунному ответу. [28] CTLA-4 является основным геном восприимчивости к аутоантителам щитовидной железы. Связь региона CTLA-4 с наличием аутоантител щитовидной железы была продемонстрирована с помощью анализа сцепления всего генома. [29] CTLA-4 был подтвержден как основной локус для аутоантител щитовидной железы. [30]
PTPN22 — это недавно идентифицированный иммунорегуляторный ген, связанный с аутоиммунным заболеванием щитовидной железы. Он расположен на хромосоме 1p13 и экспрессируется в лимфоцитах. Он действует как отрицательный регулятор активации Т-клеток. Мутация в этом гене является фактором риска для многих аутоиммунных заболеваний. Более слабая сигнализация Т-клеток может привести к нарушению тимической делеции аутореактивных Т-клеток, а повышенная функция PTPN22 может привести к ингибированию регуляторных Т-клеток, которые защищают от аутоиммунитета. [31]
IFN-γ способствует клеточно-опосредованной цитотоксичности против щитовидной железы. Мутации, вызывающие повышенную продукцию IFN-γ, были связаны с тяжестью гипотиреоза. [32] Тяжелый гипотиреоз связан с мутациями, приводящими к снижению продукции IL-4 (цитокин Th2, подавляющий клеточно-опосредованный аутоиммунитет), [33] снижением секреции TGF-β (ингибитор продукции цитокинов), [34] и мутациями FoxP3, важнейшего регуляторного фактора для развития Tregs. [35] Развитие болезни Хашимото было связано с мутацией гена TNF-α (стимулятор продукции IFN-γ), вызывающей его более высокую концентрацию. [36]
Предотвратимые факторы окружающей среды, включая высокое потребление йода, дефицит селена , инфекционные заболевания и некоторые лекарственные препараты, способствуют развитию аутоиммунного заболевания щитовидной железы у генетически предрасположенных лиц. [37]
Избыточное потребление йода является общепризнанным фактором окружающей среды, вызывающим аутоиммунитет щитовидной железы. Установлено, что аутоантитела к щитовидной железе более распространены в географических районах с более высоким содержанием йода в рационе. Было предложено несколько механизмов, посредством которых йод может способствовать аутоиммунитету щитовидной железы. Воздействие йода приводит к более высокому йодированию тиреоглобулина, увеличивая его иммуногенность за счет создания новых содержащих йод эпитопов или раскрытия скрытых эпитопов. Это может способствовать презентации АПК, усиливать сродство связывания рецептора Т-клеток и активировать специфические Т-клетки. [38]
Было показано, что воздействие йода повышает уровень активных форм кислорода. Они усиливают экспрессию внутриклеточной адгезионной молекулы-1 на фолликулярных клетках щитовидной железы, что может привлекать иммунокомпетентные клетки в щитовидную железу. [39]
Йод токсичен для тироцитов, поскольку высокореактивные формы кислорода могут связываться с мембранными липидами и белками. Он вызывает повреждение тироцитов и высвобождение аутоантигенов. Йод также способствует апоптозу фолликулярных клеток и оказывает влияние на иммунные клетки (усиление созревания дендритных клеток, увеличение количества Т-клеток, стимулирование продукции иммуноглобулинов В-клеток). [40] [41]
Данные датского исследования потребления йода и заболеваний щитовидной железы показывают, что в двух группах (мужчины, женщины) с умеренным и легким дефицитом йода уровни антител к тиреоидной пероксидазе и тиреоглобулину выше у женщин, а показатели распространенности обоих антител увеличиваются с возрастом. [42]
Исследование здоровых датских близнецов, разделенных на три группы (монозиготные и дизиготные пары близнецов одного пола и разнополые пары), показало, что генетический вклад в восприимчивость к антителам тиреопероксидазы составил 61% у мужчин и 72% у женщин, а вклад в восприимчивость к антителам тиреоглобулина составил 39% у мужчин и 75% у женщин. [43]
Высокая частота женского аутоиммунитета щитовидной железы может быть связана с Х-хромосомой. Она содержит гены, связанные с полом и иммунитетом, которые отвечают за иммунную толерантность. [44] Более высокая частота аутоиммунитета щитовидной железы была зарегистрирована у пациентов с более высоким уровнем моносомии Х-хромосомы в периферических лейкоцитах. [45]
Другим потенциальным механизмом может быть искаженная инактивация Х-хромосомы, приводящая к выходу аутоантигенов, связанных с Х-хромосомой, из зоны презентации в тимусе и потере толерантности Т-клеток. [ необходима цитата ]
Наличие других аутоиммунных заболеваний является фактором риска развития тиреоидита Хашимото, и обратное также верно. [1] Аутоиммунные заболевания, наиболее часто связанные с тиреоидитом Хашимото, включают целиакию , диабет 1 типа , витилиго и алопецию . [46]
Гены, вовлеченные в это, различаются в разных этнических группах, и заболеваемость увеличивается у людей с хромосомными нарушениями, включая синдромы Тернера , Дауна и Клайнфельтера, обычно связанные с аутоантителами против тиреоглобулина и тиреопероксидазы . Прогрессирующее истощение этих клеток в качестве цитотоксического иммунного ответа приводит к более высоким степеням первичного гипотиреоза, проявляющегося низкими уровнями Т3/Т4 и компенсаторным повышением ТТГ. [ необходима цитата ]
Механизм аутоиммунного тиреоидита не до конца изучен, но считается, что он развивается в результате сложного взаимодействия генетических и экологических факторов. [47] Аутоантитела к щитовидной железе появляются в основном при наличии лимфоцитов в целевом органе. [7] [48] Лимфоциты вырабатывают антитела, нацеленные на три различных белка щитовидной железы: антитела к тиреоидной пероксидазе (TPOAb), антитела к тиреоглобулину (TgAb) и антитела к рецепторам тиреотропного гормона (TRAb). [7] [49] Атаки антител в конечном итоге приводят к гипотиреозу, который вызван заменой фолликулярных клеток паренхиматозной тканью. [50]
Два антитела, наиболее часто участвующих в аутоиммунном тиреоидите, — это антитела против тиреопероксидазы (TPOAb) и тиреоглобулина (TgAb). [47] Предполагается, что они развиваются в результате повреждения щитовидной железы, когда Т-лимфоциты сенсибилизированы к остаточной тиреопероксидазе и тиреоглобулину, а не являются причиной повреждения щитовидной железы. [47] Однако они могут усугубить дальнейшее разрушение щитовидной железы, связывая систему комплемента и запуская апоптоз клеток щитовидной железы. [47] Факторы окружающей среды, которые могут предрасполагать пациентов к этому типу иммунной дисрегуляции, включают токсины, лекарства, диетические факторы и инфекционные агенты. [22]
Некоторые пациенты, которые здоровы или не имеют симптомов, могут быть положительными по более чем одному из этих антител. Врачи, которые лечат таких пациентов, скорее всего, будут наблюдать за ними, поскольку есть вероятность, что со временем у них разовьется какой-то тип дисфункции. [49]
Грубые морфологические изменения в щитовидной железе наблюдаются в общем увеличении, которое гораздо более локально узловатое и нерегулярное, чем более диффузные паттерны (такие как гипертиреоз ). Хотя капсула не повреждена, а сама железа все еще отличается от окружающей ткани, микроскопическое исследование может дать более показательное указание на уровень повреждения. [51]


Макроскопическая патология щитовидной железы с аутоиммунным тиреоидитом может показать симметрично увеличенную щитовидную железу. [47] Она часто более бледная по цвету по сравнению с нормальной тканью щитовидной железы, которая красновато-коричневая. [47] Микроскопическое исследование покажет инфильтрацию лимфоцитов и плазматических клеток. Лимфоциты преимущественно являются Т-лимфоцитами с представительством как CD4-положительных, так и CD8-положительных клеток. [47] Плазменные клетки являются поликлональными, с присутствующими зародышевыми центрами, напоминающими структуру лимфатического узла. [47] Фиброзная ткань также может быть обнаружена по всей пораженной щитовидной железе. [47] Как правило, патологические результаты щитовидной железы связаны с объемом существующей функции щитовидной железы - чем больше инфильтрации и фиброза, тем меньше вероятность того, что у пациента будет нормальная функция щитовидной железы. [47] На поздних стадиях заболевания щитовидная железа может быть атрофичной. [12]
Гистологически гиперчувствительность проявляется как диффузная паренхиматозная инфильтрация лимфоцитами, в частности плазматическими В-клетками , которые часто можно увидеть как вторичные лимфоидные фолликулы (герминальные центры, не путать с обычно присутствующими заполненными коллоидом фолликулами , составляющими щитовидную железу). Атрофия коллоидных телец выстлана клетками Гюртле , клетками с интенсивно эозинофильной , зернистой цитоплазмой, метаплазией нормальных кубовидных клеток, составляющих выстилку фолликулов щитовидной железы. Тяжелая атрофия щитовидной железы часто проявляется более плотными фиброзными полосами коллагена , которые остаются в пределах капсулы щитовидной железы. [51]
Также характеризуется инвазией тиреоидной ткани лейкоцитами , в основном Т-лимфоцитами . Редким, но серьезным осложнением является лимфома щитовидной железы , как правило, В-клеточного типа, неходжкинская лимфома . [52]

Диагноз обычно ставится путем обнаружения повышенных уровней антител к тиреоидной пероксидазе в сыворотке, но серонегативный (без циркулирующих аутоантител) тиреоидит также возможен. [53] Ультразвуковое исследование может быть полезным для выявления тиреоидита Хашимото, особенно у пациентов с серонегативным тиреоидитом, из-за ключевых особенностей, обнаруженных при ультразвуковом исследовании человека с тиреоидитом Хашимото, таких как «эхогенность, гетерогенность, гиперваскуляризация и наличие небольших кист». [54]
Различные тесты могут быть выбраны в зависимости от имеющихся симптомов. Для пациентов с аутоиммунным тиреоидитом, хотя известно, что у многих пациентов могут быть циркулирующие антитела до того, как у них появятся какие-либо симптомы, пациенты могут обратиться к своим врачам для оценки с симптомами гипотиреоза. [12] Врачи часто начинают с оценки сообщенных симптомов и проведения тщательного физического осмотра, включая осмотр шеи. [12]
Учитывая относительно неспецифические симптомы начального гипотиреоза, тиреоидит Хашимото часто ошибочно диагностируется как депрессия , циклотимия , предменструальный синдром , синдром хронической усталости , фибромиалгия и реже как эректильная дисфункция или тревожное расстройство . При общем осмотре часто обнаруживается твердый зоб , который не болезнен на ощупь; [51] другие симптомы, наблюдаемые при гипотиреозе, такие как периорбитальная микседема , зависят от текущего состояния прогрессирования ответа, особенно учитывая обычно постепенное развитие клинически значимого гипотиреоза. Тестирование на тиреотропный гормон (ТТГ), свободный Т3, свободный Т4 и антитела к тиреоглобулину (анти-ТГ), антитела к тиреоидной пероксидазе (анти-ТПО или TPOAb) и антимикросомальные антитела может помочь получить точный диагноз. [55] Ранняя оценка человека может показывать повышенный уровень тиреоглобулина из-за транзиторного тиреотоксикоза , поскольку воспаление в щитовидной железе вызывает повреждение целостности фолликулярного хранилища тиреоглобулина; секреция ТТГ из передней доли гипофиза увеличивается в ответ на снижение отрицательной обратной связи, вторичной по отношению к снижению сывороточных гормонов щитовидной железы. Как правило, Т4 является предпочтительным тестом на гормоны щитовидной железы при гипотиреозе. [56] Считается, что это воздействие на организм значительных количеств ранее изолированных тиреоидных ферментов способствует обострению нарушения толерантности, что приводит к более выраженным симптомам, наблюдаемым на поздних стадиях заболевания. Лимфоцитарная инфильтрация тканей, связанных с тироцитами, часто приводит к гистологически значимому обнаружению развития зародышевого центра в щитовидной железе. [ необходима цитата ]
Болезнь Хашимото, проявляющаяся в виде мании, известна как синдром Прасада по имени Ашока Прасада, психиатра, который впервые ее описал. [57]
Первичная диагностическая оценка начнется с концентрации тиреотропного гормона (ТТГ) в плазме. [16] Если она повышена, это означает гипотиреоз. [16] Повышение обычно представляет собой заметное увеличение по сравнению с нормальным диапазоном и, как правило, превышает 20 мг/дл. [18] Уровни свободного Т4 обычно будут снижены, но иногда могут быть нормальными. [58]
Врачи могут проверять антитела к тиреоглобулину (TgAb) всякий раз, когда проводится тест на тиреоглобулин, чтобы увидеть, мешают ли антитела. TgAb также может быть назначен через регулярные промежутки времени после того, как у человека диагностирован рак щитовидной железы, и, как и TPOAb, он может быть связан с тиреоидитом Хашимото. [49] Наиболее распространенным дополнением лабораторных показателей у пациентов с аутоиммунным тиреоидитом являются высокий уровень ТТГ, низкий уровень Т4 и положительные антитела к ТПО. [58]

Когда у пациентов нормальные лабораторные показатели, но есть симптомы аутоиммунного тиреоидита, ультразвуковое исследование играет роль в диагностике. [16] Изображения, полученные с помощью ультразвука, могут оценить размер щитовидной железы и дополнительно подтвердить диагноз аутоиммунного тиреоидита, выявить наличие узелков или предоставить подсказки для диагностики других заболеваний щитовидной железы. [16] Ядерная медицина Поглощение и сканирование щитовидной железы также могут быть полезны для диагностики функции щитовидной железы.

Гипотиреоз , вызванный тиреоидитом Хашимото, лечится заместительной терапией гормонами щитовидной железы, такими как левотироксин , трийодтиронин или высушенный экстракт щитовидной железы . Таблетка, принимаемая один раз в день, обычно поддерживает нормальный уровень гормонов щитовидной железы. В большинстве случаев лечение необходимо проводить в течение всей оставшейся жизни человека. Если гипотиреоз вызван тиреоидитом Хашимото, уровень ТТГ может быть рекомендован для поддержания ниже 3,0 м МЕ /л. [59]
Стандартом лечения является терапия левотироксином , который представляет собой пероральный препарат, структурированный как эндогенный Т4. [47] Левотироксин может быть дозирован в зависимости от веса, чаще всего, или повышения ТТГ. [47] Обычно назначаемая доза составляет от 1,6 мкг/кг до 1,8 мкг/кг, но может быть скорректирована в зависимости от каждого пациента. [12] Например, доза может быть снижена для пожилых пациентов или пациентов с определенными сердечными заболеваниями, но должна быть увеличена для беременных пациенток. [12] Ее следует вводить по последовательному графику. [47] Некоторые пациенты выбирают комбинированную терапию как левотироксином, так и лиотиронином , который является синтетическим Т3, однако исследования комбинированной терапии ограничены. [47]
Побочные эффекты заместительной терапии щитовидной железы связаны с ятрогенным гипертиреозом . [47] Симптомы, на которые следует обратить внимание, включают, помимо прочего, беспокойство, тремор, потерю веса, чувствительность к теплу, диарею и одышку. Более тревожные симптомы включают мерцательную аритмию и потерю плотности костей. [47]
Тиреотропный гормон (ТТГ) является лабораторным показателем выбора для мониторинга ответа на лечение левотиреоксином. [58] Когда лечение начинается впервые, уровень ТТГ можно контролировать с частотой каждые 6–8 недель. [58] Каждый раз, когда доза корректируется, уровень ТТГ можно измерять с этой частотой, пока не будет определена правильная доза. [58] После титрования до правильной дозы уровень ТТГ будет контролироваться ежегодно. [58]
Хирургия не является первоначальным методом выбора при аутоиммунном заболевании, а неосложненный тиреоидит Хашимото не является показанием к тиреоидэктомии. [47] Пациенты обычно могут обсудить операцию со своим врачом, если они испытывают значительные симптомы давления, или косметические проблемы, или у них есть узелки, обнаруженные на УЗИ. [47] Одно хорошо проведенное исследование пациентов с беспокоящими общими симптомами и с уровнями антитиреопероксидазы (анти-ТПО) более 1000 МЕ/мл (норма <100 МЕ/мл) показало, что полная тиреоидэктомия привела к разрешению симптомов, но у 14% были послеоперационные осложнения. [60]
Явная симптоматическая дисфункция щитовидной железы является наиболее распространенным осложнением, при этом около 5% людей с субклиническим гипотиреозом и хроническим аутоиммунным тиреоидитом ежегодно прогрессируют до недостаточности щитовидной железы. Иногда возникают транзиторные периоды тиреотоксикоза (чрезмерной активности щитовидной железы), и редко болезнь может прогрессировать до полной гипертиреоидной болезни Грейвса с активной орбитопатией (выпученные, воспаленные глаза). Редкие случаи фиброзного аутоиммунного тиреоидита проявляются тяжелой одышкой и затрудненным глотанием , напоминающими агрессивные опухоли щитовидной железы, но такие симптомы всегда улучшаются при хирургическом вмешательстве или терапии кортикостероидами. Хотя первичная лимфома щитовидной железы B-клеток поражает менее одного из 1000 человек, она с большей вероятностью поразит людей с длительным аутоиммунным тиреоидитом, [61] поскольку у пациентов с тиреоидитом Хашимото риск развития первичной лимфомы щитовидной железы увеличивается в 67–80 раз. [62]
Тиреоидит Хашимото считается наиболее распространенной причиной первичного гипотиреоза в Северной Америке. [51] В рамках тенденций эпидемиологии, характеризующихся описанием личности, места и времени, становится более ясно, как развивается тиреоидит Хашимото и как он влияет на различные группы населения.
Аутоиммунный тиреоидит является наиболее распространенной причиной гипотиреоза в условиях достаточного содержания йода . [12] По оценкам, он поражает 2% населения мира. [47] Он может поражать до 5% населения Соединенных Штатов. [63] Это заболевание может развиться у любого человека, но аутоиммунный тиреоидит поражает женщин чаще, чем мужчин, примерно в 10 раз. [47] Разница в распространенности между полами обусловлена действием половых гормонов . [22] Пик заболеваемости приходится на пятое десятилетие жизни, но обычно диагноз ставится пациентам в возрасте 30–50 лет. [16] [63]
Аутоиммунный тиреоидит имеет более высокую распространенность в обществах, которые имеют более высокое потребление йода в своем рационе, таких как Соединенные Штаты и Япония. Это наиболее распространенная причина гипотиреоза в регионах с достаточным содержанием йода. [12] Кроме того, скорость лимфоцитарной инфильтрации увеличилась в регионах, где потребление йода когда-то было низким, но увеличилось из-за добавления йода. [7]
Было показано, что «распространенность положительных тестов на антитела к щитовидной железе увеличивается с возрастом, с частотой до 33 процентов у женщин в возрасте 70 лет и старше». [7] Пик заболеваемости приходится на пятое десятилетие жизни, и распространенность увеличивается с возрастом. [12] [63]
В целом, тиреоидит Хашимото поражает до 2% населения в целом. [23] Около 5% европеоидов в какой-то момент жизни заболевают тиреоидитом Хашимото. [4] В США афроамериканское население страдает от него реже, но имеет более высокую сопутствующую смертность. [64] Он также реже встречается у азиатского населения. [65] Примерно от 1,0 до 1,5 из 1000 человек страдают этим заболеванием в любое время. [51] У женщин оно встречается в 8-15 раз чаще, чем у мужчин. Некоторые исследования предполагают связь с ролью плаценты как объяснение половых различий. [66] Хотя это может произойти в любом возрасте, в том числе у детей, чаще всего это наблюдается у женщин в возрасте от 30 до 60 лет. [61] Самая высокая распространенность в одном исследовании была обнаружена у пожилых членов сообщества. [67]
Те, у кого уже есть аутоиммунное заболевание, подвержены большему риску развития Хашимото, поскольку эти заболевания обычно сосуществуют друг с другом. [23] Распространенные заболевания, которые наблюдаются одновременно с Хашимото, включают целиакию , рассеянный склероз , диабет 1 типа , витилиго и ревматоидный артрит . [ необходима ссылка ]
Врожденный гипотиреоз поражает 1 из 3500–4000 новорожденных при рождении и является разновидностью умственной отсталости, которую можно лечить, если обнаружить ее на ранней стадии, но ее трудно диагностировать, учитывая, что симптомы минимальны в молодом возрасте. [67] Врожденный гипотиреоз обычно вызывается дефектами щитовидной железы, но в большинстве случаев в Европе, Азии и Африке потребление йода может вызвать гипотиреоз у новорожденных.
Диеты, состоящие из низкого или высокого потребления йода, определяют риск развития заболеваний, связанных с щитовидной железой, у населения. [68] Это чаще встречается в регионах с высоким потреблением йода в рационе и среди людей, которые генетически восприимчивы. [61] География играет большую роль в том, какие регионы имеют доступ к диетам с низким или высоким содержанием йода. Уровень йода как в воде, так и в соли должен тщательно контролироваться, чтобы защитить группы риска от развития гипотиреоза. [69]
Географические тенденции гипотиреоза различаются по всему миру, поскольку в разных местах существуют разные способы определения заболевания и сообщения о случаях. Популяции, которые рассредоточены или плохо определены, могут искажать данные неожиданным образом. [23]
С дефицитом йода (IDD) борются, увеличивая содержание йода в рационе человека. Когда в рационе человека происходят резкие изменения, он становится более подверженным риску развития гипотиреоза и других заболеваний щитовидной железы. Бороться с IDD с высоким потреблением соли следует осторожно и осмотрительно, так как может увеличиться риск развития тиреоидита Хашимото. [68] При внесении изменений в рацион важно использовать усмотрение врача, чтобы убедиться, что изменения в рационе являются наилучшим вариантом, поскольку рекомендации могут различаться у разных людей. [ необходима цитата ]
Светские тенденции гипотиреоза показывают, как болезнь изменилась с течением времени, учитывая изменения в технологиях и вариантах лечения. Несмотря на то, что ультразвуковые технологии и варианты лечения улучшились, заболеваемость гипотиреозом увеличилась, согласно данным, сосредоточенным на США и Европе. В период с 1993 по 2001 год на 1000 женщин заболевание варьировалось от 3,9 до 4,89. В период с 1994 по 2001 год на 1000 мужчин заболевание увеличилось с 0,65 до 1,01. [67]
Изменения в определении гипотиреоза и вариантах лечения изменяют заболеваемость и распространенность заболевания в целом. Лечение с использованием левотироксина индивидуализировано и, следовательно, позволяет со временем сделать болезнь более управляемой, но не работает как лекарство от болезни. [23]
Также известный как болезнь Хашимото, тиреоидит Хашимото назван в честь японского врача Хакару Хашимото (1881−1934) из медицинской школы в Университете Кюсю , [70] который впервые описал симптомы людей с лимфоматозным струмом , интенсивной инфильтрацией лимфоцитов в щитовидную железу, в 1912 году в немецком журнале Archiv für Klinische Chirurgie . [3] [71] Эта статья состояла из 30 страниц и 5 иллюстраций, все из которых описывали гистологические изменения в ткани щитовидной железы. Кроме того, все результаты в его первом исследовании были собраны у четырех женщин. Эти результаты объяснили патологические характеристики, наблюдаемые у этих женщин, особенно инфильтрацию лимфоидных и плазматических клеток, а также образование лимфоидных фолликулов с зародышевыми центрами, фиброз, дегенерированные эпителиальные клетки щитовидной железы и лейкоциты в просвете. [3] Он описал эти черты как гистологически схожие с чертами болезни Микулича. Как упоминалось выше, как только он обнаружил эти черты в этой новой болезни, он назвал болезнь struma lymphomatosa. Эта болезнь подчеркивала инфильтрацию лимфоидных клеток и образование лимфоидных фолликулов с зародышевыми центрами, ни один из которых ранее не был описан. [3]
Несмотря на открытие и публикацию доктора Хашимото, болезнь не была признана отличной от тиреоидита Рейделя , который был распространенным заболеванием в то время в Европе. Хотя многие другие статьи были опубликованы другими исследователями, лимфоматозный зоб Хашимото был признан ранней фазой тиреоидита Рейделя только в начале 1900-х годов. Только в 1931 году болезнь была признана как самостоятельное заболевание, когда исследователи Аллен Грэм и др. из Кливленда сообщили о ее симптомах и проявлениях в той же подробной манере, что и Хакару. [3]
В 1956 году доктора Роуз и Витебски смогли продемонстрировать, как иммунизация некоторых грызунов экстрактами щитовидной железы других грызунов напоминала болезнь, которую Хакару и другие исследователи пытались описать. [3] Эти врачи также смогли описать антитела к тиреоглобулину в образцах сыворотки крови этих же животных. [ необходима цитата ]
Позже в том же году исследователи из больницы Миддлсекс в Лондоне смогли провести эксперименты на людях с похожими симптомами. Они выделили антитела к тиреоглобулину из их сыворотки и смогли сделать вывод, что у этих больных пациентов наблюдалась иммунологическая реакция на человеческий тиреоглобулин. [3] На основании этих данных было высказано предположение, что зоб Хашимото может быть аутоиммунным заболеванием щитовидной железы.
В 1957 году это заболевание было признано аутоиммунным и стало первым идентифицированным органоспецифическим аутоиммунным заболеванием. [14]
После этого признания те же исследователи из больницы Миддлсекс опубликовали статью в 1962 году в журнале The Lancet , включавшую портрет Хакару Хашимото. [3] С этого момента болезнь стала более известной, и болезнь Хашимото стала чаще упоминаться в учебниках. [ необходима цитата ]
После этих открытий был обнаружен ряд аутоиммунных заболеваний, некоторые из которых связаны со специфическими антителами щитовидной железы. [ необходима цитата ]
Беременные женщины, у которых положительный результат теста на тиреоидит Хашимото, могут иметь сниженную функцию щитовидной железы или она может полностью выйти из строя. [72] Если женщина имеет положительный результат теста на АТ-ТПО, врачи могут проинформировать ее о рисках для нее и ее ребенка, если болезнь не лечить. «Антитела к тиреопероксидазе (АТ-ТПО) обнаруживаются у 10% беременных женщин», что представляет риск для этих беременностей. [72] Женщины с низкой функцией щитовидной железы, которая не была стабилизирована, подвергаются большему риску рождения ребенка с: низкой массой тела при рождении, респираторным дистрессом новорожденных, гидроцефалией , гипоспадией , выкидышем и преждевременными родами. [72] [73] Частота трансплантации эмбрионов и успешные исходы беременности улучшаются при лечении Хашимото. [73] Рекомендации заключаются в том, чтобы лечить беременных женщин, только если они имеют положительный результат теста на АТ-ТПО на протяжении всей беременности, и проводить скрининг всех беременных женщин на уровень гормонов щитовидной железы. [72] Тесное сотрудничество эндокринолога и акушера приносит пользу женщине и ребенку. [72] [74] [75] Эндокринологическое общество рекомендует проводить скрининг беременным женщинам, которые считаются подверженными высокому риску аутоиммунного заболевания щитовидной железы. [76]
Тестирование на антитела к перекиси щитовидной железы рекомендуется женщинам, которые когда-либо были беременны, независимо от исхода беременности. «[Предыдущая] беременность играет важную роль в развитии аутоиммунного явного гипотиреоза у женщин в пременопаузе, и количество предыдущих беременностей следует учитывать при оценке риска гипотиреоза у молодой женщины [ sic ]». [77]
Гормональные изменения и экспрессия трофобластом ключевых иммуномодулирующих молекул приводят к иммуносупрессии и толерантности плода. Главными игроками в регуляции иммунного ответа являются Tregs. Как клеточно-опосредованные, так и гуморальные иммунные реакции ослабевают, что приводит к иммунной толерантности и подавлению аутоиммунитета. Сообщалось, что во время беременности уровни тиреопероксидазы и антител тиреоглобулина снижаются. После родов Tregs быстро снижаются, и иммунные реакции восстанавливаются. Это может привести к возникновению или обострению аутоиммунного заболевания щитовидной железы. [78] У 50% женщин с антителами к тиреопероксидазе на ранних сроках беременности аутоиммунитет щитовидной железы в послеродовом периоде обостряется в форме послеродового тиреоидита. [79] У женщин с послеродовым тиреоидитом была зарегистрирована более высокая секреция IFN-γ и IL-4 и более низкая концентрация кортизола в плазме во время беременности, чем у здоровых женщин. Это указывает на то, что более слабая иммуносупрессия во время беременности может способствовать послеродовой дисфункции щитовидной железы. [80]
Через несколько лет после родов химерные мужские клетки можно обнаружить в периферической крови матери, щитовидной железе, легких, коже или лимфатических узлах. Иммунные клетки плода в материнской щитовидной железе могут активироваться и действовать как триггер, который может инициировать или усилить аутоиммунное заболевание щитовидной железы. У пациентов с болезнью Хашимото микрохимерные клетки плода были обнаружены в щитовидной железе в значительно большем количестве, чем у здоровых женщин. [81]
Болезнь Хашимото также известна у кур ( Gallus domesticus ), [82] [83] крыс ( Rattus rattus ), [83] мышей ( Mus musculus ), [83] собак ( Canis familiaris ) [83] и мартышек (Callitrichidae). [83]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )