Фармакотерапия , также известная как фармакологическая терапия или лекарственная терапия, определяется как медицинское лечение, при котором используется один или несколько фармацевтических препаратов для улучшения текущих симптомов (симптоматическое облегчение), лечения основного заболевания или в качестве профилактики других заболеваний ( профилактика ). [1]
Ее можно отличить от терапии с использованием хирургии (хирургическая терапия), облучения ( лучевая терапия ), движения ( физиотерапия ) или других методов. Среди врачей иногда термин медицинская терапия относится конкретно к фармакотерапии в отличие от хирургической или другой терапии; например, в онкологии медицинская онкология таким образом отличается от хирургической онкологии .
Современная фармакологическая терапия развилась из долгой истории использования лекарств, и она изменилась наиболее быстро в прошлом веке из-за достижений в области открытия лекарств . Терапия назначается и корректируется специалистами здравоохранения в соответствии с рекомендациями, основанными на фактических данных , и состоянием здоровья пациента. Персонализированная медицина также играет важную роль в фармакологической терапии. Персонализированная медицина , или прецизионная медицина, учитывает генетическую изменчивость пациента , функцию печени, функцию почек и т. д., чтобы обеспечить индивидуальное лечение для пациента. В фармакологической терапии фармацевты также будут учитывать соблюдение приема лекарств . Соблюдение приема лекарств , или приверженность приему лекарств, определяется как степень, в которой пациент следует терапии, рекомендованной специалистами здравоохранения. [2]

Использование лекарственных веществ можно проследить до 4000 г. до н. э. в шумерской цивилизации. [3] Например, целители того времени (называемые аптекарями ) понимали применение опиума для облегчения боли. [4] Историю природных средств можно найти и в других культурах, включая традиционную китайскую медицину в Китае и аюрведическую медицину в Индии, которые используются и в наши дни. [5] Диоскорид , греческий хирург I века, описал более шестисот животных, растений и их производных в своей медицинской ботанике, которая оставалась самой влиятельной фармакопеей на протяжении четырнадцати столетий. [6] Помимо веществ, полученных из живых организмов, в качестве медицинских терапий также использовались металлы, включая медь , ртуть и сурьму . [6] Считалось, что они излечивали различные болезни в эпоху позднего Возрождения . В 1657 году рвотному средству тартар , которое является соединением сурьмы, приписывали излечение Людовика XIV от брюшного тифа . [6] Препарат также вводился внутривенно для лечения шистосомоза в 20 веке. [7] Однако из-за опасений по поводу острого и хронического отравления сурьмой, роль рвотного камня как противошистосомного средства была постепенно заменена после появления празиквантела . [ 7]
Помимо использования натуральных продуктов, люди также научились составлять лекарства самостоятельно. Первый фармацевтический текст был найден на глиняных табличках у жителей Месопотамии , которые жили около 2100 г. до н. э. [5] Позже, во II веке н. э., составление лекарств было официально введено Галеном как «процесс смешивания двух или более лекарств для удовлетворения индивидуальных потребностей пациента». [5] Первоначально составление лекарств выполнялось только отдельными фармацевтами, но в период после Второй мировой войны фармацевтические производители резко возросли в числе и взяли на себя роль изготовления лекарств. [3] Между тем, наблюдался заметный рост фармацевтических исследований, что привело к росту числа новых лекарств. [3] Большинство важных вех в открытии лекарств были сделаны за последние сто лет, от антибиотиков до биологических препаратов , [5] способствуя созданию основы современной фармакологической терапии.

Большинство лекарств были открыты эмпирическим путем, включая наблюдение, случайность, пробы и ошибки. [6] Одним из известных примеров является открытие пенициллина , первого антибиотика в мире. Вещество было открыто Александром Флемингом в 1928 году после того, как в его лаборатории во время летних каникул произошло несколько непредвиденных событий. [8] Считалось, что плесень Penicillium на чашке Петри выделяет вещество (позже названное «пенициллином»), которое подавляет рост бактерий. [ 8 ] Затем крупные фармацевтические компании начали создавать свои микробиологические отделы и искать новые антибиотики. [9] Программа скрининга антимикробных соединений также привела к открытию препаратов с другими фармакологическими свойствами, таких как иммунодепрессанты , такие как Циклоспорин А. [9]

Открытие пенициллина было счастливым (т. е. случайным) открытием. Другим, более продвинутым подходом к открытию лекарств является рациональный дизайн лекарств . Метод основан на понимании биологических целей лекарств, включая ферменты , рецепторы и другие белки. В конце 19 века Пауль Эрлих наблюдал селективное сродство красителей к различным тканям и предположил существование хеморецепторов в нашем организме. [9] [10] Считалось, что рецепторы являются специфическими участками связывания для лекарств. [9] Распознавание лекарство-рецептор было описано как взаимодействие ключа и замка Эмилем Фишером в начале 1890-х годов. [11] Позднее было обнаружено, что рецепторы могут либо стимулироваться, либо ингибироваться химиотерапевтическими агентами для достижения желаемого физиологического ответа. [9] После того, как лиганд, взаимодействующий с целевой макромолекулой, идентифицирован, кандидаты на лекарства могут быть разработаны и оптимизированы на основе соотношения структура-активность . [11] В настоящее время искусственный интеллект используется в разработке лекарств для прогнозирования взаимодействия лекарств с белками, активности лекарств, трехмерной конфигурации белков и т. д. [11]
Доказательная медицина определяется как использование лучших современных научных доказательств, которые доступны, для предоставления наилучшего лечения и принятия наилучшего решения эффективно и действенно. [12] Клинические рекомендации разрабатываются на основе научных доказательств; например, рекомендации ACC / AHA (для сердечно-сосудистых заболеваний ), рекомендации GOLD (для хронической обструктивной болезни легких ), рекомендации GINA (для астмы ) и т. д. Они преобразуют и классифицируют доказательства с использованием систематического метода, стремясь оказывать качественную помощь. [13] Рекомендации не могут заменить клиническое суждение, поскольку они не могут соответствовать всем обстоятельствам. [13] Специалисты здравоохранения могут использовать клинические рекомендации в качестве ссылок или доказательств для поддержки своего клинического суждения при назначении терапии пациентам.
Пример: Клинические рекомендации по контролю артериального давления ( гипертонии )
Если пациентом является мужчина азиатской национальности в возрасте 40 лет, у которого недавно диагностировали повышенное артериальное давление (с артериальным давлением 140/90) и у которого нет других хронических заболеваний ( сопутствующих заболеваний ), таких как диабет 2 типа , подагра , доброкачественная гиперплазия предстательной железы и т. д., то его предполагаемый 10-летний риск сердечно-сосудистых заболеваний составляет 15%.
Согласно руководству NICE 2019 Hypertension, медицинский работник может рассмотреть возможность начала антигипертензивной терапии после обсуждения с пациентом. [14] Терапией первой линии будет либо ингибитор ангиотензинпревращающего фермента (ИАПФ) , либо блокатор рецепторов ангиотензина (БРА) (если пациент не переносит ИАПФ). [14] Если артериальное давление пациента не контролируется должным образом, медицинские работники могут рассмотреть возможность добавления блокатора кальциевых каналов (БКК) [15] или тиазидоподобного диуретика к предыдущей терапии, т. е. ИАПФ или БРА с БКК или тиазидоподобным диуретиком. [14]
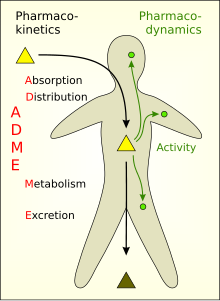
У каждого пациента есть свое собственное состояние организма, например, функция почек, функция печени, генетические вариации, история болезни и т. д. Все эти факторы должны учитываться специалистами здравоохранения перед назначением любой фармакологической терапии. Самое главное, что передовые технологии в генетике позволяют нам лучше понять связь между здоровьем и генами. [16] В фармакологической терапии развиваются две области исследований: фармакогенетика и фармакогеномика . Возраст влияет на фармакокинетику и фармакодинамику лекарств, а следовательно, и на эффективность терапии. Влияние возраста вызывает ухудшение функции органов, [17] таких как функция печени и функция почек. Фармакокинетика — это изучение влияния лекарств на абсорбцию, распределение, метаболизм и выведение. Фармакодинамика — это изучение влияния лекарств на наш организм и его механизмы.
Фармакогенетика определяется как изучение наследственных генов, вызывающих различные метаболизмы лекарственных средств , которые отличаются друг от друга, например, скоростью метаболизма и метаболитами. [18] Фармакогеномика определяется как изучение связи реакции на лекарственное средство с геном . [19] Оба термина схожи по своей природе, поэтому они используются взаимозаменяемо.
Множественные аллели могут совместно способствовать изменению реакции на лекарство, экспрессируя другую форму фермента , которая реагирует иначе, чем нормальные. [18] Различные формы ферментов ( фенотипы ) включают сверхбыстрых метаболизаторов, умеренных метаболизаторов, безферментативную активность и т. д. Генетические вариации также могут использоваться для соответствия конкретной неблагоприятной реакции на лекарство , чтобы предотвратить неблагоприятные исходы у пациента. [20] Генетическая структура может влиять на фармакокинетику .
Например, азатиоприн является иммуномодулятором при воспалительных заболеваниях кишечника . Его метаболит зависит от двух разных ферментов ( TPMT и NUDT15 ), чтобы устранить его влияние на наш организм во время метаболизма . Если у пациента фенотип ферментов , которые плохо его метаболизируют, т. е. плохой метаболизатор, в организме накапливается больше токсичных метаболитов. Таким образом, у пациента выше риск соответствующего побочного эффекта. [21] Побочный эффект вызывает корректировку дозировки [21] или переход на другой препарат.
Омализумаб — гуманизированное моноклональное антитело для лечения различных аллергических заболеваний , включая астму , крапивницу и аллергический ринит . [22] Он воздействует на иммуноглобулин E (IgE) в организме человека, который играет важную роль в аллергических реакциях . [23] Эффективность омализумаба может различаться у разных пациентов. Чтобы определить, реагируют ли люди на омализумаб , можно измерить уровень нескольких биомаркеров , включая сывороточные эозинофилы , фракционный выдыхаемый оксид азота и сывороточный IgE. [23] [24] Например, пациенты с более высоким исходным количеством эозинофилов , вероятно, лучше отреагируют на терапию омализумабом . [24]
Соблюдение режима приема лекарств определяется как степень, в которой пациент следует терапии, рекомендованной медицинскими работниками. [2] Существуют прямые и косвенные методы оценки соблюдения режима. Прямой метод относится к измерению, которое медицинские работники наблюдают или измеряют поведение пациента, связанное с приемом лекарств. Косвенный метод относится к тому, что медицинские работники не наблюдают и не измеряют поведение пациента, связанное с приемом лекарств, а используют другой источник информации для оценки соблюдения режима.
Прямой метод включает измерение концентрации препарата (или соответствующего метаболита ) [2] [25], тогда как косвенный метод включает подсчет таблеток [2] [25] и самоотчет пациента. [2] [25] Прямой метод более трудоемкий, более дорогой, более инвазивный, но он более точный. [2] Косвенный метод имеет меньшую точность, но его легче применять у пациента. [2] Если пациент не соблюдает лечение, например, не принимает лекарство в соответствии с инструкцией, это приводит к риску и плохому результату лечения.
Для больных туберкулезом терапия под непосредственным наблюдением все еще является частью лечения. [26] Это делается для повышения приверженности лечению . [27] Это делается для предотвращения неудач лечения, рецидивов и передачи инфекции в обществе. [28] Помимо традиционной терапии под непосредственным наблюдением (DOT), предлагается еще один метод, чтобы попытаться повысить приверженность лечению. Терапия под видеонаблюдением (VOT) является одним из методов. У нее есть некоторые преимущества и недостатки. Она снижает расходы на здравоохранение и транспортные расходы для пациента. [27] Недостатком вмешательства является необходимость обучения контролю качества, поскольку будет трудно подтвердить приверженность пациента. [27]
Фармацевты являются экспертами в фармакотерапии и несут ответственность за обеспечение безопасного, надлежащего и экономичного использования фармацевтических препаратов. Навыки, необходимые для работы фармацевтом, требуют знаний, обучения и опыта в биомедицинских, фармацевтических и клинических науках . [29] Фармакология — это наука, которая направлена на постоянное улучшение фармакотерапии. Фармацевтическая промышленность и академические круги используют фундаментальную науку , прикладную науку и трансляционную науку для создания новых фармацевтических препаратов.
Поскольку специалисты по фармакотерапии и фармацевты несут ответственность за непосредственный уход за пациентами , часто действуя в качестве члена многопрофильной команды и выступая в качестве основного источника информации, связанной с лекарственными средствами, для других специалистов здравоохранения . Специалист по фармакотерапии — это человек, который специализируется на назначении и назначении лекарств и требует обширных академических знаний в области фармакотерапии. [30]
В США фармацевт может получить сертификат в области фармакотерапии после выполнения требований к квалификации и успешной сдачи экзамена на сертификацию. [31] [32] Хотя фармацевты предоставляют ценную информацию о лекарствах пациентам и медицинским работникам, страховые компании обычно не считают их поставщиками услуг фармакотерапии, на которые распространяется страховое покрытие.
{{cite book}}: CS1 maint: местоположение отсутствует издатель ( ссылка ) CS1 maint: другие ( ссылка ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite book}}: CS1 maint: местоположение отсутствует издатель ( ссылка ) CS1 maint: другие ( ссылка )