Холестерин — основной стерол всех высших животных , распространенный в тканях тела, особенно в головном и спинном мозге , а также в животных жирах и маслах . [3] [4]
Холестерин биосинтезируется всеми клетками животных и является важным структурным компонентом мембран животных клеток . У позвоночных печеночные клетки обычно производят наибольшее количество. В мозге астроциты производят холестерин и транспортируют его к нейронам. [5] Он отсутствует среди прокариотов ( бактерий и архей ), хотя есть некоторые исключения, такие как микоплазмы , которым для роста необходим холестерин. [6] Холестерин также служит предшественником биосинтеза стероидных гормонов , желчной кислоты [7] и витамина D.
Повышенный уровень холестерина в крови, особенно когда он связан с липопротеинами низкой плотности (ЛПНП, часто называемый «плохим холестерином»), может увеличить риск сердечно-сосудистых заболеваний . [8]
Франсуа Пулетье де ла Саль впервые обнаружил холестерин в твердой форме в желчных камнях в 1769 году. В 1815 году химик Мишель Эжен Шеврёль назвал это соединение «холестерином». [9] [10]
Слово «холестерол» происходит от древнегреческого слова « холе» — « желчь » и «стерео » — «твердый», за которым следует химический суффикс —ол , обозначающий алкоголь .
Холестерин необходим для жизни всех животных. Хотя большинство клеток способны его синтезировать, большая часть холестерина поглощается или синтезируется гепатоцитами и транспортируется кровью к периферическим клеткам. Уровни холестерина в периферических тканях определяются балансом его поглощения и экспорта. [11] В нормальных условиях холестерин головного мозга отделен от периферического холестерина, т.е. пищевой и печеночный холестерин не проникают через гематоэнцефалический барьер. Скорее, астроциты производят и распределяют холестерин в мозге. [12]
Синтез de novo как в астроцитах, так и в гепатоцитах происходит в результате сложного 37-этапного процесса. Все начинается с пути мевалоната или ГМГ-КоА-редуктазы , мишени статиновых препаратов, который включает первые 18 этапов. За этим следуют 19 дополнительных шагов по превращению полученного ланостерола в холестерин. [13] Человек мужского пола весом 68 кг (150 фунтов) обычно синтезирует около 1 грамма (1000 мг) холестерина в день, а его тело содержит около 35 г, в основном содержащихся в клеточных мембранах.
Типичная суточная норма холестерина для мужчины в США составляет 307 мг. [14] Большая часть поступающего в организм холестерина этерифицируется , что приводит к его плохому всасыванию в кишечнике. Организм также компенсирует поглощение поступившего холестерина за счет снижения собственного синтеза холестерина. [15] По этим причинам холестерин в пище через семь-десять часов после приема практически не влияет на концентрацию холестерина в крови. Удивительно, но у крыс уровень холестерина в крови обратно коррелирует с потреблением холестерина. Чем больше холестерина съедает крыса, тем ниже уровень холестерина в крови. [16] В течение первых семи часов после приема холестерина, когда поглощенные жиры распределяются по организму во внеклеточной воде с помощью различных липопротеинов (которые транспортируют все жиры в воде за пределы клеток), концентрации увеличиваются. [17]
Растения производят холестерин в очень небольших количествах. [18] В больших количествах они производят фитостерины , химически подобные вещества, которые могут конкурировать с холестерином за реабсорбцию в кишечном тракте, тем самым потенциально снижая реабсорбцию холестерина. [19] Когда клетки слизистой оболочки кишечника поглощают фитостерины вместо холестерина, они обычно выделяют молекулы фитостерола обратно в желудочно-кишечный тракт , что является важным защитным механизмом. Потребление природных фитостеролов, к которым относятся растительные стеролы и станолы , колеблется в пределах ≈200–300 мг/день в зависимости от привычек питания. [20] Были разработаны специально разработанные вегетарианские экспериментальные диеты с содержанием более 700 мг/день. [21]
Холестерин составляет около 30% мембран всех клеток животных . [ нужна цитация ] Он необходим для построения и поддержания мембран и модулирует текучесть мембран в диапазоне физиологических температур. Гидроксильная группа каждой молекулы холестерина взаимодействует с молекулами воды, окружающими мембрану, так же, как и полярные головки мембранных фосфолипидов и сфинголипидов , в то время как объемистый стероид и углеводородная цепь встроены в мембрану вместе с неполярной жирнокислотной цепью холестерина . другие липиды. Благодаря взаимодействию с цепями фосфолипидов и жирных кислот холестерин увеличивает упаковку мембран, что одновременно изменяет текучесть мембран [22] и поддерживает целостность мембран, так что животным клеткам не нужно строить клеточные стенки (как растениям и большинству бактерий). Мембрана остается стабильной и прочной, не будучи жесткой, что позволяет клеткам животных менять форму, а животным - двигаться.
Структура тетрациклического кольца холестерина способствует текучести клеточной мембраны, поскольку молекула находится в транс- конформации, что делает всю цепь холестерина, кроме боковой цепи, жесткой и плоской. [23] Выполняя эту структурную роль, холестерин также снижает проницаемость плазматической мембраны для нейтральных растворенных веществ, [24] ионов водорода и ионов натрия . [25]
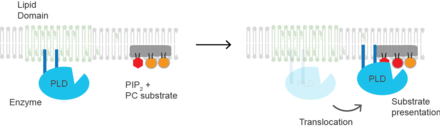
Холестерин регулирует биологический процесс презентации субстрата и ферментов, использующих презентацию субстрата, в качестве механизма их активации. Фосфолипаза D2 ( PLD2 ) является четко определенным примером фермента, активируемого презентацией субстрата. [26] Фермент пальмитоилируется , что приводит к его перемещению к холестерин-зависимым липидным доменам, которые иногда называют « липидными плотами ». Субстратом фосфолипазы D является фосфатидилхолин (ФХ), который является ненасыщенным и содержится в небольшом количестве в липидных рафтах. ПК локализуется в неупорядоченной области клетки вместе с полиненасыщенным липидом фосфатидилинозитол-4,5-бисфосфатом (PIP2). PLD2 имеет связывающий домен PIP2 . Когда концентрация PIP2 в мембране увеличивается, PLD2 покидает холестерин-зависимые домены и связывается с PIP2, где затем получает доступ к своему субстрату PC и начинает катализ, основанный на представлении субстрата.
Холестерин также участвует в процессах передачи сигналов в клетках, способствуя образованию липидных плотов в плазматической мембране , что приводит к сближению рецепторных белков с высокими концентрациями молекул вторичных мессенджеров. [27] В нескольких слоях холестерин и фосфолипиды, оба являются электрическими изоляторами, могут способствовать скорости передачи электрических импульсов по нервной ткани. Для многих нейронных волокон миелиновая оболочка, богатая холестерином, поскольку она образуется из уплотненных слоев шванновских клеток или мембран олигодендроцитов, обеспечивает изоляцию для более эффективного проведения импульсов. [28] Считается, что демиелинизация (потеря миелина) является частью основы рассеянного склероза .
Холестерин связывается и влияет на работу ряда ионных каналов , таких как никотиновый рецептор ацетилхолина , рецептор ГАМК А и калиевый канал внутреннего выпрямителя . [29] Холестерин также активирует эстроген-связанный рецептор альфа (ERRα ) и может быть эндогенным лигандом рецептора . [30] [31] Конститутивно активная природа рецептора может быть объяснена тем фактом, что холестерин присутствует в организме повсеместно. [31] Ингибирование передачи сигналов ERRα за счет снижения выработки холестерина было идентифицировано как ключевой медиатор эффектов статинов и бисфосфонатов на кости , мышцы и макрофаги . [30] [31] На основании этих результатов было предложено деорфанизировать ERRα и классифицировать его как рецептор холестерина. [30] [31]
Внутри клеток холестерин также является молекулой-предшественником нескольких биохимических путей . Например, это молекула-предшественник синтеза витамина D в метаболизме кальция и всех стероидных гормонов , включая гормоны надпочечников кортизол и альдостерон , а также половые гормоны прогестерон , эстрогены и тестостерон и их производные. [7] [32]
Роговой слой – это самый внешний слой эпидермиса. [33] [34] Он состоит из окончательно дифференцированных и энуклеированных корнеоцитов , которые расположены внутри липидной матрицы, как «кирпичи и раствор». [33] [34] Вместе с церамидами и свободными жирными кислотами холестерин образует липидный раствор, водонепроницаемый барьер, который предотвращает потерю воды при испарении. Как правило, эпидермальный липидный матрикс состоит из эквимолярной смеси церамидов (≈50% по массе), холестерина (≈25% по массе) и свободных жирных кислот (≈15% по массе) с меньшими количествами. присутствуют и другие липиды. [33] [34] Сульфат холестерина достигает максимальной концентрации в зернистом слое эпидермиса. Затем стероидсульфатаза снижает свою концентрацию в роговом слое, самом внешнем слое эпидермиса. [35] Относительное содержание сульфата холестерина в эпидермисе варьируется на разных участках тела, при этом на пятке стопы наблюдается самая низкая концентрация. [34]
Холестерин перерабатывается в организме. Печень выделяет холестерин в желчные жидкости, которые затем сохраняются в желчном пузыре , который затем выводит их в неэтерифицированной форме (через желчь) в пищеварительный тракт. Обычно около 50% выведенного холестерина реабсорбируется тонкой кишкой обратно в кровоток.
Почти все ткани животных синтезируют холестерин из ацетил-КоА . Все клетки животных (за исключением беспозвоночных) производят холестерин как для мембранных структур, так и для других целей, причем относительная скорость производства варьируется в зависимости от типа клеток и функции органа. Около 80% общего ежедневного производства холестерина происходит в печени и кишечнике ; [36] другие места с более высокой скоростью синтеза включают мозг , надпочечники и репродуктивные органы .
Синтез в организме начинается с мевалонатного пути , при котором две молекулы ацетил-КоА конденсируются с образованием ацетоацетил-КоА . За этим следует вторая конденсация между ацетил-КоА и ацетоацетил-КоА с образованием 3-гидрокси-3-метилглутарил-КоА ( HMG-CoA ). [37]

Затем эта молекула восстанавливается до мевалоната под действием фермента ГМГ-КоА-редуктазы . Производство мевалоната является лимитирующей и необратимой стадией синтеза холестерина и местом действия статинов ( класс препаратов, снижающих уровень холестерина).
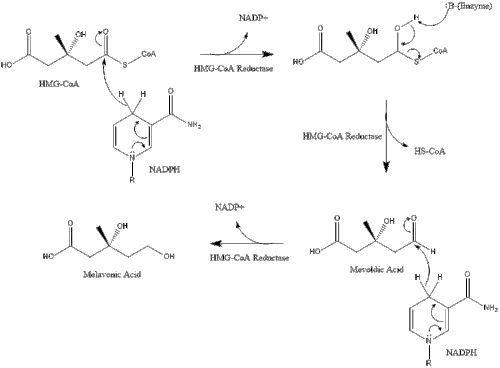
В конечном итоге мевалонат превращается в изопентенилпирофосфат (IPP) посредством двух стадий фосфорилирования и одной стадии декарбоксилирования, для которой требуется АТФ .
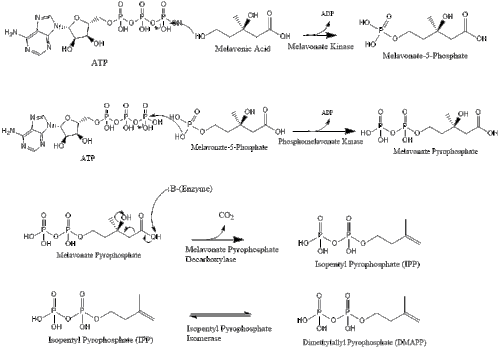
Три молекулы изопентенилпирофосфата конденсируются с образованием фарнезилпирофосфата под действием геранилтрансферазы.
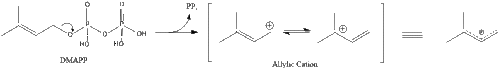

Две молекулы фарнезилпирофосфата затем конденсируются с образованием сквалена под действием скваленсинтазы в эндоплазматическом ретикулуме . [37]
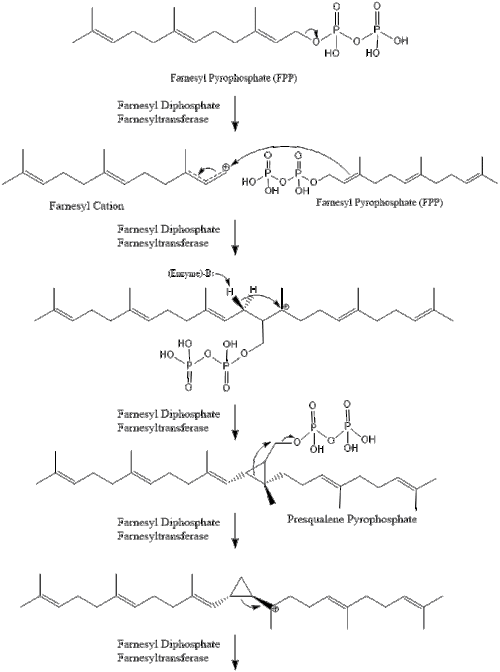
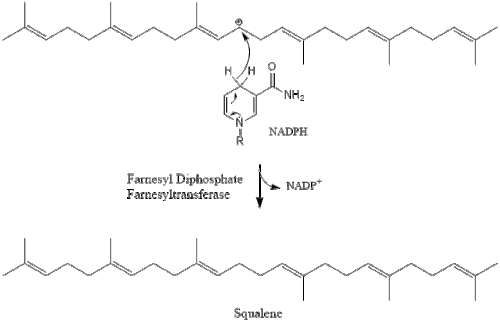
Затем оксидоскваленциклаза циклизирует сквален с образованием ланостерола .
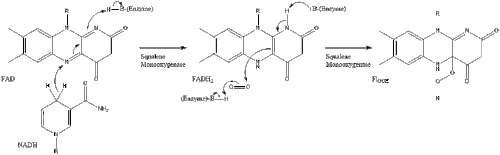
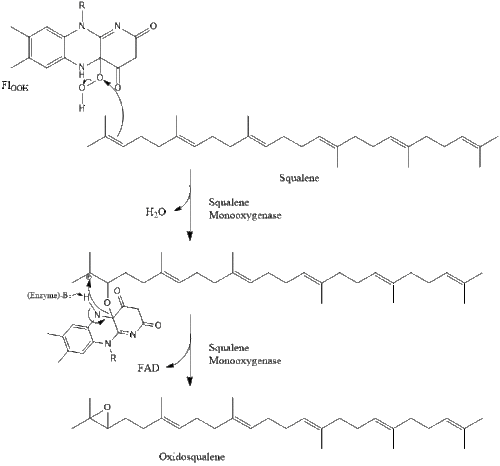
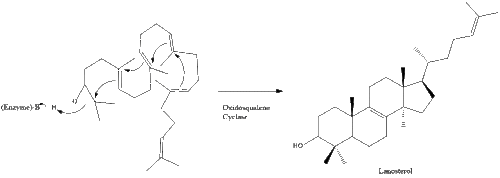
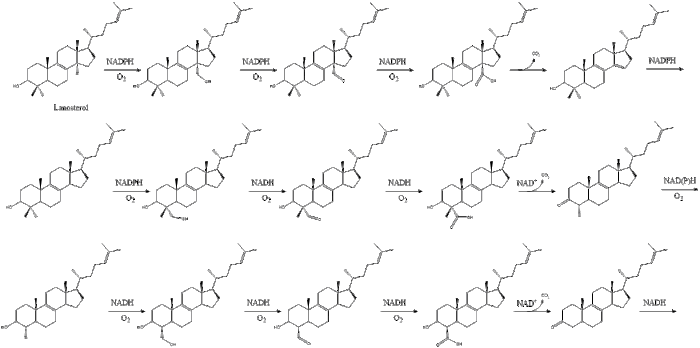
Наконец, ланостерин превращается в холестерин по одному из двух путей: пути Блоха или пути Кандуча-Рассела. [38] [39] [40] [41] [42] Последние 19 шагов к холестерину содержат НАДФН и кислород, которые помогают окислять метильные группы для удаления углерода, мутазы для перемещения алкеновых групп и НАДН , чтобы помочь восстановить кетоны .

Конрад Блох и Федор Линен получили Нобелевскую премию по физиологии и медицине в 1964 году за открытия, касающиеся некоторых механизмов и методов регуляции метаболизма холестерина и жирных кислот . [43]
Биосинтез холестерина напрямую регулируется присутствующим уровнем холестерина, хотя задействованные гомеостатические механизмы понятны лишь частично. Более высокое потребление пищи приводит к чистому снижению эндогенного производства, тогда как более низкое потребление пищи имеет противоположный эффект. Основным механизмом регуляции является восприятие внутриклеточного холестерина в эндоплазматическом ретикулуме белком SREBP ( белок , связывающий регуляторные элементы 1 и 2 стеролов). [44] В присутствии холестерина SREBP связывается с двумя другими белками: SCAP (белок, активирующий расщепление SREBP) и INSIG-1 . Когда уровень холестерина падает, INSIG-1 диссоциирует от комплекса SREBP-SCAP, что позволяет комплексу мигрировать в аппарат Гольджи . Здесь SREBP расщепляется S1P и S2P (протеаза сайта 1 и протеаза сайта 2), двумя ферментами, которые активируются SCAP при низком уровне холестерина.
Расщепленный SREBP затем мигрирует в ядро и действует как фактор транскрипции , связываясь с регуляторным элементом стерола (SRE), который стимулирует транскрипцию многих генов. Среди них рецептор липопротеинов низкой плотности ( ЛПНП ) и ГМГ-КоА-редуктаза . Рецептор ЛПНП удаляет циркулирующие ЛПНП из кровотока, тогда как ГМГ-КоА-редуктаза приводит к увеличению эндогенной продукции холестерина. [45] Большая часть этого сигнального пути была разъяснена доктором Майклом С. Брауном и доктором Джозефом Л. Гольдштейном в 1970-х годах. В 1985 году за свою работу они получили Нобелевскую премию по физиологии и медицине . Их последующая работа показывает, как путь SREBP регулирует экспрессию многих генов, которые контролируют образование и метаболизм липидов, а также распределение топлива в организме.
Синтез холестерина также может быть отключен при высоком уровне холестерина. HMG-CoA-редуктаза содержит как цитозольный домен (отвечающий за каталитическую функцию), так и мембранный домен. Мембранный домен воспринимает сигналы о своей деградации. Увеличение концентрации холестерина (и других стеринов) вызывает изменение состояния олигомеризации этого домена, что делает его более восприимчивым к разрушению протеасомой . Активность этого фермента также можно снизить за счет фосфорилирования АМФ-активируемой протеинкиназой . Поскольку эта киназа активируется АМФ, который вырабатывается при гидролизе АТФ, из этого следует, что синтез холестерина останавливается при низком уровне АТФ. [46]

Как изолированная молекула, холестерин лишь минимально растворим в воде или гидрофильен . Из-за этого он растворяется в крови в чрезвычайно малых концентрациях. Для эффективной транспортировки холестерин вместо этого упаковывается в липопротеины , сложные дискоидные частицы с внешними амфифильными белками и липидами, чьи обращенные наружу поверхности водорастворимы, а обращенные внутрь поверхности жирорастворимы. Это позволяет ему путешествовать по крови посредством эмульгирования . Несвязанный холестерин, будучи амфипатическим, транспортируется по монослойной поверхности липопротеиновой частицы вместе с фосфолипидами и белками. С другой стороны, эфиры холестерина, связанные с жирными кислотами, транспортируются внутри жирного гидрофобного ядра липопротеина вместе с триглицеридами. [47]
В крови имеется несколько типов липопротеинов. В порядке возрастания плотности это хиломикроны , липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛПНП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП). Более низкое соотношение белков и липидов приводит к менее плотным липопротеинам. Холестерин в различных липопротеинах идентичен, хотя некоторые из них переносятся в виде нативной «свободной» спиртовой формы (группа холестерина-ОН, обращенная к воде, окружающей частицы), тогда как другие в виде ациловых эфиров жирных кислот, известных также как эфиры холестерина, находятся внутри частиц. [47]
Частицы липопротеинов организованы сложными аполипопротеинами , обычно состоящими из 80–100 различных белков на частицу, которые могут распознаваться и связываться специфическими рецепторами на клеточных мембранах, направляя свою липидную нагрузку в определенные клетки и ткани, в настоящее время поглощающие эти частицы, транспортирующие жир. Эти поверхностные рецепторы служат уникальными молекулярными сигнатурами, которые затем помогают определить распределение жира по всему телу. [47]
Хиломикроны, наименее плотные частицы, транспортирующие холестерин, содержат в своих оболочках аполипопротеин B-48 , аполипопротеин C и аполипопротеин E (основной переносчик холестерина в мозге [48] ). Хиломикроны переносят жиры из кишечника в мышцы и другие ткани, нуждающиеся в жирных кислотах для производства энергии или жира. Неиспользованный холестерин остается в более богатых холестерином остатках хиломикронов и забирается оттуда в кровоток печенью. [47]
Частицы ЛПОНП производятся печенью из триацилглицерина и холестерина, которые не использовались в синтезе желчных кислот. Эти частицы содержат аполипопротеин B100 и аполипопротеин E в своей оболочке и могут расщепляться под действием липопротеинлипазы на стенке артерии до IDL. Расщепление артериальной стенки позволяет абсорбировать триацилглицерин и увеличивает концентрацию циркулирующего холестерина. Частицы ЛПНП затем потребляются в двух процессах: половина метаболизируется ХТГЛ и поглощается рецептором ЛПНП на поверхности клеток печени, в то время как другая половина продолжает терять триацилглицерины в кровотоке, пока они не превращаются в частицы ЛПНП, нагруженные холестерином. [47]
Частицы ЛПНП являются основными переносчиками холестерина в крови. Каждый из них содержит около 1500 молекул эфира холестерина. Оболочки частиц ЛПНП содержат всего одну молекулу аполипопротеина В100 , распознаваемую рецепторами ЛПНП в периферических тканях. При связывании аполипопротеина В100 многие рецепторы ЛПНП концентрируются в ямках, покрытых клатрином . И ЛПНП, и его рецептор образуют везикулы внутри клетки посредством эндоцитоза . Эти пузырьки затем сливаются с лизосомой , где фермент лизосомальной кислой липазы гидролизует эфиры холестерина. Холестерин затем можно использовать для мембранного биосинтеза или этерифицировать и хранить внутри клетки, чтобы не мешать клеточным мембранам. [47]
Рецепторы ЛПНП расходуются во время абсорбции холестерина, а его синтез регулируется SREBP , тем же белком, который контролирует синтез холестерина de novo , в зависимости от его присутствия внутри клетки. В клетке с избытком холестерина синтез рецепторов ЛПНП блокируется, чтобы предотвратить поглощение нового холестерина в частицах ЛПНП. И наоборот, синтез рецептора ЛПНП происходит, когда клетка испытывает дефицит холестерина. [47]
Когда этот процесс становится нерегулируемым, в крови начинают появляться частицы ЛПНП без рецепторов. Эти частицы ЛПНП окисляются и поглощаются макрофагами , которые набухают и образуют пенистые клетки. Эти пенистые клетки часто задерживаются в стенках кровеносных сосудов и способствуют образованию атеросклеротических бляшек . Различия в гомеостазе холестерина влияют на развитие раннего атеросклероза (толщина интимы-медиа сонных артерий). [49] Эти бляшки являются основной причиной сердечных приступов, инсультов и других серьезных медицинских проблем, приводящих к ассоциации так называемого холестерина ЛПНП (на самом деле липопротеина ) с «плохим» холестерином. [46]
Считается, что частицы ЛПВП переносят холестерин обратно в печень либо для выведения, либо в другие ткани, синтезирующие гормоны, в процессе, известном как обратный транспорт холестерина (RCT). [50] Большое количество частиц ЛПВП коррелирует с лучшими показателями здоровья, [51] тогда как низкое количество частиц ЛПВП связано с прогрессированием атероматозного заболевания в артериях. [52]
Холестерин подвержен окислению и легко образует кислородсодержащие производные, называемые оксистеринами . Они могут образовываться тремя различными механизмами: автоокислением, вторичным окислением до перекисного окисления липидов и окислением ферментов, метаболизирующих холестерин. Большой интерес к оксистеринам возник, когда было показано, что они оказывают ингибирующее действие на биосинтез холестерина. [53] Это открытие стало известно как «гипотеза оксистерола». Дополнительные роли оксистеринов в физиологии человека включают их участие в биосинтезе желчных кислот, функцию транспортных форм холестерина и регуляцию транскрипции генов. [54]
В биохимических экспериментах используются радиоактивно меченные формы холестерина, такие как тритированный холестерин. Эти производные подвергаются разложению при хранении, и перед использованием важно очищать холестерин. Холестерин можно очистить с помощью небольших колонок Sephadex LH-20. [55]
Холестерин окисляется печенью в различные желчные кислоты . [56] Они, в свою очередь, конъюгированы с глицином , таурином , глюкуроновой кислотой или сульфатом . Смесь конъюгированных и неконъюгированных желчных кислот вместе с самим холестерином выводится из печени в желчь . Примерно 95% желчных кислот реабсорбируется из кишечника, а остальная часть теряется с калом. [57] Экскреция и реабсорбция желчных кислот составляет основу энтерогепатической циркуляции , которая необходима для переваривания и всасывания пищевых жиров. При определенных обстоятельствах, когда холестерин более концентрирован, например, в желчном пузыре , он кристаллизуется и является основным компонентом большинства желчных камней ( лецитиновые и билирубиновые желчные камни также встречаются, но реже). [58] Ежедневно в толстую кишку поступает до 1 г холестерина. Этот холестерин поступает из пищи, желчи и слущенных клеток кишечника и может метаболизироваться бактериями толстой кишки. Холестерин превращается в основном в копростанол , неабсорбируемый стерин, который выводится с калом. [ нужна цитата ]
Хотя холестерин является стероидом, обычно связанным с млекопитающими, человеческий патоген Mycobacterium Tuberculosis способен полностью расщепить эту молекулу и содержит большое количество генов, которые регулируются его присутствием. [59] Многие из этих генов, регулируемых холестерином, являются гомологами генов β-окисления жирных кислот , но эволюционировали таким образом, что связывают большие стероидные субстраты, такие как холестерин. [60] [61]
Животные жиры представляют собой сложные смеси триглицеридов с меньшим количеством молекул фосфолипидов и холестерина, из которых построены клеточные мембраны всех животных (и человека). Поскольку все животные клетки производят холестерин, все продукты животного происхождения содержат холестерин в разных количествах. [62] Основные пищевые источники холестерина включают красное мясо , яичные желтки и цельные яйца , печень , почки , потроха , рыбий жир и сливочное масло . [63] Грудное молоко также содержит значительное количество холестерина. [64]
Растительные клетки синтезируют холестерин в качестве предшественника других соединений, таких как фитостерины и стероидные гликоалкалоиды , при этом холестерин остается в растительной пище лишь в незначительных количествах или отсутствует. [63] [65] Некоторые растительные продукты, такие как авокадо , семена льна и арахис , содержат фитостерины, которые конкурируют с холестерином за всасывание в кишечнике и снижают всасывание как пищевого, так и желчного холестерина. [66] Типичная диета содержит около 0,2 грамма фитостеролов, чего недостаточно, чтобы оказать существенное влияние на блокирование всасывания холестерина. Потребление фитостеринов можно дополнить за счет использования содержащих фитостерол функциональных продуктов питания или пищевых добавок , которые, как известно, обладают потенциалом снижения уровня холестерина ЛПНП . [67]
В 2015 году научная консультативная группа Министерства здравоохранения и социальных служб США и Министерства сельского хозяйства США для версии 2015 года «Руководства по питанию для американцев» снизила ранее рекомендованный предел потребления пищевого холестерина до 300 мг в день, рекомендовав новую рекомендацию: «ешьте как можно меньше пищевого холестерина» и признайте связь между диетой с низким содержанием холестерина и снижением риска сердечно-сосудистых заболеваний. [68]
В отчете Американской кардиологической ассоциации и Американского колледжа кардиологов за 2013 год рекомендуется сосредоточиться на здоровом питании, а не на конкретных ограничениях уровня холестерина, поскольку их сложно внедрить врачам и потребителям. Они рекомендуют DASH и средиземноморскую диету с низким содержанием холестерина. [69] Обзор Американской кардиологической ассоциации, проведенный в 2017 году , рекомендует заменить насыщенные жиры полиненасыщенными жирами , чтобы снизить риск сердечно-сосудистых заболеваний . [70]
В некоторых дополнительных руководствах рекомендованы дозы фитостеролов в диапазоне 1,6–3,0 граммов в день (Health Canada, EFSA, ATP III, FDA). Метаанализ продемонстрировал снижение уровня холестерина ЛПНП на 12% при средней дозе 2,1 грамма в день. [71] Польза диеты с добавлением фитостеролов также подвергалась сомнению. [72]

Согласно липидной гипотезе , повышенный уровень холестерина в крови приводит к атеросклерозу , который может увеличить риск сердечного приступа , инсульта и заболеваний периферических артерий . Поскольку более высокие концентрации ЛПНП в крови – особенно более высокие концентрации ЛПНП и меньший размер частиц ЛПНП – способствуют этому процессу больше, чем содержание холестерина в частицах ЛПВП, [8] частицы ЛПНП часто называют «плохим холестерином». Высокие концентрации функциональных ЛПВП, которые могут удалять холестерин из клеток и атером, обеспечивают защиту и обычно называются «хорошим холестерином». Этот баланс в основном определяется генетически, но может быть изменен составом тела, лекарствами , диетой [73] и другими факторами. [74] Исследование 2007 года продемонстрировало, что уровень общего холестерина в крови оказывает экспоненциальное влияние на сердечно-сосудистую и общую смертность, причем эта связь более выражена у молодых людей. Поскольку сердечно-сосудистые заболевания относительно редки среди молодого населения, влияние высокого уровня холестерина на здоровье сильнее у пожилых людей. [75]
Повышенные уровни фракций липопротеинов, ЛПНП, ЛПНП и ЛПОНП, а не уровень общего холестерина, коррелируют со степенью и прогрессированием атеросклероза. [76] И наоборот, общий холестерин может находиться в пределах нормы, но состоять в основном из мелких частиц ЛПНП и мелких частиц ЛПВП, при которых скорость роста атеромы высока. Апостериорный анализ проспективных исследований IDEAL и EPIC выявил связь между высокими уровнями холестерина ЛПВП (с поправкой на аполипопротеин AI и аполипопротеин B) и повышенным риском сердечно-сосудистых заболеваний, что ставит под сомнение кардиозащитную роль «хорошего холестерина». [77] [78]
Примерно у одного из 250 человек может быть генетическая мутация рецептора холестерина ЛПНП, которая приводит к семейной гиперхолестеринемии. [79] Наследственный высокий уровень холестерина может также включать генетические мутации в гене PCSK9 и гене аполипопротеина B. [80]
Повышенный уровень холестерина поддается лечению с помощью диеты, которая уменьшает или исключает насыщенные жиры, трансжиры и продукты с высоким содержанием холестерина, [81] [82] с последующим применением одного из различных гиполипидемических средств , таких как статины , фибраты , ингибиторы абсорбции холестерина, моноклональные антитела. терапия ( ингибиторы PCSK9 ), производные никотиновой кислоты или секвестранты желчных кислот. [83] Существует несколько международных рекомендаций по лечению гиперхолестеринемии. [84]
Испытания на людях с использованием ингибиторов редуктазы HMG-CoA , известных как статины , неоднократно подтверждали, что изменение моделей транспорта липопротеинов с нездоровых на более здоровые значительно снижает частоту сердечно-сосудистых заболеваний даже у людей, уровень холестерина в которых в настоящее время считается низким для взрослых. [85] Исследования показали, что снижение уровня холестерина ЛПНП примерно на 38,7 мг/дл с помощью статинов может снизить риск сердечно-сосудистых заболеваний и инсульта примерно на 21%. [86] Исследования также показали, что статины замедляют прогрессирование атеромы. [87] В результате люди с сердечно-сосудистыми заболеваниями в анамнезе могут получить пользу от статинов независимо от уровня холестерина (общий холестерин ниже 5,0 ммоль/л [193 мг/дл]) [88] , а у мужчин без сердечно-сосудистых заболеваний есть польза от снижения аномально высокого уровня холестерина («первичная профилактика»). [89] Первоначально первичная профилактика у женщин практиковалась только путем распространения результатов исследований на мужчин, [90] поскольку у женщин ни одно из крупных исследований статинов, проведенных до 2007 года, не продемонстрировало значительного снижения общей смертности или сердечно-сосудистых конечных точек. . [91] Мета-анализ продемонстрировал значительное снижение смертности от всех причин и смертности от сердечно-сосудистых заболеваний без значительной гетерогенности по полу. [92]
В отчете Национальной образовательной программы по холестерину « Комиссии по лечению взрослых» за 1987 год предполагается, что общий уровень холестерина в крови должен быть: < 200 мг/дл нормального холестерина в крови, 200–239 мг/дл пограничного уровня холестерина, > 240 мг/дл высокого уровня холестерина. [93] Американская кардиологическая ассоциация предоставляет аналогичный набор рекомендаций по общему уровню холестерина в крови (натощак) и риску сердечно-сосудистых заболеваний: [81] Статины эффективны для снижения уровня холестерина ЛПНП и широко используются для первичной профилактики у людей с высоким риском сердечно-сосудистых заболеваний. заболеваний, а также во вторичной профилактике для тех, у кого развились сердечно-сосудистые заболевания. [94]
Более современные методы тестирования определяют холестерин ЛПНП («плохой») и ЛПВП («хороший») отдельно, что позволяет сделать анализ холестерина более детальным. Желательным уровнем ЛПНП считается менее 100 мг/дл (2,6 ммоль /л). [95] [96]

Общий холестерин определяется как сумма ЛПВП, ЛПНП и ЛПОНП. Обычно измеряют только общее количество, ЛПВП и триглицериды. Из соображений стоимости ЛПОНП обычно оценивают как одну пятую триглицеридов, а ЛПНП оценивают по формуле Фридевальда (или ее варианту ) : расчетный ЛПНП = [общий холестерин] - [общий ЛПВП] - [оцененный ЛПОНП]. Прямые измерения ЛПНП используются, когда уровень триглицеридов превышает 400 мг/дл. Расчетные значения ЛПОНП и ЛПНП имеют большую погрешность, когда уровень триглицеридов превышает 400 мг/дл. [97]
Во Фрамингемском исследовании сердца каждое увеличение уровня общего холестерина на 10 мг/дл (0,6 ммоль /л) повышало общую 30-летнюю смертность на 5%, а смертность от сердечно-сосудистых заболеваний на 9%. В то время как у пациентов старше 50 лет наблюдалось увеличение общей смертности на 11% и увеличение смертности от сердечно-сосудистых заболеваний на 14% на каждые 1 мг/дл (0,06 ммоль /л) годового снижения уровня общего холестерина. Исследователи объяснили это явление другой корреляцией , согласно которой болезнь сама по себе увеличивает риск смерти, а также изменяет множество факторов, таких как потеря веса и неспособность есть, которые снижают уровень холестерина в сыворотке. [98] Этот эффект был также показан у мужчин всех возрастов и женщин старше 50 лет в рамках Программы мониторинга и укрепления здоровья Форарльберга. Эти группы чаще умирали от рака, заболеваний печени и психических заболеваний при очень низком уровне общего холестерина — 186 мг/дл (10,3 ммоль /л) и ниже. Этот результат указывает на то, что эффект низкого уровня холестерина наблюдается даже среди более молодых респондентов, что противоречит предыдущей оценке среди когорт пожилых людей, согласно которой это является маркером слабости, возникающей с возрастом. [99]
Аномально низкий уровень холестерина называется гипохолестеринемией . Исследования причин этого состояния относительно ограничены, но некоторые исследования предполагают связь с депрессией , раком и кровоизлиянием в мозг . В целом низкий уровень холестерина кажется следствием, а не причиной основного заболевания. [75] Генетический дефект синтеза холестерина вызывает синдром Смита-Лемли-Опитца , который часто связан с низким уровнем холестерина в плазме. Гипертиреоз или любое другое эндокринное нарушение, вызывающее активацию рецептора ЛПНП , может привести к гипохолестеринемии. [100]
Американская кардиологическая ассоциация рекомендует проверять уровень холестерина каждые 4–6 лет людям в возрасте 20 лет и старше. [101] В отдельном наборе рекомендаций Американской кардиологической ассоциации, выпущенном в 2013 году, указано, что люди, принимающие статины , должны проверять уровень холестерина через 4–12 недель после первой дозы, а затем каждые 3–12 месяцев после этого. [102] [103] Мужчинам в возрасте от 45 до 65 лет и женщинам в возрасте от 55 до 65 лет тест на холестерин следует проводить каждые 1–2 года, а пожилым людям старше 65 лет тест следует проводить ежегодно. [102]
Образец крови после 12-часового голодания берется медицинским работником из вены руки для измерения липидного профиля : а) общего холестерина, б) холестерина ЛПВП, в) холестерина ЛПНП и г) триглицеридов . [3] [102] Результаты могут быть выражены как «расчетные», что означает расчет общего холестерина, ЛПВП и триглицеридов. [3]
Холестерин тестируется для определения «нормального» или «желательного» уровня, если у человека общий уровень холестерина составляет 5,2 ммоль/л или менее (200 мг/дл), а уровень ЛПВП превышает 1 ммоль/л (40 мг/дл). «чем выше, тем лучше»), значение ЛПНП менее 2,6 ммоль/л (100 мг/дл) и уровень триглицеридов менее 1,7 ммоль/л (150 мг/дл). [102] [3] Уровень холестерина в крови у людей с образом жизни, старением или факторами риска сердечно-сосудистых заболеваний, такими как сахарный диабет , гипертония , семейный анамнез ишемической болезни сердца или стенокардия , оценивается на разных уровнях. [102]
Нажмите на гены, белки и метаболиты ниже, чтобы перейти к соответствующим статьям. [§ 1]
Известно, что некоторые производные холестерина (среди других простых холестерических липидов) образуют жидкокристаллическую « холестерическую фазу». Холестерическая фаза по сути является хиральной нематической фазой и меняет цвет при изменении ее температуры. Это делает производные холестерина полезными для индикации температуры в термометрах с жидкокристаллическими дисплеями и в термочувствительных красках. [ нужна цитата ]
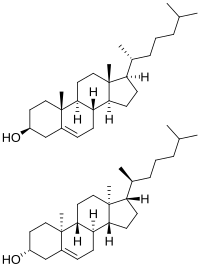
Холестерин имеет 256 стереоизомеров , которые возникают из его восьми стереоцентров, хотя только два из стереоизомеров имеют биохимическое значение ( нат -холестерин и энт -холестерин, для природного и энантиомера соответственно), [104] [105] и только один встречается в природе ( нат -холестерин).
Je nommerai
cholesterine
, de χολη, желчь, et στερεος, Solide, la вещество cristallisée des Calculs biliares Humanes, ...[Назову холестерин – от χολη (желчь) и στερεος (твердое) – кристаллизованное вещество из желчных камней человека.. .]