В ядерной науке цепочка распада относится к предсказуемой серии радиоактивных распадов, которым подвергаются ядра некоторых нестабильных химических элементов.
Радиоактивные изотопы обычно не распадаются непосредственно на стабильные изотопы , а скорее на другой радиоизотоп. Этот дочерний изотоп затем распадается на другой, часто радиоактивный изотоп. Эта цепочка распадов всегда заканчивается стабильным изотопом, ядро которого больше не имеет избытка энергии, необходимого для создания радиоактивного излучения. Такие стабильные изотопы затем называются имеющими ядра, которые достигли своих основных состояний .
Стадии или шаги в цепочке распада называются по их отношению к предыдущим или последующим стадиям. Следовательно, родительский изотоп - это тот, который распадается с образованием дочернего изотопа . Например, изотоп элемента 92, урана , со 143 нейтронами ( 236 U ), распадается на изотоп элемента 90, тория , со 142 нейтронами ( 232 Th ). Дочерний изотоп может быть стабильным или сам распадаться с образованием другого дочернего изотопа, например 232 Th, который распадается на радий-228 . Дочерний изотоп дочернего изотопа, например 228 Ra, иногда называют внучатым изотопом .
Время, необходимое для распада родительского изотопа на дочерний изотоп, принципиально непредсказуемо и сильно варьируется. Для отдельных ядер неизвестно, имеет ли этот процесс определяемые причины, и время, в которое он происходит, поэтому полностью случайно . Единственное предсказание, которое можно сделать, использует среднюю скорость распада. Эту скорость можно представить, настроив кривую распадающегося экспоненциального распределения с константой распада ( λ ), специфичной для изотопа. При таком понимании радиоактивный распад начальной популяции нестабильных атомов с течением времени t следует кривой, заданной выражением e − λt .
Из этого анализа следует одно из важнейших свойств любого радиоактивного материала — его период полураспада . Это время, необходимое для распада половины заданного числа радиоактивных атомов, и оно обратно пропорционально постоянной распада изотопа λ . Периоды полураспада были определены в лабораториях для многих радионуклидов и могут варьироваться от почти мгновенных (менее 10−23 секунд ) до на девять порядков больше возраста Вселенной (1019 лет ).

Уравнение Бейтмана предсказывает относительные количества всех изотопов, которые составляют данную цепочку распада, как только эта цепочка распада продолжается достаточно долго, чтобы некоторые из ее дочерних продуктов достигли стабильного (т. е. нерадиоактивного) конца цепочки. Цепочка распада, которая достигла этого состояния, что может потребовать миллиардов лет, называется равновесной . Образец радиоактивного материала в равновесии производит устойчивое и неуклонно уменьшающееся количество радиоактивности по мере того, как изотопы, которые его составляют, проходят цепочку распада. С другой стороны, если образец радиоактивного материала был изотопно обогащен, что означает, что радиоизотоп присутствует в больших количествах, чем существовало бы, если бы цепочка распада была единственной причиной его присутствия, то этот образец считается неравновесным . Неинтуитивным следствием этого неравновесия является то, что образец обогащенного материала может иногда увеличивать радиоактивность, поскольку дочерние продукты, которые более радиоактивны, чем их родительские, накапливаются. Как обогащенный , так и обедненный уран являются примерами этого явления.
Химические элементы появились в два этапа. Первый начался вскоре после Большого взрыва . От десяти секунд до 20 минут после начала Вселенной самая ранняя конденсация легких атомов была ответственна за производство четырех самых легких элементов. Подавляющее большинство этого первичного производства состояло из трех известных изотопов водорода — протия , дейтерия и трития — и двух из девяти известных изотопов гелия — гелия-3 и гелия-4 . Следовые количества лития-7 и бериллия-7, вероятно, также были получены.
Насколько известно, все более тяжелые элементы появились примерно 100 миллионов лет спустя, во второй фазе нуклеосинтеза , которая началась с рождением первых звезд . [1] Ядерные печи, которые питают звездную эволюцию, были необходимы для создания больших количеств всех элементов тяжелее гелия, и r- и s-процессы захвата нейтронов, которые происходят в звездных ядрах, как полагают, создали все такие элементы вплоть до железа и никеля (атомные номера 26 и 28). Экстремальные условия , которые сопровождают взрывы сверхновых, способны создавать элементы между кислородом и рубидием (т. е. атомные номера от 8 до 37). Создание более тяжелых элементов, включая те, которые не имеют стабильных изотопов — все элементы с атомными номерами больше, чем у свинца, 82 — по-видимому, зависит от r-процесса нуклеосинтеза, действующего среди огромных концентраций свободных нейтронов, высвобождаемых во время слияний нейтронных звезд .
Большинство изотопов каждого химического элемента, присутствующего на Земле сегодня, были образованы такими процессами не позднее времени конденсации нашей планеты из солнечного протопланетного диска , около 4,5 миллиардов лет назад. Исключениями из этих так называемых первичных элементов являются те, которые возникли в результате радиоактивного распада нестабильных родительских ядер по мере их продвижения по одной из нескольких цепочек распада, каждая из которых заканчивается образованием одного из 251 известных стабильных изотопов. Помимо космического или звездного нуклеосинтеза и цепочек распада, единственные другие способы получения химического элемента полагаются на атомное оружие , ядерные реакторы ( естественные или искусственные ) или трудоемкую сборку атом за атомом ядер с помощью ускорителей частиц .
Нестабильные изотопы распадаются на свои дочерние продукты (которые иногда могут быть еще более нестабильными) с заданной скоростью; в конечном итоге, часто после серии распадов, достигается стабильный изотоп: во Вселенной существует 251 стабильный изотоп. В стабильных изотопах легкие элементы обычно имеют более низкое отношение нейтронов к протонам в своем ядре, чем более тяжелые элементы. Легкие элементы, такие как гелий-4, имеют близкое к 1:1 отношение нейтронов к протонам. Самые тяжелые элементы, такие как уран, имеют близкое к 1,5 нейтрона на протон (например, 1,587 в уране-238 ). Ни один нуклид тяжелее свинца-208 не является стабильным; эти более тяжелые элементы должны сбрасывать массу, чтобы достичь стабильности, в основном за счет альфа-распада . Другим распространенным способом распада изотопов с высоким отношением нейтронов к протонам (n/p) является бета-распад , при котором нуклид меняет элементную идентичность, сохраняя то же массовое число и снижая свое отношение n/p. Для некоторых изотопов с относительно низким отношением n/p существует обратный бета-распад , при котором протон преобразуется в нейтрон, таким образом двигаясь к стабильному изотопу; однако, поскольку деление почти всегда производит продукты, которые являются тяжелыми нейтронами, эмиссия позитронов или захват электронов редки по сравнению с эмиссией электронов. Существует много относительно коротких цепочек бета-распада, по крайней мере две (тяжелая, бета-распад и легкая, позитронный распад) для каждого дискретного веса примерно до 207 и некоторые выше, но для элементов с большей массой (изотопы тяжелее свинца) существует только четыре пути, которые охватывают все цепочки распада. [ необходима цитата ] Это связано с тем, что существует всего два основных метода распада: альфа-излучение , которое уменьшает массу на 4 атомные единицы массы (а.е.м.), и бета-излучение, которое не изменяет массовое число (только атомный номер и отношение p/n). Четыре пути называются 4n, 4n + 1, 4n + 2 и 4n + 3; остаток от деления атомной массы на четыре дает цепочку, которую изотоп будет использовать для распада. Существуют и другие режимы распада, но они неизменно происходят с меньшей вероятностью, чем альфа- или бета-распад. (Не следует предполагать, что эти цепочки не имеют ответвлений: на схеме ниже показано несколько ответвлений цепочек, и на самом деле их гораздо больше, потому что возможных изотопов гораздо больше, чем показано на схеме.) Например, третий синтезированный атом нихония-278 претерпел шесть альфа-распадов до менделевия-254 [ 2], за которыми последовал захват электрона (форма бета-распада) до фермия-254 [2] , а затем седьмой альфа-распад до калифорния-250 [ 2]после чего он бы следовал цепочке 4n + 2 (ряд радия), как указано в этой статье. Однако самые тяжелые синтезированные сверхтяжелые нуклиды не достигают четырех цепочек распада, поскольку они достигают спонтанно делящегося нуклида после нескольких альфа-распадов, который завершает цепочку: это то, что произошло с первыми двумя синтезированными атомами нихония-278 [3] [4], а также со всеми произведенными более тяжелыми нуклидами.
Три из этих цепочек имеют долгоживущий изотоп (или нуклид) вблизи вершины; этот долгоживущий нуклид является узким местом в процессе, через который цепочка протекает очень медленно, и поддерживает цепочку под ними «живой» с течением. Три долгоживущих нуклида — это уран-238 (период полураспада 4,5 миллиарда лет), уран-235 (период полураспада 700 миллионов лет) и торий-232 (период полураспада 14 миллиардов лет). Четвертая цепочка не имеет такого долгоживущего нуклида-узкого места вблизи вершины, поэтому почти все нуклиды в этой цепочке давно распались до самого конца: висмута-209. Этот нуклид долгое время считался стабильным, но в 2003 году было обнаружено, что он нестабилен, с очень долгим периодом полураспада 20,1 миллиарда миллиардов лет; [5] это последний шаг в цепочке перед стабильным таллием-205. Поскольку это узкое место существует так долго, было произведено очень малое количество конечного продукта распада, и для большинства практических целей конечным продуктом распада является висмут-209.
В далеком прошлом, в течение первых нескольких миллионов лет истории Солнечной системы, существовало больше видов нестабильных массивных нуклидов, и четыре цепочки были длиннее, так как включали нуклиды, которые с тех пор распались. Примечательно, что 244 Pu, 237 Np и 247 Cm имеют периоды полураспада более миллиона лет и тогда были бы меньшими узкими местами в верхних цепочках 4n, 4n+1 и 4n+3 соответственно. [6] (Нет ни одного нуклида с периодом полураспада более миллиона лет выше 238 U в цепочке 4n+2.) Сегодня некоторые из этих ранее исчезнувших изотопов снова существуют, поскольку они были изготовлены. Таким образом, они снова занимают свои места в цепочке: плутоний-239, используемый в ядерном оружии, является основным примером, распадающимся до урана-235 посредством альфа-излучения с периодом полураспада 24 500 лет. Также было осуществлено крупномасштабное производство нептуния-237, который возродил доселе неактивированную четвертую цепь. [7] Таким образом, в таблицах ниже четыре цепи распада начинаются с изотопов калифорния с массовыми числами от 249 до 252.
Эти четыре цепочки обобщены в таблице в следующем разделе.

Четыре наиболее распространенных способа радиоактивного распада: альфа-распад, бета-распад, обратный бета-распад (рассматриваемый как испускание позитронов и захват электронов) и изомерный переход . Из этих процессов распада только альфа-распад (деление ядра гелия-4 ) изменяет атомное массовое число ( A ) ядра и всегда уменьшает его на четыре. Из-за этого почти любой распад приведет к ядру, атомное массовое число которого имеет тот же остаток mod 4. Это делит список нуклидов на четыре класса. Все члены любой возможной цепочки распада должны быть взяты полностью из одного из этих классов.
В природе наблюдаются три основные цепочки распада (или семейства). Их обычно называют ториевой серией, радиевой или урановой серией и актиниевой серией, представляющими три из этих четырех классов и заканчивающимися тремя различными стабильными изотопами свинца . Массовое число каждого изотопа в этих цепочках можно представить как A = 4 n , A = 4 n + 2 и A = 4 n + 3 соответственно. Долгоживущие начальные изотопы этих трех изотопов, соответственно торий-232 , уран-238 и уран-235 , существовали с момента образования Земли, игнорируя искусственные изотопы и их распады, созданные с 1940-х годов.
Из-за относительно короткого периода полураспада его начального изотопа нептуния-237 (2,14 миллиона лет), четвертая цепь, серия нептуния с A = 4 n + 1, уже вымерла в природе, за исключением конечной стадии, ограничивающей скорость, распада висмута -209 . Следы 237 Np и продуктов его распада встречаются в природе, однако в результате захвата нейтронов в урановой руде. [8] Конечным изотопом этой цепи теперь, как известно, является таллий-205 . Некоторые старые источники называют конечный изотоп висмутом-209, но в 2003 году было обнаружено, что он очень слабо радиоактивен, с периодом полураспада2,01 × 10 19 лет . [9]
Существуют также нетрансурановые цепочки распада нестабильных изотопов легких элементов, например, магния-28 и хлора-39 . На Земле большинство исходных изотопов этих цепочек до 1945 года были получены под воздействием космической радиации . С 1945 года испытания и применение ядерного оружия также привели к выбросу многочисленных радиоактивных продуктов деления . Почти все такие изотопы распадаются либо по типу β −, либо по типу β + , переходя от одного элемента к другому без изменения атомной массы. Эти более поздние дочерние продукты, будучи ближе к стабильности, обычно имеют более длительные периоды полураспада, пока они окончательно не распадутся на стабильность.
В четырех таблицах ниже незначительные ветви распада (с вероятностью ветвления менее 0,0001%) опущены. Выделяющаяся энергия включает в себя полную кинетическую энергию всех испущенных частиц ( электронов , альфа-частиц , гамма-квантов , нейтрино , оже-электронов и рентгеновских лучей ) и ядра отдачи, предполагая, что исходное ядро находилось в состоянии покоя. Буква «a» обозначает год (от латинского annus ).
В таблицах ниже (кроме нептуния) также даны исторические названия природных нуклидов. Эти названия использовались в то время, когда цепочки распада были впервые обнаружены и исследованы. По этим историческим названиям можно найти конкретную цепочку, к которой принадлежит нуклид, и заменить ее современным названием.
Три природных актиноидных альфа-распада цепочек, представленных ниже — тория, урана/радия (из урана-238) и актиния (из урана-235) — каждая заканчивается своим собственным специфическим изотопом свинца (свинец-208, свинец-206 и свинец-207 соответственно). Все эти изотопы стабильны и также присутствуют в природе в качестве первичных нуклидов , но их избыточные количества по сравнению со свинцом-204 (который имеет только первичное происхождение) могут быть использованы в технике уран-свинцового датирования для датирования пород.
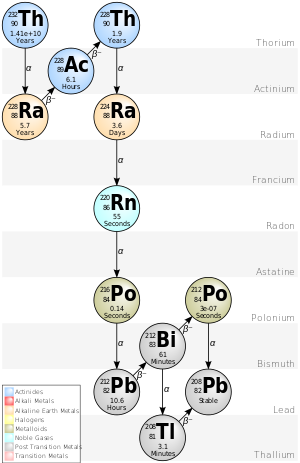
Цепочку 4n тория-232 обычно называют «ториевым рядом» или «ториевым каскадом». Начиная с природного тория-232, этот ряд включает следующие элементы: актиний , висмут , свинец, полоний , радий, радон и таллий . Все они присутствуют, по крайней мере временно, в любом природном образце, содержащем торий, будь то металл, соединение или минерал. Ряд заканчивается свинцом-208.
Плутоний-244 (который находится на несколько ступеней выше тория-232 в этой цепочке, если расширить ее до трансурановых элементов) присутствовал в ранней Солнечной системе [6] и является достаточно долгоживущим, чтобы он все еще мог существовать в следовых количествах сегодня [15] , хотя неизвестно, был ли он обнаружен. [16]
Общая энергия, выделяемая торием-232 в свинец-208, включая энергию, потерянную на нейтрино, составляет 42,6 МэВ.
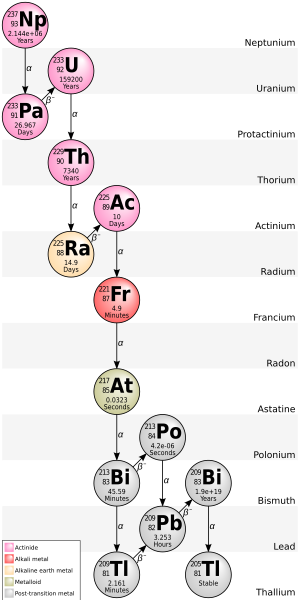
Цепочку 4n + 1 нептуния-237 обычно называют «серией нептуния» или «каскадом нептуния». В этой серии только два из участвующих изотопа встречаются в природе в значительных количествах, а именно последние два: висмут-209 и таллий-205. Некоторые из других изотопов были обнаружены в природе, происходящие от следовых количеств 237 Np, полученных в результате реакции выбивания (n,2n) в первичном 238 U. [8] Детектор дыма , содержащий ионизационную камеру с америцием-241, накапливает значительное количество нептуния -237 по мере распада америция. В ней также присутствуют, по крайней мере временно, следующие элементы как продукты распада нептуния: актиний, астат , висмут, франций , свинец, полоний, протактиний , радий, радон, таллий, торий и уран . Поскольку эта серия была открыта и изучена только в 1947–1948 годах, [21] ее нуклиды не имеют исторических названий. Одной из уникальных особенностей этой цепочки распада является то, что благородный газ радон образуется только в редкой ветви (не показанной на иллюстрации), но не в основной последовательности распада; таким образом, радон из этой цепочки распада не мигрирует через породу почти так же сильно, как из трех других. Еще одной уникальной особенностью этой последовательности распада является то, что она заканчивается таллием, а не свинцом. Эта серия заканчивается стабильным изотопом таллием-205.
Общая энергия, выделившаяся из калифорния-249 в таллий-205, включая энергию, потерянную на нейтрино , составляет 66,8 МэВ.
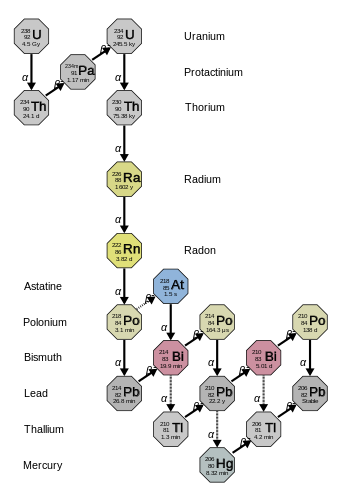
Цепочка 4n+2 урана-238 называется «урановым рядом» или «радиевым рядом». Начиная с природного урана-238, этот ряд включает следующие элементы: астат, висмут, свинец , ртуть, полоний, протактиний , радий , радон , таллий и торий. Все они присутствуют, по крайней мере временно, в любом образце, содержащем природный уран, будь то металл, соединение или минерал. Ряд заканчивается свинцом-206.
Общая энергия, выделяемая из урана-238 в свинец-206, включая энергию, потерянную на нейтрино, составляет 51,7 МэВ.
Цепочку 4n+3 урана-235 обычно называют «актиниевым рядом» или «актиниевым каскадом». Начиная с природного изотопа урана-235, этот ряд распада включает следующие элементы: актиний, астат , висмут , франций , свинец , полоний , протактиний , радий, радон, таллий и торий . Все они присутствуют, по крайней мере временно, в любом образце, содержащем уран-235, будь то металл, соединение, руда или минерал. Этот ряд заканчивается стабильным изотопом свинец-207 .
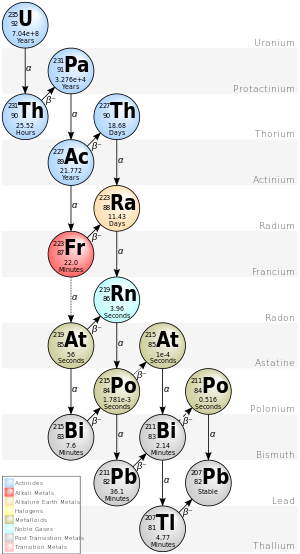
В ранней Солнечной системе эта цепочка восходила к 247 Cm. Сегодня это проявляется в виде изменений в соотношениях 235 U/ 238 U, поскольку кюрий и уран имеют заметно различную химию и разделились бы по-разному. [6] [24]
Общая энергия, выделяемая ураном-235 в свинец-207, включая энергию, потерянную на нейтрино, составляет 46,4 МэВ.
{{cite web}}: CS1 maint: multiple names: authors list (link)