Диборан(6) , широко известный как диборан , представляет собой химическое соединение формулы B 2 H 6 . Это высокотоксичный , бесцветный, пирофорный газ с отвратительно сладким запахом. Учитывая свою простую формулу, боран является фундаментальным соединением бора . Он привлек широкое внимание своей электронной структурой. Некоторые из его производных являются полезными реагентами .
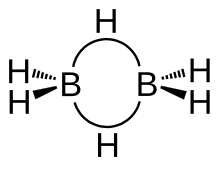
Структура диборана имеет симметрию D 2h . Четыре гидрида являются концевыми, а два мостиковыми между центрами бора. Длины мостиковых связей B–H и концевых связей B–H составляют 1,33 и 1,19 Å соответственно. Эта разница в длинах связей отражает разницу в их прочности: мостиковые связи B – H относительно слабее. На слабость мостика B–H по сравнению с концевыми связями B–H указывают их колебательные характеристики в инфракрасном спектре , составляющие ≈2100 и 2500 см –1 соответственно. [7]
Модель, определенная теорией молекулярных орбиталей, описывает связи между бором и концевыми атомами водорода как обычные 2-центровые 2-электронные ковалентные связи . Однако связь между атомами бора и мостиковыми атомами водорода отличается от связи в таких молекулах, как углеводороды. Каждый бор использует два электрона для связи с концевыми атомами водорода и имеет один валентный электрон, остающийся для дополнительной связи. Мостиковые атомы водорода обеспечивают по одному электрону каждый. Кольцо B 2 H 2 удерживается вместе четырьмя электронами, образующими две 3-центровые 2-электронные связи . Этот тип облигации иногда называют «банановой облигацией».
B 2 H 6 изоэлектронен с C 2 H 6 2+ , что могло бы возникнуть в результате дипротонирования плоской молекулы этилена . [8] Диборан – одно из многих соединений с такой необычной связью. [9]
Известно, что из других элементов группы IIIA галлий образует аналогичное соединение дигаллан Ga 2 H 6 . Алюминий образует полимерный гидрид (AlH 3 ) n ; Al 2 H 6 хотя и нестабилен, но был выделен в твердом водороде и изоструктурен диборану. [10]
Обширные исследования диборана привели к разработке нескольких путей синтеза. Большинство препаратов основано на реакциях доноров гидридов с галогенидами или алкоксидами бора . Промышленный синтез диборана включает восстановление BF 3 гидридом натрия (NaH), гидридом лития (LiH) или литийалюминийгидридом (LiAlH 4 ): [11]
Используемый для этой цели гидрид лития должен быть очень тонко измельчен во избежание образования пассивирующего слоя тетрафторбората лития на реагенте. В качестве альтернативы можно добавить небольшое количество диборана с образованием боргидрида лития , который разложит фторборат и сделает реакцию автокаталитической . [12]
Два лабораторных метода начинаются с трихлорида бора с алюмогидридом лития или с эфирного раствора трифторида бора с боргидридом натрия . Оба метода дают доходность до 30%:
При нагревании с NaBH 4 хлорид олова(II) восстанавливается до элементарного олова, образуя при этом диборан:
Более старые методы предполагают прямую реакцию солей боргидрида с неокисляющей кислотой , такой как фосфорная кислота или разбавленная серная кислота .
Аналогичным образом было продемонстрировано окисление солей боргидрида, которое остается удобным для получения в небольших масштабах. Например, используя йод в качестве окислителя: [13]
В другом мелкомасштабном синтезе в качестве исходных материалов используются боргидрид калия и фосфорная кислота. [14]

Диборан — высокореактивный и универсальный реагент. [16]
Как пирофорное вещество, диборан экзотермически реагирует с кислородом с образованием триоксида бора и воды:
Диборан бурно реагирует с водой с образованием водорода и борной кислоты :
Аналогично реагирует диборан и со спиртами. Метанол, например, дает водород и триметилборат : [17]
Одна из доминирующих моделей реакций включает образование аддуктов с основаниями Льюиса . Часто такие первоначальные аддукты быстро превращаются в другие продукты. Например, боран-тетрагидрофуран, который часто ведет себя так же, как диборан, разлагается до сложных эфиров борной кислоты. Его аддукт с диметилсульфидом — важный реагент в органическом синтезе .
С дибораном аммиака образуется диаммониат диборана DADB с небольшими количествами борана аммиака в качестве побочного продукта. Пропорция зависит от условий.
В реакции гидроборирования диборан также легко реагирует с алкенами с образованием триалкилборанов . Эта схема реакции является довольно общей, и полученные алкилбораты можно легко превратить в производные, например, в спирты. Хотя ранние работы по гидроборированию основывались на диборане, его заменил диметилсульфид борана, обращение с которым более безопасно.
Пиролиз диборана дает водород и разнообразные кластеры гидрида бора. Например, пентаборан впервые был получен пиролизом диборана при температуре около 200 °С. [18] [19] Хотя этот путь пиролиза используется редко, он открыл большую тему исследований в области химии борановых кластеров.
Обработка диборана амальгамой натрия дает NaBH 4 и Na[B 3 H 8 ] [17]. При обработке диборана гидридом лития в диэтиловом эфире образуется боргидрид лития: [17]
Диборан реагирует с безводным хлористым водородом или газообразным бромистым водородом с образованием галогенгидрида бора: [17]
Обработка диборана окисью углерода при 470 К и 20 бар дает H 3 BCO . [17]
Диборан и его варианты являются центральными реагентами органического синтеза для гидроборирования . Алкены присоединяются по связям B–H с образованием триалкилборанов, которые можно получить в дальнейшем. [20] Диборан используется в качестве восстановителя, примерно дополняющего по реакционной способности литийалюминийгидрид . Соединение легко восстанавливает карбоновые кислоты до соответствующих спиртов , тогда как кетоны реагируют медленно.
Диборан был впервые синтезирован в 19 веке путем гидролиза боридов металлов, но никогда не анализировался. С 1912 по 1936 год Альфред Сток , главный пионер в области химии гидридов бора, провел исследования, которые привели к разработке методов синтеза и обращения с высокореактивными, летучими и часто токсичными гидридами бора. Он предложил первую этаноподобную структуру диборана. [21] Измерения дифракции электронов , проведенные С.Х. Бауэром, первоначально казались подтверждающими предложенную им структуру. [22] [23]
Из-за личного общения с Л. Полингом (который поддерживал этаноподобную структуру), Х. И. Шлезингер и А. Б. Бург специально не обсуждали 3-центровую 2-электронную связь в своем тогдашнем классическом обзоре в начале 1940-х годов. [24] Однако в обзоре довольно подробно обсуждается мостиковая структура D 2h : «Следует признать, что эта формулировка легко объясняет многие химические свойства диборана…»
В 1943 году Х. Кристофер Лонге-Хиггинс , еще будучи студентом Оксфорда, первым объяснил структуру и связь гидридов бора. В статье, сообщающей о работе, написанной совместно с его наставником Р. П. Беллом [25] , также рассматривается история предмета, начиная с работ Дильтея. [26] Вскоре после этого теоретическая работа Лонге-Хиггинса была подтверждена Прайсом в инфракрасном исследовании диборана. [27] Структура была повторно подтверждена электронодифракционными измерениями в 1951 году К. Хедбергом и В. Шомакером, с подтверждением структуры, показанной на схемах на этой странице. [28]
Уильям Нанн Липскомб -младший дополнительно подтвердил молекулярную структуру боранов с помощью рентгеновской кристаллографии в 1950-х годах и разработал теории, объясняющие их связь. Позже он применил те же методы к смежным проблемам, в том числе к структуре карборанов, исследованиями которой руководил будущий лауреат Нобелевской премии 1981 года Роальд Хоффманн . Нобелевская премия по химии 1976 года была присуждена Липскомбу «за исследования структуры боранов, освещающие проблемы химической связи». [29]
Традиционно диборан часто называют электронодефицитным , поскольку 12 валентных электронов могут образовывать только 6 обычных 2-центровых 2-электронных связей, которых недостаточно для соединения всех 8 атомов. [30] [31] Однако более правильное описание с использованием 3-центровых связей показывает, что диборан действительно является электронно-точным, поскольку валентных электронов достаточно, чтобы заполнить 6 связывающих молекулярных орбиталей . [32] Тем не менее, в некоторых ведущих учебниках до сих пор используется термин «электронодефицитный». [33]
Из-за экзотермичности реакции с кислородом диборан был испытан в качестве ракетного топлива . [34] Полное сгорание сильно экзотермично. Однако сгорание в ракетном двигателе не является полным, так как образуется некоторое количество монооксида бора B 2 O. Это преобразование отражает неполное сгорание углеводородов с образованием монооксида углерода (CO). С Дибораном также оказалось трудно справиться. [35] [36] [37]
Диборан исследовался в качестве предшественника пленок боридов металлов [38] и для p-легирования кремниевых полупроводников. [39]
Диборан — пирофорный газ. Вместо этого обычно используются коммерчески доступные аддукты , по крайней мере, для приложений в органической химии. Эти аддукты включают боран-тетрагидрофуран (боран-ТГФ) и боран-диметилсульфид . [16] Токсическое воздействие диборана смягчается, поскольку это соединение нестабильно на воздухе. Была исследована токсичность по отношению к лабораторным крысам. [40]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )Одним из простых следствий этих исследований было то, что молекулы с дефицитом электронов, определенные как имеющие больше валентных орбиталей, чем электроны, на самом деле не являются электронодефицитными.
Электронодефицитные виды обладают меньшим количеством валентных электронов, чем требуется для схемы локализованной связи.
{{cite web}}: CS1 maint: местоположение ( ссылка )