Рецептор Т-клеток ( TCR ) представляет собой белковый комплекс , обнаруженный на поверхности Т-клеток или Т-лимфоцитов [1] , который отвечает за распознавание фрагментов антигена в виде пептидов, связанных с молекулами главного комплекса гистосовместимости (MHC). Связывание между TCR и антигенными пептидами имеет относительно низкую аффинность и является вырожденным : то есть многие TCR распознают один и тот же антигенный пептид, и многие антигенные пептиды распознаются одним и тем же TCR. [2]
TCR состоит из двух разных белковых цепей (то есть представляет собой гетеродимер ) . У человека в 95% Т-клеток TCR состоит из альфа-(α)-цепи и бета-(β)-цепи (кодируемых TRA и TRB соответственно), тогда как в 5% Т-клеток TCR состоит из гамма- и дельта-цепи. (γ/δ)-цепочки (кодируются TRG и TRD соответственно). Это соотношение меняется в процессе онтогенеза и при болезненных состояниях (например, при лейкемии ). Он также различается между видами. Ортологи четырех локусов картированы у разных видов. [3] [4] Каждый локус может производить множество полипептидов с константными и вариабельными областями. [3]
Когда TCR взаимодействует с антигенным пептидом и MHC (пептид/MHC), Т-лимфоцит активируется посредством передачи сигнала , то есть серии биохимических событий, опосредованных ассоциированными ферментами, корецепторами, специализированными молекулами-адаптерами, а также активированной или высвобождаемой транскрипцией . факторы . По механизму запуска начального рецептора TCR принадлежит к семейству некаталитических тирозинфосфорилированных рецепторов (NTR). [5]
В 1982 году нобелевский лауреат Джеймс П. Эллисон впервые обнаружил клонально экспрессируемый поверхностный эпитоп Т-клеток при Т-лимфоме мышей. [6] В 1983 году Эллис Рейнхерц впервые определил структуру человеческого рецептора Т-клеток, используя антиидиотипические моноклональные антитела к клонам Т-клеток, что было дополнено исследованиями на мышах, проведенными Филиппой Маррак и Джоном Капплером . [7] [8] Затем в 1984 году Так Ва Мак [9] и Марк М. Дэвис [10] идентифицировали клоны кДНК, кодирующие TCR человека и мыши соответственно. Эти открытия позволили определить сущность и структуру неуловимого TCR, известного ранее. как «Святой Грааль иммунологии», который предстоит раскрыть. Это позволило ученым со всего мира провести исследования TCR, что привело к важным исследованиям в области CAR-T , иммунотерапии рака и ингибирования контрольных точек .
TCR представляет собой дисульфидно-связанный гетеродимерный белок, закрепленный на мембране, обычно состоящий из сильно вариабельных альфа-(α) и бета-(β)-цепей, экспрессируемых как часть комплекса с инвариантными молекулами цепи CD3 . Т-клетки, экспрессирующие этот рецептор, называются Т-клетками α:β (или αβ), хотя меньшинство Т-клеток экспрессируют альтернативный рецептор, образованный вариабельными гамма-(γ) и дельта-(δ)-цепями, называемыми γδ-Т-клетками . [11]
Каждая цепь состоит из двух внеклеточных доменов: вариабельной (V) области и константной (C) области, оба из доменов суперсемейства иммуноглобулинов (IgSF) , образующих антипараллельные β-листы . Константная область расположена проксимальнее клеточной мембраны, за ней следует трансмембранная область и короткий цитоплазматический хвост, а вариабельная область связывается с комплексом пептид/MHC.
Вариабельный домен как α-цепи, так и β-цепи TCR имеет по три гипервариабельных или определяющих комплементарность участка (CDR). Существует также дополнительная область гипервариабельности β-цепи (HV4), которая обычно не контактирует с антигеном и, следовательно, не считается CDR. [ нужна цитата ]
Остатки в этих вариабельных доменах расположены в двух областях TCR: на границе раздела α- и β-цепей и в каркасной области β-цепи , которая, как полагают, находится вблизи комплекса передачи сигнала CD3. [12] CDR3 является основным CDR, ответственным за распознавание процессированного антигена , хотя также было показано, что CDR1 альфа-цепи взаимодействует с N-концевой частью антигенного пептида, тогда как CDR1 β-цепи взаимодействует с C-концевой частью антигенного пептида. часть пептида.
Считается, что CDR2 распознает MHC. Считается, что HV4 β-цепи не участвует в распознавании антигена, как классические CDR, но было показано, что он взаимодействует с суперантигенами . [13]
Константный домен TCR состоит из коротких соединительных последовательностей, в которых остаток цистеина образует дисульфидные связи, образующие связь между двумя цепями.
TCR является членом суперсемейства иммуноглобулинов, большой группы белков, участвующих в связывании, распознавании и адгезии; семейство названо в честь антител (также называемых иммуноглобулинами). TCR подобен полуантителу, состоящему из одной тяжелой и одной легкой цепи, за исключением того, что тяжелая цепь не содержит кристаллизующейся фракции (Fc). Две основные субъединицы TCR (α- и β-цепи) скручены вместе. CD3 и дзета-субъединицы необходимы для осуществления передачи сигнала. Взаимодействие MHC-TCR-CD3 для Т-клеток функционально аналогично взаимодействию антиген(Ag)-иммуноглобулин(Ig)-FcR для миелоидных лейкоцитов и взаимодействию Ag-Ig-CD79 для В-клеток.
Генерация разнообразия TCR аналогична генерации антител и антигенных рецепторов B-клеток . Оно возникает главным образом в результате генетической рекомбинации кодируемых ДНК сегментов в отдельных соматических Т-клетках путем соматической рекомбинации V(D)J с использованием рекомбиназ RAG1 и RAG2 . Однако, в отличие от иммуноглобулинов , гены TCR не подвергаются соматической гипермутации, а Т-клетки не экспрессируют цитидиндезаминазу, индуцированную активацией (AID). Процесс рекомбинации, который создает разнообразие в BCR ( антителах ) и TCR, уникален для лимфоцитов (Т- и В-клеток) на ранних стадиях их развития в первичных лимфоидных органах ( тимус для Т-клеток, костный мозг для В-клеток).
Каждый рекомбинантный TCR обладает уникальной антигенной специфичностью, определяемой структурой антигенсвязывающего сайта , образованного α- и β-цепями в случае αβ-Т-клеток или γ- и δ-цепями в случае γδ-Т-клеток. [14]
Пересечение этих специфических областей (V и J для альфа- или гамма-цепи; V, D и J для бета- или дельта-цепи) соответствует области CDR3, которая важна для распознавания пептида/MHC (см. выше).
Это уникальная комбинация сегментов в этой области, а также палиндромные и случайные добавления нуклеотидов (соответственно называемые «P-» и «N-»), которая объясняет еще большее разнообразие специфичности Т-клеточных рецепторов для процессированных антигенных пептидов. .
Позже во время развития отдельные петли CDR TCR могут быть повторно отредактированы на периферии за пределами тимуса путем реактивации рекомбиназ с использованием процесса, называемого ревизией (редактированием) TCR , и изменить его антигенную специфичность.
В плазматической мембране цепи рецепторов TCR α и β связываются с шестью дополнительными белками-адаптерами, образуя октамерный комплекс. Комплекс содержит как α- и β-цепи, образующие лиганд-связывающий сайт, так и сигнальные модули CD3δ , CD3γ, CD3ε и CD3ζ в стехиометрии TCR αβ - CD3εγ - CD3εδ - CD3ζζ. Заряженные остатки в трансмембранном домене каждой субъединицы образуют полярные взаимодействия, обеспечивающие правильную и стабильную сборку комплекса. [15] Цитоплазматический хвост TCR очень короткий, поэтому белки-адаптеры CD3, содержащие сигнальные мотивы, необходимы для распространения сигнала от запущенного TCR в клетку .
Сигнальные мотивы, участвующие в передаче сигналов TCR, представляют собой остатки тирозина в цитоплазматическом хвосте этих адаптерных белков, которые могут фосфорилироваться в случае связывания TCR-pMHC. Остатки тирозина находятся в определенной аминокислотной последовательности сигнатуры Yxx(L/I)x6-8Yxx(L/I), где Y, L, I обозначают остатки тирозина, лейцина и изолейцина, x обозначает любые аминокислоты, нижний индекс 6-8 обозначает последовательность длиной от 6 до 8 аминокислот. Этот мотив очень распространен в рецепторах-активаторах семейства некаталитических тирозин-фосфорилированных рецепторов (NTR) и называется мотивом активации иммунорецептора на основе тирозина (ITAM). [5] Каждый из CD3δ, CD3γ и CD3ε содержит один ITAM, а CD3ζ содержит три ITAM. Всего в комплекс ТКР входит 10 ИТАМ. [15] Фосфорилированные ITAM действуют как сайт связывания для SH2-доменов дополнительно привлеченных белков.

Каждая Т-клетка экспрессирует клональные TCR, которые распознают специфический пептид, загруженный на молекулу MHC (pMHC), либо на MHC класса II на поверхности антигенпрезентирующих клеток , либо на MHC класса I на любом другом типе клеток. [16] Уникальной особенностью Т-клеток является их способность различать пептиды, полученные из здоровых эндогенных клеток, и пептиды из чужеродных или аномальных (например, инфицированных или раковых) клеток организма. [17] Антигенпрезентирующие клетки не различают собственные и чужеродные пептиды и обычно экспрессируют большое количество собственных pMHC на своей клеточной поверхности и лишь несколько копий любых чужеродных pMHC. Например, клетки, инфицированные ВИЧ, содержат только 8–46 ВИЧ-специфичных пМНС по сравнению со 100 000 общих пМНС на клетку. [18] [19]
Поскольку Т-клетки подвергаются положительной селекции в тимусе, существует немалое сродство между собственным pMHC и TCR. Тем не менее, передача сигналов рецептора Т-клеток не должна активироваться собственным pMHC, так что эндогенные, здоровые клетки игнорируются Т-клетками. Однако, когда эти самые клетки содержат даже незначительное количество pMHC, полученного из патогена, Т-клетки должны активироваться и инициировать иммунные реакции. Способность Т-клеток игнорировать здоровые клетки, но реагировать, когда эти же клетки экспрессируют небольшое количество чужеродных pMHC, известна как дискриминация антигенов. [20] [21]
Для этого Т-клетки обладают очень высокой степенью антигенной специфичности, несмотря на то, что сродство к пептиду/лиганду MHC довольно низкое по сравнению с другими типами рецепторов. [22] Сродство, выраженное как константа диссоциации ( K d ), между TCR и pMHC, было определено с помощью поверхностного плазмонного резонанса (SPR) в диапазоне 1–100 мкМ, со скоростью ассоциации ( k on ) 1000-10000 М -1 с -1 и скорость диссоциации ( k off ) 0,01 -0,1 с -1 . [23] Для сравнения, цитокины имеют сродство KD = 10–600 пМ к своему рецептору. [24] Было показано, что даже изменение одной аминокислоты в представленном пептиде, которое влияет на сродство pMHC к TCR, снижает ответ Т-клеток и не может быть компенсировано более высокой концентрацией pMHC. [25] Наблюдалась отрицательная корреляция между скоростью диссоциации комплекса pMHC-TCR и силой ответа Т-клеток. [26] Это означает, что pMHC, которые связывают TCR в течение более длительного времени, инициируют более сильную активацию Т-клеток. Более того, Т-клетки очень чувствительны; взаимодействия с одним pMHC достаточно, чтобы вызвать активацию. [27] Т-клетки быстро уходят от антигенов, которые не вызывают ответов, быстро сканируя pMHC на антигенпрезентирующей клетке (APC), чтобы увеличить вероятность обнаружения конкретного pMHC. В среднем Т-клетка сталкивается с 20 АПК в час. [28]
Были предложены различные модели молекулярных механизмов, лежащих в основе этого высокоспецифичного и высокочувствительного процесса распознавания антигенов. Профессиональная модель просто предполагает, что ответ TCR пропорционален количеству pMHC, связанного с рецептором. Учитывая эту модель, более короткое время жизни пептида может быть компенсировано более высокой концентрацией, так что максимальный ответ Т-клетки останется прежним. Однако этого нельзя увидеть в экспериментах, и модель была широко отвергнута. [26] Наиболее общепринятой точкой зрения является то, что TCR занимается кинетической корректурой. Модель кинетической корректуры предполагает, что сигнал не создается непосредственно при связывании, а серия промежуточных шагов обеспечивает временную задержку между связыванием и выводом сигнала. Такими промежуточными этапами «корректуры» могут быть несколько циклов фосфорилирования тирозина. Эти шаги требуют энергии и поэтому не происходят спонтанно, а только тогда, когда рецептор связан со своим лигандом. Таким образом, только лиганды с высоким сродством, которые связывают TCR в течение достаточно длительного времени, могут инициировать сигнал. Все промежуточные этапы обратимы: при диссоциации лиганда рецептор возвращается в исходное нефосфорилированное состояние до того, как свяжется новый лиганд. [29] Эта модель предсказывает, что максимальный ответ Т-клеток снижается для pMHC с более коротким сроком жизни. Эксперименты подтвердили эту модель. [26] Однако базовая модель кинетической корректуры требует компромисса между чувствительностью и специфичностью. Увеличение количества шагов корректуры увеличивает специфичность, но снижает чувствительность рецептора. Таким образом, этой модели недостаточно, чтобы объяснить наблюдаемую высокую чувствительность и специфичность TCR. (Алтан Боннет, 2005) Было предложено несколько моделей, расширяющих модель кинетической корректуры, но доказательства существования этих моделей все еще противоречивы. [17] [30] [31]
Чувствительность к антигену выше у Т-клеток, подвергнутых антигену, чем у наивных Т-клеток. Наивные Т-клетки проходят процесс созревания функциональной авидности без изменения аффинности. Он основан на том факте, что эффекторные и память (испытавшие антиген) Т-клетки менее зависят от костимулирующих сигналов и более высокой концентрации антигена, чем наивные Т-клетки. [32]
Основной функцией комплекса TCR является идентификация специфического связанного антигена, полученного из потенциально опасного патогена, и вызывание четкого и критического ответа. В то же время он должен игнорировать любые аутоантигены и толерантно относиться к безвредным антигенам, таким как пищевые антигены. Механизм передачи сигнала, с помощью которого Т-клетка вызывает этот ответ при контакте со своим уникальным антигеном, называется активацией Т-клетки. При связывании с pMHC TCR инициирует сигнальный каскад, включающий активацию фактора транскрипции и ремоделирование цитоскелета, что приводит к активации Т-клеток. Активные Т-клетки секретируют цитокины, быстро пролиферируют, обладают цитотоксической активностью и дифференцируются в эффекторные клетки и клетки памяти. Когда TCR запускается, Т-клетки образуют иммунологический синапс, позволяющий им оставаться в контакте с антигенпрезентирующей клеткой в течение нескольких часов. [33] На популяционном уровне активация Т-клеток зависит от силы стимуляции TCR, кривая доза-реакция лиганда на выработку цитокинов имеет сигмоидальную форму. Однако активация Т-клеток на уровне одной клетки может характеризоваться реакцией, подобной цифровому переключателю, что означает, что Т-клетка полностью активируется, если стимул превышает заданный порог; в противном случае Т-клетка остается в неактивированном состоянии. Промежуточного состояния активации не существует. Устойчивая сигмовидная кривая «доза-эффект» на популяционном уровне является результатом того, что отдельные Т-клетки имеют несколько разные пороговые значения. [25]
Т-клеткам необходимы три сигнала, чтобы полностью активироваться. Сигнал 1 подается рецептором Т-клеток при распознавании специфического антигена на молекуле MHC. Сигнал 2 исходит от костимулирующих рецепторов, таких как CD28 , представленных на поверхности других иммунных клеток. Он выражен только тогда, когда инфекция обнаружена системой врожденного иммунитета, это «сигнал, указывающий на опасность». Эта двухсигнальная система гарантирует, что Т-клетки реагируют только на вредные патогены, а не на аутоантигены. Дополнительный третий сигнал обеспечивается цитокинами , которые регулируют дифференцировку Т-клеток в различные субпопуляции эффекторных Т-клеток. [33] Существует множество молекул, участвующих в сложном биохимическом процессе (называемом трансмембранной передачей сигналов ), посредством которого происходит активация Т-клеток. Ниже сигнальный каскад описан подробно.
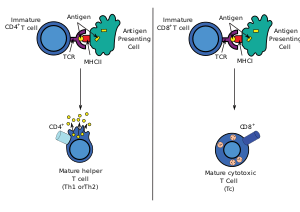
Первоначальный запуск соответствует механизму, общему для всех членов семейства рецепторов NTR . Как только TCR связывается со специфическим pMHC, тирозиновые остатки тирозиновых мотивов активации иммунорецепторов (ITAM) в его адаптерных белках CD3 фосфорилируются. Остатки служат местами стыковки для нижестоящих сигнальных молекул, которые могут распространять сигнал. [34] [35] Фосфорилирование ITAM опосредуется киназой Src Lck . Lck закрепляется на плазматической мембране путем ассоциации с корецептором CD4 или CD8 , в зависимости от подтипа Т-клеток. CD4 экспрессируется на Т-хелперах и регуляторных Т-клетках и специфичен для MHC класса II . С другой стороны, CD8, специфичный для MHC класса I , экспрессируется на цитотоксических Т-клетках . Связывание корецептора с MHC приближает Lck к CD3 ITAM. Было показано, что 40% Lck активны еще до того, как TCR связывает pMHC и, следовательно, обладают способностью постоянно фосфорилировать TCR. [36] Тоническая передача сигналов TCR предотвращается присутствием фосфатазы CD45 , которая удаляет фосфорилирование остатков тирозина и ингибирует инициацию сигнала. При связывании баланс активности киназы и активности фосфатазы нарушается, что приводит к избыточному фосфорилированию и инициации сигнала. Как такое возмущение достигается за счет связывания TCR, все еще обсуждается. Были предложены механизмы , включающие конформационные изменения TCR, агрегацию и кинетическую сегрегацию TCR. [34] Тирозинкиназа Fyn может участвовать в фосфорилировании ITAM, но не является существенной для передачи сигналов TCR. [37] [38]
Фосфорилированные ITAM в цитоплазматических хвостах CD3 рекрутируют протеинтирозинкиназу Zap70 , которая может связываться с фосфорилированными остатками тирозина с помощью своего домена SH2 . Это приближает Zap70 к Lck, что приводит к его фосфорилированию и активации с помощью Lck. [39] Lck фосфорилирует ряд различных белков пути TCR. [40] После активации Zap70 способен фосфорилировать несколько остатков тирозина трансмембранного белка LAT . LAT представляет собой каркасный белок , связанный с мембраной. Сам по себе он не обладает никакой каталитической активностью, но обеспечивает сайты связывания для сигнальных молекул через фосфорилированные остатки тирозина. LAT связывается с другим каркасным белком Slp-76 через адаптерный белок Grap2 , который обеспечивает дополнительные сайты связывания. Вместе LAT и Slp-76 обеспечивают платформу для рекрутирования многих нижестоящих сигнальных молекул. Приблизив эти сигнальные молекулы в непосредственной близости, они затем могут быть активированы киназами Lck, Zap70 и другими. Следовательно, комплекс LAT/Slp76 действует как высококооперативная сигналосома. [39]
Молекулы, которые связывают комплекс LAT/Slp76, включают: фосфолипазу C γ1 (PLCγ1), SOS через адаптер Grb2 , Itk , Vav , Nck1 и Fyb . [39]
PLCγ является очень важным ферментом в этом пути, поскольку он генерирует молекулы вторичного мессенджера . Он активируется тирозинкиназой Itk, которая рекрутируется на клеточную мембрану путем связывания с фосфатидилинозитол (3,4,5)-трифосфатом (PIP3). PIP3 вырабатывается под действием фосфоинозитид-3-киназы (PI-3K), которая фосфорилирует фосфатидилинозитол-4,5-бисфосфат (PIP2) с образованием PIP3. Неизвестно, активируется ли PI-3K самим рецептором Т-клеток, но есть свидетельства того, что CD28, костимулирующий рецептор, обеспечивающий второй сигнал, способен активировать PI-3K. Взаимодействие между PLCγ, Itk и PI-3K может быть точкой пути, где объединяются первый и второй сигналы. Только если присутствуют оба сигнала, PLCγ активируется. [33] Как только PLCγ активируется фосфорилированием. Он гидролизует PIP2 на две вторичные молекулы-мессенджеры, а именно мембраносвязанный диацилглицерин (DAG) и растворимый инозитол-1,4,5-трифосфат (IP3). [41]
Эти молекулы второго мессенджера усиливают сигнал TCR и распространяют предыдущую локализованную активацию на всю клетку и активируют белковые каскады, которые в конечном итоге приводят к активации факторов транскрипции . Факторами транскрипции, участвующими в сигнальном пути Т-клеток, являются NFAT , NF-κB и AP1 , гетеродимер белков Fos и Jun . Все три транскрипционных фактора необходимы для активации транскрипции гена интерлейкина-2 (IL2). [33]
Активация NFAT зависит от передачи сигналов кальция . IP3, продуцируемый PLC-γ, больше не связан с мембраной и быстро диффундирует в клетке. Связывание IP3 с рецепторами кальциевых каналов эндоплазматического ретикулума (ER) индуцирует высвобождение кальция (Ca 2+ ) в цитозоль. Возникающая в результате низкая концентрация Ca 2+ в ЭР вызывает кластеризацию STIM1 на мембране ЭР, что, в свою очередь, приводит к активации каналов CRAC клеточной мембраны , что позволяет дополнительному кальцию поступать в цитозоль из внеклеточного пространства. Следовательно, уровни Ca 2+ сильно повышаются в Т-клетках. Этот цитозольный кальций связывает кальмодулин , вызывая конформационные изменения белка, так что он может затем связывать и активировать кальциневрин . Кальцинеурин, в свою очередь, дефосфорилирует NFAT. В деактивированном состоянии NFAT не может проникнуть в ядро , поскольку его последовательность ядерной локализации (NLS) не может распознаваться ядерными переносчиками из-за фосфорилирования с помощью GSK-3 . При дефосфорилировании кальциневрином возможна транслокация NFAT в ядро. [33] Кроме того, есть доказательства того, что PI-3K через сигнальные молекулы рекрутирует протеинкиназу AKT на клеточную мембрану. AKT способна деактивировать GSK3 и тем самым ингибировать фосфорилирование NFAT, что может способствовать активации NFAT. [39]
Активация NF-κB инициируется DAG, вторым мембраносвязанным продуктом PLCγ-гидролиза PIP2. DAG связывает и рекрутирует протеинкиназу C θ (PKCθ) к мембране, где она может активировать мембраносвязанный каркасный белок CARMA1 . Затем CARMA1 претерпевает конформационные изменения, которые позволяют ему олигомеризоваться и связываться с адаптерными белками BCL10 , доменом CARD и MALT1 . Этот мультисубъединичный комплекс связывает убиквитинлигазу TRAF6 . Убиквитинирование TRAF6 служит каркасом для рекрутирования NEMO , киназы IκB (IKK) и TAK1 . [33] TAK 1 фосфорилирует IKK, который, в свою очередь, фосфорилирует ингибитор NF-κB I-κB , что приводит к убиквитинированию и последующей деградации I-κB. I-κB блокирует NLS NF-κB, тем самым предотвращая его транслокацию в ядро. Как только I-κB разрушается, он не может связываться с NF-κB, и NLS NF-κB становится доступным для ядерной транслокации. [33]
Активация AP1 включает три сигнальных пути MAPK . Этот путь использует каскад фосфорилирования трех последовательно действующих протеинкиназ для передачи сигнала. Три пути MAPK в Т-клетках включают киназы различной специфичности, принадлежащие каждому из семейств MAP3K , MAP2K , MAPK . Первоначальная активация осуществляется ГТФазой Ras или Rac , которая фосфорилирует MAP3K. [33] Каскад с участием ферментов Raf , MEK1 , ERK приводит к фосфорилированию Jun, конформационные изменения позволяют Jun связываться с Fos и, следовательно, образовывать AP-1. AP-1 затем действует как фактор транскрипции. Раф активируется через второй мессенджер DAG, SOS и Ras. DAG привлекает к мембране, среди других белков, белок, высвобождающий гуанилнуклеотиды RAS ( RasGRP ), фактор обмена гуаниновых нуклеотидов (GEF). RasGRP активирует малую ГТФазу Ras путем замены гуанозиндифосфата (GDP), связанного с Ras, на гуанозинтрифосфат (GTP). Ras также может быть активирован фактором обмена гуаниновых нуклеотидов SOS, который связывается с сигналосомой LAT. Затем Ras инициирует каскад MAPK. [39] Второй каскад MAPK с MEKK1 , JNKK, JNK индуцирует экспрессию белка Jun. Другой каскад, также вовлекающий MEKK1 в качестве MAPK3, но затем активирующий MKK3 /6 и p38 , индуцирует транскрипцию Fos. Активация MEKK1, помимо активации Ras, включает в себя Slp-76, привлекающий GEF Vav к сигналосоме LAT, которая затем активирует GTPase Rac. Rac и Ras активируют MEKK1 и тем самым инициируют каскад MAPK. [39]