Toll-подобные рецепторы ( TLR ) представляют собой класс белков , которые играют ключевую роль во врожденной иммунной системе . Это однопролетные рецепторы , обычно экспрессируемые на сторожевых клетках, таких как макрофаги и дендритные клетки , которые распознают структурно консервативные молекулы, полученные из микробов . Как только эти микробы достигают физических барьеров, таких как кожа или слизистая оболочка кишечного тракта , они распознаются TLR, которые активируют реакцию иммунных клеток . TLR включают TLR1 , TLR2 , TLR3 , TLR4 , TLR5 , TLR6 , TLR7 , TLR8 , TLR9 , TLR10 , TLR11 , TLR12 и TLR13. У людей отсутствуют гены TLR11, TLR12 и TLR13 [1] , а у мышей отсутствует функциональный ген TLR10. [2] Рецепторы TLR1, TLR2, TLR4, TLR5, TLR6 и TLR10 расположены на клеточной мембране , тогда как TLR3, TLR7, TLR8 и TLR9 расположены во внутриклеточных везикулах (поскольку они являются сенсорами нуклеиновых кислот ). [3]
TLR получили свое название из-за сходства с белком, кодируемым геном toll . [4]
Способность иммунной системы распознавать молекулы , которые широко распространены среди патогенов , отчасти обусловлена наличием иммунных рецепторов , называемых толл-подобными рецепторами (TLR), которые экспрессируются на мембранах лейкоцитов, включая дендритные клетки , макрофаги , природные клетки-киллеры , клетки адаптивного иммунитета Т-клетки и В-клетки , а также неиммунные клетки ( эпителиальные и эндотелиальные клетки и фибробласты ). [5]
Связывание лигандов - либо в форме адъюванта, используемого при вакцинации , либо в форме инвазивных фрагментов во время естественной инфекции - с TLR отмечает ключевые молекулярные события, которые в конечном итоге приводят к врожденным иммунным ответам и развитию антигенспецифических приобретенных иммунитет. [6] [7]
После активации TLR рекрутируют адаптерные белки (белки, которые опосредуют другие белок-белковые взаимодействия) в цитозоле иммунной клетки для распространения антиген-индуцированного пути передачи сигнала . Эти рекрутированные белки затем отвечают за последующую активацию других нижестоящих белков, включая протеинкиназы (IKKi, IRAK1 , IRAK4 и TBK1 ), которые дополнительно усиливают сигнал и в конечном итоге приводят к активации или подавлению генов , которые управляют воспалительными реакциями и другими транскрипционными реакциями. события. Некоторые из этих событий приводят к выработке, пролиферации и выживанию цитокинов , тогда как другие приводят к усилению адаптивного иммунитета. [7] Если лиганд является бактериальным фактором, патоген может быть фагоцитирован и переварен, а его антигены представлены CD4+ Т-клеткам . В случае вирусного фактора инфицированная клетка может прекратить синтез белка и подвергнуться запрограммированной гибели клеток ( апоптоз ). Иммунные клетки, обнаружившие вирус, также могут выделять противовирусные факторы, такие как интерфероны .
Также было показано, что Toll-подобные рецепторы являются важным связующим звеном между врожденным и адаптивным иммунитетом благодаря их присутствию в дендритных клетках . [8] Флагеллин , лиганд TLR5, индуцирует секрецию цитокинов при взаимодействии с TLR5 на Т-клетках человека. [8]

TLR представляют собой тип рецептора распознавания образов (PRR) и распознают молекулы, которые в целом являются общими для патогенов , но отличаются от молекул хозяина, что в совокупности называется молекулярными паттернами, связанными с патогенами (PAMP). Помимо распознавания экзогенных PAMP, TLR могут также связываться с эндогенными молекулярными структурами, связанными с повреждением (DAMP), такими как белки теплового шока (HSP) или компоненты плазматической мембраны. [9] TLR вместе с рецепторами интерлейкина-1 образуют суперсемейство рецепторов , известное как «суперсемейство рецепторов интерлейкина-1/толл-подобных рецепторов»; все члены этого семейства имеют общий так называемый домен TIR (рецептор toll-IL-1).
Существуют три подгруппы доменов TIR. Белки с TIR-доменами подгруппы 1 являются рецепторами интерлейкинов , которые продуцируются макрофагами , моноцитами и дендритными клетками , и все они имеют внеклеточные домены иммуноглобулина (Ig). Белки с TIR-доменами подгруппы 2 представляют собой классические TLR и прямо или косвенно связываются с молекулами микробного происхождения. Третья подгруппа белков, содержащих TIR-домены, состоит из адаптерных белков , которые являются исключительно цитозольными и опосредуют передачу сигналов от белков подгрупп 1 и 2.
TLRs присутствуют как у позвоночных , так и у беспозвоночных . Молекулярные строительные блоки TLR представлены в бактериях и растениях, а рецепторы распознавания образов растений, как хорошо известно, необходимы для защиты хозяина от инфекции. Таким образом, TLRs являются одним из самых древних и консервативных компонентов иммунной системы .
В последние годы TLR были идентифицированы и в нервной системе млекопитающих. Члены семейства TLR были обнаружены в глии, нейронах и нейрональных клетках-предшественниках, в которых они регулируют решение клеточной судьбы. [10]
Было подсчитано, что большинство видов млекопитающих имеют от десяти до пятнадцати типов толл-подобных рецепторов. Тринадцать TLR (названных просто от TLR1 до TLR13) были идентифицированы вместе у людей и мышей, а эквивалентные формы многих из них были обнаружены у других видов млекопитающих. [11] [12] [13] Однако эквиваленты некоторых TLR, обнаруженные у человека, присутствуют не у всех млекопитающих. Например, ген, кодирующий белок, аналогичный TLR10 у людей, присутствует у мышей , но, по-видимому, в какой-то момент в прошлом он был поврежден ретровирусом . С другой стороны, мыши экспрессируют TLR 11, 12 и 13, ни один из которых не представлен у человека. Другие млекопитающие могут экспрессировать TLR, которых нет у человека. Другие виды, не относящиеся к млекопитающим, могут иметь TLR, отличные от млекопитающих, о чем свидетельствует TLR14, направленный против клеточной стенки, который обнаружен у рыбы-фугу Такифугу . [14] Это может усложнить процесс использования экспериментальных животных в качестве моделей врожденного иммунитета человека.
TLR позвоночных делятся по сходству на семейства TLR 1/2/6/10/14/15, TLR 3, TLR 4, TLR 5, TLR 7/8/9 и TLR 11/12/13/16/21. /22/23. [14]

Участие toll-сигналов в иммунитете было впервые продемонстрировано на плодовой мушке Drosophila melanogaster . [19] У плодовых мушек есть только врожденные иммунные реакции, что позволяет исследованиям избежать вмешательства адаптивных иммунных механизмов в передачу сигнала. Реакция мух на грибковую или бактериальную инфекцию происходит через два отдельных сигнальных каскада, один из которых представляет собой путь платных сигналов, а другой — путь иммунодефицита . Путь toll подобен передаче сигналов TLR млекопитающих, но в отличие от TLR млекопитающих, toll не активируется непосредственно патоген-ассоциированными молекулярными паттернами ( PAMPs ). Его рецепторный эктодомен распознает расщепленную форму цитокина spätzle, который секретируется в гемолимфе как неактивный димерный предшественник. Toll-рецептор разделяет цитоплазматический домен TIR с TLR млекопитающих, но эктодомен и внутрицитоплазматический хвост различны. Это различие может отражать функцию этих рецепторов как цитокиновых рецепторов, а не PRR .
Путь оплаты активируется различными стимулами, такими как грамположительные бактерии , грибы и факторы вирулентности . [17] [20] Во-первых, процессирующий фермент Spätzle (SPE) активируется в ответ на инфекцию и расщепляет spätzle ( spz ). Расщепленный spätzle затем связывается с платным рецептором и сшивает его эктодомены. Это запускает конформационные изменения в рецепторе, приводящие к передаче сигналов через toll. С этого момента сигнальный каскад очень похож на передачу сигналов млекопитающих через TLR. Toll-индуцированный сигнальный комплекс (TICS) состоит из MyD88 , Tube и Pelle (ортолога IRAK млекопитающих). Сигнал от TICS затем передается в Cactus (гомолог IκB млекопитающих ), фосфорилированный Cactus полиубиквитилируется и деградирует, обеспечивая ядерную транслокацию DIF (дорсальный фактор иммунитета; гомолог NF-κB млекопитающих ) и индукцию транскрипции генов антимикробного действия. пептиды (AMP), такие как дрозомицин . [21]
У дрозофилы всего 9 генов семейства toll и 6 генов семейства spz , которые в разной степени взаимодействуют друг с другом. [22]
TLR2 также обозначают как CD282 (кластер дифференцировки 282).
TLR3 не использует MyD88-зависимый путь. Его лигандом является ретровирусная двухцепочечная РНК ( дсРНК ), которая активирует TRIF- зависимый сигнальный путь. Чтобы изучить роль этого пути в ретровирусном перепрограммировании, были разработаны методы нокдауна TLR3 или TRIF, и результаты показали, что только путь TLR3 необходим для полной индукции экспрессии целевого гена вектором экспрессии ретровируса. Эта ретровирусная экспрессия четырех транскрипционных факторов ( Oct4 , Sox2 , Klf4 и c-Myc ; OSKM) индуцирует плюрипотентность в соматических клетках. Это подтверждается исследованием, которое показывает, что эффективность и количество генерации ИПСК человека с использованием ретровирусных векторов снижаются при нокдауне этого пути пептидными ингибиторами или нокдауне shRNA TLR3 или его адаптерного белка TRIF. В совокупности стимуляция TLR3 вызывает большие изменения в ремоделировании хроматина и ядерном перепрограммировании, и для этих изменений необходима активация воспалительных путей, индукция генов плюрипотентности и создание колоний индуцированных человеком плюрипотентных стволовых клеток (ИПСК). [23]
Как отмечалось выше, клетки человека не экспрессируют TLR11 , а клетки мыши — экспрессируют. TLR11, специфичный для мышей, распознает уропатогенную E.coli и апикомплексного паразита Toxoplasma gondii . У токсоплазмы его лигандом является белок профилин, а у E. coli — флагеллин . Флагеллин энтеропатогена Salmonella также распознается TLR11. [24]
Поскольку мышиный TLR11 способен эффективно распознавать сальмонеллу , нормальные мыши не заражаются пероральной сальмонеллой Typhi , которая вызывает у людей пищевой и водный гастроэнтерит и брюшной тиф . С другой стороны, мыши с нокаутом TLR11 эффективно заражаются. В результате эта нокаутная мышь может служить моделью брюшного тифа человека. [25]
Толл-подобные рецепторы связываются и активируются разными лигандами, которые, в свою очередь, расположены на разных типах организмов или структур. Они также имеют различные адаптеры, реагирующие на активацию, и располагаются иногда на поверхности клетки, а иногда и во внутренних отсеках клетки . Кроме того, они экспрессируются различными типами лейкоцитов или другими типами клеток :

Из-за специфичности толл-подобных рецепторов (и других рецепторов врожденного иммунитета) их нелегко изменить в ходе эволюции, эти рецепторы распознают молекулы, которые постоянно связаны с угрозами (т. е. с патогеном или клеточным стрессом) и высокоспецифичны для эти угрозы (т.е. их нельзя спутать с собственными молекулами, которые обычно экспрессируются в физиологических условиях). Считается, что ассоциированные с патогеном молекулы, отвечающие этому требованию, имеют решающее значение для функции патогена и их трудно изменить путем мутации; Говорят, что они эволюционно консервативны. Несколько консервативные свойства патогенов включают липополисахариды бактериальной клеточной поверхности (ЛПС), липопротеины , липопептиды и липоарабиноманнан ; белки, такие как флагеллин бактериальных жгутиков ; двухцепочечная РНК вирусов; или неметилированные CpG -островки бактериальной и вирусной ДНК ; а также CpG-островков, обнаруженных в промоторах эукариотической ДНК; а также некоторые другие молекулы РНК и ДНК. Поскольку лиганды TLR присутствуют в большинстве патогенов, они также могут присутствовать в вакцинах, полученных из патогенов (например, вакцинах против MMR, гриппа, полиомиелита). Большинство коммерчески доступных вакцин были оценены на предмет присущей им способности лигандов TLR активировать отдельные подгруппы иммунных клеток. [45] [46] Для большинства TLR специфичность распознавания лигандов теперь установлена с помощью генного нацеливания (также известного как «нокаут гена»): метода, с помощью которого отдельные гены могут быть избирательно удалены у мышей. [47] [48] В таблице выше приведен обзор известных лигандов TLR.
Стереотипная воспалительная реакция, вызванная активацией толл-подобных рецепторов, привела к предположению, что эндогенные активаторы толл-подобных рецепторов могут участвовать в аутоиммунных заболеваниях. Предполагается, что TLR связываются с молекулами хозяина, включая фибриноген (участвующий в свертывании крови ), белки теплового шока (HSP), HMGB1 , компоненты внеклеточного матрикса и собственную ДНК (обычно она разрушается нуклеазами, но при воспалительных и аутоиммунных состояниях может образовывать комплекс с эндогенными белками, становятся устойчивыми к этим нуклеазам и получают доступ к эндосомальным TLRs как TLR7 или TLR9). Эти эндогенные лиганды обычно образуются в результате нефизиологической гибели клеток. [49]
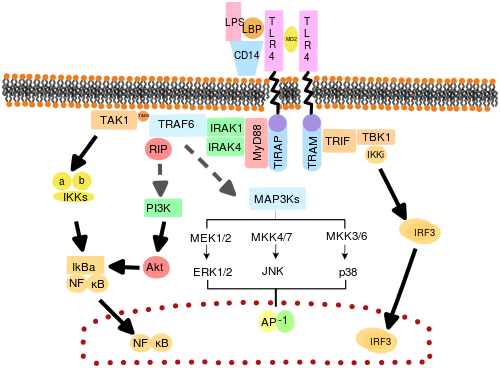
Считается, что TLR функционируют как димеры . Хотя большинство TLR, по-видимому, функционируют как гомодимеры , TLR2 образует гетеродимеры с TLR1 или TLR6, причем каждый димер имеет разную лигандную специфичность. TLRs также могут зависеть от других корецепторов для обеспечения полной чувствительности к лигандам, например, в случае распознавания TLR4 LPS , для которого требуется MD-2. Известно, что CD14 и LPS-связывающий белок ( LBP ) облегчают презентацию LPS MD-2.
Набор эндосомальных TLR, включающий TLR3, TLR7, TLR8 и TLR9, распознает нуклеиновую кислоту , полученную из вирусов, а также эндогенные нуклеиновые кислоты в контексте патогенных событий. Активация этих рецепторов приводит к выработке воспалительных цитокинов , а также интерферонов типа I ( интерферон типа I ), которые помогают бороться с вирусной инфекцией.
Также были нацелены на адаптерные белки и киназы, которые опосредуют передачу сигналов TLR. Кроме того, для расшифровки сигнальных путей TLR использовался случайный мутагенез зародышевой линии с помощью ENU . При активации TLR рекрутируют адаптерные молекулы в цитоплазме клеток для распространения сигнала. Известно, что в передаче сигнала участвуют четыре адаптерные молекулы. Эти белки известны как MyD88 , TIRAP (также называемый Mal), TRIF и TRAM (адаптерная молекула, связанная с TRIF). [50] [51] [52]
Передача сигналов TLR разделена на два отдельных сигнальных пути: MyD88-зависимый и TRIF-зависимый путь.
MyD88-зависимый ответ возникает при димеризации TLR и используется всеми TLR, кроме TLR3. Его основным эффектом является активация NFκB и митоген-активируемой протеинкиназы . Связывание лиганда и конформационные изменения, происходящие в рецепторе, привлекают адаптерный белок MyD88, член семейства TIR . Затем MyD88 задействует IRAK4 , IRAK1 и IRAK2 . Затем киназы IRAK фосфорилируют и активируют белок TRAF6 , который, в свою очередь, полиубиквинирует белок TAK1, а также сам по себе, чтобы облегчить связывание с IKK-β . При связывании TAK1 фосфорилирует IKK-β, который затем фосфорилирует IκB, вызывая его деградацию и позволяя NFκB диффундировать в ядро клетки и активировать транскрипцию и, как следствие, индукцию воспалительных цитокинов. [49]
И TLR3, и TLR4 используют TRIF-зависимый путь, который запускается дцРНК и ЛПС соответственно. Для TLR3 дсРНК приводит к активации рецептора, рекрутируя адаптер TRIF . TRIF активирует киназы TBK1 и RIPK1 , что создает ветвь сигнального пути. Сигнальный комплекс TRIF/TBK1 фосфорилирует IRF3, обеспечивая его транслокацию в ядро и продукцию интерферона типа I. Между тем, активация RIPK1 вызывает полиубиквитинирование и активацию транскрипции TAK1 и NFκB таким же образом, как и MyD88-зависимый путь. [49]
Передача сигналов TLR в конечном итоге приводит к индукции или подавлению генов, которые управляют воспалительной реакцией. В целом тысячи генов активируются посредством передачи сигналов TLR, и в совокупности TLRs представляют собой один из наиболее плейотропных , но жестко регулируемых шлюзов для генной модуляции.
TLR4 — единственный TLR, использующий все четыре адаптера. Комплекс, состоящий из TLR4, MD2 и LPS, рекрутирует адаптеры, содержащие домен TIRAP, TIRAP и MyD88 и, таким образом, инициирует активацию NFκB (ранняя фаза) и MAPK. Комплекс TLR4-MD2-LPS затем подвергается эндоцитозу и в эндосоме образует сигнальный комплекс с адаптерами TRAM и TRIF. Этот TRIF-зависимый путь снова приводит к активации IRF3 и выработке интерферонов типа I, но он также активирует позднюю фазу активации NFκB. Для продукции воспалительных цитокинов необходима как поздняя, так и ранняя фаза активации NFκB. [49]
Имиквимод (широко используемый в дерматологии ) является агонистом TLR7, а его преемник резиквимод — агонистом TLR7 и TLR8. [53] Недавно резиквимод был исследован в качестве агента для иммунотерапии рака, [54] действуя посредством стимуляции опухолеассоциированных макрофагов.
Несколько лигандов TLR находятся в клинической разработке или тестируются на животных моделях в качестве вакцинных адъювантов [55] , причем в 2017 году было впервые клиническое применение у людей в рекомбинантной вакцине против опоясывающего герпеса , которая содержит компонент монофосфориллипида А.
Сообщалось об уровнях экспрессии информационной РНК TLR7 у молочных животных при естественной вспышке ящура. [56]
Было показано, что TLR4 важен для долгосрочных побочных эффектов опиоидов . Его активация приводит к высвобождению модуляторов воспаления, включая TNF-α и IL-1β , и считается, что постоянное высвобождение этих модуляторов на низком уровне со временем снижает эффективность лечения опиоидными препаратами и участвует в толерантности к опиоидам [57] . [58] гипералгезия и аллодиния . [59] [60] Морфин-индуцированная активация TLR4 ослабляет подавление боли опиоидами и усиливает развитие толерантности к опиоидам и зависимости , злоупотребления наркотиками и других негативных побочных эффектов, таких как угнетение дыхания и гипералгезия. [61] Было показано, что препараты, блокирующие действие TNF-α или IL-1β, усиливают обезболивающее действие опиоидов и уменьшают развитие толерантности и других побочных эффектов, [62] [63] и это также было продемонстрировано. с препаратами, которые блокируют сам TLR4.
«Неестественные» энантиомеры опиоидных препаратов, таких как (+)-морфин и (+)-налоксон, не имеют сродства к опиоидным рецепторам, но по-прежнему производят ту же активность в отношении TLR4, что и их «нормальные» энантиомеры. [64] [65] Так, «неприродные» энтианомеры опиоидов, такие как (+)-налоксон, могут быть использованы для блокирования активности TLR4 опиоидных анальгетиков, не имея при этом никакого сродства к μ-опиоидному рецептору [66] [65] [ 67]
Когда микробы были впервые признаны причиной инфекционных заболеваний, сразу стало ясно, что многоклеточные организмы должны быть способны распознавать их при заражении и, следовательно, способны распознавать молекулы, уникальные для микробов. Большой объем литературы, охватывающий большую часть прошлого столетия, свидетельствует о поиске ключевых молекул и их рецепторов. Более 100 лет назад Ричард Пфайффер , ученик Роберта Коха , ввёл термин « эндотоксин » для описания вещества, вырабатываемого грамотрицательными бактериями , которое могло провоцировать лихорадку и шок у экспериментальных животных . В последующие десятилетия эндотоксин был химически охарактеризован и идентифицирован как липополисахарид (ЛПС), продуцируемый большинством грамотрицательных бактерий. Этот липополисахарид является неотъемлемой частью мембраны грамотрицательных бактерий и высвобождается при разрушении бактерии. Было показано , что другие молекулы (бактериальные липопептиды , флагеллин и неметилированная ДНК ), в свою очередь, провоцируют реакции хозяина, которые обычно являются защитными. Однако эти реакции могут быть вредными, если они чрезмерно продолжительны или интенсивны. Логически отсюда следовало, что должны существовать рецепторы для таких молекул, способные предупредить хозяина о наличии инфекции, но они оставались неуловимыми в течение многих лет. Толл-подобные рецепторы теперь считаются одними из ключевых молекул, которые предупреждают иммунную систему о наличии микробных инфекций.
Прототипический член семейства, толл- рецептор ( P08953 ; Tl) у плодовой мухи Drosophila melanogaster , был открыт в 1985 году лауреатами Нобелевской премии 1995 года Кристианой Нюсляйн-Фольхард и Эриком Вишаусом и их коллегами. Он был известен своей функцией развития в эмбриогенезе путем установления дорсально - вентральной оси. Он был назван в честь восклицания Кристианы Нюсляйн-Фольхард в 1985 году: « Das ist ja toll! » («Это потрясающе!»), В отношении недоразвитой брюшной части личинки плодовой мухи. [4] Он был клонирован в лаборатории Кэтрин Андерсон в 1988 году. [68] В 1996 году Жюль А. Хоффманн и его коллеги обнаружили, что толль играет важную роль в иммунитете мухи к грибковой инфекции , чего он достигает путем активации синтез антимикробных пептидов. [19]
Первый известный человеческий толл-подобный рецептор был описан Номурой и его коллегами в 1994 году, [69] картирован на хромосоме Тагучи и его коллегами в 1996 году. [70] Поскольку иммунная функция toll у дрозофилы тогда не была известна, предполагалось, что что TIL (теперь известный как TLR1) может участвовать в развитии млекопитающих. Однако в 1991 г. (до открытия TIL) было обнаружено, что молекула, играющая явную роль в иммунной функции млекопитающих, рецептор интерлейкина-1 (IL-1), также имеет гомологию с toll дрозофилы; цитоплазматические части обеих молекул были сходны. [71]
В 1997 году Чарльз Джейнвей и Руслан Меджитов показали, что толл-подобный рецептор, ныне известный как TLR4, может при искусственном лигировании с помощью антител вызывать активацию определенных генов, необходимых для инициации адаптивного иммунного ответа . [7] Функция TLR 4 как рецептора, воспринимающего ЛПС, была обнаружена Брюсом А. Бейтлером и его коллегами. [72] Эти исследователи использовали позиционное клонирование, чтобы доказать, что мыши, которые не могли реагировать на ЛПС, имели мутации, которые нарушали функцию TLR4. Это идентифицировало TLR4 как один из ключевых компонентов рецептора ЛПС.

В свою очередь, другие гены TLR были удалены у мышей путем генного таргетинга, в основном в лаборатории Шизуо Акиры и его коллег. В настоящее время считается, что каждый TLR обнаруживает дискретный набор молекул (некоторые из которых имеют микробное происхождение, а некоторые являются продуктами повреждения клеток) и сигнализирует о наличии инфекций. [73]
Растительные гомологи toll были открыты Памелой Рональд в 1995 г. (рис XA21) [74] и Томасом Боллером в 2000 г. ( Arabidopsis FLS2). [75]
В 2011 году Бойтлер и Хоффманн были удостоены Нобелевской премии по медицине и физиологии за свою работу. [76] Хоффманн и Акира получили Международную премию Канады Гайрднера в 2011 году. [77]
{{cite journal}}: CS1 maint: местоположение ( ссылка )