Проточная цитометрия ( FC ) — это метод, используемый для обнаружения и измерения физических и химических характеристик популяции клеток или частиц. [1] [2] [3] [4]
В этом процессе образец, содержащий клетки или частицы, суспендируется в жидкости и вводится в проточный цитометр . Образец фокусируется так, чтобы в идеале проходить по одной клетке через лазерный луч, где рассеянный свет характерен для клеток и их компонентов. Клетки часто метят флуоресцентными маркерами, поэтому свет поглощается, а затем излучается в определенном диапазоне длин волн. Можно быстро исследовать десятки тысяч клеток, а собранные данные обрабатываются компьютером. [5]
Проточная цитометрия обычно используется в фундаментальных исследованиях, клинической практике и клинических испытаниях . Применение проточной цитометрии включает:
Анализатор проточной цитометрии — это прибор, который предоставляет количественные данные из образца. Другие инструменты, использующие проточную цитометрию, включают сортировщики клеток, которые физически разделяют и тем самым очищают интересующие клетки на основе их оптических свойств.
Первое устройство проточной цитометрии на основе импеданса , использующее принцип Коултера , было раскрыто в патенте США № 2656508, выданном в 1953 году Уоллесу Х. Коултеру . Мак Фулвайлер был изобретателем предшественника современных проточных цитометров, в частности, сортировщика клеток. [6] Фулвайлер разработал это в 1965 году в своей публикации в журнале Science . [7] Первое устройство проточной цитометрии на основе флуоресценции (ICP 11) было разработано в 1968 году Вольфгангом Гёде из Мюнстерского университета , заявка на патент была подана 18 декабря 1968 года [8] и впервые коммерциализирована в 1968/69 году немецким разработчиком и производителем. Partec через Phywe AG в Геттингене . В то время другие ученые все еще предпочитали методы абсорбции методам флуоресценции . [9] Вскоре после этого были разработаны инструменты проточной цитометрии, в том числе цитофлюорограф (1971) от Bio/Physics Systems Inc. (позже: Ortho Diagnostics), PAS 8000 (1973) от Partec, первый FACS (сортировка клеток, активируемая флуоресценцией). ) инструмент от Becton Dickinson (1974), ICP 22 (1975) от Partec/Phywe и Epics от Coulter (1977/78). Первый высокочастотный импедансный проточный цитометр без меток , основанный на запатентованной микрофлюидной «лаборатории на чипе» Ampha Z30, был представлен компанией Amphasys (2012). [ нужна цитата ]
Первоначальное название технологии проточной цитометрии на основе флуоресценции было «импульсная цитофотометрия» ( нем . Impulszytophotometrie ), основанное на первой патентной заявке на проточную цитометрию на основе флуоресценции. На 5-й конференции Американского инженерного фонда по автоматизированной цитологии в Пенсаколе (Флорида) в 1976 году – через восемь лет после появления первого проточного цитометра на основе флуоресценции (1968) – было решено широко использовать название «проточная цитометрия», термин это быстро стало популярным. [10]
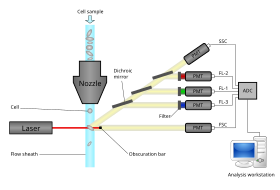
Современные проточные цитометры способны анализировать многие тысячи частиц в секунду в «реальном времени» и, если они настроены как сортировщики клеток, могут активно разделять и изолировать частицы с заданными оптическими свойствами с одинаковой скоростью. Проточный цитометр похож на микроскоп , за исключением того, что вместо получения изображения клетки проточная цитометрия предлагает высокопроизводительную автоматическую количественную оценку определенных оптических параметров для каждой клетки. Для анализа твердых тканей сначала необходимо приготовить одноклеточную суспензию. [ нужна цитата ]
Проточный цитометр состоит из пяти основных компонентов: проточной кюветы, измерительной системы, детектора, системы амплификации и компьютера для анализа сигналов. Проточная ячейка имеет поток жидкости (оболочечная жидкость), который переносит и выравнивает клетки так, что они проходят по одному ряду через световой луч для измерения. В качестве измерительной системы обычно используются измерения импеданса (или проводимости) и оптические системы — лампы ( ртутные , ксеноновые ); мощные лазеры с водяным охлаждением ( аргоновые , криптоновые , лазеры на красителях); маломощные лазеры с воздушным охлаждением (аргоновые (488 нм), красные-HeNe (633 нм), зеленые-HeNe, HeCd (УФ)); диодные лазеры (синий, зеленый, красный, фиолетовый), дающие световые сигналы. Детектор и система аналого-цифрового преобразования (АЦП) преобразуют аналоговые измерения прямого рассеянного света (FSC) и бокового рассеянного света (SSC), а также сигналы флуоресценции, специфичные для красителей, в цифровые сигналы, которые могут быть обработаны компьютером. . Система усиления может быть линейной или логарифмической . [ нужна цитата ]
Процесс сбора данных из образцов с помощью проточного цитометра называется «сбором». Сбор данных осуществляется с помощью компьютера, физически подключенного к проточному цитометру, и программного обеспечения, которое обеспечивает цифровой интерфейс с цитометром. Программное обеспечение способно регулировать параметры (например, напряжение, компенсацию) для тестируемого образца, а также помогает отображать исходную информацию о образце при получении данных об образце, чтобы гарантировать правильность установки параметров. Первые проточные цитометры были, как правило, экспериментальными устройствами, но технологические достижения позволили широко использовать их в различных клинических и исследовательских целях. Благодаря этим разработкам возник значительный рынок приборов, программного обеспечения для анализа, а также реагентов, используемых для сбора данных, таких как флуоресцентно меченные антитела .
Современные инструменты обычно имеют несколько лазеров и детекторов флуоресценции. Текущий рекорд для коммерческого прибора — десять лазеров [11] и 30 детекторов флуоресценции. [12] Увеличение количества лазеров и детекторов позволяет маркировать несколько антител и более точно идентифицировать целевую популяцию по фенотипическим маркерам. Некоторые инструменты могут даже делать цифровые изображения отдельных клеток, что позволяет анализировать расположение флуоресцентного сигнала внутри или на поверхности клеток. [ нужна цитата ]
Клетки должны равномерно проходить через центр сфокусированных лазерных лучей, чтобы точно измерить оптические свойства клеток в любом проточном цитометре. [13] [14] [15] Целью жидкостной системы является перемещение клеток одна за другой через луч лазера и по всему инструменту. Жидкостная система в проточном цитометре с возможностью сортировки клеток также использует поток для переноса отсортированных клеток в пробирки или лунки для сбора. [13]
Для точного позиционирования клеток в струе жидкости в большинстве цитометров используется гидродинамическая фокусировка. [13] [14] Клетки в суспензии попадают в инструмент, окруженный внешней оболочкой жидкости. Керн образца удерживается в центре обтекающей жидкости. Скорость ввода образца или скорость прохождения клеток к лазерному исследованию можно контролировать с помощью давления покровной жидкости на ядро образца. В оптимальных условиях центральный поток жидкости и оболочка жидкости не смешиваются. [ нужна цитата ]
Технология акустической фокусировки используется в некоторых проточных цитометрах для поддержки гидродинамической фокусировки. [13] [15] Акустические волны (>2 МГц) предварительно фокусируют образец перед введением в проточную жидкость. Затем предварительно сфокусированный образец вводится в гидродинамический керн и пропускается через прибор. Это может помочь повысить точность данных при высоких скоростях ввода выборки.
Свет, излучаемый флуорофорами , находится в спектре длин волн, поэтому объединение нескольких флуорофоров может привести к перекрытию. Чтобы добавить специфичности, для фильтрации и подачи света на детекторы, такие как фотоумножители (ФЭУ) или лавинные фотодиоды (ЛФД) , используются оптические фильтры и дихроичные зеркала . [13] Оптические фильтры бывают полосовыми (BP), длиннопроходными (LP) или короткопроходными (SP). В большинстве проточных цитометров используются дихроичные зеркала и полосовые фильтры для выделения определенных полос оптического спектра.
В спектральной проточной цитометрии используются призмы или дифракционные решетки для рассеивания излучаемого света маркера по матрице детекторов. [13] [16] Это позволяет измерять полный спектр каждой частицы. Измеренные спектры отдельных клеток впоследствии несмешиваются с использованием эталонных спектров всех использованных красителей и спектра автофлуоресценции. Это может позволить расширить дизайн панели и применить новые биологические маркеры. [ нужна цитата ]
Визуальная проточная цитометрия (IFC) позволяет получать многоканальные изображения клеток. [13] [17] Детекторы, используемые в платформах визуализации, могут быть оснащены устройствами с зарядовой связью (ПЗС) или комплементарными металл-оксид-полупроводник (КМОП) для захвата изображений отдельных клеток.
Каждый флуорохром имеет широкий спектр флуоресценции. При использовании более одного флуорохрома может произойти перекрытие между флуорохромами. Такая ситуация называется перекрытием спектра. Эту ситуацию необходимо преодолеть. Например, спектр излучения FITC и PE таков, что свет, излучаемый флуоресцеином, перекрывает ту же длину волны, когда он проходит через фильтр, используемый для PE. Это спектральное перекрытие корректируется путем удаления части сигнала FITC из сигналов PE или наоборот. Этот процесс называется цветовой компенсацией, при которой флуорохром рассчитывается в процентах для измерения самого себя. [18]
Компенсация — это математический процесс, с помощью которого корректируется спектральное перекрытие многопараметрических данных проточной цитометрии. Поскольку флуорохромы могут иметь широкий спектр, они могут перекрываться, что приводит к нежелательному результату – путанице при анализе данных. Это перекрытие, известное как перекрытие и количественно выражаемое коэффициентом перекрытия, обычно вызывается тем, что детекторы определенного флуорохрома измеряют значительный пик длины волны от другого флуорохрома. Для внесения этой поправки чаще всего используется линейная алгебра. [18]
В общем, когда отображаются графики одного или нескольких параметров, это означает, что другие параметры не вносят вклада в показанное распределение. Эта проблема становится более серьезной, особенно при использовании параметров, которые превышают вдвое. В настоящее время не обнаружено инструментов для эффективного отображения многомерных параметров. Компенсация очень важна, чтобы увидеть различие между ячейками.

[ нужна цитата ]
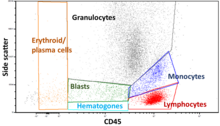
Данные, генерируемые проточными цитометрами, можно отображать в одном измерении для создания гистограммы , в виде двумерных точечных графиков или даже в трех измерениях. Области на этих графиках можно последовательно разделить на основе интенсивности флуоресценции , создав серию выделений подмножества, называемых «воротами». Существуют специальные протоколы гейтирования для диагностических и клинических целей, особенно в гематологии . Отдельные одиночные клетки часто отличаются от дублетов клеток или более высоких агрегатов по их «времени прохождения» (обозначаемому также как «ширина импульса») через узко сфокусированный лазерный луч [19].
Графики часто строятся в логарифмическом масштабе. Поскольку спектры излучения различных флуоресцентных красителей перекрываются, [20] [21] сигналы на детекторах должны компенсироваться как электронно, так и вычислительно. Данные, накопленные с помощью проточного цитометра, можно анализировать с помощью программного обеспечения. После сбора данных нет необходимости оставаться на связи с проточным цитометром, и анализ чаще всего выполняется на отдельном компьютере. [ нужна цитата ] Это особенно необходимо на основных объектах, где использование этих машин пользуется большим спросом. [ нужна цитата ]
Недавний прогресс в автоматизированной идентификации населения с использованием вычислительных методов предложил альтернативу традиционным стратегиям пропуска. Автоматизированные системы идентификации потенциально могут помочь в обнаружении редких и скрытых популяций. Типичные автоматизированные методы включают FLOCK [22] в базе данных иммунологии и портале анализа (ImmPort), [23] SamSPECTRAL [24] и flowClust [25] [26] [27] в Bioconductor и FLAME [28] в GenePattern . T-Distributed Stochastic Neighbor Embedding (tSNE) — это алгоритм, предназначенный для уменьшения размерности , позволяющий визуализировать сложные многомерные данные на двумерной «карте». [29] Совместные усилия привели к созданию открытого проекта под названием FlowCAP (Проточная цитометрия: критическая оценка методов идентификации населения, [30] ), призванного обеспечить объективный способ сравнения и оценки методов кластеризации данных проточной цитометрии, а также разработать рекомендации по надлежащее использование и применение этих методов.
Контроль флуоресценции минус один (FMO) важен для интерпретации данных при построении многоцветных панелей, в которых клетка одновременно окрашивается несколькими флуорохромами. Средства управления FMO позволяют измерить распространение флуоресценции в данном канале и обеспечить компенсацию. Для создания контроля FMO образец окрашивается всеми флуорохромами, кроме испытуемого – это означает, что если вы используете 4 разных флуорохрома, ваш контроль FMO должен содержать только 3 из них (пример: флуорохромы – A, B, C, D; предприятия – ABC_, AB_D, A_CD, _BCD). [ нужна цитата ]
Сортировка клеток — это метод очистки клеточных популяций на основе наличия или отсутствия определенных физических характеристик. [13] [15] [31] В проточных цитометрах с возможностью сортировки прибор обнаруживает клетки, используя такие параметры, как размер клеток, морфологию и экспрессию белка, а затем капельную технологию для сортировки клеток и выделения подмножеств для постэкспериментального использования. [13] [15]
Первый прототип сортировщика был построен в Лос-Аламосской национальной лаборатории (LANL) в 1965 году физиком Маком Дж. Фулвайлером путем соединения датчика объема Коултера с недавно изобретенным струйным принтером. [32] Сортировщик живых клеток или сортировщик клеток, активируемых флуоресценцией (FACS) [a] был создан Леном Герценбергом , который впоследствии получил Киотскую премию в 2006 году за свою плодотворную работу. [34]
_B.jpg/440px-Fluorescence_Assisted_Cell_Sorting_(FACS)_B.jpg)
В отличие от анализаторов проточной цитометрии, сортировщики клеток для проточной цитометрии имеют систему сбора. Процесс сбора начинается, когда образец вводится в поток проточной жидкости, который проходит через проточную ячейку и перехватывается лазером. [35] Затем поток переносит клетку через вибрирующее сопло, которое генерирует капли, большинство из которых содержат либо одну клетку, либо не содержат клеток. Электрическое зарядное кольцо помещается непосредственно в точку, где поток разбивается на капли, а заряд помещается на кольцо непосредственно перед измерением интенсивности флуоресценции; противоположный заряд задерживается на капле, когда она вырывается из потока, и поэтому капли заряжаются. Заряженные капли затем падают через систему электростатического отклонения , которая направляет капли в контейнеры в зависимости от их заряда. В некоторых системах заряд прикладывается непосредственно к потоку, и оторвавшаяся капля сохраняет заряд того же знака, что и поток. Затем поток возвращается в нейтральное состояние после отрыва капли. После сбора эти клетки можно далее культивировать, манипулировать ими и изучать. [ нужна цитата ]

Проточная цитометрия использует свойства света, рассеянного клетками или частицами, для идентификации или количественного измерения физических свойств. Этикетки, красители и красители можно использовать для многопараметрического анализа (чтобы узнать больше о свойствах клетки). Иммунофенотипирование — это анализ гетерогенных популяций клеток с использованием меченых антител [36] и других флуорофорсодержащих реагентов, таких как красители и красители.
В качестве меток в проточной цитометрии можно использовать широкий спектр флуорофоров. [20] Флуорофоры, или просто «флюоры», [ нужна ссылка ] обычно прикрепляются к антителу, которое распознает целевой признак на клетке или внутри нее; они также могут быть присоединены к химическому веществу, имеющему сродство к клеточной мембране или другой клеточной структуре. Каждый флуорофор имеет характерный пик возбуждения и длину волны излучения , а спектры излучения часто перекрываются. Следовательно, комбинация меток, которую можно использовать, зависит от длины волны лампы (ламп) или лазера (лазеров), используемых для возбуждения флуорохромов, и от имеющихся детекторов. [37] Считается, что максимальное количество различимых флуоресцентных меток составляет 17 или 18, и этот уровень сложности требует кропотливой оптимизации для ограничения артефактов, а также сложных алгоритмов деконволюции для разделения перекрывающихся спектров. [38] Проточная цитометрия использует флуоресценцию в качестве количественного инструмента; максимальная чувствительность проточной цитометрии не имеет себе равных среди других платформ флуоресцентного обнаружения, таких как конфокальная микроскопия . Абсолютная чувствительность флуоресценции обычно ниже в конфокальной микроскопии , поскольку сигналы, находящиеся вне фокуса, отвергаются конфокальной оптической системой и поскольку изображение строится последовательно из отдельных измерений в каждом месте клетки, что сокращает время, доступное для сбора сигнала. . [39]
Квантовые точки иногда используются вместо традиционных флуорофоров из-за их более узких пиков излучения. [ нужна цитата ]
Массовая цитометрия преодолевает ограничение флуоресцентной маркировки за счет использования изотопов лантаноидов , прикрепленных к антителам. Этот метод теоретически может позволить использовать от 40 до 60 различимых меток и был продемонстрирован для 30 меток. [38] Массовая цитометрия фундаментально отличается от проточной цитометрии: клетки вводятся в плазму , ионизируются, а связанные с ними изотопы количественно оцениваются с помощью времяпролетной масс-спектрометрии . Хотя этот метод позволяет использовать большое количество меток, в настоящее время он имеет меньшую пропускную способность, чем проточная цитометрия. Он также разрушает анализируемые клетки, исключая их восстановление путем сортировки. [38]
Помимо способности маркировать и идентифицировать отдельные клетки с помощью флуоресцентных антител, также можно измерять клеточные продукты, такие как цитокины, белки и другие факторы. Подобно сэндвич-анализам ELISA , в анализах с использованием цитометрической матрицы ( CBA ) используются несколько популяций шариков, обычно различающихся по размеру и разным уровням интенсивности флуоресценции, чтобы различать несколько аналитов в одном анализе. Количество захваченного аналита определяют с помощью биотинилированного антитела против вторичного эпитопа белка с последующей обработкой стрептавидин-R-фикоэритрином. Интенсивность флуоресценции R-фикоэритрина на гранулах количественно определяют на проточном цитометре, оснащенном источником возбуждения 488 нм. Концентрации интересующего белка в образцах можно получить путем сравнения флуоресцентных сигналов с сигналами стандартной кривой, полученной при серийном разведении известной концентрации аналита. Обычно также называется массивом цитокиновых шариков (CBA).
Системы анализа отдельных ячеек, основанные на импедансе , широко известны как счетчики Коултера . Они представляют собой хорошо зарекомендовавший себя метод подсчета и определения размера практически любого типа клеток и частиц. Технология без маркировки недавно была усовершенствована за счет подхода, основанного на « лаборатории на чипе », и применения высокочастотного переменного тока (AC) в радиочастотном диапазоне (от 100 кГц до 30 МГц) вместо статического постоянного тока . ток (постоянный ток) или низкочастотное переменное поле. [40] [41] Эта запатентованная технология позволяет проводить высокоточный анализ клеток и предоставляет дополнительную информацию, такую как емкость мембраны и жизнеспособность . Относительно небольшой размер и надежность позволяют использовать аккумуляторное питание на месте в полевых условиях.
Измеримые факторы клеточного анализа и проточной цитометрии включают разнообразный набор характеристик и индикаторов, которые дают важную информацию о биологии и функциях клеток. Методы проточной цитометрии позволяют количественно определить и оценить эти факторы, что позволяет исследователям исследовать и анализировать различные аспекты клеток. Вот некоторые важные количественные параметры, которые часто исследуются:
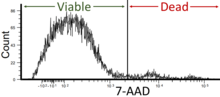
Технология находит применение в ряде областей, включая молекулярную биологию , патологию , иммунологию , вирусологию, [44] биологию растений и морскую биологию . [45] Он широко применяется в медицине , особенно в трансплантологии, гематологии, иммунологии опухолей и химиотерапии, пренатальной диагностике, генетике и сортировке спермы для предварительного выбора пола . Проточная цитометрия широко применяется для выявления аномалий сперматозоидов, связанных с фрагментацией ДНК [46] в анализах мужской фертильности . [47] Кроме того, он широко используется в исследованиях для обнаружения повреждений ДНК , [48] [49] расщепления каспаз и апоптоза . [50] Фотоакустическая проточная цитометрия используется при изучении бактерий с множественной лекарственной устойчивостью (чаще всего MRSA) для обнаружения, дифференциации и количественного определения бактерий в крови, меченных окрашенными бактериофагами. [51] В нейробиологии также можно анализировать совместную экспрессию клеточных поверхностных и внутриклеточных антигенов. [52] В микробиологии его можно использовать для скрининга и сортировки библиотек мутантных транспозонов, сконструированных с использованием транспозона, кодирующего GFP (TnMHA), [53] или для оценки жизнеспособности. [54] В белковой инженерии проточная цитометрия используется в сочетании с дрожжевым и бактериальным дисплеем для идентификации отображаемых на клеточной поверхности вариантов белка с желаемыми свойствами. Основными преимуществами проточной цитометрии перед гистологией и ИГХ является возможность точного измерения количества антигенов и возможность окрашивания каждой клетки несколькими антителами-флуорофорами; в современных лабораториях с каждой клеткой можно связывать около 10 антител. Это намного меньше, чем масс-цитометром, где в настоящее время можно измерить до 40, но по более высокой цене и медленнее.
В водных системах проточная цитометрия используется для анализа автофлуоресцирующих клеток или клеток, флуоресцентно помеченных добавленными красителями. Это исследование началось в 1981 году, когда Кларис Йенч использовала проточную цитометрию для измерения флуоресценции красного прилива, производящего динофлагелляты. [55] В следующем году исследователи опубликовали результаты проточной цитометрии нескольких видов водорослей, которые можно было различить по характеристикам их флуоресценции. [56] К 1983 году морские исследователи собирали свои собственные проточные цитометры [57] или использовали коммерчески доступные проточные цитометры для анализа образцов морской воды, собранных у Бермудских островов, чтобы продемонстрировать, что клетки фитопланктона можно отличить от неживого материала и что цианобактерии можно отделить от смешанное сообщество и впоследствии культивировано в лаборатории. [58] Проточная цитометрия также позволила морским исследователям различать тускло флуоресцирующие прохлорококки и гетеротрофные микроорганизмы, что затруднительно для оценок на основе микроскопии. [59] Достижения в области технологий теперь позволяют ученым-водникам постоянно использовать проточные цитометры во время исследовательских круизов [60], а проточные цитометры используются для получения изображений отдельных клеток фитопланктона. [61] [62] Морские ученые используют сортирующую способность проточных цитометров для дискретных измерений клеточной активности и разнообразия, [63] [64] для проведения исследований мутуалистических отношений между микроорганизмами, живущими в непосредственной близости, [65] и для измерения биогеохимических скоростей множества процессов в океане. [66]
Пролиферация клеток является основной функцией иммунной системы. Часто для того, чтобы сделать какие-то выводы, требуется проанализировать пролиферативную природу клеток. Одним из таких анализов для определения пролиферации клеток является отслеживающий краситель карбоксифлуоресцеин диацетат сукцинимидиловый эфир (CFSE). Это помогает контролировать пролиферативные клетки. Этот анализ дает количественные, а также качественные данные в ходе экспериментов с временными рядами. [67] Этот краситель ковалентно связывается с долгоживущими молекулами, присутствующими внутри клетки. Когда клетки делятся, молекулы тоже делятся, и дочерние клетки содержат половину красителя, чем родительская популяция. Это снижение интенсивности можно визуализировать с помощью проточной цитометрии. [68] В литературе этот мощный метод проточной цитометрии и CFSE использовался для определения эффективности Т-клеток в уничтожении клеток-мишеней при раке, таком как лейкемия. Чтобы визуализировать гибель клеток-мишеней, как быструю, так и медленную, ученые использовали маркировку CFSE с окрашиванием антителами определенных типов клеток и флуоресцентно меченные микрогранулы. Это также дало информацию о пролиферации клеток-мишеней при воздействии определенных цитокинов. [69]
Проточная цитометрия использовалась для измерения размеров генома или, точнее, количества ДНК в клетке или ядре . Хотя геномы можно проанализировать с большей точностью путем секвенирования , это часто бывает затруднительно из-за высокой доли микрохромосом или повторяющихся последовательностей , которые могут быть пропущены при секвенировании (или которые отфильтровываются на этапе анализа, когда их нельзя отнести к хромосомы ). Однако проточная цитометрия также не идеальна. Полученные размеры генома могут различаться в зависимости от используемого красителя. Анализ геномов рыб привел к значительному различию размеров геномов при использовании йодида пропидия (PI) и DAPI соответственно. Например, было обнаружено, что геном Anguilla japonica содержит 1,09 пг ДНК при использовании PI по сравнению с 1,25 пг при использовании DAPI. Аналогичным образом было обнаружено, что геном Myxocyprinus asiaticus содержит 2,75 пг ДНК (PI) против 3,08 пг (DAPI). То есть различия составляли порядка 12–14%. [70]
{{cite web}}: CS1 maint: другие ( ссылка )