Известно 37 изотопов йода ( 53 I) от 108 I до 144 I ; все подвергаются радиоактивному распаду, за исключением 127 I, который стабилен. Таким образом, йод является моноизотопным элементом .
Его самый долгоживущий радиоактивный изотоп , 129 I, имеет период полураспада 15,7 миллиона лет, что слишком мало для его существования в качестве первичного нуклида . Космогенные источники 129 I производят очень малые количества его, которые слишком малы, чтобы повлиять на измерения атомного веса; Таким образом, йод также является мононуклидным элементом , который встречается в природе только в виде одного нуклида. Большая часть радиоактивности, полученной 129 I на Земле, является антропогенной и является нежелательным долгоживущим побочным продуктом ранних ядерных испытаний и аварий ядерного деления.
Все остальные радиоизотопы йода имеют период полураспада менее 60 дней, и четыре из них используются в медицине в качестве индикаторов и терапевтических средств. Это 123 I, 124 I, 125 I и 131 I. Все промышленное производство радиоактивных изотопов йода включает в себя эти четыре полезных радионуклида.
Изотоп 135 I имеет период полураспада менее семи часов, что слишком мало для использования в биологии. Неизбежное производство этого изотопа на месте важно для управления ядерным реактором, поскольку он распадается до 135 Xe, самого мощного известного поглотителя нейтронов , и нуклида, ответственного за так называемое явление йодной ямы .
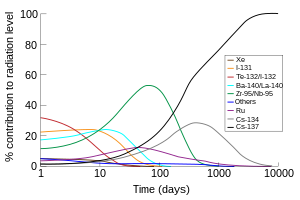
Помимо коммерческого производства, 131 I (период полураспада 8 дней) является одним из распространенных радиоактивных продуктов ядерного деления и, таким образом, непреднамеренно производится в очень больших количествах внутри ядерных реакторов . Из-за своей летучести, короткого периода полураспада и высокого содержания в продуктах деления 131 I (вместе с короткоживущим изотопом йода 132 I, который образуется в результате распада 132 Te с периодом полураспада 3 дня) ответственны за большую часть радиоактивного загрязнения в течение первой недели после аварийного загрязнения окружающей среды радиоактивными отходами атомной электростанции. Таким образом, высокодозированные добавки йода (обычно йодид калия ) назначаются населению после ядерных аварий или взрывов (а в некоторых случаях до любого такого инцидента в качестве механизма гражданской обороны ), чтобы уменьшить поглощение соединений радиоактивного йода щитовидной железой до того, как произойдет высокодозированная йодная добавка. радиоактивные изотопы успели распасться.
Радиоизотопы йода называются радиоактивным йодом или радиойодом . Их существуют десятки, но около полдюжины являются наиболее известными в прикладных науках, таких как науки о жизни и ядерная энергетика, как подробно описано ниже. Упоминания о радиойоде в контексте здравоохранения чаще относятся к йоду-131, чем к другим изотопам.
Из множества изотопов йода в медицинских целях обычно используются только два: йод-123 и йод-131. Поскольку 131 I имеет режим как бета-, так и гамма-распада, его можно использовать для лучевой терапии или для визуализации. 123 I, не обладающий бета-активностью, больше подходит для рутинной ядерной медицинской визуализации щитовидной железы и других медицинских процессов и менее вреден для внутренних органов пациента. Есть ситуации, когда йод-124 и йод-125 также используются в медицине. [4]
Из-за преимущественного поглощения йода щитовидной железой радиойод широко используется для визуализации и, в случае 131 I, разрушения дисфункциональных тканей щитовидной железы. Другие типы тканей избирательно поглощают определенные радиофармацевтические агенты, содержащие йод-131, нацеленные на ткани и убивающие их (такие как MIBG ). Йод-125 — единственный другой радиоизотоп йода, используемый в лучевой терапии, но только в виде имплантируемой капсулы при брахитерапии , где у изотопа никогда не бывает возможности высвободиться для химического взаимодействия с тканями организма.
Гамма -излучающие изотопы йод-123 (период полураспада 13 часов) и (реже) более долгоживущий и менее энергичный йод-125 (период полураспада 59 дней) используются в качестве индикаторов ядерной визуализации для оценки анатомических и физиологических функция щитовидной железы. Аномальные результаты могут быть вызваны такими заболеваниями, как болезнь Грейвса или тиреоидит Хашимото . Оба изотопа распадаются в результате электронного захвата (EC) до соответствующих нуклидов теллура , но ни в одном случае это не метастабильные нуклиды 123m Te и 125m Te (которые имеют более высокую энергию и не производятся из радиойода). Вместо этого возбужденные нуклиды теллура немедленно распадаются (период полураспада слишком короток, чтобы его можно было обнаружить). После ЕС возбужденный 123 Te из 123 I испускает высокоскоростной внутренний конверсионный электрон с энергией 127 кэВ (не бета-луч ) примерно в 13% случаев, но это наносит небольшой вред клеткам из-за короткого периода полураспада нуклида и относительно малая часть таких событий. В остальных случаях излучается гамма-луч с энергией 159 кэВ, который хорошо подходит для гамма-визуализации.
Возбужденный 125 Te, возникающий в результате электронного захвата 125 I, также испускает внутренний конверсионный электрон с гораздо более низкой энергией (35,5 кэВ), который наносит относительно небольшой ущерб из-за своей низкой энергии, хотя его испускание более распространено. Относительно низкоэнергетическая гамма- распад 125 I/ 125 Te плохо подходит для визуализации, но ее все же можно увидеть, и этот более долгоживущий изотоп необходим в тестах, требующих нескольких дней визуализации, например, при сканировании фибриногена для обнаружения сгустки крови.
И 123 I, и 125 I после распада испускают обильное количество оже-электронов низкой энергии , но они не вызывают серьезных повреждений (двухцепочечные разрывы ДНК) в клетках, если только нуклид не включен в лекарство, которое накапливается в ядре, или в ДНК. (в клинической медицине такого не бывает, но это наблюдалось на экспериментальных моделях животных). [5]
Йод-125 также широко используется радиационными онкологами в брахитерапии с низкой мощностью дозы при лечении рака других локализаций, кроме щитовидной железы, особенно рака простаты . Когда 125 I используется в терапевтических целях, его инкапсулируют в титановые семена и имплантируют в область опухоли, где он и остается. Низкая энергия гамма-спектра в этом случае ограничивает радиационное поражение тканей, удаленных от имплантированной капсулы. Йод-125 из-за его более длительного периода полураспада и меньшей проникающей способности гамма-спектра также часто предпочтителен для лабораторных тестов, в которых йод используется в качестве индикатора, подсчитываемого с помощью гамма-счетчика , например, при радиоиммуноанализе .
125 I используется в качестве радиоактивной метки при исследовании того, какие лиганды к каким рецепторам распознавания образов растений (PRR) передаются. [6]
Йод-124 представляет собой богатый протонами изотоп йода с периодом полураспада 4,18 дня. Его способы распада: 74,4% захват электронов, 25,6% испускание позитронов. 124 I распадается до 124 Te. Йод-124 можно получить в результате многочисленных ядерных реакций на циклотроне . Наиболее распространенным исходным материалом является 124 Te.
Йод-124 в виде йодистой соли можно использовать для прямого изображения щитовидной железы с помощью позитронно-эмиссионной томографии (ПЭТ). [7] Йод-124 также можно использовать в качестве радиофармпрепарата для ПЭТ с более длительным периодом полураспада по сравнению с фтором-18 . [8] При таком использовании нуклид химически связывается с фармацевтическим препаратом с образованием радиофармпрепарата, испускающего позитроны, и вводится в организм, где он снова визуализируется с помощью ПЭТ-сканирования.
Йод-129 ( 129 I; период полураспада 15,7 миллионов лет) является продуктом расщепления космическими лучами на различные изотопы ксенона в атмосфере , при взаимодействии мюонов космических лучей с теллуром-130, а также деления урана и плутония , как в недрах, так и в атмосфере. камни и ядерные реакторы. Искусственные ядерные процессы, в частности, переработка ядерного топлива и испытания ядерного оружия в атмосфере, теперь затмили естественный сигнал этого изотопа. Тем не менее, теперь он служит индикатором грунтовых вод и индикатором распространения ядерных отходов в природную среду. Подобным образом 129 I использовался в исследованиях дождевой воды для отслеживания продуктов деления после чернобыльской катастрофы .
В чем-то 129 I похож на 36 Cl . Это растворимый галоген, существует в основном в виде несорбирующего аниона и образуется в результате космогенных, термоядерных реакций и реакций in-situ. В гидрологических исследованиях концентрации 129 I обычно указывают как отношение 129 I к общему I (который практически представляет собой весь 127 I). Как и в случае с 36 Cl/Cl, отношения 129 I/I в природе весьма малы: от 10 -14 до 10 -10 (пики термоядерного 129 I/I в 1960-е и 1970-е годы достигали примерно 10 -7 ). 129 I отличается от 36 Cl тем, что его период полураспада длиннее (15,7 против 0,301 миллиона лет), он очень биофильен и встречается в нескольких ионных формах (обычно I - и IO 3 - ), которые имеют различное химическое поведение. . Это позволяет 129 I довольно легко проникать в биосферу при его включении в растительность, почву, молоко, ткани животных и т. д. Было показано, что избытки стабильного 129 Xe в метеоритах возникают в результате распада «первичного» образующегося йода-129. недавно сверхновыми, которые создали пыль и газ, из которых сформировалась Солнечная система. Этот изотоп уже давно распался, поэтому его называют «потухшим». Исторически 129 I был первым потухшим радионуклидом , обнаруженным в ранней Солнечной системе . Его распад лежит в основе схемы радиометрического датирования йод-ксенон I-Xe , которая охватывает первые 85 миллионов лет эволюции Солнечной системы .

Йод-131 (131
я
) представляет собой бета-излучающий изотоп с периодом полураспада восемь дней и сравнительно энергичным (средняя энергия 190 кэВ и максимальная энергия 606 кэВ) бета-излучением, которое проникает на расстояние от 0,6 до 2,0 мм от места поглощения. Это бета-излучение можно использовать для разрушения узлов щитовидной железы или гиперфункционирующей ткани щитовидной железы, а также для удаления оставшейся ткани щитовидной железы после операции при лечении болезни Грейвса . Целью этой терапии, которая была впервые исследована доктором Саулом Герцем в 1941 году [9] , является разрушение ткани щитовидной железы, которую невозможно удалить хирургическим путем. При этой процедуре 131 I вводят внутривенно или перорально после диагностического сканирования. Эту процедуру также можно использовать с более высокими дозами радиоактивного йода для лечения пациентов с раком щитовидной железы .
131 I попадает в ткань щитовидной железы и концентрируется там. Бета-частицы, испускаемые радиоизотопом, разрушают соответствующую ткань щитовидной железы с небольшим повреждением окружающих тканей (более 2,0 мм от тканей, поглощающих йод). Из-за аналогичного разрушения 131 I является радиоизотопом йода, используемым в других водорастворимых радиофармпрепаратах , меченных йодом (таких как МИБГ ), используемых в терапевтических целях для разрушения тканей.
Бета-излучение высокой энергии (до 606 кэВ) 131 I делает его наиболее канцерогенным из изотопов йода. Считается, что он вызывает большинство случаев избыточного рака щитовидной железы, наблюдаемых после радиоактивного загрязнения (например, выпадение бомб или тяжелые аварии на ядерных реакторах, такие как Чернобыльская катастрофа ). Однако эти эпидемиологические эффекты наблюдаются в первую очередь у детей, а лечение взрослых и детей терапевтическими препаратами 131 I, а эпидемиология взрослых, подвергшихся воздействию низких доз 131 I, не выявила канцерогенности. [10]
Йод-135 — изотоп йода с периодом полураспада 6,6 часов. Это важный изотоп с точки зрения физики ядерных реакторов . Он образуется в относительно больших количествах в виде продукта деления и распадается до ксенона-135 , который является ядерным ядом с очень большим сечением тепловых нейтронов , что является причиной многочисленных осложнений при управлении ядерными реакторами . Процесс накопления ксенона-135 из накопленного йода-135 может временно помешать перезапуску остановленного реактора. Это известно как отравление ксеноном или «падение в йодную яму ».
Изотопы йода, полученные в результате деления йода, не обсуждавшиеся выше (йод-128, йод-130, йод-132 и йод-133), имеют период полураспада в несколько часов или минут, что делает их практически бесполезными в других применимых областях. Упомянутые вещества богаты нейтронами и подвергаются бета-распаду до изотопов ксенона. Йод-128 (период полураспада 25 минут) может распадаться либо на теллур-128 путем захвата электронов, либо на ксенон-128 путем бета-распада. Имеет специфическую радиоактивность2,177 × 10 6 ТБк/г .
В разговорной речи радиоактивные материалы можно охарактеризовать как «горячие», а нерадиоактивные материалы — как «холодные». Есть случаи, когда людям вводят холодный йодид, чтобы предотвратить поглощение горячего йодида щитовидной железой. Например, блокада поглощения йода щитовидной железой с помощью йодида калия используется в сцинтиграфии ядерной медицины и терапии некоторыми радиоактивными йодсодержащими соединениями, которые не нацелены на щитовидную железу, такими как йобенгуан ( МИБГ ), который используется для визуализации или лечения опухолей нервной ткани, или йодированный фибриноген, который используется при сканировании фибриногена для исследования свертывания крови. Эти соединения содержат йод, но не в форме йодида. Однако, поскольку в конечном итоге они могут метаболизироваться или расщепляться до радиоактивного йодида, обычно вводят нерадиоактивный йодид калия, чтобы гарантировать, что метаболиты этих радиофармпрепаратов не секвестрируются щитовидной железой и непреднамеренно не вводят радиологическую дозу в эту ткань.
Йодид калия был распространен среди населения, пострадавшего от аварий ядерного деления , таких как чернобыльская катастрофа . Раствор йодида SSKI , насыщенный раствор йодида калия ( K ) в воде, использовался для блокирования поглощения радиойода (он не оказывает влияния на другие радиоизотопы в результате деления). Таблетки, содержащие йодид калия, в настоящее время также производятся и хранятся в центральных местах стихийных бедствий правительствами некоторых стран с этой целью. Теоретически, многие вредные последствия ядерных осадков на поздних стадиях рака можно было бы предотвратить, поскольку избыточное количество случаев рака щитовидной железы, предположительно из-за поглощения радиоактивного йода, является единственным доказанным эффектом загрязнения радиоизотопами после аварии ядерного деления или загрязнения выпадениями радиоактивных осадков. атомная бомба (мгновенное облучение от бомбы также напрямую вызывает другие виды рака, такие как лейкозы). Прием больших количеств йода насыщает рецепторы щитовидной железы и предотвращает поглощение большей части радиоактивного йода-131 , который может присутствовать в результате воздействия продуктов деления (хотя он не защищает ни от других радиоизотопов, ни от любой другой формы прямого излучения). Защитный эффект KI длится примерно 24 часа, поэтому его следует вводить ежедневно до тех пор, пока не исчезнет риск значительного воздействия радиоактивного йода из продуктов деления. [11] [12] Йод-131 (наиболее распространенный загрязнитель радиоактивного йода в выпадениях) также распадается относительно быстро с периодом полураспада восемь дней, так что 99,95% исходного радиоактивного йода исчезло через три месяца.