Радон — химический элемент ; он имеет символ Rn и атомный номер 86. Это радиоактивный благородный газ , бесцветный и не имеющий запаха. Из трех встречающихся в природе изотопов радона только радон-222 имеет достаточно длительный период полураспада (3,825 дня), чтобы он мог высвобождаться из почвы и горных пород, где он образуется. Изотопы радона являются непосредственными продуктами распада изотопов радия . Нестабильность радона-222, его наиболее стабильного изотопа, делает радон одним из самых редких элементов. Радон будет присутствовать на Земле еще несколько миллиардов лет, несмотря на его короткий период полураспада, поскольку он постоянно образуется на ступенях цепочки распада урана-238 и тория -232 , каждый из которых является чрезвычайно Обильный радиоактивный нуклид с периодом полураспада в несколько миллиардов лет. Распад радона приводит к образованию многих других короткоживущих нуклидов , известных как «дочери радона», заканчивающихся стабильными изотопами свинца . [3] Радон-222 встречается в значительных количествах как один из этапов нормальной цепи радиоактивного распада урана-238, также известного как урановый ряд , который медленно распадается на различные радиоактивные нуклиды и в конечном итоге распадается на свинец-206 , который стабильный. Радон-220 встречается в незначительных количествах как промежуточный этап в цепочке распада тория-232, также известного как ряд тория , который в конечном итоге распадается на стабильный свинец-208 .
В обычных условиях радон является газообразным и легко вдыхается, что представляет опасность для здоровья. Однако основная опасность исходит не от самого радона, а от продуктов его распада, так называемых дочерей радона. Эти продукты распада, часто существующие в виде отдельных атомов или ионов, могут прикрепляться к переносимым по воздуху частицам пыли. Хотя радон является благородным газом и не прилипает к легочной ткани, а это означает, что он часто выдыхается перед распадом, дочерние элементы радона, прикрепленные к пыли, с большей вероятностью прилипают к легким. Это увеличивает риск причинения вреда, так как дочери радона могут вызвать повреждение легочной ткани. [4] Радон и его дочерние элементы, вместе взятые, часто вносят наибольший вклад в дозу фоновой радиации человека , но из-за местных различий в геологии [5] уровень воздействия газа радона различается от места к месту. Распространенным источником являются урансодержащие минералы в земле, поэтому он накапливается в подземных областях, таких как подвалы. Радон также может присутствовать в некоторых грунтовых водах, таких как родниковые воды и горячие источники. [6] Радон, захваченный вечной мерзлотой, может высвобождаться в результате таяния вечной мерзлоты, вызванного изменением климата . [7] Можно проверить наличие радона в зданиях и использовать такие методы, как разгерметизация подпанелей для смягчения последствий . [8] [9]
Эпидемиологические исследования показали четкую связь между вдыханием высоких концентраций радона и заболеваемостью раком легких . Радон является загрязнителем, который влияет на качество воздуха в помещениях во всем мире. По данным Агентства по охране окружающей среды США (EPA), радон является второй по распространенности причиной рака легких после курения сигарет, вызывая 21 000 смертей от рака легких в год в Соединенных Штатах. Около 2900 из этих смертей происходят среди людей, которые никогда не курили. Хотя радон является второй по распространенности причиной рака легких, согласно оценкам EPA, он является причиной номер один среди некурящих. [10] Существуют значительные неопределенности относительно последствий воздействия низких доз на здоровье. [11]
Радон представляет собой газ без цвета, запаха и вкуса [12] , поэтому его невозможно обнаружить только органами чувств человека. При стандартных температуре и давлении он образует одноатомный газ с плотностью 9,73 кг/м 3 , что примерно в 8 раз превышает плотность земной атмосферы на уровне моря, 1,217 кг/м 3 . [13] Это один из самых плотных газов при комнатной температуре (некоторые из них плотнее, например, CF 3 (CF 2 ) 2 CF 3 и WF 6 ) и самый плотный из благородных газов. Хотя он бесцветен при стандартной температуре и давлении, при охлаждении ниже точки замерзания 202 К (-71 ° C; -96 ° F) он излучает яркую радиолюминесценцию , которая при понижении температуры меняет цвет с желтого на оранжево-красный. [14] При конденсации он светится из-за интенсивного излучения, которое он производит. [15] Он умеренно растворим в воде, но более растворим, чем более легкие благородные газы. Он значительно лучше растворяется в органических жидкостях, чем в воде. Уравнение его растворимости выглядит следующим образом: [16] [17] [18]
где – мольная доля радона, – абсолютная температура, – константы растворителя.
Радон входит в число элементов нулевой валентности , называемых благородными газами, и химически не очень активен . Период полураспада радона-222 составляет 3,8 дня, что делает его полезным в физических науках в качестве естественного индикатора . Поскольку радон в стандартных условиях является газом, в отличие от его родителей в цепочке распада, его можно легко извлечь из них для исследования. [19]
Он инертен к большинству распространенных химических реакций, таких как горение , поскольку внешняя валентная оболочка содержит восемь электронов . Это создает стабильную конфигурацию с минимальной энергией, в которой внешние электроны прочно связаны. [20] Его первая энергия ионизации — минимальная энергия, необходимая для извлечения из него одного электрона — составляет 1037 кДж/моль. [21] В соответствии с периодическими тенденциями , радон имеет более низкую электроотрицательность, чем элемент, расположенный за один период до него, ксенон , и поэтому более реакционноспособен. Ранние исследования пришли к выводу, что стабильность гидрата радона должна быть того же порядка, что и гидратов хлора ( Cl
2) или диоксид серы ( SO
2), и значительно выше, чем стабильность гидрата сероводорода ( H
2С ). [22]
Из-за его стоимости и радиоактивности экспериментальные химические исследования с радоном проводятся редко, и в результате сообщается об очень небольшом количестве соединений радона, все они либо фториды , либо оксиды . Радон может окисляться мощными окислителями, такими как фтор , образуя дифторид радона ( RnF
2). [23] [24] Он разлагается обратно на свои элементы при температуре выше 523 К (250 ° C; 482 ° F) и восстанавливается водой до газообразного радона и фтористого водорода: он также может быть восстановлен обратно до своих элементов. газообразным водородом . [25] Он имеет низкую волатильность и считался RnF.
2. Из-за короткого периода полураспада радона и радиоактивности его соединений детально изучить это соединение не удалось. Теоретические исследования этой молекулы предсказывают, что она должна иметь расстояние связи Rn-F 2,08 ангстрема (Å) и что это соединение термодинамически более стабильно и менее летучее, чем его более легкий аналог дифторид ксенона ( XeF
2). [26] Октаэдрическая молекула RnF6Было предсказано, что он будет иметь еще более низкую энтальпию образования , чем дифторид. [27] Считается, что ион [RnF] + образуется в результате следующей реакции: [28]
По этой причине пентафторид сурьмы вместе с трифторидом хлора и N
2Ф
2Сб
2Ф
11были рассмотрены для удаления газа радона на урановых рудниках из-за образования соединений радона и фтора. [19] Соединения радона могут образовываться в результате распада радия в галогенидах радия — реакции, которая использовалась для уменьшения количества радона, выходящего из мишеней во время облучения . [25] Кроме того, соли катиона [RnF] + с анионами SbF−
6, ТаФ−
6и БиФ−
6известны. [25] Радон также окисляется дифторидом кислорода до RnF.
2при 173 К (-100 ° C; -148 ° F). [25]
Оксиды радона являются одними из немногих других известных соединений радона ; [29] только триоксид ( RnO
3) было подтверждено. [30] Высшие фториды RnF
4и РнФ
6были заявлены [30] и считаются стабильными, [31] но их идентификация неясна. [30] Их, возможно, наблюдали в экспериментах, когда неизвестные радонсодержащие продукты перегоняли вместе с гексафторидом ксенона : это могли быть RnF.
4, РнФ
6, или оба. [25] Утверждалось , что незначительное нагревание радона с ксеноном, фтором, пентафторидом брома и фторидом натрия или фторидом никеля также приводит к образованию более высокого фторида, который гидролизуется с образованием RnO.
3. Хотя было высказано предположение, что эти утверждения на самом деле были связаны с осаждением радона в виде твердого комплекса [RnF]+
2[NiF 6 ] 2− , то, что радон соосаждается из водного раствора с CsXeO
3F был принят как подтверждение того, что RnO
3Образовалось, что было подтверждено дальнейшими исследованиями гидролизованного раствора. То, что [RnO 3 F] − не образовывалось в других экспериментах, возможно, связано с высокой концентрацией использованного фторида. Электромиграционные исследования также предполагают наличие катионной [HRnO 3 ] + и анионной [HRnO 4 ] − форм радона в слабокислом водном растворе (pH > 5), причем эта процедура ранее была подтверждена исследованием гомологичного триоксида ксенона. [30]
Также использовалась техника распада . Аврорин и др. в 1982 году сообщил, что соединения 212 Fr , сокристаллизованные со своими аналогами цезия, по-видимому, сохраняют химически связанный радон после захвата электронов; аналогии с ксеноном предполагали образование RnO 3 , но подтвердить это не удалось. [32]
Вполне вероятно, что трудность в идентификации высших фторидов радона связана с тем, что радон кинетически препятствует окислению за пределы двухвалентного состояния из-за сильной ионности дифторида радона ( RnF
2) и высокий положительный заряд радона в RnF + ; пространственное разделение RnF
2молекулы могут быть необходимы для четкой идентификации высших фторидов радона, из которых RnF
4ожидается, что он будет более стабильным, чем RnF
6из-за спин-орбитального расщепления 6p-оболочки радона (Rn IV будет иметь закрытую оболочку 6s2
6р2
1/2конфигурация). Следовательно, хотя РнФ
4должен иметь такую же стабильность, как и тетрафторид ксенона ( XeF
4), РнФ
6вероятно, будет гораздо менее стабильным, чем гексафторид ксенона ( XeF
6): гексафторид радона, вероятно, также будет правильной октаэдрической молекулой, в отличие от искаженной октаэдрической структуры XeF.
6, из-за эффекта инертной пары . [33] [34] Поскольку радон является весьма электроположительным по отношению к благородному газу, вполне возможно, что фториды радона на самом деле принимают структуры с высоким содержанием фтор-мостиков и не являются летучими. [34] Экстраполяция вниз по группе благородных газов предполагает также возможное существование RnO, RnO 2 и RnOF 4 , а также первых химически стабильных хлоридов благородных газов RnCl 2 и RnCl 4 , но ни один из них еще не был обнаружен. [25]
Было предсказано, что карбонил радона (RnCO) стабилен и имеет линейную молекулярную геометрию . [35] Молекулы Rn
2Было обнаружено, что и RnXe значительно стабилизируются за счет спин-орбитального взаимодействия . [36] Радон, заключенный в фуллерен , был предложен в качестве лекарства от опухолей . [37] [38] Несмотря на существование Xe(VIII), не утверждается, что существуют соединения Rn(VIII); РнФ
8должен быть крайне нестабильным химически (XeF 8 термодинамически нестабилен). Прогнозируется, что наиболее стабильным соединением Rn(VIII) будет перрадонат бария (Ba 2 RnO 6 ), аналог перксената бария . [31] Нестабильность Rn(VIII) обусловлена релятивистской стабилизацией оболочки 6s, также известной как эффект инертной пары . [31]
Радон реагирует с жидкими фторидами галогенов ClF, ClF.
3, КФ
5, БрФ
3, БрФ
5, и если
7сформировать РнФ
2. В растворе фторида галогена радон нелетуч и существует в виде катионов RnF + и Rn2 + ; присоединение фторид-анионов приводит к образованию комплексов RnF−
3и РнФ2−
4, что соответствует химии бериллия (II) и алюминия (III). [25] Стандартный электродный потенциал пары Rn 2+ /Rn оценивается как +2,0 В, [39] хотя нет никаких доказательств образования стабильных ионов радона или соединений в водном растворе. [25]
Радон не имеет стабильных изотопов . Охарактеризовано тридцать девять радиоактивных изотопов с массовыми числами от 193 до 231. [40] [41] Шесть из них, от 217 до 222 включительно, встречаются в природе. Наиболее стабильным изотопом является 222 Rn (период полураспада 3,82 дня), который является продуктом распада 226 Ra , причем последний сам является продуктом распада 238 U. [42] Следовое количество (крайне нестабильного) изотопа 218 Rn (период полураспада около 35 миллисекунд ) также имеется среди дочерних элементов 222 Rn. Изотоп 216 Rn будет производиться в результате двойного бета-распада природного 216 Po; хотя этот процесс энергетически возможен, однако этот процесс никогда не наблюдался. [43]
Три других изотопа радона имеют период полураспада более часа: 211 Rn (около 15 часов), 210 Rn (2,4 часа) и 224 Rn (около 1,8 часа). Однако ни один из этих трех факторов не встречается в природе. 220 Rn, также называемый тороном, является естественным продуктом распада наиболее стабильного изотопа тория ( 232 Th). Он имеет период полураспада 55,6 секунды, а также излучает альфа-излучение . Точно так же 219 Rn получен из наиболее стабильного изотопа актиния ( 227 Ac ), называемого «актинон», и является альфа-излучателем с периодом полураспада 3,96 секунды. [40] В серии распада нептуния ( 237 Np) изотопы радона не встречаются в значительных количествах , хотя следовые количества изотопов 221 Rn (26 минут) и 217 Rn (0,5 миллисекунды) образуются в второстепенных ветвях .
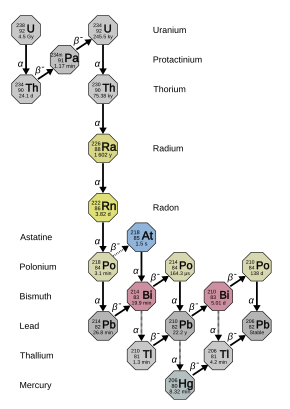
222 Rn принадлежит к цепочке распада радия и урана-238 и имеет период полураспада 3,8235 дней. Его первые четыре продукта (исключая схемы маргинального распада ) очень недолговечны, а это означает, что соответствующие распады указывают на начальное распределение радона. Его распад происходит в следующей последовательности: [40]
Коэффициент равновесия радона [44] представляет собой соотношение между активностью всех короткопериодических дочерних элементов радона (которые ответственны за большую часть биологических эффектов радона) и активностью, которая находилась бы в равновесии с родительским радоном.
Если замкнутый объем постоянно снабжается радоном, концентрация короткоживущих изотопов будет увеличиваться до тех пор, пока не будет достигнуто равновесие, при котором общая скорость распада продуктов распада равна скорости самого радона. Коэффициент равновесия равен 1, когда обе активности равны, что означает, что продукты распада оставались близко к родительскому радону достаточно долго, чтобы достичь равновесия, в течение нескольких часов. В этих условиях каждый дополнительный пКи/л радона увеличит воздействие на 0,01 рабочего уровня (WL, мера радиоактивности, обычно используемая в горнодобывающей промышленности). Эти условия не всегда выполняются; во многих домах коэффициент равновесия обычно составляет 40%; то есть на каждый пКи/л радона в воздухе будет приходиться 0,004 WL дочерних элементов. [45] 210 Pb требуется гораздо больше времени (десятилетия), чтобы прийти в равновесие с радоном, но, если окружающая среда допускает накопление пыли в течение длительных периодов времени, 210 Pb и продукты его распада также могут способствовать повышению общего уровня радиации.
Из-за своего электростатического заряда дочерние частицы радона прилипают к поверхностям или частицам пыли, тогда как газообразный радон этого не делает. Приставка удаляет их из воздуха, в результате чего коэффициент равновесия в атмосфере обычно становится меньше 1. Коэффициент равновесия также снижается за счет циркуляции воздуха или устройств фильтрации воздуха и увеличивается за счет переносимых по воздуху частиц пыли, включая сигаретный дым. Коэффициент равновесия, обнаруженный в эпидемиологических исследованиях, составляет 0,4. [46]
Радон был открыт в 1899 году Эрнестом Резерфордом и Робертом Б. Оуэнсом в Университете Макгилла в Монреале . [47] Это был пятый радиоактивный элемент, открытый после урана, тория, радия и полония. [48] [49] [50] [51] В 1899 году Пьер и Мария Кюри заметили, что газ, выделяемый радием, оставался радиоактивным в течение месяца. [52] Позже в том же году Резерфорд и Оуэнс заметили различия при попытке измерить излучение оксида тория. [47] Резерфорд заметил, что соединения тория непрерывно выделяют радиоактивный газ, который остаётся радиоактивным в течение нескольких минут, и назвал этот газ «эманацией» (от латинского : emanare — вытекать, и emanatio — истечение), [53] и позднее «эманация тория» («Th Em»). В 1900 году Фридрих Эрнст Дорн сообщил о некоторых экспериментах, в которых он заметил, что соединения радия выделяют радиоактивный газ, который он назвал «эманацией радия» («Ra Em»). [54] [55] В 1901 году Резерфорд и Гарриет Брукс продемонстрировали, что эманации радиоактивны, но приписали Кюри открытие элемента. [56] В 1903 году подобные эманации актиния наблюдал Андре-Луи Дебьерн , [57] [58] и были названы «эманацией актиния» («Ac Em»).
Вскоре для трех эманаций было предложено несколько сокращенных названий: exradio , exthorio и actinio в 1904 году; [59] радон (Ро), торон (То) и актон или актон (Ао) в 1918 г.; [60] радон , тореон и актинон в 1919 году, [61] и, наконец, радон , торон и актинон в 1920 году. [62] (Название радон не связано с именем австрийского математика Иоганна Радона .) Сходство Спектры этих трех газов со спектрами аргона, криптона и ксенона, а также их наблюдаемая химическая инерция побудили сэра Уильяма Рамзи предположить в 1904 году, что «эманации» могут содержать новый элемент семейства благородных газов. [59]
В 1909 году Рамзи и Роберт Уитлоу-Грей выделили радон и определили его температуру плавления и приблизительную плотность . В 1910 году они определили, что это самый тяжелый из известных газов. [63] Они написали, что « L’expression l’émanation du radium est fort incommode » («выражение «эманация радия» очень неуклюже») и предложили новое название нитон (Nt) (от латыни : nitens , сияющий) для подчеркивают свойство радиолюминесценции, [64] и в 1912 году оно было принято Международной комиссией по атомным весам . В 1923 году Международный комитет химических элементов и Международный союз теоретической и прикладной химии (ИЮПАК) выбрали в качестве названия элемента название наиболее стабильного изотопа — радона. Изотопы торон и актинон позже были переименованы в 220 Rn и 219 Rn. Это вызвало некоторую путаницу в литературе относительно открытия элемента, поскольку, хотя Дорн открыл изотоп радон, он не был первым, кто открыл радон. [65]
Еще в 1960-х годах этот элемент также называли просто эманацией . [66] Первое синтезированное соединение радона, фторид радона, было получено в 1962 году. [67] Даже сегодня слово радон может относиться либо к самому элементу, либо к его изотопу 222 Rn, при этом торон по-прежнему используется как краткое название для 220. Rn, чтобы устранить эту двусмысленность. Название актинон для 219 Rn сегодня встречается редко, вероятно, из-за короткого периода полураспада этого изотопа. [65]
Давно известна опасность высокого воздействия радона в шахтах, где уровень воздействия может достигать 1 000 000 Бк /м 3 . В 1530 году Парацельс описал истощающую болезнь горняков — мала металлорум , а Георг Агрикола рекомендовал вентиляцию в шахтах, чтобы избежать этой горной болезни ( Бергсухт ). [68] [69] В 1879 году это состояние было идентифицировано как рак легких Хартингом и Гессе при исследовании горняков из Шнеберга, Германия. Первые крупные исследования радона и здоровья произошли в контексте добычи урана в регионе Иоахимсталь в Богемии . [70] В США исследования и меры по смягчению последствий только последовали за десятилетиями воздействия на здоровье шахтеров урана на юго-западе США, работавших в начале холодной войны ; стандарты не применялись до 1971 года. [71]
В начале 20 века в США золото, загрязненное дочерним элементом радона 210 Pb, поступило в ювелирную промышленность. Это были золотые семена для брахитерапии , содержащие 222 Rn, которые были расплавлены после распада радона. [72] [73]
Присутствие радона в воздухе помещений было зарегистрировано еще в 1950 году. Начиная с 1970-х годов были начаты исследования по изучению источников радона в помещениях, факторов, определяющих концентрацию, воздействия на здоровье и подходов к смягчению последствий. В США проблема радона в помещениях получила широкую огласку и усиленное расследование после широко разрекламированного инцидента в 1984 году. Во время планового мониторинга на атомной электростанции в Пенсильвании было обнаружено, что рабочий был заражен радиоактивностью. Причиной инцидента впоследствии была признана высокая концентрация радона в его доме. [74]

Все обсуждения концентрации радона в окружающей среде относятся к 222 Rn. Хотя средняя скорость образования 220 Rn (из ряда распада тория) примерно такая же, как и у 222 Rn, количество 220 Rn в окружающей среде значительно меньше, чем у 222 Rn из-за короткого периода полураспада 220 Рн (55 секунд против 3,8 суток соответственно). [3]
Концентрация радона в атмосфере обычно измеряется в беккерелях на кубический метр (Бк/м 3 ), производной единице системы СИ . Другая единица измерения, распространенная в США, — пикокюри на литр (пКи/л); 1 пКи/л = 37 Бк/м 3 . [45] Типичное бытовое облучение в среднем составляет около 48 Бк/м 3 в помещении, хотя этот показатель широко варьируется, и 15 Бк/м 3 на открытом воздухе. [76]
В горнодобывающей промышленности риск традиционно измеряется в рабочем уровне (WL) и совокупном уровне риска в месяце рабочего уровня (WLM); 1 WL соответствует любой комбинации короткоживущих дочерних элементов 222 Rn ( 218 Po, 214 Pb, 214 Bi и 214 Po) в 1 литре воздуха, которая выделяет 1,3 × 10 5 МэВ потенциальной альфа-энергии; [45] 1 WL эквивалентен 2,08 × 10 −5 джоулей на кубический метр воздуха (Дж/м 3 ). [3] Единица СИ совокупного воздействия выражается в джоулях-часах на кубический метр (Дж·ч/м 3 ). Один WLM эквивалентен 3,6 × 10 −3 Дж·ч/м 3 . Воздействие 1 WL в течение 1 рабочего месяца (170 часов) равно совокупному риску 1 WLM. Совокупное воздействие 1 WLM примерно эквивалентно проживанию в течение одного года в атмосфере с концентрацией радона 230 Бк/м 3 . [77]
222 Rn распадается на 210 Pb и другие радиоизотопы. Уровни 210 Pb можно измерить. Скорость осаждения этого радиоизотопа зависит от погоды.
Концентрации радона, обнаруженные в естественной среде, слишком малы, чтобы их можно было обнаружить химическими методами. Концентрация 1000 Бк/м 3 (относительно высокая) соответствует 0,17 пикограмма на кубический метр (пг/м 3 ). Средняя концентрация радона в атмосфере составляет около 6 × 10−18 мольных процентов , или около 150 атомов в каждом миллилитре воздуха. [78] Радоновая активность всей атмосферы Земли возникает всего лишь из нескольких десятков граммов радона, последовательно замещаемых распадом более крупных количеств радия, тория и урана. [79]
Радон образуется в результате радиоактивного распада радия-226, который содержится в урановых рудах, фосфоритах, сланцах, магматических и метаморфических породах, таких как гранит, гнейс и сланец, и, в меньшей степени, в обычных горных породах, таких как известняк. [5] [80] Каждая квадратная миля поверхности почвы на глубине 6 дюймов (2,6 км 2 на глубину 15 см) содержит около 1 грамма радия, который выделяет радон в небольших количествах в атмосферу. [3] По оценкам, ежегодно во всем мире из почвы выделяется 2,4 миллиарда кюри (90 ЭБк) радона. [81] Это эквивалентно примерно 15,3 кг (34 фунта).
Концентрация радона может сильно различаться от места к месту. На открытом воздухе она колеблется от 1 до 100 Бк/м 3 , над океаном еще меньше (0,1 Бк/м 3 ). В пещерах, вентилируемых шахтах или плохо вентилируемых домах его концентрация достигает 20–2000 Бк/м 3 . [82]
Концентрация радона может быть намного выше в условиях горнодобывающей промышленности. Правила вентиляции предписывают поддерживать концентрацию радона в урановых рудниках на уровне ниже «рабочего уровня», при этом уровни 95-го процентиля достигают почти 3 WL (546 пКи 222 Rn на литр воздуха; 20,2 кБк/м 3 , замеры с 1976 по 1985 год). [3] Концентрация в воздухе в (невентилируемой) Галерее исцеления Гастейна составляет в среднем 43 кБк/м 3 (1,2 нКи/л) при максимальном значении 160 кБк/м 3 (4,3 нКи/л). [83]
Радон в основном появляется в ряду радий/ уран (цепочка распада) ( 222 Rn) и незначительно в ряду тория ( 220 Rn). Этот элемент естественным образом выделяется из земли и некоторых строительных материалов по всему миру, везде, где обнаруживаются следы урана или тория, и особенно в регионах с почвами, содержащими гранит или сланец , которые имеют более высокую концентрацию урана. Не все гранитные регионы склонны к высоким выбросам радона. Будучи редким газом, он обычно свободно мигрирует по разломам и фрагментированным грунтам и может накапливаться в пещерах или воде. Из-за очень короткого периода полураспада (четыре дня для 222 Rn) концентрация радона очень быстро снижается по мере удаления от места производства. Концентрация радона сильно меняется в зависимости от сезона и атмосферных условий. Например, было показано, что он накапливается в воздухе при метеорологической инверсии и слабом ветре. [84]
Высокие концентрации радона можно обнаружить в некоторых родниковых водах и горячих источниках. [85] Города Боулдер, Монтана ; Мисаса ; Бад-Кройцнах , Германия; и в Японии есть богатые радием источники, выделяющие радон. Чтобы классифицироваться как радоновая минеральная вода, концентрация радона должна быть выше 2 нКи/л (74 кБк/м 3 ). [86] Активность радоновой минеральной воды достигает 2 МБк/м 3 в Мерано и 4 МБк/м 3 в Лурисии (Италия). [83]
Концентрация естественного радона в атмосфере Земли настолько мала, что богатая радоном вода, контактирующая с атмосферой, будет постоянно терять радон в результате улетучивания . Следовательно, подземные воды имеют более высокую концентрацию 222 Rn, чем поверхностные воды , поскольку радон постоянно образуется в результате радиоактивного распада 226 Ra, присутствующего в горных породах. Аналогичным образом, насыщенная зона почвы часто имеет более высокое содержание радона, чем ненасыщенная зона, из-за диффузионных потерь в атмосферу. [87] [88]
В 1971 году Аполлон-15 пролетел на высоте 110 км (68 миль) над плато Аристарх на Луне и обнаружил значительный рост альфа-частиц , предположительно вызванный распадом 222 Rn. Присутствие 222 Rn было установлено позже на основе данных, полученных с помощью спектрометра альфа-частиц Lunar Prospector . [89]
Радон содержится в некоторых нефти . Поскольку радон имеет аналогичную кривую давления и температуры, что и пропан , а нефтеперерабатывающие заводы разделяют нефтехимические продукты в зависимости от их температуры кипения, трубопроводы, по которым поступает свежевыделенный пропан на нефтеперерабатывающих заводах, могут загрязняться из-за распада радона и его продуктов. [90]
Остатки нефтяной и газовой промышленности часто содержат радий и его дочерние элементы. Сульфатные отложения нефтяной скважины могут быть богаты радием, тогда как вода, нефть и газ из скважины часто содержат радон. Радон распадается с образованием твердых радиоизотопов, которые образуют покрытия на внутренней стороне трубопроводов. [90]
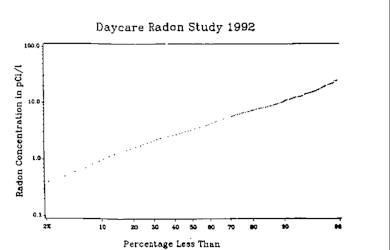

Высокие концентрации радона в домах были случайно обнаружены в 1985 году после того, как строгие радиационные испытания, проведенные на новой атомной электростанции в Лимерике, показали, что Стэнли Уотрас , инженер-строитель станции, был загрязнен радиоактивными веществами, хотя реактор никогда не работал. был подпитан. [91] Типичное бытовое облучение составляет примерно 100 Бк/м 3 (2,7 пКи/л) внутри помещений. Некоторый уровень радона можно обнаружить во всех зданиях. Радон в основном попадает в здание непосредственно из почвы через самый нижний уровень здания, соприкасающийся с землей. Высокий уровень радона в системе водоснабжения также может повысить уровень радона в воздухе внутри помещений. Типичными местами проникновения радона в здания являются трещины в прочных фундаментах и стенах, строительные швы, щели в подвесных полах и вокруг инженерных труб, полости внутри стен и системы водоснабжения. [12] Концентрация радона в одном и том же месте может отличаться в два/половину в течение часа. Также концентрация в одном помещении здания может существенно отличаться от концентрации в соседнем помещении. [3] Характеристики почвы жилых домов являются наиболее важным источником радона на первом этаже, а более высокая концентрация радона в помещениях наблюдается на нижних этажах. Большинство высоких концентраций радона наблюдалось в местах вблизи зон разломов ; следовательно, существование связи между скоростью выдоха из разломов и концентрацией радона в помещениях очевидно. [ нужна цитата ]
Распределение концентрации радона обычно различается в разных комнатах, а показания усредняются в соответствии с нормативными протоколами. Обычно предполагается, что концентрация радона в помещениях имеет логарифмически нормальное распределение на данной территории. [92] Таким образом, среднее геометрическое обычно используется для оценки «средней» концентрации радона на территории. [93]
Средняя концентрация колеблется от менее 10 Бк/м 3 до более 100 Бк/м 3 в некоторых европейских странах. [94]
Некоторые из самых высоких радоновых опасностей в США наблюдаются в Айове и в горных районах Аппалачей на юго-востоке Пенсильвании. [95] В Айове самая высокая средняя концентрация радона в США из-за значительного оледенения , которое размололо гранитные породы Канадского щита и отложило его в виде почв, составляющих богатые сельскохозяйственные угодья Айовы. [96] Многие города штата, такие как Айова-Сити , приняли требования к устойчивому к радону строительству новых домов. Вторые по величине показатели в Ирландии были обнаружены в офисных зданиях в ирландском городе Мэллоу, графство Корк , что вызвало у местных опасения относительно рака легких. [97]
В некоторых местах урановые хвостохранилища использовались для захоронения отходов , а затем застраивались, что привело к возможному увеличению воздействия радона. [3]
Поскольку радон — бесцветный газ без запаха, единственный способ узнать, сколько его содержится в воздухе или воде, — это провести тесты. В США наборы для тестирования на радон доступны в розничных магазинах, например, в хозяйственных магазинах, для домашнего использования, а тестирование можно провести у лицензированных специалистов, которые часто являются домашними инспекторами . Усилия по снижению уровня радона в помещениях называются смягчением воздействия радона . В США Агентство по охране окружающей среды рекомендует проверять все дома на наличие радона. В Великобритании в соответствии с Системой оценки здоровья и безопасности жилья (HHSRS) владельцы недвижимости обязаны оценивать потенциальные риски и опасности для здоровья и безопасности в жилой недвижимости. [98]
Радон получают как побочный продукт переработки урансодержащих руд после перевода в 1%-ные растворы соляной или бромистоводородной кислот . Газовая смесь, выделенная из растворов, содержит H
2, О
2, He, Rn, CO
2, Ч
2О и углеводороды . Смесь очищают, пропуская ее через медь при температуре 993 К (720 ° C; 1328 ° F), чтобы удалить H.
2и О
2, а затем КОН и P2О5используются для удаления кислот и влаги путем сорбции . Радон конденсируют жидким азотом и очищают от остаточных газов сублимацией . [99]
Коммерциализация радона регулируется, но он доступен в небольших количествах для калибровки систем измерения 222 Rn по цене в 2008 году почти 6000 долларов США (что эквивалентно 8491 доллару США в 2023 году) за миллилитр раствора радия (который содержит всего около 15 пикограмм фактического содержания радона в любой момент времени). [100] Радон производится раствором радия-226 (период полураспада 1600 лет). Радий-226 распадается с испусканием альфа-частиц, образуя радон, который накапливается над образцами радия-226 со скоростью около 1 мм 3 /день на грамм радия; равновесие достигается быстро, и радон образуется в устойчивом потоке с активностью, равной активности радия (50 Бк). Газообразный 222 Rn (период полураспада около четырех дней) выходит из капсулы путем диффузии . [101]
Одной из форм шарлатанства начала 20-го века было лечение болезней в радиотории . [106] Это была небольшая герметичная комната, в которой пациенты подвергались воздействию радона из-за его «лечебного эффекта». Канцерогенная природа радона вследствие его ионизирующего излучения стала очевидна позднее. Радиоактивность радона, повреждающая молекулы, использовалась для уничтожения раковых клеток [107] , но она не улучшает здоровье здоровых клеток. [ нужна цитата ] Ионизирующее излучение вызывает образование свободных радикалов , что приводит к повреждению клеток , вызывая повышенный уровень заболеваний, включая рак .
Было высказано предположение, что воздействие радона смягчает аутоиммунные заболевания, такие как артрит, посредством процесса, известного как радиационный гормезис . [108] [109] В результате в конце 20-го и начале 21-го века «рудники здоровья», созданные в Басине, штат Монтана , привлекли людей, ищущих облегчения от таких проблем со здоровьем, как артрит, за счет ограниченного воздействия радиоактивной шахтной воды и радона. Такая практика не рекомендуется из-за хорошо задокументированных пагубных последствий высоких доз радиации на организм. [110]
Радиоактивные водяные ванны применялись с 1906 года в Яхимове (Чехия), но еще до открытия радона они использовались в Бад-Гаштайне (Австрия). Богатые радием источники также используются в традиционных японских онсэнах в Мисасе , префектура Тоттори . Питьевая терапия применяется в Бад-Брамбахе , Германия, и в начале 20-го века воду из источников, содержащую радон, разливали в бутылки и продавали (к тому времени, когда она попала к потребителям, в этой воде почти не было радона из-за короткого содержания радона) -жизнь). [111] Ингаляционная терапия проводится в Гаштайнер-Хайльстоллене, Австрия; Сверадув-Здруй , Чернява-Здруй, Ковары , Лендек-Здруй , Польша; Харгита Бай , Румыния; и Боулдер, Монтана . В США и Европе есть несколько «радоновых спа», где люди сидят в течение нескольких минут или часов в атмосфере с высоким содержанием радона, например, в Бад-Шмидеберге , Германия. [109] [112]
Радон производился в промышленных масштабах для использования в лучевой терапии, но по большей части был заменен радионуклидами, полученными в ускорителях частиц и ядерных реакторах . Радон использовался в имплантируемых семенах, сделанных из золота или стекла, которые в основном использовались для лечения рака, известного как брахитерапия . Золотые семена были изготовлены путем заполнения длинной трубки радоном, накачиваемым из источника радия, а затем трубка была разделена на короткие секции путем обжима и разрезания. Слой золота удерживает радон внутри и отфильтровывает альфа- и бета-излучение, позволяя при этом уйти гамма-лучам (которые убивают больные ткани). Активность может варьироваться от 0,05 до 5 милликюри на семя (от 2 до 200 МБк). [107] Гамма-лучи производятся радоном и первыми короткоживущими элементами его цепи распада ( 218 Po, 214 Pb, 214 Bi, 214 Po).
После 11 периодов полураспада (42 дня) радиоактивность радона достигает 1/2048 от исходного уровня. На этом этапе преобладающая остаточная активность затравки обусловлена продуктом распада радона 210 Pb, период полураспада которого (22,3 года) в 2000 раз превышает период полураспада радона и его потомков 210 Bi и 210 Po.
Выделение радона из почвы зависит от типа почвы и содержания урана на поверхности, поэтому концентрации радона на открытом воздухе можно в ограниченной степени использовать для отслеживания воздушных масс . Этот факт был использован некоторыми учеными-атмосферниками ( Радоновый шторм ). Из-за быстрой потери радона в воздухе и сравнительно быстрого распада радон используется в гидрологических исследованиях, изучающих взаимодействие между грунтовыми водами и ручьями . Любая значительная концентрация радона в ручье является хорошим индикатором локального поступления подземных вод.
Концентрация радона в почве использовалась экспериментальным способом для картирования погребенных близко расположенных геологических разломов, поскольку концентрации радона обычно выше над разломами. [113] Точно так же он нашел ограниченное применение при поиске геотермических градиентов . [114]
Некоторые исследователи исследовали изменения концентрации радона в грунтовых водах для прогнозирования землетрясений . [115] [116] [117] Увеличение содержания радона было отмечено перед землетрясениями в Ташкенте в 1966 году [118] и Миндоро в 1994 году [117] . Период полураспада радона составляет примерно 3,8 дня, а это означает, что его можно обнаружить только вскоре после того, как он образовался в цепочке радиоактивного распада. По этой причине была выдвинута гипотеза, что увеличение концентрации радона происходит из-за образования новых подземных трещин, которые позволят увеличить циркуляцию грунтовых вод, вымывая радон. Небезосновательно можно предположить, что образование новых трещин предшествует сильным землетрясениям. В 1970-х и 1980-х годах научные измерения выбросов радона вблизи разломов показали, что землетрясения часто происходили без сигнала радона, а радон часто обнаруживался без последующего землетрясения. Затем многие отвергли его как ненадежный индикатор. [119] По состоянию на 2009 год НАСА исследовало его как возможного предшественника . [120]
Радон является известным загрязнителем, выбрасываемым геотермальными электростанциями, поскольку он присутствует в материале, выкачиваемом из глубоких подземных зон. Он быстро рассеивается, и в различных исследованиях не было выявлено никакой радиологической опасности. Кроме того, типичные системы повторно закачивают материал глубоко под землю, а не выбрасывают его на поверхность, поэтому его воздействие на окружающую среду минимально. [121] Однако то же самое можно сказать и о тривиальных выбросах от действующих атомных электростанций . [ нужна цитата ]
В 1940-х и 1950-х годах радон использовался для промышленной рентгенографии . [122] [123] Другие источники рентгеновского излучения, которые стали доступны после Второй мировой войны, быстро заменили радон для этого применения, поскольку они были дешевле и имели меньшую опасность альфа-излучения .
Продукты распада радона-222 были классифицированы Международным агентством по изучению рака как канцерогенные для человека [124] , а поскольку газ можно вдыхать, рак легких вызывает особую озабоченность у людей, подвергающихся длительному воздействию повышенных уровней радона. периоды. В 1940-х и 1950-х годах, когда стандарты безопасности, требующие дорогостоящей вентиляции в шахтах, не были широко внедрены, [125] воздействие радона было связано с раком легких среди некурящих шахтеров, добывающих уран и другие твердые горные породы на территории современной Чешской Республики, и позже среди шахтеров юго-запада США [126] [127] [128] и Южной Австралии . [129] Несмотря на то, что об этих опасностях было известно в начале 1950-х годов, [130] эти профессиональные опасности оставались плохо управляемыми на многих шахтах до 1970-х годов. В этот период несколько предпринимателей открыли для широкой публики бывшие урановые рудники в США и рекламировали предполагаемую пользу для здоровья от дыхания радоном под землей. Заявленные преимущества для здоровья включали облегчение боли, проблем с носовыми пазухами, астмы и артрита, [131] [132] но это оказалось ложным [ нужна цитация ] , и правительство запретило такую рекламу в 1975 году. [133]
С тех пор вентиляция и другие меры использовались для снижения уровня радона в наиболее пострадавших шахтах, которые продолжают работать. В последние годы среднегодовое воздействие на шахтеров урана упало до уровней, аналогичных концентрациям, вдыхаемым в некоторых домах. Это снизило риск профессионального рака, вызванного радоном, хотя проблемы со здоровьем могут сохраняться как у тех, кто в настоящее время работает на пострадавших шахтах, так и у тех, кто работал там в прошлом. [134] Поскольку относительный риск для шахтеров снизился, уменьшилась и способность выявлять избыточные риски среди этой группы населения. [135]
Источником радона также могут быть остатки переработки урановой руды. Радон, образующийся из-за высокого содержания радия в открытых отвалах и хвостохранилищах, может легко выбрасываться в атмосферу и поражать людей, живущих поблизости. [136]
Помимо рака легких, исследователи предположили, что из-за воздействия радона может повыситься риск развития лейкемии . Эмпирическая поддержка исследований среди населения в целом противоречива, а исследование шахтеров урана выявило корреляцию между воздействием радона и хроническим лимфоцитарным лейкозом . [137]
Шахтеры (а также рабочие по переработке и транспортировке руды), которые работали в урановой промышленности США в период с 1940-х по 1971 год, могут иметь право на компенсацию в соответствии с Законом о компенсации за радиационное воздействие (RECA). Выжившие родственники также могут подать заявление в случае смерти бывшего работавшего лица.
Не только урановые рудники страдают от повышенного уровня радона. Особенно страдают угольные шахты, поскольку уголь может содержать больше урана и тория, чем коммерчески действующие урановые рудники.
Длительное воздействие более высоких концентраций радона связано с увеличением заболеваемости раком легких. [84] С 1999 года во всем мире проводятся исследования по оценке концентрации радона. Только в Соединенных Штатах зафиксировано, что средние значения составляют не менее 40 Бк/м 3 . Штек и др. провел исследование различий между радоном внутри и снаружи помещений в Айове и Миннесоте. Более высокая радиация была обнаружена в населенном регионе, а не в незаселенных регионах Центральной Америки в целом. В некоторых округах на северо-западе Айовы и юго-западе Миннесоты концентрация радона на открытом воздухе превышает среднюю по стране концентрацию радона в помещениях. [84] Несмотря на выше среднего, цифры в Миннесоте и Айове были исключительно близкими, независимо от расстояния. Точные исследования воздействия радона необходимы для дальнейшего понимания проблем, которые воздействие радона может иметь для общества. Текущие исследования подтверждают связь между воздействием радона и плохими последствиями для здоровья (например, повышенным риском рака легких), но дальнейшие исследования могут поддержать более строгие ограничения на радон как внутри, так и за пределами жилых домов. [84]
Воздействие радона (в основном дочерних элементов радона) было связано с раком легких в многочисленных исследованиях «случай-контроль», проведенных в США, Европе и Китае. Ежегодно в США происходит около 21 000 смертей (0,0063% населения в 333 миллиона человек) из-за рака легких, вызванного радоном. [10] [138] В Словении, стране с высокой концентрацией радона, ежегодно из-за радона умирают около 120 человек (0,0057% населения в 2,11 миллиона человек). [139] [140] Одно из наиболее полных исследований радона, проведенное в США эпидемиологом Р. Уильямом Филдом и его коллегами, выявило увеличение риска рака легких на 50% даже при длительном воздействии при уровне действия EPA 4 пКи/л. Объединенные анализы Северной Америки и Европы еще раз подтверждают эти выводы. [141] Однако дискуссия о противоположных результатах все еще продолжается, [142] [143] [144] особенно в ретроспективном исследовании «случай-контроль» 2008 года по риску рака легких, которое показало существенное снижение заболеваемости раком при концентрациях радона от 50 до 123 Бк. /м 3 . [145]
Большинство моделей воздействия радона в жилых помещениях основаны на исследованиях шахтеров, и более желательны прямые оценки рисков, которым подвергаются домовладельцы. [134] Из-за трудностей измерения риска, связанного с радоном по сравнению с курением, в моделях его воздействия часто использовались их.
Агентство по охране окружающей среды считает радон второй по значимости причиной рака легких и ведущей экологической причиной смертности от рака, причем первой из них является курение . [146] Другие пришли к аналогичным выводам в отношении Великобритании [134] и Франции. [147] Воздействие радона в домах и офисах может быть вызвано некоторыми подземными горными породами, а также некоторыми строительными материалами (например, некоторыми гранитами). Наибольший риск воздействия радона возникает в зданиях, которые герметичны, недостаточно вентилируются, имеют негерметичность фундамента, пропускающую воздух из грунта в подвалы и жилые помещения.
Торон ( 220 Rn) был измерен в сравнительно высоких концентрациях в зданиях с земляной архитектурой, таких как традиционные фахверковые дома и современные дома с глиняной отделкой стен. Из-за короткого периода полураспада торон в качестве источника встречается только вблизи земляных поверхностей, тогда как его потомство можно обнаружить в воздухе помещений таких зданий. Таким образом, радиационное облучение происходит в любом месте внутри таких домов. Исследование обнаружило, что в различных жилищах с земляной архитектурой в Германии годовые дозы внутреннего облучения из-за вдыхания торона и его потомков достигают нескольких миллизивертов . [148]
В 2009 году ВОЗ представила рекомендуемый референтный уровень (национальный референтный уровень) 100 Бк/м 3 для радона в жилых помещениях. В рекомендации также сказано, что там, где это невозможно, в качестве наивысшего уровня следует выбрать 300 Бк/м 3 . Национальный эталонный уровень не должен быть пределом, а должен представлять собой максимально допустимую среднегодовую концентрацию радона в жилом помещении. [149]
Допустимая концентрация радона в доме варьируется в зависимости от организации, дающей рекомендации. Например, Агентство по охране окружающей среды рекомендует принимать меры при концентрациях всего лишь 74 Бк/м 3 (2 пКи/л) [76] , а Европейское Союз рекомендует принимать меры, когда концентрация достигает 400 Бк/м 3 (11 пКи/л) для старых домов и 200 Бк/м 3 (5 пКи/л) для новых. [150] 8 июля 2010 года Агентство по охране здоровья Великобритании выпустило новую рекомендацию, устанавливающую «целевой уровень» в 100 Бк/м 3 при сохранении «уровня действия» на уровне 200 Бк/м 3 . [151] Подобные уровни (как и в Великобритании) публикуются Норвежским управлением по радиационной и ядерной безопасности (DSA) [152] с максимальным пределом для школ, детских садов и новых жилых домов, установленным на уровне 200 Бк/м 3 , где 100 Бк/м 3 установлен как уровень действия. [153] Во всех новых домах следует принимать профилактические меры против накопления радона.
Результаты эпидемиологических исследований показывают, что риск рака легких увеличивается при воздействии радона в жилых помещениях. Хорошо известным примером источника ошибки является курение, основной фактор риска рака легких. По оценкам, в США курение сигарет является причиной от 80% до 90% всех случаев рака легких. [154]
По данным EPA, риск рака легких для курильщиков значителен из-за синергетического воздействия радона и курения. В этой группе населения около 62 человек из 1000 умрут от рака легких по сравнению с 7 людьми из 1000 среди людей, которые никогда не курили. [10] Не исключено, что риск некурящих в первую очередь следует объяснять воздействием радона.
Радон, как и другие известные или предполагаемые внешние факторы риска рака легких, представляет угрозу для курильщиков и бывших курильщиков. Это было продемонстрировано европейским объединенным исследованием. [155] В комментарии [155] к объединенному исследованию говорится: «Неуместно говорить просто о риске, связанном с радоном в домах. Риск связан с курением, усугубляемым синергическим эффектом радона на курильщиков. Без курения эффект кажется настолько малым, что кажется незначительным».
Согласно европейскому объединенному исследованию, существует разница в риске гистологических подтипов рака легких и воздействия радона. Мелкоклеточная карцинома легких , которая имеет высокую корреляцию с курением, имеет более высокий риск после воздействия радона. Для других гистологических подтипов, таких как аденокарцинома , тип, который в первую очередь поражает некурящих, риск воздействия радона оказывается ниже. [155] [156]
Исследование радиации при лучевой терапии после мастэктомии показывает, что необходимо разработать простые модели, ранее использовавшиеся для оценки комбинированных и отдельных рисков от радиации и курения. [157] Это также подтверждается новым обсуждением метода расчета, линейной беспороговой модели , которая обычно используется. [158]
Исследование 2001 года, в котором приняли участие 436 некурящих с раком легких и контрольная группа из 1649 некурящих без рака легких, показало, что воздействие радона увеличивает риск рака легких у некурящих. Группа, которая подвергалась воздействию табачного дыма дома, имела гораздо более высокий риск, в то время как у тех, кто не подвергался пассивному курению, не было выявлено какого-либо повышенного риска с увеличением воздействия радона. [159]
Эффекты радона при попадании в организм неизвестны, хотя исследования показали, что его биологический период полураспада колеблется от 30 до 70 минут, при этом 90% выводится за 100 минут. В 1999 году Национальный исследовательский совет США исследовал проблему радона в питьевой воде. Риск, связанный с проглатыванием, считался практически незначительным. [160] Вода из подземных источников может содержать значительное количество радона в зависимости от условий окружающей породы и почвы, тогда как поверхностные источники обычно этого не делают. [161]
Основная важность понимания потока 222 Rn из океана заключается в том, чтобы знать, что увеличение использования радона также циркулирует и увеличивается в атмосфере. Концентрации на поверхности океана обмениваются внутри атмосферы, вызывая увеличение содержания 222 Rn через границу раздела воздух-море. [162] Хотя исследованные районы были очень мелководными, дополнительные измерения в самых разных прибрежных режимах должны помочь определить природу наблюдаемого 222 Rn. [162] Радон не только попадает в организм с питьевой водой, но и выделяется из воды при повышении температуры, понижении давления и при аэрации воды. Оптимальные условия для выделения и воздействия радона создавались во время принятия душа. Вода с концентрацией радона 10 4 пКи/л может увеличить концентрацию радона в воздухе внутри помещений на 1 пКи/л при нормальных условиях. [80]


Существуют относительно простые тесты на радон. В некоторых странах эти тесты методично проводятся в районах известных систематических опасностей. Устройства обнаружения радона имеются в продаже. Цифровые детекторы радона обеспечивают постоянные измерения, выдавая на цифровой дисплей как ежедневные, еженедельные, краткосрочные, так и долгосрочные средние значения. Устройства для кратковременного тестирования радона, используемые для целей первоначального скрининга, недороги, а в некоторых случаях бесплатны. Существуют важные протоколы проведения краткосрочных тестов на радон, и их строгое соблюдение необходимо обязательно. В комплект входит коллектор, который пользователь подвешивает на самом нижнем жилом этаже дома на срок от двух до семи дней. Затем пользователь отправляет коллектор в лабораторию для анализа. Также доступны долгосрочные комплекты, рассчитанные на сбор средств на срок до одного года и более. Тестовый комплект для открытой местности может проверить выбросы радона с земли до начала строительства. [10] Концентрация радона может меняться ежедневно, и точные оценки воздействия радона требуют долгосрочных средних измерений радона в местах, где человек проводит значительное количество времени. [163]
Уровни радона колеблются естественным образом из-за таких факторов, как переменчивые погодные условия, поэтому первоначальный тест может не дать точную оценку среднего уровня радона в доме. Уровни радона максимальны в самое прохладное время дня, когда перепады давления самые большие. [80] Таким образом, высокий результат (более 4 пКи/л) оправдывает повторение теста, прежде чем предпринимать более дорогостоящие проекты по снижению выбросов. Измерения между 4 и 10 пКи/л требуют проведения долгосрочного теста на радон. Измерения выше 10 пКи/л требуют только проведения еще одного краткосрочного теста, чтобы меры по снижению выбросов не были неоправданно отложены. Покупателям недвижимости рекомендуется отложить покупку или отказаться от нее, если продавцу не удалось снизить концентрацию радона до 4 пКи/л или ниже. [10]
Поскольку период полураспада радона составляет всего 3,8 дня, удаление или изоляция источника значительно снизит опасность в течение нескольких недель. Еще один метод снижения уровня радона — изменить вентиляцию здания. Как правило, концентрация радона в помещении увеличивается по мере снижения интенсивности вентиляции. [3] В хорошо вентилируемых местах концентрация радона имеет тенденцию соответствовать значениям на открытом воздухе (обычно 10 Бк/м 3 в диапазоне от 1 до 100 Бк/м 3 ). [10]
Четыре основных способа уменьшения количества радона, накапливающегося в доме: [10] [164]
По данным EPA, [10] метод снижения уровня радона «...в основном используется с помощью системы вентиляционных труб и вентилятора, который вытягивает радон из-под дома и выбрасывает его наружу», что также называется разгерметизацией подплиты. , активная разгерметизация грунта или подсасывание грунта. Обычно уровень радона в помещениях можно уменьшить за счет разгерметизации подпанелей и выведения такого насыщенного радоном воздуха на улицу, вдали от окон и других проемов зданий. «[Агентство по охране окружающей среды] обычно рекомендует методы, которые предотвращают проникновение радона. Например, всасывание почвы предотвращает попадание радона в ваш дом, вытягивая радон из-под дома и выпуская его через трубу или трубы в воздух над домом. дома, где он быстро разбавляется» и «Агентство по охране окружающей среды не рекомендует использовать только герметизацию для снижения уровня радона, потому что само по себе герметизация не продемонстрировала значительного или последовательного снижения уровня радона». [165]
Системы вентиляции с положительным давлением можно комбинировать с теплообменником для рекуперации энергии в процессе обмена воздуха с наружным воздухом, и простое выведение воздуха из подвала наружу не обязательно является жизнеспособным решением, поскольку это может фактически привести к попаданию газа радона в жилище. Дома, построенные на подвале, могут получить выгоду от установки коллектора радона под «радоновым барьером» (листом пластика, закрывающим подвал). [10] [166] В отношении подвальных помещений Агентство по охране окружающей среды заявляет: «Эффективный метод снижения уровня радона в домах с подвальными помещениями включает в себя покрытие земляного пола пластиковым листом высокой плотности. Вентиляционная труба и вентилятор используются для вытягивания радона из под листом и выбрасывайте его на улицу. Эта форма всасывания почвы называется подмембранным всасыванием, и при правильном применении она является наиболее эффективным способом снижения уровня радона в подвальных помещениях домов». [165]
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка ){{cite book}}: |journal=игнорируется ( помощь )