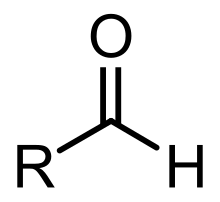
В органической химии альдегид ( / ˈæ l d ɪ h aɪ d / ) — органическое соединение , содержащее функциональную группу структуры R -CH=O . [1] Сама функциональная группа (без боковой цепи «R» ) может называться альдегидом , но также может быть классифицирована как формильная группа . Альдегиды являются общим мотивом во многих химических веществах, важных в технологии и биологии. [2] [3]
Молекулы альдегидов имеют центральный атом углерода, который соединен двойной связью с кислородом, одинарной связью с водородом и еще одной одинарной связью с третьим заместителем, которым является углерод или, в случае формальдегида, водород. Центральный углерод часто описывают как sp 2 -гибридизованный . Альдегидная группа несколько полярна . Длина связи C=O составляет около 120–122 пикометров . [4]
Альдегиды обладают разнообразными свойствами, зависящими от остальной части молекулы. Альдегиды меньшего размера более растворимы в воде, формальдегид и ацетальдегид — полностью. Летучие альдегиды имеют резкий запах.
Альдегиды можно идентифицировать спектроскопическими методами. С помощью ИК-спектроскопии они обнаруживают сильную полосу ν CO около 1700 см -1 . В их спектрах ЯМР 1 Н формильный водородный центр поглощает вблизи δ H от 9,5 до 10, что является отличительной частью спектра. Этот сигнал показывает характерное взаимодействие с любыми протонами α-углерода с небольшой константой взаимодействия, обычно менее 3,0 Гц. Спектры ЯМР 13 С альдегидов и кетонов дают подавленный (слабый), но отчетливый сигнал при δ C от 190 до 205.
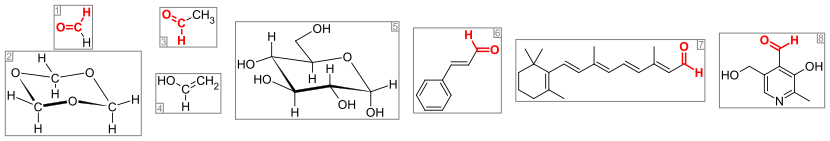
Важные альдегиды и родственные соединения. Альдегидная группа (или формильная группа ) окрашена в красный цвет. Слева направо: (1) формальдегид и (2) его тример 1,3,5-триоксан , (3) ацетальдегид и (4) его енолвиниловый спирт , (5) глюкоза (форма пиранозы в виде α- D -глюкопиранозы), (6) ароматизатор коричный альдегид , (7) ретиналь , который образует фоторецепторы опсинов , и (8) витамин пиридоксаль .
Следы многих альдегидов содержатся в эфирных маслах и часто способствуют их приятному запаху, например коричный альдегид , кинза и ванилин . Возможно, из-за высокой реакционной способности формильной группы альдегиды не распространены в некоторых природных строительных блоках: аминокислотах, нуклеиновых кислотах, липидах. Однако большинство сахаров являются производными альдегидов. Эти альдозы существуют в виде полуацеталей , своего рода замаскированной формы исходного альдегида. Например, в водном растворе лишь небольшая часть глюкозы существует в виде альдегида.
Существует несколько методов получения альдегидов, [2] но доминирующей технологией является гидроформилирование . [5] Показательным является получение бутиральдегида гидроформилированием пропена :
Альдегиды обычно образуются при окислении спиртов . В промышленности формальдегид в больших масштабах получают путем окисления метанола. [6] Кислород является предпочтительным реагентом, поскольку он «зеленый» и дешевый. В лаборатории используются более специализированные окислители , но популярностью пользуются реагенты хрома(VI). Окисления можно добиться нагреванием спирта с подкисленным раствором дихромата калия . В этом случае избыток дихромата будет дополнительно окислять альдегид до карбоновой кислоты , поэтому либо альдегид отгоняют по мере его образования (если он летуч ), либо используются более мягкие реагенты, такие как PCC . [7]
Окисление первичных спиртов с образованием альдегидов может быть достигнуто в более мягких условиях, не содержащих хром, с использованием таких методов или реагентов, как кислота IBX , периодинан Десса-Мартина , окисление Сверна , TEMPO . или окисление Оппенауэра . [ нужна цитата ]
Другим важным для промышленности путем окисления является процесс Вакера , при котором этилен окисляется до ацетальдегида в присутствии медных и палладиевых катализаторов (ацетальдегид также производится в больших масштабах путем гидратации ацетилена).
В лабораторных масштабах α-гидроксикислоты используются в качестве предшественников для получения альдегидов посредством окислительного расщепления . [8] [9]
Альдегиды участвуют во многих реакциях. [2] С промышленной точки зрения важными реакциями являются:
Из-за резонансной стабилизации сопряженного основания α-водород в альдегиде является слабокислотным с pKa около 17. Однако обратите внимание, что он гораздо более кислый, чем алкановый или эфирный водород, у которого pKa около 50 . приблизительно и даже более кислый, чем кетон α-водород, у которого p K a около 20. Это подкисление α-водорода в альдегиде объясняется:
Сам формильный протон не подвергается депротонированию.
Альдегиды (за исключением тех, которые не содержат альфа-углерода или протонов на альфа-углероде, таких как формальдегид и бензальдегид) могут существовать либо в кето-, либо в енольном таутомере . Кето-енольная таутомерия катализируется кислотой или основанием. В нейтральном растворе енол является миноритарным таутомером, меняющим свое направление несколько раз в секунду. [14] Но он становится доминирующим таутомером в растворах сильных кислот или оснований, а енолизированные альдегиды подвергаются нуклеофильной атаке в α-положении . [15] [16]
Формильная группа легко восстанавливается до первичного спирта ( -CH 2 OH ). Обычно это преобразование осуществляется путем каталитического гидрирования либо напрямую, либо путем трансфертного гидрирования . Также популярно стехиометрическое восстановление, которое можно осуществить с помощью боргидрида натрия .
Формильная группа легко окисляется до соответствующей карбоксильной группы ( -СООН ). Предпочтительным окислителем в промышленности является кислород или воздух. В лаборатории популярные окислители включают перманганат калия , азотную кислоту , оксид хрома (VI) и хромовую кислоту . Комбинация диоксида марганца , цианида , уксусной кислоты и метанола преобразует альдегид в метиловый эфир . [2]
Другая реакция окисления лежит в основе теста с серебряным зеркалом . В этом тесте альдегид обрабатывают реактивом Толленса , который готовят путем добавления капли раствора гидроксида натрия в раствор нитрата серебра с образованием осадка оксида серебра(I), а затем добавления разбавленного раствора аммиака , достаточного для повторного растворения. осаждают в водном растворе аммиака с образованием комплекса [Ag(NH 3 ) 2 ] + . Этот реагент превращает альдегиды в карбоновые кислоты, не разрушая двойные связи углерод-углерод. Название « тест с серебряным зеркалом» возникло потому, что в результате этой реакции образуется осадок серебра, присутствие которого можно использовать для проверки наличия альдегида.
Для дальнейшей реакции окисления в качестве теста используется реактив Фелинга . Комплексные ионы Cu 2+ восстанавливаются до осадка Cu 2 O красно - кирпичного цвета .
Если альдегид не может образовывать енолят (например, бензальдегид ), добавление сильного основания вызывает реакцию Канниццаро . Эта реакция приводит к диспропорционированию , в результате чего образуется смесь спирта и карбоновой кислоты.
Нуклеофилы легко присоединяются к карбонильной группе. В продукте карбонильный углерод становится sp 3 -гибридизированным, связываясь с нуклеофилом, а кислородный центр протонируется:
Во многих случаях молекула воды удаляется после присоединения; в этом случае реакция классифицируется как реакция присоединения - отщепления или присоединения - конденсации . Существует множество вариантов реакций нуклеофильного присоединения.
В реакции ацетализации в кислых или основных условиях к карбонильной группе присоединяется спирт и переносится протон с образованием полуацеталя . В кислых условиях полуацеталь и спирт могут вступать в реакцию с образованием ацеталя и воды. Простые полуацетали обычно нестабильны, хотя циклические, такие как глюкоза, могут быть стабильными. Ацетали стабильны, но в присутствии кислоты превращаются в альдегид. Альдегиды могут реагировать с водой с образованием гидратов R -CH(OH) 2 . Эти диолы стабильны, когда присутствуют сильные электроноакцепторные группы , как в хлоралгидрате . Механизм образования идентичен образованию гемиацеталя.
При алкилимино-де-оксо-бизамещении первичный или вторичный амин присоединяется к карбонильной группе, и протон переносится от атома азота к атому кислорода с образованием карбиноламина . В случае первичного амина молекула воды может быть удалена из промежуточного карбиноламина с образованием имина или его тримера, гексагидротриазина. Эта реакция катализируется кислотой. Гидроксиламин ( NH 2 OH ) также может присоединяться к карбонильной группе. После удаления воды образуется оксим . Производное аммиака формы H 2 NNR 2 , такое как гидразин ( H 2 NNH 2 ) или 2,4-динитрофенилгидразин , также может быть нуклеофилом и после удаления воды приводит к образованию гидразона , который обычно имеет оранжевую кристаллическую форму. твердые вещества. Эта реакция составляет основу теста на альдегиды и кетоны . [17]
Цианогруппа в HCN может присоединяться к карбонильной группе с образованием циангидринов R - CH(OH)CN . В этой реакции ион CN- является нуклеофилом , который атакует частично положительный атом углерода карбонильной группы . Механизм включает передачу пары электронов от двойной связи карбонильной группы к атому кислорода, оставляя его одинарной связью с углеродом и придавая атому кислорода отрицательный заряд. Этот промежуточный ион быстро реагирует с H + , например, из молекулы HCN, с образованием спиртовой группы циангидрина.
Металлоорганические соединения , такие как литийорганические реагенты , реактивы Гриньяра или ацетилиды , подвергаются реакциям нуклеофильного присоединения , в результате чего образуется замещенная спиртовая группа. Связанные реакции включают присоединение станнана , реакции Барбье и реакцию Нодзаки-Хиямы-Киши .
В альдольной реакции еноляты металлов кетонов , эфиров , амидов и карбоновых кислот присоединяются к альдегидам с образованием β-гидроксикарбонильных соединений ( альдолов ) . Дегидратация, катализируемая кислотой или основанием, затем приводит к образованию α,β-ненасыщенных карбонильных соединений. Комбинация этих двух стадий известна как альдольная конденсация .
Реакция Принса происходит , когда нуклеофильный алкен или алкин реагирует с альдегидом в качестве электрофила. Продукт реакции Принса варьируется в зависимости от условий реакции и используемых субстратов.
Альдегиды обычно образуют с бисульфитами «соединения присоединения» :
Эта реакция используется в качестве теста на альдегиды и полезна для разделения или очистки альдегидов. [17] [18]
Диальдегид – органическое химическое соединение с двумя альдегидными группами . В номенклатуре диальдегидов имеется окончание -диальдегид или иногда -диальдегид . Короткие алифатические диальдегиды иногда называют в честь двухосновной кислоты , из которой они могут быть получены. Примером является бутандиаль , который еще называют сукцинальдегидом (от янтарной кислоты ).
Некоторые альдегиды являются субстратами для ферментов альдегиддегидрогеназы , которые метаболизируют альдегиды в организме. Некоторые альдегиды обладают токсичностью , вызывающей нейродегенеративные заболевания, болезни сердца и некоторые виды рака . [19]
Из всех альдегидов формальдегид производится в наибольших масштабах.6 000 000 тонн в год . В основном он используется в производстве смол в сочетании с мочевиной , меламином и фенолом (например, бакелитом ). Это предшественник метилендифенилдиизоцианата ( «MDI»), предшественника полиуретанов . [6] Вторым основным альдегидом является бутиральдегид , из которого около2 500 000 тонн в год получают методом гидроформилирования . Это основной предшественник 2-этилгексанола , который используется в качестве пластификатора . [20] Когда-то ацетальдегид был доминирующим продуктом, но уровень производства упал до менее чем1 000 000 тонн в год , поскольку он в основном служил предшественником уксусной кислоты , которую сейчас получают карбонилированием метанола . Многие другие альдегиды находят коммерческое применение, часто в качестве предшественников спиртов, так называемых оксоспиртов , которые используются в моющих средствах. Некоторые альдегиды производятся лишь в небольших масштабах (менее 1000 тонн в год) и используются в качестве ингредиентов ароматизаторов и духов , таких как Chanel № 5 . К ним относятся коричный альдегид и его производные, цитраль и лилиал .
Общие названия альдегидов не строго соответствуют официальным рекомендациям, например тем, которые рекомендованы ИЮПАК , но эти правила полезны. ИЮПАК предписывает следующую номенклатуру альдегидов: [21] [22] [23]
Слово альдегид было придумано Юстусом фон Либихом как сокращение латинского al cohol dehyd rogenatus (дегидрированный спирт). [24] [25] В прошлом альдегиды иногда называли в честь соответствующих спиртов , например, винный альдегид вместо ацетальдегида . ( Vinous — от латинского vinum «вино», традиционного источника этанола , родственного винилу .)
Термин формильная группа происходит от латинского слова formica «муравей». Это слово можно узнать в простейшем альдегиде — формальдегиде и в простейшей карбоновой кислоте — муравьиной кислоте .