Азотная кислота – неорганическое соединение формулы HNO3 . _ Это очень агрессивная минеральная кислота . [6] Соединение бесцветно, но образцы со временем имеют тенденцию приобретать желтый оттенок из-за разложения на оксиды азота . Большая часть коммерчески доступной азотной кислоты имеет концентрацию в воде 68%. Когда раствор содержит более 86% HNO 3 , его называют дымящей азотной кислотой . В зависимости от количества присутствующего диоксида азота дымящая азотная кислота далее характеризуется как красная дымящая азотная кислота при концентрации выше 86% или белая дымящая азотная кислота при концентрации выше 95%.
Азотная кислота является основным реагентом, используемым для нитрования – присоединения нитрогруппы , обычно к органической молекуле . Хотя некоторые образующиеся нитросоединения являются взрывчатыми веществами , чувствительными к ударам и температуре , некоторые из них достаточно стабильны, чтобы их можно было использовать в боеприпасах и при сносе зданий, в то время как другие еще более стабильны и используются в качестве пигментов в чернилах и красителях. Азотная кислота также широко используется в качестве сильного окислителя .
Считается, что открытие минеральных кислот, таких как азотная кислота, восходит к европейской алхимии 13-го века . [7] Традиционно считается, что азотная кислота была впервые описана в книге псевдо-Гебера De Invente Veritatis («Об открытии истины», около 1300 г. ). [8]
Однако, по словам Эрика Джона Холмьярда и Ахмада Й. аль-Хасана , азотная кислота также встречается в различных более ранних арабских произведениях , таких как «Шундук аль-Хикма » («Сундук мудрости»), приписываемый Джабиру ибн Хайяну (8 век) или Тавид аль-Хаким приписывают фатимидскому халифу аль-Хакиму би-Амру Аллаху (985–1021). [9]
Рецепт в «Шундук аль-хикма» , приписываемый Джабиру, переведен следующим образом: [10] [11]
Возьмите пять частей чистых цветков селитры, три части кипрского купороса и две части йеменских квасцов . Хорошо растолочь их отдельно, пока они не станут похожими на пыль, а затем поместить в колбу. Последний заткните пальмовым волокном и прикрепите к нему стеклянный приемник. Затем переверните аппарат и нагрейте верхнюю часть (т. е. колбу, содержащую смесь) на слабом огне. От жары потечет масло, подобное коровьему маслу.
Азотная кислота также встречается в работах после 1300 года, ошибочно приписываемых Альберту Великому и Рамону Луллию (оба XIII век). В этих работах описана перегонка смеси, содержащей селитру и медный купорос , которую они называют «форте» (aqua fortis). [12] [13] [14]
В 17 веке Иоганн Рудольф Глаубер разработал способ получения азотной кислоты путем перегонки нитрата калия с серной кислотой. В 1776 году Антуан Лавуазье процитировал работу Джозефа Пристли , указав, что его можно преобразовать из оксида азота (который он называет «азотистым воздухом»), «в сочетании с примерно равным объемом чистейшей части обычного воздуха и со значительной количество воды». [15] [а] В 1785 году Генри Кавендиш определил его точный состав и показал, что его можно синтезировать, пропуская поток электрических искр через влажный воздух . [16] В 1806 году Хамфри Дэви сообщил о результатах обширных экспериментов по электролизу дистиллированной воды, придя к выводу, что азотная кислота вырабатывается на аноде из растворенного атмосферного газообразного азота. Он использовал батарею высокого напряжения, нереактивные электроды и сосуды, такие как конусы золотых электродов, которые одновременно служили сосудами, покрытыми влажным асбестом. [17]
Промышленное производство азотной кислоты из атмосферного воздуха началось в 1905 году с процесса Биркеланда-Эйда , также известного как дуговой процесс. [18] Этот процесс основан на окислении атмосферного азота кислородом воздуха до оксида азота с помощью электрической дуги очень высокой температуры. Выходы оксида азота примерно до 4–5% были получены при 3000 ° C и меньше при более низких температурах. [18] [19] Оксид азота охлаждался и окислялся оставшимся кислородом воздуха до диоксида азота, а затем поглощался водой в серии насадочных или тарельчатых абсорбционных колонн с получением разбавленной азотной кислоты. Первые башни барботировали диоксид азота через воду и нереактивные фрагменты кварца. Около 20% образовавшихся оксидов азота остались непрореагировавшими, поэтому в конечные башни добавляли раствор щелочи для нейтрализации остальных. [20] Этот процесс был очень энергоемким и был быстро вытеснен процессом Оствальда, как только стал доступен дешевый аммиак.
Другой ранний метод производства был изобретен французским инженером Альбертом Нодоном примерно в 1913 году. Его метод производил азотную кислоту путем электролиза нитрата кальция, преобразованного бактериями из азотистых веществ в торфяных болотах. Глиняный горшок, окруженный известняком, погружали в торф и обкладывали просмоленными бревнами, чтобы образовалось отделение для угольного анода, вокруг которого образуется азотная кислота. Азотную кислоту откачивали из глиняной [21] трубы, опущенной на дно горшка. Свежая вода закачивалась в верх через другую глиняную трубу для замены откачанной жидкости. Внутри было полно кокса . Чугунные катоды были затоплены в окружающий его торф. Сопротивление составляло около 3 Ом на кубический метр, а напряжение питания составляло около 10 Вольт. Добыча с одного месторождения составила 800 тонн в год. [21] [22]
После того, как в 1913 году был внедрен процесс Габера для эффективного производства аммиака, производство азотной кислоты из аммиака с использованием процесса Оствальда обогнало производство процесса Биркеланда-Эйда. Этот метод производства используется до сих пор.
Коммерчески доступная азотная кислота представляет собой азеотроп с водой в концентрации 68% HNO 3 . Этот раствор имеет температуру кипения 120,5 ° C (249 ° F) при 1 атм. Она известна как «концентрированная азотная кислота». Азеотроп азотной кислоты и воды представляет собой бесцветную жидкость при комнатной температуре.
Известны два твердых гидрата: моногидрат HNO 3 ·H 2 O или нитрат оксония [H 3 O] + [NO 3 ] - и тригидрат HNO 3 ·3H 2 O .
Иногда можно увидеть более старую шкалу плотности с концентрированной азотной кислотой, обозначаемой как 42 Baumé . [23]

Азотная кислота подвержена термическому или световому разложению, поэтому ее часто хранили в бутылках из коричневого стекла:
Эта реакция может привести к некоторым значительным изменениям давления пара над жидкостью, поскольку образующиеся оксиды азота частично или полностью растворяются в кислоте.
Диоксид азота ( NO 2 ) и/или четырехокись азота ( N 2 O 4 ) остаются растворенными в азотной кислоте, окрашивая ее в желтый или даже красный цвет при более высоких температурах. В то время как чистая кислота имеет тенденцию выделять белые пары при контакте с воздухом, кислота с растворенным диоксидом азота выделяет красновато-коричневые пары, что привело к общим названиям «красная дымящая азотная кислота» и «белая дымящая азотная кислота». Оксиды азота ( NOx ) растворимы в азотной кислоте .
Техническая дымящая азотная кислота содержит 98% HNO 3 и имеет плотность 1,50 г/см 3 . Этот сорт часто используется в промышленности взрывчатых веществ. Она не такая летучая и не такая агрессивная, как безводная кислота, и ее приблизительная концентрация составляет 21,4 М.
Красная дымящая азотная кислота , или RFNA, содержит значительные количества растворенного диоксида азота ( NO 2 ), придающего раствору красновато-коричневый цвет. За счет растворенного диоксида азота плотность красной дымящей азотной кислоты ниже и составляет 1,490 г/см 3 .
Ингибированную дымящую азотную кислоту, либо белую ингибированную дымящую азотную кислоту (IWFNA), либо красную ингибированную дымящую азотную кислоту (IRFNA), можно получить путем добавления от 0,6 до 0,7% фтористого водорода (HF). Этот фторид добавляют для устойчивости к коррозии в металлических резервуарах. Фторид создает слой фторида металла, который защищает металл.
Белая дымящая азотная кислота, чистая азотная кислота или WFNA, очень близка к безводной азотной кислоте. По данным анализа он доступен в виде 99,9% азотной кислоты. Одной из характеристик белой дымящей азотной кислоты является то, что она содержит максимум 2% воды и максимум 0,5% растворенного NO 2 . Безводная азотная кислота имеет плотность 1,513 г/см 3 и приблизительную молярную концентрацию 24. Безводная азотная кислота представляет собой бесцветную подвижную жидкость плотностью 1,512 г/см 3 , которая затвердевает при -42 °C (-44 °F) с образованием белых кристаллов [ необходимы разъяснения ] . При разложении на NO 2 и воду приобретает желтый оттенок. Он кипит при 83 ° C (181 ° F). Обычно его хранят в стеклянной небьющейся бутылке янтарного цвета с двойным объемом свободного пространства над головкой, чтобы обеспечить возможность повышения давления, но даже с учетом этих мер предосторожности бутылку необходимо вентилировать ежемесячно, чтобы сбросить давление.
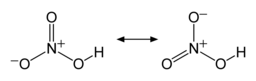
Две концевые связи N–O почти эквивалентны и относительно короткие: 1,20 и 1,21 Å. [24] Это можно объяснить теориями резонанса ; две основные канонические формы демонстрируют некоторый характер двойных связей в этих двух связях, в результате чего они короче, чем одинарные связи NO . Третья связь N–O удлинена, поскольку ее атом O связан с атомом H [25] [26] с длиной связи 1,41 Å в газовой фазе. [24] Молекула слегка апланарна ( плоскости NO 2 и NOH наклонены друг от друга на 2°) и имеет ограниченное вращение вокруг одинарной связи N–OH. [6] [27]
Азотная кислота обычно считается сильной кислотой при температуре окружающей среды. Существуют некоторые разногласия по поводу значения константы диссоциации кислоты, хотя значение p K a обычно указывается как меньше -1. Это означает, что азотная кислота в разбавленном растворе полностью диссоциирует, за исключением очень кислых растворов. Значение p K a возрастает до 1 при температуре 250 °C. [28]
Азотная кислота может действовать как основание по отношению к такой кислоте, как серная кислота :
Ион нитрония [ NO 2 ] + является активным реагентом в реакциях ароматического нитрования . Поскольку азотная кислота обладает как кислотными, так и основными свойствами, она может подвергаться реакции автопротолиза, аналогичной самоионизации воды :
Азотная кислота реагирует с большинством металлов, но детали зависят от концентрации кислоты и природы металла. Разбавленная азотная кислота ведет себя как обычная кислота в реакции с большинством металлов. Магний , марганец и цинк выделяют H 2 :
Азотная кислота может окислять неактивные металлы, такие как медь и серебро . Продукты этих неактивных или менее электроположительных металлов зависят от температуры и концентрации кислоты. Например, медь реагирует с разбавленной азотной кислотой при температуре окружающей среды со стехиометрией 3:8:
Образующийся оксид азота может реагировать с кислородом воздуха с образованием диоксида азота . При более концентрированной азотной кислоте диоксид азота образуется непосредственно в реакции со стехиометрией 1:4:
Большинство металлов при реакции с азотной кислотой дают соответствующие нитраты . Некоторые металлоиды и металлы дают оксиды ; например, Sn , As , Sb и Ti окисляются до SnO 2 , As 2 O 5 , Sb 2 O 5 и TiO 2 соответственно. [29]
Некоторые драгоценные металлы , такие как чистое золото и металлы платиновой группы, не реагируют с азотной кислотой, хотя чистое золото реагирует с царской водкой — смесью концентрированной азотной и соляной кислот . Однако некоторые менее благородные металлы ( Ag , Cu , ...), присутствующие в некоторых золотых сплавах, относительно бедных золотом, например, в цветном золоте , могут легко окисляться и растворяться азотной кислотой, что приводит к изменению цвета поверхности золотого сплава. Азотная кислота используется в ювелирных магазинах как дешевое средство для быстрого обнаружения сплавов с низким содержанием золота (< 14 карат ) и быстрой оценки чистоты золота.
Являясь мощным окислителем, азотная кислота реагирует со многими неметаллическими соединениями, иногда взрывоопасно. В зависимости от концентрации кислоты, температуры и используемого восстановителя конечные продукты могут быть разными. Реакция протекает со всеми металлами, кроме ряда благородных металлов и некоторых сплавов . Как правило, окислительные реакции протекают преимущественно с концентрированной кислотой, способствующей образованию диоксида азота ( NO 2 ). Однако мощные окислительные свойства азотной кислоты носят термодинамический характер, но иногда реакции ее окисления протекают весьма кинетически невыгодно. Присутствие небольших количеств азотистой кислоты ( HNO 2 ) значительно увеличивает скорость реакции. [29]
Хотя хром (Cr), железо (Fe) и алюминий (Al) легко растворяются в разбавленной азотной кислоте, концентрированная кислота образует слой оксида металла, защищающий основную массу металла от дальнейшего окисления. Образование этого защитного слоя называется пассивацией . Типичные концентрации пассивации варьируются от 20% до 50% по объему (см. ASTM A967-05 [ где? ] [ необходимы пояснения ] ). Металлы, пассивируемые концентрированной азотной кислотой, — железо , кобальт , хром , никель , алюминий . [29]
Являясь мощной кислотой-окислителем , азотная кислота вступает в реакцию со многими органическими веществами, причем реакции могут быть взрывоопасными. Гидроксильная группа обычно удаляет водород из органической молекулы с образованием воды, а место водорода занимает оставшаяся нитрогруппа. Нитрование органических соединений азотной кислотой является основным методом синтеза многих распространенных взрывчатых веществ, таких как нитроглицерин и тринитротолуол (ТНТ). Поскольку возможно очень много менее стабильных побочных продуктов, эти реакции необходимо тщательно контролировать термически и удалять побочные продукты, чтобы выделить желаемый продукт.
Реакция с неметаллическими элементами, за исключением азота, кислорода, благородных газов , кремния и галогенов , кроме йода, обычно окисляет их до высших степеней окисления как кислот с образованием диоксида азота для концентрированной кислоты и оксида азота для разбавленной кислоты. кислота.
Концентрированная азотная кислота окисляет I 2 , P 4 и S 8 до HIO 3 , H 3 PO 4 и H 2 SO 4 соответственно. [29] Хотя он реагирует с графитом и аморфным углеродом, он не реагирует с алмазом; он может отделить алмаз от графита, который он окисляет. [30]
Азотная кислота реагирует с белками с образованием желтых нитрованных продуктов. Эта реакция известна как ксантопротеиновая реакция . Это испытание проводится путем добавления к испытуемому веществу концентрированной азотной кислоты и последующего нагревания смеси. Если присутствуют белки, содержащие аминокислоты с ароматическими кольцами, смесь окрашивается в желтый цвет. При добавлении основания, такого как аммиак , цвет становится оранжевым. Эти изменения цвета вызваны нитрованными ароматическими кольцами белка. [31] [32] Ксантопротеиновая кислота образуется при контакте кислоты с эпителиальными клетками . Соответствующие местные изменения цвета кожи указывают на неадекватные меры предосторожности при обращении с азотной кислотой.
Азотная кислота получается реакцией диоксида азота ( NO 2 ) с водой .
Чистая реакция:
Обычно оксид азота, образующийся в результате реакции, повторно окисляется кислородом воздуха с образованием дополнительного диоксида азота.
Барботирование диоксида азота через перекись водорода может помочь улучшить выход кислоты.
Растворы азотной кислоты промышленного качества обычно содержат от 52% до 68% азотной кислоты. Производство азотной кислоты осуществляется методом Оствальда , названным в честь немецкого химика Вильгельма Оствальда . В этом процессе безводный аммиак окисляется до оксида азота в присутствии катализатора из платиновой или родиевой сетки при высокой температуре около 500 К (227 ° C; 440 ° F) и давлении 9 стандартных атмосфер (910 кПа).
Затем оксид азота реагирует с кислородом воздуха с образованием диоксида азота.
Впоследствии он поглощается водой с образованием азотной кислоты и оксида азота.
Оксид азота возвращается на повторное окисление. Альтернативно, если последний этап выполняется на воздухе:
Полученный водный раствор HNO 3 можно концентрировать перегонкой примерно до 68% по массе. Дальнейшее концентрирование до 98% может быть достигнуто обезвоживанием концентрированной H 2 SO 4 . Используя аммиак, полученный в процессе Габера , конечный продукт можно производить из азота, водорода и кислорода, которые получают из воздуха и природного газа в качестве единственного сырья. [33]
В лаборатории азотную кислоту можно получить путем термического разложения нитрата меди(II) с образованием диоксида азота и газообразного кислорода, которые затем пропускают через воду с образованием азотной кислоты.
Затем, следуя процессу Оствальда :
Альтернативно, реакция равных молей любой нитратной соли, такой как нитрат натрия , с серной кислотой ( H 2 SO 4 ) и перегонка этой смеси при температуре кипения азотной кислоты 83 ° C. Нелетучий остаток гидросульфата металла остается в дистилляционном сосуде. [26]
Разбавленную азотную кислоту можно концентрировать перегонкой до 68,5 % кислоты, что является максимально кипящим азеотропом. Дальнейшее концентрирование азотной кислоты включает перегонку с серной кислотой или нитратом магния , которые служат дегидратирующими агентами в процессе экстракции, снижая летучесть воды. Этот метод используется как в промышленности, так и в лабораториях. [34]
В промышленности более высокие концентрации азотной кислоты также получали путем растворения дополнительного диоксида азота в азотной кислоте в абсорбционной башне в процессе, называемом DSN (прямая сильная азотная кислота). Сегодня этот процесс является редкостью: последний завод DSN, производивший высококонцентрированную азотную кислоту в США, прекратил производство в 2012 году и был заменен заводом по производству слабой азотной кислоты с дополнительной установкой экстрактивной дистилляции. [34]
Растворенные оксиды азота либо удаляются в случае белой дымящей азотной кислоты, либо остаются в растворе с образованием красной дымящей азотной кислоты. Совсем недавно были разработаны электрохимические способы получения безводной кислоты из концентрированного азотнокислого сырья. [35]

Основное промышленное применение азотной кислоты — производство удобрений . Азотную кислоту нейтрализуют аммиаком с образованием нитрата аммония . Это приложение потребляет 75–80% из 26 миллионов тонн, производимых ежегодно (1987 г.). Другими основными сферами применения являются производство взрывчатых веществ, прекурсоров нейлона и специальных органических соединений. [36]
В органическом синтезе , промышленном и других, нитрогруппа является универсальной функциональной группой . Смесь азотной и серной кислот вводит нитрозаместитель в различные ароматические соединения путем электрофильного ароматического замещения . Многие взрывчатые вещества, например тротил , готовятся следующим образом:
Лишняя вода поглощается либо концентрированной серной кислотой, либо олеумом.
Нитрогруппа может быть восстановлена с образованием аминогруппы , что позволяет синтезировать соединения анилина из различных нитробензолов :
Предшественник нейлона , адипиновая кислота , производится в больших масштабах путем окисления «масла КА» — смеси циклогексанона и циклогексанола — азотной кислотой. [36]
Азотная кислота использовалась в различных формах в качестве окислителя в ракетах на жидком топливе . К этим формам относятся красная дымящая азотная кислота, белая дымящая азотная кислота, смеси с серной кислотой и эти формы с ингибитором HF. [37] IRFNA (ингибированная красная дымящая азотная кислота ) была одним из трех компонентов жидкого топлива для ракеты BOMARC . [38]
Азотную кислоту можно использовать для перевода металлов в окисленные формы, например, для преобразования металлической меди в нитрат меди . Его также можно использовать в сочетании с соляной кислотой в качестве царской водки для растворения благородных металлов, таких как золото (в виде золотохлористоводородной кислоты ). Эти соли можно использовать для очистки золота и других металлов с чистотой выше 99,9% с помощью процессов перекристаллизации и селективного осаждения . Его способность избирательно растворять определенные металлы или быть растворителем для многих солей металлов делает его полезным в процессах разделения золота .
В элементном анализе методами ICP-MS , ICP-AES , GFAA и Flame AA в качестве матричного соединения для определения следов металлов в растворах используют разбавленную азотную кислоту (0,5–5,0%). [39] Для такого определения необходима сверхчистая кислота со следами металлов, поскольку небольшие количества ионов металлов могут повлиять на результат анализа.
Он также обычно используется в процессе разложения проб мутной воды, проб ила, твердых проб, а также других типов уникальных проб, которые требуют элементного анализа с помощью ICP-MS , ICP-OES , ICP-AES , GFAA и пламенной атомно-абсорбционной спектроскопии. . Обычно при таком расщеплении используется 50% раствор покупной HNO 3, смешанный с деионизированной водой типа 1.
В электрохимии азотная кислота используется в качестве химического легирующего агента для органических полупроводников и в процессах очистки необработанных углеродных нанотрубок .
В низкой концентрации (около 10%) азотную кислоту часто используют для искусственного состаривания сосны и клена . Цвет получается серо-золотой, очень похожий на очень старое дерево, обработанное воском или маслом ( отделка дерева ). [40]
Коррозионное воздействие азотной кислоты используется для некоторых специальных применений, таких как травление в гравюре, травление нержавеющей стали или очистка кремниевых пластин в электронике. [41]
Раствор азотной кислоты, воды и спирта нитал применяют для травления металлов с целью выявления микроструктуры. ISO 14104 — один из стандартов, подробно описывающих эту хорошо известную процедуру.
Азотная кислота используется либо в сочетании с соляной кислотой, либо отдельно для очистки покровных стекол и предметных стекол для высокотехнологичных приложений микроскопии. [42] Его также используют для очистки стекла перед серебрением при изготовлении серебряных зеркал. [43]
Коммерчески доступные водные смеси 5–30% азотной кислоты и 15–40% фосфорной кислоты обычно используются для очистки пищевого и молочного оборудования, главным образом, для удаления осажденных соединений кальция и магния (либо осаждающихся из технологического потока, либо образующихся в результате использования жесткой воды). во время производства и очистки). Содержание фосфорной кислоты помогает пассивировать ферросплавы от коррозии разбавленной азотной кислотой. [ нужна цитата ]
Азотную кислоту можно использовать в качестве точечного теста на алкалоиды , такие как ЛСД , что дает различные цвета в зависимости от алкалоида. [44]
Азотная кислота играет ключевую роль в PUREX и других методах переработки ядерного топлива , где она может растворять множество различных актинидов . Полученные нитраты превращаются в различные комплексы, которые можно вводить в реакцию и избирательно экстрагировать, чтобы отделить металлы друг от друга.
Азотная кислота является едкой кислотой и сильным окислителем . Основная опасность, которую он представляет, — это химические ожоги , поскольку он осуществляет кислотный гидролиз с белками ( амид ) и жирами ( эфир ), что приводит к разложению живых тканей (например, кожи и плоти ). Концентрированная азотная кислота окрашивает кожу человека в желтый цвет из-за реакции с кератином . Эти желтые пятна при нейтрализации становятся оранжевыми. [45] Системные эффекты маловероятны, вещество не считается канцерогеном или мутагеном. [46]
Стандартной мерой первой помощи при попадании кислоты на кожу, как и при других разъедающих веществах, является промывание большим количеством воды. Промывание продолжают не менее 10–15 минут для охлаждения тканей, окружающих ожог кислотой, и предотвращения вторичного повреждения. Загрязненную одежду немедленно снимают, а кожу тщательно промывают.
Являясь сильным окислителем, азотная кислота может бурно реагировать со многими соединениями.
Азотная кислота является одним из наиболее распространенных типов кислот, используемых при кислотных атаках . [47]