Класс препаратов, влияющих на половые гормоны
Агонист гонадотропин-рилизинг-гормона ( агонист ГнРГ ) — это тип лекарств, который влияет на гонадотропины и половые гормоны . [1] Они используются по различным показаниям, в том числе в медицине бесплодия , а также для снижения уровня половых гормонов при лечении гормоночувствительных видов рака , таких как рак простаты и рак молочной железы , некоторых гинекологических заболеваний, таких как обильные менструации и эндометриоз , повышенного уровня тестостерона у женщин. женщин, раннее половое созревание у детей, как часть гормональной терапии трансгендеров , а также для задержки полового созревания у трансгендерной молодежи, среди прочего. Он также используется для подавления спонтанной овуляции в рамках контролируемой гиперстимуляции яичников, что является важным компонентом ЭКО . Агонисты ГнРГ вводятся путем инъекций в жир , в виде имплантатов, помещаемых в жир , и в виде назальных спреев .
Побочные эффекты агонистов ГнРГ связаны с дефицитом половых гормонов и включают симптомы низкого уровня тестостерона и низкого уровня эстрогена, такие как приливы , сексуальная дисфункция , вагинальная атрофия , атрофия полового члена , остеопороз , бесплодие и снижение половых физических характеристик . Они являются агонистами рецептора ГнРГ и действуют путем увеличения или уменьшения высвобождения гонадотропинов и выработки половых гормонов гонадами . При использовании для подавления высвобождения гонадотропинов агонисты ГнРГ могут снизить уровень половых гормонов на 95% у представителей обоих полов. [2] [3] [4] [5]
ГнРГ был открыт в 1971 году, а аналоги ГнРГ были введены для медицинского использования в 1980-х годах. [6] [7] Их непатентованные имена обычно заканчиваются на -relin . Наиболее известными и широко используемыми аналогами ГнРГ являются лейпрорелин (торговая марка Лупрон) и трипторелин (торговая марка Декапептил). Аналоги ГнРГ доступны в виде непатентованных лекарств . Несмотря на это, они продолжают оставаться очень дорогими.
Медицинское использование
Агонисты ГнРГ полезны в:
- Подавление спонтанной овуляции как часть контролируемой гиперстимуляции яичников , которая является важным компонентом экстракорпорального оплодотворения (ЭКО). Обычно после того, как агонисты ГнРГ вызывают состояние гипоэстрогенизма, вводят экзогенный ФСГ для стимуляции фолликула яичника, а затем хорионические гонадотропины человека (ХГЧ) для запуска высвобождения ооцитов . Для этой цели обычно используются агонисты ГнРГ: бусерелин, лейпрорелин, нафарелин и трипторелин. [8]
- Окончательная индукция созревания после проведения контролируемой гиперстимуляции яичников. Использование агониста GnRH для этой цели требует использования антагониста GnRH вместо агониста GnRH для подавления спонтанной овуляции , поскольку использование агониста GnRH для этой цели также инактивирует ось, для которой он предназначен для индукции окончательного созревания.
- Лечение рака , гормонально чувствительного и при котором гипогонадическое состояние снижает вероятность рецидива. Таким образом, они обычно используются при лечении рака простаты и у пациентов с раком молочной железы .
- Задержка полового созревания у лиц с преждевременным половым созреванием .
- Задержка полового созревания задерживает развитие вторичных половых признаков у детей с гендерной дисфорией .
- Управление женскими расстройствами, которые зависят от выработки эстрогена . Женщины с меноррагией , эндометриозом , аденомиозом или миомой матки могут получать агонисты ГнРГ для подавления активности яичников и индукции гипоэстрогенного состояния.
- Подавление уровня половых гормонов у трансгендеров , особенно у трансгендерных женщин .
- Тяжелые случаи гиперандрогении , например, при врожденной гиперплазии надпочечников .
- В составе фармакологического лечения парафильных расстройств у лиц, совершивших сексуальные преступления, или мужчин с высоким риском совершения сексуальных преступлений. [9]
Женщин репродуктивного возраста, проходящих цитотоксическую химиотерапию, предварительно лечили агонистами ГнРГ, чтобы снизить риск потери ооцитов во время такой терапии и сохранить функцию яичников. Необходимы дальнейшие исследования, чтобы доказать, что этот подход полезен.
Доступные формы
Агонисты ГнРГ, которые поступили в продажу и доступны для медицинского применения, включают бусерелин , гонадорелин , гозерелин , гистрелин , лейпрорелин , нафарелин и трипторелин . Агонисты ГнРГ, которые используются преимущественно или исключительно в ветеринарной медицине, включают дезлорелин и фертирелин . Агонисты ГнРГ можно вводить путем инъекции , имплантации или интраназально в виде назального спрея . Инъекционные препараты разработаны для ежедневного, ежемесячного и ежеквартального использования, а также доступны имплантаты, срок службы которых может составлять от одного месяца до года. За исключением гонадорелина, который используется в качестве прогонадотропина , все одобренные агонисты ГнРГ используются в качестве антигонадотропинов .
Клинически используемые десенсибилизирующие агонисты ГнРГ доступны в следующих фармацевтических формах : [10] [11] [12] [13]
Противопоказания
Агонисты ГнРГ относятся к препаратам категории X при беременности.
Побочные эффекты
Общие побочные эффекты агонистов и антагонистов ГнРГ включают симптомы гипогонадизма, такие как приливы жара, гинекомастия, утомляемость, увеличение веса, задержка жидкости, эректильная дисфункция и снижение либидо. Длительная терапия может привести к метаболическим нарушениям, увеличению веса, ухудшению течения диабета и остеопороза. Редкие, но потенциально серьезные побочные эффекты включают преходящее ухудшение течения рака простаты из-за резкого повышения уровня тестостерона при первоначальной инъекции агонистов ГнРГ и апоплексию гипофиза у пациентов с аденомой гипофиза. Сообщалось об единичных случаях клинически выраженного поражения печени при применении некоторых агонистов ГнРГ (гистрелин, гозерелин), но эти сообщения не были очень убедительными. Нет никаких доказательств того, что существует перекрестная чувствительность к повреждению печени среди различных аналогов ГнРГ, несмотря на их сходство по структуре. [14]
Существует также сообщение о том, что агонисты ГнРГ, используемые при лечении распространенного рака простаты, могут увеличить риск проблем с сердцем на 30%. [15]
Фармакология
Агонисты ГнРГ действуют как агонисты рецептора ГнРГ , биологической мишени гонадотропин -высвобождающего гормона (ГнРГ). Эти препараты могут быть как пептидами , так и низкомолекулярными . Они созданы по образцу гипоталамического нейрогормона ГнРГ, который взаимодействует с рецептором ГнРГ, вызывая его биологический ответ, высвобождение гормонов гипофиза — фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ). Однако после первоначальной реакции «вспышки» продолжающаяся стимуляция агонистами ГнРГ снижает чувствительность гипофиза (вызывая подавление рецептора ГнРГ) к ГнРГ. Десенсибилизация гипофиза снижает секрецию ЛГ и ФСГ и, таким образом, вызывает состояние гипогонадотропной гипогонадной ановуляции, иногда называемое «псевдоменопаузой» или «медицинской овариэктомией». [1] Агонисты ГнРГ способны полностью остановить выработку тестостерона гонадами и тем самым подавить уровень циркулирующего тестостерона на 95% или до уровня кастрации/женщины у мужчин. [5]
Агонисты не быстро диссоциируют от рецептора ГнРГ. В результате первоначально происходит увеличение секреции ФСГ и ЛГ (так называемый «эффект вспышки»). Уровни ЛГ могут увеличиваться до 10 раз, [16] [17], в то время как уровни тестостерона обычно увеличиваются до 140–200% от исходных значений. [18] Однако после непрерывного введения глубокий гипогонадальный эффект (т.е. снижение уровня ФСГ и ЛГ) достигается за счет подавления рецепторов путем интернализации рецепторов. [16] Обычно терапевтической целью является индуцированный и обратимый гипогонадизм . Во время обострения пиковые уровни тестостерона достигаются через 2–4 дня, исходные уровни тестостерона возвращаются к 7–8 дням, а кастратные уровни тестостерона достигаются через 2–4 недели. [18] [16] 7-дневное исследование бесплодных женщин показало, что восстановление нормальной секреции гонадотропинов занимает от 5 до 8 дней после прекращения приема экзогенных агонистов ГнРГ. [19]
Для предотвращения повышения уровня тестостерона и/или его эффектов в начале терапии агонистами ГнРГ можно использовать различные лекарства. [17] [20] [21] К ним относятся антигонадотропины , такие как прогестагены , такие как ацетат ципротерона и ацетат хлормадинона , и эстрогены , такие как диэтилстильбестрол , фосфестрол (диэтилстильбестролдифосфат) и фосфат эстрамустина ; антиандрогены , такие как нестероидные антиандрогены, такие как флутамид , нилутамид и бикалутамид ; и ингибиторы синтеза андрогенов , такие как кетоконазол и ацетат абиратерона . [17] [20] [21] [22] [23] [24] [25]
Уровни тестостерона в течение первого месяца андрогенной депривационной терапии у мужчин с раком простаты, получавших подкожные инъекции антагониста ГнРГ (дегареликса) или агониста (лейпрорелина). Дозы составляли 240, затем 80 мг/мес и 7,5 мг/мес соответственно. [26]
Уровни тестостерона при длительной андрогенной депривационной терапии мужчин с раком предстательной железы различными агонистами ГнРГ, назначаемыми с интервалом в 3 месяца (гозерелин, трипторелин и лейпрорелин). Пунктирная линия — порог кастрационного диапазона. [27]
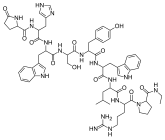
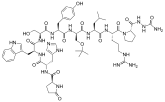
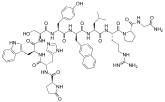
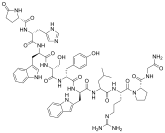
Химия
Агонисты ГнРГ синтетически моделируются по образцу природного декапептида ГнРГ со специфическими модификациями, обычно с двойными и одинарными заменами и обычно в положении 6 (замена аминокислот), 9 (алкилирование) и 10 (делеция). Эти замены тормозят быструю деградацию. К агонистам с двумя заменами относятся: лейпрорелин , бусерелин , гистрелин , гозерелин и дезлорелин . Препараты нафарелин и трипторелин являются агонистами с одиночными заменами в положении 6.
Химическая структура агонистов ГнРГ
Ветеринарное использование
Аналоги ГнРГ также используются в ветеринарии . Использование включает:
- Временное подавление фертильности у сук собак
- Индукция овуляции у кобыл
Смотрите также
Рекомендации
- ^ ab Magon N (октябрь 2011 г.). «Агонисты гонадотропин-рилизинг-гормона: расширяющиеся перспективы». Индийский журнал эндокринологии и метаболизма . 15 (4): 261–7. дои : 10.4103/2230-8210.85575 . ПМЦ 3193774 . ПМИД 22028996.
- ^ Хемат РА (2 марта 2003 г.). Андропатия. Уротекст. стр. 120–. ISBN 978-1-903737-08-8.
- ^ Беккер К.Л. (2001). Принципы и практика эндокринологии и обмена веществ. Липпинкотт Уильямс и Уилкинс. стр. 973–. ISBN 978-0-7817-1750-2.
- ^ Корсон С.Л., Дерман Р.Дж. (15 декабря 1995 г.). Контроль рождаемости. ЦРК Пресс. стр. 249–250. ISBN 978-0-9697978-0-7.
- ^ аб Новара Г., Галфано А., Секко С., Фикарра В., Артибани В. (2009). «Влияние хирургической и медицинской кастрации на уровень тестостерона в сыворотке крови у больных раком простаты». Международная урология . 82 (3): 249–55. дои : 10.1159/000209352 . ПМИД 19440008.
- ↑ Гарднер Д.К., Симон С. (26 июня 2017 г.). Справочник по экстракорпоральному оплодотворению (Четвертое изд.). ЦРК Пресс. стр. 131–. ISBN 978-1-4987-2947-5.
- ↑ Джеймсон Дж.Л., Де Гроот LJ (25 февраля 2015 г.). Эндокринология: электронная книга для взрослых и детей. Elsevier Науки о здоровье. стр. 2135–. ISBN 978-0-323-32195-2.
- ^ ван Лоенен AC, Хуирне Дж. А., Шатс Р., Хомпес П.Г., Ламбалк CB (ноябрь 2002 г.). «Агонисты, антагонисты ГнРГ и вспомогательное зачатие». Семинары по репродуктивной медицине . 20 (4): 349–64. дои : 10.1055/с-2002-36713. PMID 12536358. S2CID 45436435.
- ^ Тернер Д., Брикен П. (январь 2018 г.). «Лечение парафилических расстройств у лиц, совершивших сексуальные преступления, или мужчин с риском совершения сексуальных преступлений с помощью агонистов рилизинг-лютеинизирующего гормона: обновленный систематический обзор». Журнал сексуальной медицины . 15 (1): 77–93. дои : 10.1016/j.jsxm.2017.11.013 . ПМИД 29289377.
- ↑ Ричард А. Лене, Лаура Розенталь (25 июня 2014 г.). Фармакология сестринского дела - Электронная книга. Elsevier Науки о здоровье. стр. 1296–. ISBN 978-0-323-29354-9.
- ↑ Джеймс Л. Галли (20 декабря 2011 г.). Рак простаты. Медицинское издательство Демос. стр. 503–. ISBN 978-1-936287-46-8.
- ^ Чарльз Г.Д. Брук, Питер Клейтон, Розалинд Браун (22 сентября 2011 г.). Клиническая детская эндокринология Брука. Джон Уайли и сыновья. стр. 242–. ISBN 978-1-4443-1673-5.
- ↑ Сюрвин Гумман (22 сентября 2015 г.). Принципы и практика контролируемой стимуляции яичников в ВРТ. Спрингер. стр. 96–. ISBN 978-81-322-1686-5.
- ^ LiverTox: Клиническая и исследовательская информация о повреждении печени, вызванном лекарствами [Интернет]. Бетесда (Мэриленд): Национальный институт диабета, заболеваний органов пищеварения и почек; 2012-. Аналоги гонадотропин-рилизинг-гормона (ГнРГ). [Обновлено 20 марта 2018 г.]. Доступно по адресу: https://www.ncbi.nlm.nih.gov/books/NBK547863/.
- ^ «Исследователи предполагают, что гормональная терапия рака простаты может вызвать серьезные проблемы с сердцем и смерть» . Новости генной инженерии и биотехнологии . 22 сентября 2009 г.
- ^ abc Wein AJ, Кавусси LR, Новик AC, Партин AW, Питерс CA (25 августа 2011 г.). Урология Кэмпбелла-Уолша: Expert Consult Premium Edition: расширенные онлайн-функции и печать, набор из 4 томов. Elsevier Науки о здоровье. стр. 2939–. ISBN 978-1-4160-6911-9.
- ^ abc Томпсон IM (2001). «Вспышка, связанная с терапией агонистами ЛГРГ». Преподобный Урол . 3 (Приложение 3): С10–4. ПМК 1476081 . ПМИД 16986003.
- ^ аб Краковский Ю., Моргенталер А (июль 2017 г.). «Риск вспышки тестостерона в эпоху модели насыщения: еще один исторический миф». Евро Урол Фокус . 5 (1): 81–89. doi :10.1016/j.euf.2017.06.008. PMID 28753828. S2CID 10011200.
Начальное введение агонистов ЛГРГ достоверно вызывает преходящее повышение уровня Т в сыворотке, при этом пиковые значения Т наблюдаются на 2–4 день с последующим снижением до исходных значений на 7–8 дней и достижением кастрационного уровня на 2 дня. –4 недели [10]. Большинство исследований демонстрируют увеличение пиковых концентраций тестостерона в сыворотке на 40–100% выше исходного уровня во время обострения тестостерона.
- ^ Седрин-Дюрнерин I, Бидар Дж. М., Роберт П., Вольф Дж. П., Узан М., Хьюг Дж. Н. (май 2000 г.). «Последствия раннего прекращения приема агонистов гонадотропин-рилизинг-гормона в краткосрочном протоколе экстракорпорального оплодотворения на секрецию гонадотропинов». Репродукция человека . 15 (5): 1009–14. дои : 10.1093/humrep/15.5.1009. ПМИД 10783343.
- ^ аб Скалецки Р., Смит Дж. А. (апрель 1993 г.). «Вспышка заболевания при применении аналогов гонадотропин-рилизинг-гормона (ГнРГ). Насколько это серьезно?». Препарат Саф . 8 (4): 265–70. дои : 10.2165/00002018-199308040-00001. PMID 8481213. S2CID 36964191.
- ^ ab Vis AN, van der Sluis TM, Al-Itejawi HH, van Moorselaar RJ, Meuleman EJ (январь 2015 г.). «Риск обострения заболевания при терапии агонистами ЛГРГ у мужчин с раком простаты: миф или факт?». Урол. Онкол . 33 (1): 7–15. дои : 10.1016/j.urolonc.2014.04.016. ПМИД 25159013.
- ^ Котаке Т, Усами М, Аказа Х, Койсо К, Хомма Ю, Кавабе К, Асо Ю, Орикаса С, Симадзаки Дж, Исака С, Ёсида О, Хирао Ю, Окадзима Е, Найто С, Кумазава Дж, Канетакэ Х, Сайто Ю, Охи Ю, Охаши Ю (ноябрь 1999 г.). «Гозерелина ацетат с антиандрогеном или эстрогеном или без него в лечении пациентов с распространенным раком простаты: многоцентровое рандомизированное контролируемое исследование в Японии. Исследовательская группа Золадекса». Япония. Дж. Клин. Онкол . 29 (11): 562–70. дои : 10.1093/jjco/29.11.562 . ПМИД 10678560.
- ^ Симидзу Т.С., Сибата Ю, Джинбо Х, Сато Дж, Яманака Х (1995). «Эстрамустина фосфат для предотвращения обострений при депо-терапии аналогами рилизинг-гормона лютеинизирующего гормона». Евро. Урол . 27 (3): 192–5. дои : 10.1159/000475159. ПМИД 7541359.
- ^ Сугионо М., Винклер М.Х., Океке А.А., Бенни М., Гиллатт Д.А. (2005). «Бикалутамид против ципротерона ацетата в предотвращении обострения рака простаты с помощью терапии аналогами ЛГРГ - пилотное исследование». Рак предстательной железы . 8 (1): 91–4. дои : 10.1038/sj.pcan.4500784. PMID 15711607. S2CID 9151853.
- ^ Покури В.К., Нуркейхани Х., Бетси Б., Хербст Л., Сикорски М., Спангенталь Э., Фабиано А., Джордж С. (июль 2015 г.). «Стратегии предотвращения всплеска тестостерона и обострения заболевания при распространенном раке простаты: новые парадигмы лечения». J Natl Compr Canc Netw . 13 (7): с49–55. дои : 10.6004/jnccn.2015.0109 . ПМИД 26150586.
- ^ Клотц Л., Боккон-Гибод Л., Шор Н.Д., Андреу С., Перссон Б.Е., Кантор П., Йенсен Дж.К., Олесен Т.К., Шредер Ф.Х. (декабрь 2008 г.). «Эффективность и безопасность дегареликса: 12-месячное сравнительное рандомизированное открытое исследование III фазы в параллельных группах у пациентов с раком простаты». БЖУ Междунар . 102 (11): 1531–8. дои : 10.1111/j.1464-410X.2008.08183.x. ПМИД 19035858.
- ↑ Шим М., Банг WJ, О Сай, Ли Ю.С., Чо Дж.С. (июль 2019 г.). «Эффективность трех различных агонистов рилизинг-гормона лютеинизирующего гормона при химической кастрации пациентов с раком простаты: гозерелина по сравнению с трипторелином и лейпролидом». Следователь Клин Урол . 60 (4): 244–250. дои : 10.4111/icu.2019.60.4.244. ПМК 6607074 . ПМИД 31294133.
Внешние ссылки
- Сайт Бусерелина
- Применение агонистов при эндометриозе
- Люпрон, производитель
- СупрелинЛА от Endo Pharmaceuticals, Inc.
- Информация о применении Золадекса при раке простаты

![Уровни тестостерона в течение первого месяца андрогенной депривационной терапии у мужчин с раком простаты, получавших подкожные инъекции антагониста ГнРГ (дегареликса) или агониста (лейпрорелина). Дозы составляли 240, затем 80 мг/мес и 7,5 мг/мес соответственно.[26]](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f8/Testosterone_levels_in_men_with_prostate_cancer_treated_with_GnRH_agonists_and_antagonists.png/300px-Testosterone_levels_in_men_with_prostate_cancer_treated_with_GnRH_agonists_and_antagonists.png)
![Уровни тестостерона при длительной андрогенной депривационной терапии мужчин с раком предстательной железы различными агонистами ГнРГ, назначаемыми с интервалом в 3 месяца (гозерелин, трипторелин и лейпрорелин). Пунктирная линия — порог кастрационного диапазона.[27]](http://upload.wikimedia.org/wikipedia/commons/thumb/3/39/Testosterone_levels_in_long-term_androgen_deprivation_therapy_with_different_GnRH_agonists.png/300px-Testosterone_levels_in_long-term_androgen_deprivation_therapy_with_different_GnRH_agonists.png)