Диэтилстильбэстрол ( ДЭС ), также известный как стильбэстрол или стильбоэстрол , представляет собой нестероидный эстрогенный препарат, который в настоящее время используется редко. [5] [6] [7] В прошлом он широко использовался по различным показаниям, включая поддержку беременности у женщин с привычным выкидышем в анамнезе , гормональную терапию симптомов менопаузы и дефицита эстрогена , лечение рака простаты и молочной железы. рак и другие применения. [5] К 2007 году его использовали только при лечении рака простаты и рака молочной железы. [8] В 2011 году Гувер и его коллеги сообщили о неблагоприятных последствиях для здоровья, связанных с DES, включая бесплодие , выкидыш , внематочную беременность , преэклампсию , преждевременные роды , мертворождение , младенческую смертность , менопаузу до 45 лет, рак молочной железы, рак шейки матки и рак влагалища. . [9] Хотя DES чаще всего принимают перорально , его можно использовать и другими способами , например, вагинально , местно и путем инъекций .
DES является эстрогеном или агонистом эстрогеновых рецепторов , биологической мишенью эстрогенов, таких как эстрадиол . [7] Это синтетический и нестероидный эстроген группы стильбестрола , который по-разному отличается от природного эстрогена эстрадиола . [7] По сравнению с эстрадиолом, DES значительно улучшает биодоступность при пероральном приеме, более устойчив к метаболизму и демонстрирует относительно повышенное воздействие на определенные части тела, такие как печень и матка . [7] Эти различия приводят к тому, что DES имеет повышенный риск образования тромбов , сердечно-сосудистых проблем и некоторых других побочных эффектов. [7]
DES был открыт в 1938 году и введен в медицинское применение в 1939 году. [10] [11] Примерно с 1940 по 1971 год этот препарат давали беременным женщинам из-за ошибочного убеждения, что он снизит риск осложнений и потерь во время беременности. [10] В 1971 году было показано, что DES вызывает светлоклеточную карциному , редкую опухоль влагалища , у тех, кто подвергся воздействию этого препарата внутриутробно . [10] [5] Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США впоследствии отозвало одобрение DES для лечения беременных женщин. [10] [5] Последующие исследования показали, что DES также может вызывать ряд серьезных неблагоприятных медицинских осложнений в течение жизни тех, кто подвергся воздействию, включая XY- генитальную недостаточность мужественности . [10] [12]
Национальный институт рака США рекомендует [13] детям, рожденным от матерей, принимавших DES, регулярно проходить специальные медицинские осмотры для выявления осложнений в результате приема препарата. Людей, подвергшихся воздействию DES во время беременности их матерей, обычно называют «дочерями DES» и «сыновьями DES». [10] [14] С момента открытия токсических эффектов DES его производство в основном было прекращено, и в настоящее время он практически больше не продается. [10] [15]
DES использовался в прошлом по следующим показаниям: [5] [ необходимы дополнительные ссылки ]
DES использовался в дозировке от 0,2 до 0,5 мг/день при менопаузальной гормональной терапии . [27] [5]
Интерес к использованию DES для лечения рака простаты сохраняется и сегодня. [28] [29] [30] [31] [32] [33] [34] Однако использование биоидентичных парентеральных эстрогенов, таких как полиэстрадиолфосфат, было рекомендовано в пользу пероральных синтетических эстрогенов, таких как DES, из-за их гораздо меньшего риска сердечно-сосудистых заболеваний. токсичность. [35] [32] [34] Помимо рака простаты, некоторый интерес к использованию DES для лечения рака молочной железы сохраняется и сегодня. [36] [37] Однако, как и в случае с раком простаты, были приведены аргументы [38] в пользу использования биоидентичных эстрогенов, таких как эстрадиол , вместо DES при раке молочной железы. [36] [38]
Пероральный DES в дозе 0,25–0,5 мг/день эффективен при лечении приливов жара у мужчин, проходящих андрогенную терапию по поводу рака простаты. [39]
Хотя DES использовался для поддержания беременности, позже выяснилось, что он не эффективен для этого применения и даже вреден. [40] [41] [42] [43]
При дозе более 1 мг/день DES связан с высокой частотой побочных эффектов , включая тошноту , рвоту , дискомфорт в животе , головную боль и вздутие живота (частота 15–50%). [44]
Пигментация ареол молочной железы часто очень темная и почти черная при терапии DES . [5] [45] [46] [47] [48] [49] [50] [51] Пигментация, возникающая при использовании синтетических эстрогенов, таких как DES, намного сильнее, чем при использовании натуральных эстрогенов, таких как эстрадиол . [5] [45] Механизм разницы неизвестен. [5] Сообщалось, что прогестагены , такие как гидроксипрогестерон капроат, уменьшают гиперпигментацию сосков, вызванную терапией высокими дозами эстрогенов. [52]
Было обнаружено, что у мужчин, лечившихся им от рака простаты, DES вызывает высокий уровень гинекомастии (развития молочных желез) от 41 до 77%. [53]
В исследованиях DES как формы терапии высокими дозами эстрогенов у пациентов с раком простаты было установлено, что он связан со значительной сердечно-сосудистой заболеваемостью и смертностью . [29] [5] Риск зависит от дозы. [29] Доза 5 мг/день DES была связана с 36% увеличением смертности, не связанной с раком (в основном сердечно-сосудистой). [29] Кроме того, в 15% случаев наблюдается венозная тромбоэмболия . [54] Доза DES в дозе 3 мг/день была связана с частотой тромбоэмболий от 9,6 до 17%, а частота сердечно-сосудистых осложнений - 33,3%. [29] Более низкая доза DES (1 мг/день) была связана с уровнем смертности от сердечно-сосудистых событий в 14,8% (по сравнению с 8,3% при одной только орхиэктомии ). [29]
DES связан с различными долгосрочными побочными эффектами у женщин, принимавших его во время беременности, и/или у их потомства, включая повышенный риск следующих заболеваний: [40]
Комплексное исследование на животных, проведенное в 1993 году, выявило множество побочных эффектов от DES, таких как (но не ограничиваясь ими)
Исследования на грызунах выявляют рак и аномалии женских репродуктивных путей, достигающие поколения F2 , а также есть данные о побочных эффектах, таких как нерегулярные менструальные циклы при интерсексуальности у внуков матерей DES. [57] Кроме того, данные также указывают на трансгенерационные эффекты у сыновей F2, такие как гипоспадия . [58] Однако в настоящее время степень трансгенерационного воздействия DES на человека до конца не изучена. [ нужна цитата ]
В прошлом DES оценивался в клинических исследованиях при чрезвычайно высоких дозах - от 1500 до 5000 мг/день. [36] [59] [60]
DES представляет собой эстроген ; в частности, это очень мощный полный агонист обоих рецепторов эстрогена (ER). [61] [62] Он имеет примерно 468% и 295% сродства эстрадиола к ERα и ERβ соответственно . [63] Тем не менее, сообщалось о значениях EC 50 0,18 нМ и 0,06 нМ DES для ERα и ERβ соответственно, что позволяет предположить, что, несмотря на его аффинность связывания с двумя рецепторами, в несколько раз предпочтительнее активация ERβ. над ERα. [64] В дополнение к ядерным ЭР, DES является агонистом рецептора эстрогена, связанного с G-белком (GPER), хотя и с относительно низким сродством (~ 1000 нМ). [65] DES оказывает те же биологические эффекты, что и природные эстрогены, такие как эстрадиол. [66] [67] Это включает воздействие на матку , влагалище , молочные железы , гипофиз и другие ткани . [66] [67] [68] [69]
Дозировка 1 мг/день ДЭС примерно эквивалентна дозе 50 мкг/день этинилэстрадиола с точки зрения системной эстрогенной активности. [1] [4] Подобно этинилэстрадиолу , ДЭС оказывает заметное и непропорционально сильное влияние на синтез белка в печени . [7] В то время как его системная эстрогенная активность была примерно в 3,8 раза выше, чем у эстропипата (сульфат пиперазина эстрона), который имеет аналогичную эффективность с микронизированным эстрадиолом , печеночная эстрогенная активность DES была в 28 раз выше, чем у эстропипата (или примерно в 7,5 раза). более высокая эффективность для дозировки с эквивалентным системным эстрогенным эффектом). [1]
DES имеет как минимум три механизма действия при лечении рака простаты. [70] Он подавляет выработку андрогенов гонадами и, следовательно, уровень циркулирующих андрогенов из-за его антигонадотропного действия; он стимулирует выработку печеночного глобулина, связывающего половые гормоны (ГСПГ), тем самым повышая уровень ГСПГ в крови и уменьшая свободную фракцию тестостерона и дигидротестостерона (ДГТ) в кровообращении ; и он может оказывать прямое цитотоксическое действие на яички и предстательную железу . [70] Также было обнаружено, что DES снижает синтез ДНК при высоких дозах. [70]
DES представляет собой эстроген длительного действия с ядерным удержанием около 24 часов. [71] [72]


Благодаря своей эстрогенной активности ДЭС оказывает антигонадотропное действие. [83] [70] [94] [95] То есть он оказывает отрицательную обратную связь на гипоталамо-гипофизарно-гонадную ось (ось ГПГ), подавляет секрецию гонадотропинов , лютеинизирующего гормона ( ЛГ) и фолликулостимулирующего гормона ( ФСГ) и подавляет выработку половых гормонов , а также выработку или созревание гамет в гонадах . [83] [70] [94] [95] Исследование ингибирования овуляции показало, что пероральный прием 5 мг/день DES был эффективен на 92%, при этом овуляция происходила только за один цикл. [96] [90] DES последовательно подавляет уровень тестостерона у мужчин до кастрационного уровня (<50 нг/дл) в течение 1–2 недель при дозах 3 мг/день и выше. [83] [95] [97] И наоборот, доза 1 мг/день DES не способна полностью подавить уровень тестостерона до кастрационного уровня у мужчин, который вместо этого часто стабилизируется на уровне, чуть превышающем кастратный (>50 нг/дл). [29] [70] [94] Однако также сообщалось, что 1 мг/день DES приводит примерно к 50% подавлению уровня тестостерона, хотя и с широкой индивидуальной вариабельностью . [83] [98] Было сказано, что дозы DES менее 1 мг/день не влияют на уровень тестостерона. [83] Однако было обнаружено, что добавление «чрезвычайно низкой» дозы 0,1 мг/день DES к ацетату ципротерона приводит к синергическому антигонадотропному эффекту и снижению уровня тестостерона до кастрационного уровня у мужчин. [99] [100] [101] DES в дозе 3 мг/день оказывает такое же подавление тестостерона, что и доза 300 мг/день, что позволяет предположить, что подавление уровня тестостерона максимально при дозе 3 мг/день. [102]
В дополнение к ER, исследование in vitro показало, что DES также обладает активностью, хотя и относительно слабой, в отношении множества других рецепторов стероидных гормонов . [64] Хотя исследование выявило значения ЕС 50 0,18 нМ и 0,06 нМ DES для ERα и ERβ соответственно, препарат показал значительную глюкокортикоидную активность в концентрации 1 мкМ, которая превосходила активность 0,1 нМ дексаметазона , а также значительную антагонизм к андрогенным , прогестероновым и минералокортикоидным рецепторам (75%, 85% и 50% ингибирование стимуляции положительного контроля соответственно, все в концентрации 1 мкМ). [64] Также было показано примерно 25% ингибирование активации PPARγ и LXRα в концентрации 10 мкМ. [64] Исследователи заявили, что, насколько им известно, они были первыми, кто сообщил о таком действии DES, и предположили, что эти действия могут быть связаны с клиническими эффектами DES, например, при раке простаты (особенно при раке простаты). где используются особенно высокие дозы DES). [64] Однако они также отметили, что важность этого действия требует дальнейшего изучения на животных моделях в фармакологически значимых дозах. [64]
DES был идентифицирован как антагонист всех трех изотипов эстроген -связанных рецепторов (ERR): ERRα , ERRβ и ERRγ . [103] [104] Полумаксимальное ингибирование происходит при концентрации около 1 мкМ. [104]
DES хорошо всасывается при пероральном приеме . [1] При пероральном приеме DES в дозе 1 мг/день уровни DES в плазме через 20 часов после приема последней дозы колебались от 0,9 до 1,9 нг/мл (от 3,4 до 7,1 нмоль/л). [1] Сублингвальное введение DES, по-видимому, имеет примерно такую же эстрогенную активность, как и пероральный DES у женщин. [105] Внутриматочный СПС изучался для лечения гипоплазии матки . [106] Считается, что пероральный DES имеет от 17 до 50% клинической эстрогенной активности DES при инъекции. [107]
Период полувыведения DES составляет 80 минут . [1] Он не имеет сродства к ГСПГ или кортикостероидсвязывающему глобулину и, следовательно, не связывается с этими белками в кровообращении. [108] Связывание DES с белками плазмы превышает 95%. [2]
На гидроксилирование ароматических колец ДЭС и последующее сопряжение этильных боковых цепей приходится от 80 до 90% метаболизма ДЭС , тогда как на окисление приходится оставшиеся 10-20%, и в нем преобладают реакции конъюгации. [2] [3] Конъюгация DES состоит из глюкуронидации , тогда как окисление включает дегидрирование в ( Z , Z )-диенэстрол . [1] [2] [3] Также известно, что препарат вырабатывает пароксипропион в качестве метаболита . [109] DES производит временные хинон -подобные реактивные промежуточные соединения , которые вызывают клеточные и генетические повреждения , что может помочь объяснить известные канцерогенные эффекты DES у людей. [1] Однако другие исследования показывают, что токсическое воздействие DES может быть просто связано с чрезмерной активацией ER. [110] В отличие от эстрадиола , гидроксильные группы ДЭС не подвергаются окислению в эстрон -подобный эквивалент. [111]
Период полувыведения ДЭС составляет 24 часа. [1] Метаболиты ДЭС выводятся с мочой и калом . [2] [3]
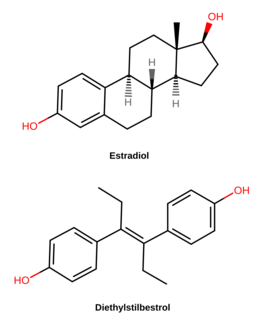
DES принадлежит к группе соединений стильбестрола (4,4'-дигидрокси стильбена ). [115] Это нестероидный аналог стероидного эстрогена эстрадиола с открытым кольцом . [112] DES можно получить из анетола , который также обладает слабым эстрогенным действием. [115] [116] [114] [113] Анетол был деметилирован с образованием анола , а затем анол спонтанно димеризовался в дианол и гексэстрол , с последующим синтезом DES посредством структурной модификации гексэстрола. [115] [116] [114] [113] Как показала рентгеновская кристаллография , молекулярные размеры DES почти идентичны размерам эстрадиола, особенно в отношении расстояния между концевыми гидроксильными группами . [113]
DES был впервые синтезирован в начале 1938 года Леоном Гольбергом, тогдашним аспирантом сэра Роберта Робинсона в лаборатории Дайсона Перринса в Оксфордском университете . Исследование Гольберга было основано на работе Уилфрида Лоусона из Института биохимии Курто (под руководством сэра Эдварда Чарльза Доддса в Медицинской школе больницы Миддлсекса, которая сейчас является частью Университетского колледжа Лондона ). Отчет о его синтезе был опубликован в журнале Nature 5 февраля 1938 года .
Исследование DES финансировалось Советом медицинских исследований Великобритании (MRC) , который придерживался политики против патентования лекарств, обнаруженных с использованием государственных средств. Поскольку он не был запатентован, DES производился более чем 200 фармацевтическими и химическими компаниями по всему миру. [ нужна цитата ]
DES впервые поступил на рынок для медицинского применения в 1939 году. [11] Он был одобрен Управлением по контролю за продуктами и лекарствами США (FDA) 19 сентября 1941 года в таблетках по 5 мг для четырех показаний: гонорейный вагинит , атрофический вагинит , менопаузальный период. симптомов и подавление послеродовой лактации для предотвращения нагрубания молочных желез. [119] Показания к гонорейному вагиниту были исключены, когда стал доступен антибиотик пенициллин . С самого начала препарат вызвал большие споры. [120] [121]
В 1941 году Чарльз Хаггинс и Кларенс Ходжес из Чикагского университета обнаружили бензоат эстрадиола и DES как первые эффективные препараты для лечения метастатического рака простаты . [122] [123] DES был первым лекарством от рака. [124]
Орхиэктомия или DES или оба были стандартным начальным лечением симптоматического распространенного рака простаты на протяжении более 40 лет, пока не было обнаружено, что агонист GnRH лейпрорелин имеет эффективность, аналогичную DES, но без эстрогенных эффектов и не был одобрен в 1985 году. [97]
С 1940-х до конца 1980-х годов DES был одобрен FDA в качестве заместительной терапии эстрогенами при состояниях дефицита эстрогена, таких как дисгенезия яичников , преждевременная недостаточность яичников и после овариэктомии . [ нужна цитата ]
В 1940-х годах DES использовался не по назначению для предотвращения неблагоприятных исходов беременности у женщин, перенесших выкидыш в анамнезе. 1 июля 1947 года FDA одобрило использование DES по этому показанию. Первое такое разрешение было предоставлено компании Bristol-Myers Squibb , разрешающее использование таблеток DES по 25 мг (а позже и по 100 мг) во время беременности. Позже в том же году разрешения были предоставлены другим фармацевтическим компаниям. [125] Рекомендуемый режим начинался с 5 мг в день на седьмой и восьмой неделях беременности (с первого дня последней менструации), увеличивался каждую вторую неделю на 5 мг в день до 14-й недели, а затем увеличивался каждую неделю на 5 мг в сутки от 25 мг в сутки на 15-й неделе до 125 мг в сутки на 35-й неделе беременности. [126] Первоначально DES считался эффективным и безопасным как для беременной женщины, так и для развивающегося ребенка. Его активно рекламировали и регулярно прописывали. Пик продаж пришелся на 1953 год.
В начале 1950-х годов в двойном слепом клиническом исследовании, проведенном в Чикагском университете, оценивались исходы беременности у женщин, которым было назначено либо получать, либо не получать DES. [127] Исследование не выявило пользы от приема DES во время беременности; неблагоприятные исходы беременности не были снижены у женщин, получавших DES. К концу 1960-х годов в шести из семи ведущих учебников по акушерству говорилось, что DES неэффективен для предотвращения выкидыша. [125] [128]
Несмотря на отсутствие доказательств, подтверждающих использование DES для предотвращения неблагоприятных исходов беременности, DES продолжали назначать беременным женщинам на протяжении 1960-х годов. В 1971 году отчет, опубликованный в Медицинском журнале Новой Англии , показал вероятную связь между DES и светлоклеточной аденокарциномой влагалища у девочек и молодых женщин, подвергшихся воздействию этого препарата внутриутробно . Позже в том же году FDA разослало всем врачам США Бюллетень FDA, в котором рекомендовалось воздержаться от использования DES у беременных женщин. FDA также исключило предотвращение выкидыша из числа показаний к использованию DES и добавило беременность в качестве противопоказания к использованию DES. [129] 5 февраля 1975 г. FDA приказало отменить таблетки ДЭС по 25 и 100 мг с 18 февраля 1975 г. [130] Число лиц, подвергшихся воздействию ДЭС во время беременности или внутриутробно в период с 1940 по 1971 г. неизвестно, но в Соединенных Штатах их число может достигать 2 миллионов. DES также использовался в других странах, особенно во Франции, Нидерландах и Великобритании.
С 1950-х по начало 1970-х годов DES назначался девочкам препубертатного возраста, чтобы начать половое созревание и, таким образом, остановить рост путем закрытия пластинок роста в костях. Несмотря на явную связь с раком, врачи продолжали рекомендовать этот гормон при «избыточном росте». [131]
В 1960 году было обнаружено, что DES более эффективен, чем андрогены , при лечении распространенного рака молочной железы у женщин в постменопаузе. [132] DES был гормональным методом выбора при распространенном раке молочной железы у женщин в постменопаузе до 1977 года, когда FDA одобрило тамоксифен , селективный модулятор эстрогеновых рецепторов с эффективностью, аналогичной DES, но с меньшим количеством побочных эффектов. [133]
В нескольких источниках медицинской литературы 1970-х и 1980-х годов указывается, что DES использовался в качестве компонента гормональной терапии трансгендерных женщин . [134] [135] [136]
В 1973 году, в попытке ограничить использование DES не по назначению в качестве посткоитального контрацептива (который стал распространенным во многих университетских службах здравоохранения после публикации влиятельного исследования в 1971 году в JAMA ) чрезвычайными ситуациями, такими как изнасилование, FDA Drug Bulletin было разослано всем врачам и фармацевтам США, которые сообщили, что FDA одобрило, при ограниченных условиях, использование DES в качестве посткоитальной контрацепции. [137]
В 1975 году FDA заявило, что оно фактически не давало (и никогда не давало) разрешения ни одному производителю на продажу DES в качестве посткоитального контрацептива, но одобрило бы это показание для экстренных ситуаций, таких как изнасилование или инцест, если бы производитель предоставил маркировку для пациентов и специальные инструкции. Упаковка соответствует окончательному правилу FDA, опубликованному в 1975 году. [138] Чтобы препятствовать использованию DES не по назначению в качестве посткоитального контрацептива, FDA в 1975 году удалило с рынка таблетки DES по 25 мг и приказало маркировать более низкие дозы (5 мг и ниже) DES, все еще одобренного для других показаний, изменено на: «Этот лекарственный препарат не следует использовать в качестве посткоитального противозачаточного средства» печатными заглавными буквами в первой строке вкладыша с информацией о назначении врачом и на видном и заметном месте. тары и картонной этикетки. [130] [139] В 1980-х годах использование режима Юзпе не по назначению некоторых регулярных комбинированных пероральных контрацептивов заменило использование DES не по назначению в качестве посткоитального контрацептива. [140]
В 1978 году FDA исключило подавление послеродовой лактации , чтобы предотвратить нагрубание молочных желез, из утвержденных показаний для DES и других эстрогенов. [141] В 1990-х годах единственными одобренными показаниями для СЛП были лечение распространенного рака простаты и лечение распространенного рака молочной железы у женщин в постменопаузе. Последний оставшийся производитель DES в США, компания Eli Lilly , прекратила его производство и продажу в 1997 году .
Диэтилстильбэстрол бесчисленное количество раз использовался в исследованиях на крысах. Как только было обнаружено, что DES вызывает рак влагалища, эксперименты начались как на самцах, так и на самках крыс. [142] Многим из этих самцов крыс вводили DES, в то время как другим самцам крыс вводили оливковое масло, и они считались контрольной группой. [142] Каждая группа получала одинаковую дозу в одни и те же дни, и исследователи проводили световую, электронную и конфокальную лазерную микроскопию. Как при электронной, так и при конфокальной лазерной микроскопии было обнаружено, что клетки Сертоли, представляющие собой соматические клетки, в которых в семенниках развиваются сперматиды, формировались через 35 дней у крыс, которым вводили диэтилстильбестрол, по сравнению с крысами в контрольной группе. [142] По завершении исследования стало понятно, что у крыс старшего возраста, которым вводили DES, наблюдалась задержка созревания клеток Сертоли, недоразвитие придатков яичка и резкое снижение веса по сравнению с его аналогами. [142]
Использованные самки крыс были инбредными, и большинству из них DES вводили в пищу. Эти крысы были разделены на три группы: одна группа, которая не получала диэтилстильбестрол, одна группа, в которую добавляли DES, и третья группа, в которую DES вводили в рацион после 13-го дня беременности. [143] Некоторые крысы, которым вводили DES, к сожалению, умерли до рождения детенышей. [143] В группе, которая получала DES с пищей в течение 13 дней во время беременности, произошел ранний аборт и неудачные роды. [143] Эти результаты показали, что DES оказывает вредное воздействие на беременность при столь частом приеме. Введение дозы диэтилстильбестрола на более поздних сроках беременности также сделало видимым возникновение абортов среди крыс. [143] В целом, любое взаимодействие с DES у самок крыс приводило к абортам, неправильному развитию плода и увеличению бесплодия. [143]
Был проведен обзор людей, которые лечились или подвергались воздействию DES, чтобы выяснить, какие долгосрочные эффекты проявятся. [144] Люди в течение длительного времени получали DES во время беременности, и известно о токсических и побочных эффектах гормональной терапии. «Воздействие DES было связано с повышенным риском рака молочной железы у матерей DES (относительный риск <2,0) и с пожизненным риском развития светлоклеточного цервиковагинального рака у дочерей DES от 1/1000 до 1/10 000». [144] Побочные эффекты DES оказываются долгосрочными, поскольку после использования он может вызвать повышенный риск развития рака. [144] Будет продолжена работа, чтобы увидеть, насколько далеко зайдут побочные эффекты DES после предыдущей терапии и как это повлияет на потомство и матерей в долгосрочной перспективе. [144]
В 1938 году FDA впервые получило возможность проверить безопасность DES на животных. Результаты предварительных испытаний показали, что ДЭС наносит вред репродуктивной системе животных. Применение этих результатов к людям определить не удалось, поэтому FDA не могло действовать регулирующим образом. [145]
Заявки на новые лекарства, одобренные DES, были отозваны в 1940 году по решению FDA, основанному на научной неопределенности. Однако это решение вызвало значительное политическое давление, поэтому FDA пришло к компромиссу. Компромисс означал, что DES будет доступен только по рецепту и на бутылке должно быть предупреждение о его воздействии, но в 1945 году предупреждение было снято. В 1947 году DES наконец получил одобрение FDA на назначение беременным женщинам, страдающим диабетом, в качестве лекарства. метод предотвращения выкидышей. Это привело к широкому назначению DES всем беременным женщинам. [145]
В 1971 году FDA рекомендовало не назначать DES беременным женщинам. [146] В результате DES начал отходить с рынка США, начиная с 1972 года, и с европейского рынка, начиная с 1978 года, но FDA до сих пор не отозвало свое одобрение на использование DES у людей. [147]
Международное агентство по исследованию рака отнесло DES к канцерогенам группы 1. После того, как DES был классифицирован как канцероген, в 2000 году его одобрение FDA было отозвано. [146] В настоящее время DES используется только в ветеринарной практике и в исследовательских испытаниях, как это разрешено FDA. [148]
Медицинская этика в отношении одобрения и использования диэтилстильбестрола была отклонена из-за действий FDA и фармацевтических компаний, которые производили DES во время его использования. Вице-президент Американской ассоциации производителей лекарств Карсон Фрейли работал в фармацевтических компаниях, создавших DES, чтобы помочь получить его одобрение Управления по контролю за продуктами и лекарствами (FDA). Нэнси Лэнгстон, автор книги «Отступление от мер предосторожности: регулирование диэтилстильбестрола (DES), эндокринных разрушителей и здоровья окружающей среды», утверждает, что «Фрейли убедил пятьдесят четыре врача со всей страны написать в FDA, описав свой клинический опыт в общей сложности Только четверо из этих пятидесяти четырех врачей считали, что DES не следует одобрять, и в результате, вопреки опасениям многих медицинских сотрудников FDA, руководитель фармацевтического отдела FDA Теодор Клампп рекомендовал FDA утвердить DES». [149] Этот отрывок описывает, как DES был неэтично одобрен, и показывает, что мотивацией его одобрения была выгода фармацевтических компаний, а не людей, которые собирались использовать препарат. Такое одобрение DES нарушает ценности медицинской этики, автономии , непричинения вреда , благодеяния и справедливости , поскольку мало кто задумывался о том, как DES повлияет на его пользователей. [150] Решения, принятые руководителями FDA, одобрить DES без дальнейшего изучения и убедить врачей скрыть свое мнение по поводу использования DES, являются неэтичными. После того, как DES был одобрен для общественного пользования, «предупреждения [для DES] стали доступны только в отдельном циркуляре, который пациенты не видели. Врачи могли получить этот предупреждающий циркуляр, только написав фармацевтическим компаниям и запросив его. Письма между компаниями и FDA Регулирующие органы сообщают, что обе группы опасались, что, если женщина когда-нибудь увидит, сколько потенциальных рисков может представлять собой DES, она может отказаться принимать препарат или же она может подать в суд на компанию и назначающих врачей, если у нее действительно возникнет рак или повреждение печени после приема препарата. лекарство." [149] Женщины не были проинформированы о возможных последствиях DES, поскольку врачи и регулирующие органы FDA боялись, что DES потерпит неудачу и никогда не будет одобрен, что обойдется фармацевтическим компаниям в миллионы долларов. Раздача потенциально опасных лекарств пациентам, независимо от эффекта и вреда, которые они могут нанести, исключительно ради денежной выгоды, неэтична. [ нужна цитата ]
В 1970-х годах негативная огласка вокруг открытия долгосрочных эффектов DES привела к огромной волне судебных исков в Соединенных Штатах против его производителей. Кульминацией этих событий стало принятие в 1980 году знаменательного решения Верховного суда Калифорнии по делу Синделл против Abbott Laboratories , в котором суд наложил на всех производителей DES опровержимую презумпцию ответственности за долю рынка , пропорциональную их доле рынка на момент выпуска препарата. потребляется матерью конкретного истца. [ нужна цитата ]
Компания Eli Lilly, фармацевтическая компания, производящая DES, и Чикагский университет подали иск против них в отношении клинических испытаний 1950-х годов. Три женщины обратились с заявлением о том, что у их дочерей возникли аномальные клеточные образования шейки матки, а также репродуктивные нарушения у них самих и сыновей. [151] Истцы просили суды признать их дело коллективным иском, но суды им отказали. Однако суды пришли к выводу, что их дело обосновано. Суд постановил, что Eli Lilly была обязана уведомить о рисках DES, как только о них стало известно или должно было стать известно. [151] Согласно закону штата Иллинойс о правонарушениях, чтобы истцы могли получить возмещение в соответствии с теориями нарушения обязанности предупреждать и строгой ответственности, истцы должны заявить о причинении себе вреда. В конечном итоге, по их заявлениям о нарушении обязанности предупреждать и строгой ответственности, поскольку истцы ссылались на риск причинения телесных повреждений другим, а не себе, дело было прекращено судами. [151] Хотя дело не было квалифицировано как групповой иск, а их требования о нарушении обязанности предупреждать и строгой ответственности были отклонены, суды не отклонили обвинения в нанесении побоев. [151] Тогда вопрос заключался в том, чтобы определить, совершил ли Чикагский университет побои в отношении этих женщин, но дело было урегулировано до суда. [151] В рамках мирового соглашения по делу «Минк против Чикагского университета» адвокаты истцов договорились о том, чтобы университет проводил бесплатные медицинские осмотры для всех детей, подвергшихся воздействию DES внутриутробно во время экспериментов 1950 года, а также лечил дочерей. всех вовлеченных женщин, у которых развивается DES-ассоциированный рак влагалища или шейки матки. [151]
По состоянию на февраль 1991 года против производителей DES было возбуждено более тысячи судебных исков. [151] Более 300 компаний производят DES по одной и той же формуле, и самым большим препятствием на пути к выздоровлению является определение того, какой производитель поставлял препарат в каждом конкретном случае. [151] Многие из успешных дел основывались на совместной или нескольких сторонах, несущих ответственность.
Иск был подан в Федеральный суд Бостона 53 дочерьми DES, которые утверждают, что их рак молочной железы стал результатом того, что DES был прописан их матерям во время беременности. Их дела выдержали слушания в Добере . В 2013 году сестры Фечо, инициировавшие судебный процесс по делу о связи рака молочной железы и DES, согласились на нераскрытую сумму урегулирования на второй день судебного разбирательства. Остальные истцы получили различные компенсации. [152]
Правозащитная группа DES Action USA помогла предоставить информацию и поддержку лицам, подвергшимся воздействию DES, участвующим в судебных процессах. [153]
Алан Тьюринг , новаторский криптограф , основатель компьютерной науки и программируемых компьютеров, который также предложил реальную теоретическую модель биологического морфогенеза , вскоре был насильно прописан этому препарату, чтобы вызвать химическую кастрацию в качестве карательного и дискредитированного «лечения» гомосексуального поведения. прежде чем он умер при неоднозначных обстоятельствах. [154]
По крайней мере, однажды в Новой Зеландии в начале 1960-х годов диэтилстильбэстрол был прописан для «лечения» гомосексуализма. [155]
Джеймс Хэрриот описывает случай лечения опухоли яичек из клеток Сертоли у маленькой собаки в своей книге 1974 года « Все яркое и красивое» . Херриот решил прописать высокую дозу стильбоэстрола при рецидивирующей опухоли, с забавным побочным эффектом: кобель стал «привлекательным для других кобелей», которые следовали за терьером по деревне в течение нескольких недель. В статье Эрриот комментирует, что он знал: «Говорят, что новый препарат оказывает феминизирующий эффект, но, конечно, не в такой степени».
DES добился больших успехов в лечении недержания мочи у собак, вызванного плохим контролем сфинктера. Его по-прежнему можно приобрести в аптеках, и в низкой дозе (1 мг) он не обладает канцерогенными свойствами, которые были столь проблематичны для людей. [156] Обычно его вводят один раз в день в течение семи-десяти дней, а затем один раз в неделю по мере необходимости. [ нужна цитата ]
Наибольшее использование DES наблюдалось в животноводстве, где он использовался для улучшения конверсии корма при производстве говядины и птицы. В 1960-е годы DES использовался в качестве гормона роста в мясной и птицеводческой промышленности. Позже к 1971 году было обнаружено, что он вызывает рак, но его прекращение не прекращалось до 1979 года. [157] [158] Хотя было обнаружено, что DES вреден для человека, его использование в ветеринарии не было немедленно прекращено. По состоянию на 2011 год DES все еще использовался в качестве стимулятора роста наземного скота или рыбы в некоторых частях мира, включая Китай. [159]
Сульфат пиперазина эстрона и микронизированный эстрадиол были одинаково эффективны в отношении увеличения ГСПГ, тогда как [...] ДЭС был в 28,4 раза более эффективным [...]. Что касается снижения ФСГ, [...] ДЭС был в 3,8 раза, а этинилэстрадиол был в 80–200 раз более эффективным, чем сульфат пиперазина эстрона. Эквиваленты доз этинилэстрадиола (50 мкг) и ДЭС (1 мг) отражают эту относительную эффективность.220 [...] ДЭС, мощный синтетический эстроген (рис. 6-12), хорошо всасывается после перорального приема. У пациентов, получавших 1 мг DES ежедневно, концентрация в плазме через 20 часов колебалась от 0,9 до 1,9 нг на мл. Начальный период полувыведения ДЭС составляет 80 минут, а вторичный период полувыведения — 24 часа.223 Основными путями метаболизма являются превращение в глюкуронид и окисление. Окислительные пути включают ароматическое гидроксилирование этильных боковых цепей и дегидрирование до (Z,Z)-диенестрола с образованием временных хиноноподобных промежуточных продуктов, которые реагируют с клеточными макромолекулами и вызывают генетические повреждения в эукариотических клетках.223 Метаболическая активация DES может хорошо объяснить его действие. -установленные канцерогенные свойства.224
С начала 1940-х до 1970-х годов DES назначали беременным женщинам для предотвращения выкидыша, который часто сопровождается снижением уровня эстрогена.
Позже стало очевидно, что лечение СЛС по большей части неэффективно для предотвращения выкидыша [66], но, тем не менее, врачи продолжали назначать СПС беременным женщинам.
В недавней статье обобщаются эффекты воздействия DES на мать во время беременности и его неблагоприятное воздействие на беременность и развитие плода у женщин [67] и показано, что это воздействие увеличивает выкидыши во 2-м триместре в 3,8 раза.
Несколько десятилетий назад диэтилстильбестрол (ДЭС) считался эффективным средством улучшения исхода беременности.
Более поздние данные не подтвердили это, а матери и дети, подвергшиеся воздействию препарата, страдали от множества проблем, связанных с действием препарата.
[Диэтилстильбестрол] имеет серьезный недостаток: в дозах выше 1 мг.
в день он может вызвать тошноту, рвоту, дискомфорт в животе, головную боль и вздутие живота у части пациентов, по разным оценкам от 15 до 50%.
Было показано, что [диэтилстильбэстрол], явно отличающийся по химической структуре от ранее известных эстрогенов, оказывает все приписываемые ему биологические эффекты, такие как подавление антуитальной системы (2), ингибирование роста тела (2), пролиферация пластичных системы молочной железы (3), подавление нагрубания, связанного с лактацией (4), гиперемии, отека и вздутия матки (5), пролиферации эндометрия (6), ороговения влагалища (7), набухания половых органов. кожа (8).
Вероятно, он также обладает предполагаемыми канцерогенными свойствами настоящих эстрогенов (9).
После того, как Доддс, Голдберг, Лоусон и Робинсон показали, что стильбоэстрол (4,4'-диокси-α-β-диэтилстильбен оказывает такое же действие, как и природные эстроны, на слизистую оболочку влагалища кастрированных самок крыс, появилось большое количество работ, которые показывают, что это вещество, несмотря на его очень большое химическое отличие от естественных женских половых гормонов, оказывает практически тот же эффект, что и они во всех отношениях. Наиболее важные из этих исследований были сделаны Доддсом, Лоусоном и Ноблом, Ноблом, Бишопом. , Бойкот и Цукерманн, Эрик Гульдберг, Энгельхардт, Уинтертон и МакГрегор, Эрик Якобсен и совсем недавно Крейтмайр и Зикман, Бушбек и Хаускнехт, Кобет, Ратшоу и Штехнер.Предыдущие эксперименты были проведены на курах, мышах. , крысы, морские свинки, кролики, обезьяны и люди.
Не подлежит сомнению, что конверсия эндометрия при инъекциях как синтетических, так и нативных препаратов эстрогенных гормонов удается, однако мнение о том, могут ли нативные, перорально вводимые препараты вызывать пролиферацию слизистой оболочки, у разных авторов меняется.
ПЕДЕРСЕН-БЬЕРГААРД (1939) сумел показать, что 90% фолликулина, поступившего в кровь воротной вены, инактивируется в печени.
Ни KAUFMANN (1933, 1935), ни RAUSCHER (1939, 1942), ни HERRNBERGER (1941) не смогли вызвать пролиферацию кастрационного эндометрия с помощью больших доз перорально вводимых препаратов эстрона или эстрадиола.
Другие результаты сообщают НЕЙСТАЕДТЕР (1939), ЛАУТЕРВЕЙН (1940) и ФЕРИН (1941);
им удалось превратить атрофический кастрационный эндометрий в однозначную пролиферацию слизистой оболочки с помощью 120–300 эстрадиола или 380 эстрона.