Ацетон ( 2-пропанон или диметилкетон ) — органическое соединение формулы ( CH 3 ) 2 CO . [22] Это самый простой и наименьший кетон ( >C=O ). Это бесцветная, легколетучая и легковоспламеняющаяся жидкость с характерным резким запахом.
Ацетон смешивается с водой и служит важным органическим растворителем в промышленности, быту и лаборатории. В 2010 году во всем мире было произведено около 6,7 миллионов тонн , в основном для использования в качестве растворителя и для производства метилметакрилата и бисфенола А , которые являются предшественниками широко используемых пластмасс . [23] [24] Это обычный строительный блок в органической химии . Он служит растворителем в бытовых продуктах, таких как жидкость для снятия лака и растворитель для краски . В США он имеет статус освобождения от летучих органических соединений (ЛОС). [25]
Ацетон вырабатывается и утилизируется в организме человека посредством обычных метаболических процессов. Обычно он присутствует в крови и моче. Люди с диабетическим кетоацидозом производят его в больших количествах. Кетогенные диеты , повышающие кетоновые тела (ацетон, β-гидроксимасляную кислоту и ацетоуксусную кислоту ) в крови, используются для противодействия эпилептическим приступам у детей, страдающих рефрактерной эпилепсией. [26]
Начиная с 17 века и до современных разработок в номенклатуре органической химии , ацетону давали много разных названий. Эти названия включают дух Сатурна, который был дан, когда считалось, что он представляет собой соединение свинца , а затем пироуксусный спирт и пироуксусный эфир. [6]
До названия «ацетон», данного Антуаном Бюсси , его называл «месит» (от греческого μεσίτης, что означает посредник) Карлом Райхенбахом , который также утверждал, что метиловый спирт состоит из мезита и этилового спирта . [27] [6] Названия, полученные от слова «мезит», включают мезитилен и мезитилоксид , которые были впервые синтезированы из ацетона.
В отличие от многих соединений с префиксом ацет, имеющим двухуглеродную цепь, ацетон имеет трехуглеродную цепь, что вызвало путаницу, поскольку не может быть кетона с двумя атомами углерода. Приставка указывает на отношение ацетона к уксусу ( acetum на латыни , также источник слов «кислота» и «уксус»), а не на его химическую структуру. [28]
Ацетон был впервые получен Андреасом Либавиусом в 1606 году путем перегонки ацетата свинца (II) . [29] [30]
В 1832 году французский химик Жан-Батист Дюма и немецкий химик Юстус фон Либих определили эмпирическую формулу ацетона. [31] [32] В 1833 году французские химики Антуан Бюсси и Мишель Шеврёль решили назвать ацетон, добавив суффикс -один к основе соответствующей кислоты (а именно, уксусной кислоты ), точно так же, как полученный аналогичным образом продукт того, что тогда было перепутано. с маргариновой кислотой получил название маргарон. [33] [28] К 1852 году английский химик Александр Уильям Уильямсон понял, что ацетон — это метилацетил ; [34] В следующем году французский химик Шарль Фредерик Герхардт согласился. [35] В 1865 году немецкий химик Август Кекуле опубликовал современную структурную формулу ацетона. [36] [37] Иоганн Йозеф Лошмидт представил структуру ацетона в 1861 году, [38] но его частно изданный буклет не получил большого внимания. Во время Первой мировой войны Хаим Вейцман разработал процесс промышленного производства ацетона (процесс Вейцмана). [39]
В 2010 году мировые мощности по производству ацетона оценивались в 6,7 миллиона тонн в год. [40] С 1,56 млн тонн в год Соединенные Штаты имели самую высокую производственную мощность, [41] за ними следовали Тайвань и материковый Китай . Крупнейшим производителем ацетона является INEOS Phenol , владеющий 17% мировых мощностей, а также значительные мощности (7–8%) у Mitsui , Sunoco и Shell в 2010 году. [40] INEOS Phenol также владеет крупнейшей в мире производственной площадкой (420 000 тонн/год) в Беверене (Бельгия). Спотовая цена ацетона летом 2011 года в США составляла 1100–1250 долларов США за тонну. [42]
Ацетон производят прямо или косвенно из пропена . Примерно 83% ацетона производится кумоловым процессом ; [24] в результате производство ацетона связано с производством фенола. В кумоловом процессе бензол алкилируется пропиленом с образованием кумола , который окисляется воздухом с образованием фенола и ацетона:
Другие процессы включают прямое окисление пропилена ( процесс Вакера-Хехста ) или гидратацию пропилена с образованием 2-пропанола , который окисляется (дегидрируется) до ацетона. [24]
Раньше ацетон получали сухой перегонкой ацетатов , например ацетата кальция при кетоновом декарбоксилировании .
После этого, во время Первой мировой войны , ацетон производился с использованием ферментации ацетон-бутанол-этанол с бактериями Clostridium acetobutylicum , которая была разработана Хаимом Вейцманом (впоследствии первым президентом Израиля ), чтобы помочь британским военным усилиям, [24] при получении кордита . [43] От ферментации ацетон-бутанол-этанол в конечном итоге отказались, когда были найдены новые методы с лучшими выходами. [24]
Температура пламени чистого ацетона составляет 1980°С. [44]
Как и большинство кетонов, ацетон демонстрирует кето-еноловую таутомерию , при которой номинальная кето- структура (CH 3 ) 2 C=O самого ацетона находится в равновесии с енольным изомером (CH 3 )C(OH)=(CH 2 ) ( prop -1-ен-2-ол ). В парах ацетона при температуре окружающей среды всего 2,4 × 10−7 % молекул находятся в енольной форме. [45]
В присутствии подходящих катализаторов две молекулы ацетона также объединяются с образованием соединения диацетонового спирта (CH 3 )C=O(CH 2 )C(OH)(CH 3 ) 2 , которое при дегидратации дает мезитилоксид (CH 3 )C. =О(СН)=С(СН 3 ) 2 . Этот продукт может далее соединяться с другой молекулой ацетона с потерей другой молекулы воды, образуя форон и другие соединения. [46]
Ацетон — слабое основание Льюиса, которое образует аддукты с мягкими кислотами, такими как I 2 , и жесткими кислотами, такими как фенол . Ацетон также образует комплексы с двухвалентными металлами. [47] [48]
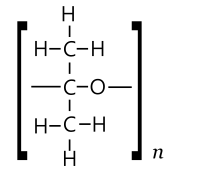
Можно было бы ожидать, что ацетон также образует полимеры и (возможно, циклические ) олигомеры двух типов. В одном типе звеньями могут быть молекулы ацетона, связанные эфирными мостиками -O-, образующимися в результате разрыва двойной связи, с образованием поликетальподобной (ПКА) цепи [-O-C(CH 3 ) 2 -] n . Другой тип может быть получен путем повторной альдольной конденсации, при которой на каждой стадии удаляется одна молекула воды, что дает цепь поли(метилацетилена) (ПМА) [-CH=C(CH 3 )-] n . [49]
Превращение ацетона в поликеталь (ПКА) будет аналогично образованию параформальдегида из формальдегида и тритиоацетона из тиоацетона . В 1960 году советские химики заметили, что термодинамика этого процесса неблагоприятна для жидкого ацетона, поэтому не ожидается его самопроизвольной полимеризации (в отличие от тиоацетона и формола), даже с использованием катализаторов. Однако они заметили, что термодинамика стала благоприятной для кристаллического твердого ацетона при температуре плавления (-96 ° C). Они утверждали, что получили такой полимер (белое эластичное твердое вещество, растворимое в ацетоне, стабильное в течение нескольких часов при комнатной температуре) путем нанесения паров ацетона с небольшим количеством магния в качестве катализатора на очень холодную поверхность. [50] В 1962 году Васабуро Каваи сообщил о синтезе аналогичного продукта из жидкого ацетона, охлажденного до -70 до -78 ° C, с использованием н -бутиллития или триэтилалюминия в качестве катализаторов. Он утверждал, что инфракрасный спектр поглощения показывает наличие связей -O- , но отсутствие групп C=O . [51] Однако позже другие исследователи получили противоречивые результаты. [49]
Полимеры ацетона типа ПМА будут эквивалентны продукту полимеризации пропина , за исключением концевой кетогруппы. [49]
Человек выдыхает несколько миллиграммов ацетона в день. Он возникает в результате декарбоксилирования ацетоацетата . [52] [53] Небольшое количество ацетона вырабатывается в организме в результате декарбоксилирования кетоновых тел . Определенные режимы питания, в том числе длительное голодание и диета с высоким содержанием жиров и низким содержанием углеводов, могут вызывать кетоз , при котором в тканях организма образуется ацетон. Определенные состояния здоровья, такие как алкоголизм и диабет, могут вызывать кетоацидоз — неконтролируемый кетоз, который приводит к резкому и потенциально смертельному повышению кислотности крови. Поскольку ацетон является побочным продуктом брожения, он является побочным продуктом ликеро-водочной промышленности. [52]
Затем ацетон может метаболизироваться либо с помощью CYP2E1 через метилглиоксаль до D -лактата и пирувата и, в конечном итоге, глюкозы /энергии, либо другим путем через пропиленгликоль до пирувата , лактата , ацетата (используемого для получения энергии) и пропиональдегида . [54] [55] [56]
Около трети мирового ацетона используется в качестве растворителя, а четверть потребляется в виде ацетонциангидрина , предшественника метилметакрилата . [23]
Ацетон является хорошим растворителем для многих пластмасс и некоторых синтетических волокон. Он используется для разжижения полиэфирной смолы , очистки инструментов, используемых с ней, а также растворения двухкомпонентных эпоксидных смол и суперклея до их затвердевания. Используется как один из летучих компонентов некоторых красок и лаков . В качестве обезжиривателя для тяжелых условий эксплуатации он полезен при подготовке металла перед покраской или пайкой , а также для удаления канифольного флюса после пайки (для предотвращения прилипания грязи и электрических утечек и, возможно, коррозии или по косметическим причинам), хотя он может разъедать некоторые электронные компоненты, такие как полистироловые конденсаторы. [57]
Хотя ацетон сам по себе легковоспламеняющийся , он широко используется в качестве растворителя для безопасной транспортировки и хранения ацетилена , который не может безопасно находиться под давлением в чистом виде. Сосуды, содержащие пористый материал, сначала наполняют ацетоном, а затем ацетиленом, который растворяется в ацетоне. Один литр ацетона может растворить около 250 литров ацетилена при давлении 10 бар (1,0 МПа). [58] [59]
Ацетон используется в качестве растворителя в фармацевтической промышленности и как денатурирующий агент в денатурированном спирте . [60] Ацетон также присутствует в качестве вспомогательного вещества в некоторых фармацевтических препаратах . [61]
Ацетон используется для синтеза метилметакрилата . Он начинается с первоначального превращения ацетона в ацетонциангидрин посредством реакции с цианидом водорода (HCN):
На следующем этапе нитрил гидролизуется до ненасыщенного амида , который этерифицируется :
Третьим основным применением ацетона (около 20%) [23] является синтез бисфенола А. Бисфенол А является компонентом многих полимеров, таких как поликарбонаты , полиуретаны и эпоксидные смолы . Синтез включает конденсацию ацетона с фенолом :
Многие миллионы килограммов ацетона расходуются на производство растворителей метилизобутилового спирта и метилизобутилкетона . Эти продукты возникают в результате начальной альдольной конденсации с образованием диацетонового спирта . [24]
Конденсация с ацетиленом дает 2-метилбут-3-ин-2-ол, предшественник синтетических терпенов и терпеноидов . [62]
В ряде органических реакций ацетон используется в качестве полярного апротонного растворителя . Это имеет решающее значение для окисления Джонса . Поскольку ацетон дешев, летуч и растворяется или разлагается с большинством лабораторных химикатов, промывание ацетоном является стандартным методом удаления твердых остатков из лабораторной посуды перед окончательной промывкой. [63] Несмотря на широко распространенное использование в сушильных машинах , ацетон высыхает только за счет объемного вытеснения и разбавления. Не образует азеотропов с водой (см. таблицы азеотропов ). [64]
Ацетон замерзает значительно ниже -78 ° C. Смесь ацетона и сухого льда охлаждает многие низкотемпературные реакции. [65]
Под ультрафиолетом ацетон флуоресцирует. В экспериментах по потоку жидкости ее пары используются в качестве индикатора . [66]
Белки осаждаются в ацетоне. [67] Химическое вещество модифицирует пептиды как по α- или ε-аминогруппам, так и посредством плохо изученной, но быстрой модификации некоторых остатков глицина. [67]
При патологии ацетон помогает найти лимфатические узлы в жировых тканях (например, в брыжейке ) для определения стадии опухоли . [68] Жидкость растворяет жир и затвердевает узлы, благодаря чему их легче найти. [69]
Ацетон также удаляет определенные пятна с предметных стекол . [70]
Дерматологи используют ацетон со спиртом для лечения прыщей, чтобы химически отшелушивать сухую кожу. Обычными агентами, используемыми сегодня для химического пилинга, являются салициловая кислота , гликолевая кислота , азелаиновая кислота , 30%-ная салициловая кислота в этаноле и трихлоруксусная кислота (ТСА). Перед химэксфолиацией кожа очищается и удаляется лишний жир в процессе, называемом обезжириванием. В этом процессе использовали ацетон, гексахлорофен или комбинацию этих агентов. [71]
Было показано, что ацетон оказывает противосудорожное действие на животных моделях эпилепсии при отсутствии токсичности при введении в миллимолярных концентрациях. [72] Была выдвинута гипотеза, что кетогенная диета с высоким содержанием жиров и низким содержанием углеводов , используемая в клинических целях для контроля лекарственно-устойчивой эпилепсии у детей, способствует повышению уровня ацетона в мозге. [72] Из-за более высоких энергетических потребностей дети производят больше ацетона, чем большинство взрослых – и чем младше ребенок, тем выше ожидаемое производство. Это указывает на то, что дети не являются уникальными восприимчивыми к воздействию ацетона. Внешнее воздействие невелико по сравнению с воздействием, связанным с кетогенной диетой. [73]
Визажисты используют ацетон для удаления кожного клея с сеток париков и усов, погружая изделие в ванну с ацетоном, а затем удаляя размягченные остатки клея жесткой кистью. [74]
Ацетон часто используется для полировки паром артефактов печати на 3D-моделях, напечатанных из АБС-пластика. Техника, называемая сглаживанием в паровой ванне с ацетоном, предполагает помещение напечатанной детали в герметичную камеру, содержащую небольшое количество ацетона, и нагревание примерно до 80 градусов по Цельсию в течение 10 минут. Это создает пары ацетона в контейнере. Ацетон конденсируется равномерно по всей детали, в результате чего поверхность размягчается и разжижается. Поверхностное натяжение затем разглаживает полужидкий пластик. Когда деталь извлекается из камеры, ацетоновый компонент испаряется, оставляя гладкую как стекло деталь без полос, узоров и видимых краев слоя, что является общим признаком необработанных деталей, напечатанных на 3D-принтере. [75]
Ацетон эффективно удаляет следы фломастера со стекла и металлов.
Самым опасным свойством ацетона является его чрезвычайная воспламеняемость. В небольших количествах ацетон горит тусклым синим пламенем ; в больших количествах испарение топлива вызывает неполное сгорание и ярко-желтое пламя . Если температура вспышки превышает температуру вспышки ацетона -20 °C (-4 °F), воздушные смеси с содержанием ацетона 2,5–12,8% (по объему) могут взорваться или вызвать вспышку возгорания . Пары могут стекать по поверхностям к удаленным источникам возгорания и вспыхивать обратно.
Статический разряд также может воспламенить пары ацетона, хотя ацетон имеет очень высокую энергию инициирования воспламенения, и случайное возгорание встречается редко. [76] Температура самовоспламенения ацетона относительно высока и составляет 465 ° C (869 ° F); [19] более того, температура самовоспламенения зависит от условий эксперимента, таких как время воздействия, и составляет 535 °C. [77] Даже обливание или распыление ацетона на раскаленный докрасна уголь не приведет к его воспламенению из-за высокой концентрации паров и охлаждающего эффекта испарения. [76]
Ацетон следует хранить вдали от сильных окислителей, таких как концентрированные смеси азотной и серной кислот . [78] Он также может взорваться при смешивании с хлороформом в присутствии основания. [79] [ необходимы разъяснения ] При окислении без горения, например, перекисью водорода , ацетон может образовывать перекись ацетона , крайне нестабильное первичное взрывчатое вещество . Пероксид ацетона может образоваться случайно, например, когда отработанный пероксид выливается в отработанные растворители. [80]
Ацетон возникает в природе как часть определенных метаболических процессов в организме человека, был тщательно изучен и считается, что при нормальном использовании он проявляет лишь незначительную токсичность. Нет убедительных доказательств хронических последствий для здоровья при соблюдении основных мер предосторожности. [81] Общепризнано, что он обладает низкой острой и хронической токсичностью при проглатывании и/или вдыхании. [82] Ацетон в настоящее время не считается канцерогеном , мутагеном или источником хронической нейротоксичности . [76]
Ацетон можно найти в качестве ингредиента в различных потребительских товарах, от косметики до обработанных и необработанных пищевых продуктов. Ацетон был признан общепризнанным безопасным веществом (GRAS) при его присутствии в напитках, выпечке, десертах и консервах в концентрациях от 5 до 8 мг/л. [82]
Однако ацетон является раздражителем, вызывающим легкое раздражение кожи и умеренное или сильное раздражение глаз. При высоких концентрациях паров он может угнетать центральную нервную систему , как и многие другие растворители. [83] Острая токсичность для мышей при проглатывании (LD 50 ) составляет 3 г/кг, а при вдыхании (LC 50 ) – 44 г/м 3 в течение 4 часов. [84]
Хотя ацетон в природе встречается в окружающей среде в растениях, деревьях, вулканических газах, лесных пожарах и как продукт распада жировых отложений, [85] большая часть ацетона, выбрасываемого в окружающую среду, имеет промышленное происхождение. [ нужны разъяснения ] Ацетон быстро испаряется даже из воды и почвы. Попав в атмосферу, он имеет период полураспада 22 дня и разлагается под воздействием УФ-излучения посредством фотолиза (в первую очередь на метан и этан . [86] ). Потребление микроорганизмами способствует рассеиванию ацетона в почве, животных или водных путях. [85]
В 1995 году Агентство по охране окружающей среды США (EPA) исключило ацетон из списка летучих органических соединений . Компании, запросившие удаление, утверждали, что это «будет способствовать достижению нескольких важных экологических целей и поддержит усилия Агентства по охране окружающей среды по предотвращению загрязнения», и что ацетон может использоваться в качестве заменителя некоторых соединений, внесенных в список опасных загрязнителей воздуха (HAP). в соответствии со статьей 112 Закона о чистом воздухе . [87] Принимая решение, Агентство по охране окружающей среды провело обширный анализ имеющихся данных о токсичности ацетона, который продолжался на протяжении 2000-х годов. Было обнаружено, что поддающиеся оценке «данные недостаточны для оценки канцерогенного потенциала ацетона для человека». [9]
30 июля 2015 года ученые сообщили , что после первого приземления спускаемого аппарата Philae на поверхность кометы 67P измерения с помощью инструментов COSAC и Ptolemy выявили шестнадцать органических соединений , четыре из которых были впервые обнаружены на комете, включая ацетамид. , ацетон, метилизоцианат и пропиональдегид . [88] [89] [90]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite web}}: CS1 maint: неподходящий URL ( ссылка ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ){{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )