Кальмодулин ( CaM ) (аббревиатура от кальций - модулированного белка ) представляет собой многофункциональный промежуточный кальций -связывающий белок-мессенджер, экспрессируемый во всех эукариотических клетках . [1] Это внутриклеточная мишень вторичного мессенджера Ca 2+ , и связывание Ca 2+ необходимо для активации кальмодулина. После связывания с Ca 2+ кальмодулин действует как часть пути передачи сигнала кальция , изменяя его взаимодействие с различными белками-мишенями, такими как киназы или фосфатазы . [2] [3] [4]
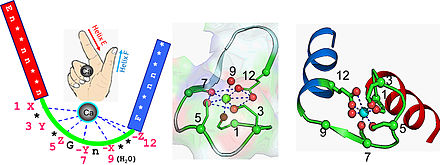
Кальмодулин представляет собой небольшой высококонсервативный белок длиной 148 аминокислот (16,7 кДа). Белок имеет два примерно симметричных глобулярных домена (N- и C-домены), каждый из которых содержит пару мотивов руки EF [5] , разделенных гибкой линкерной областью, всего четыре сайта связывания Ca 2+ , по два в каждом глобулярном домене. . [6] В состоянии, свободном от Ca 2+ , спирали, образующие четыре EF-руки, свернуты в компактной ориентации, а центральный линкер неупорядочен; [5] [6] [7] [8] в состоянии, насыщенном Ca 2+ , EF-ручные спирали принимают открытую ориентацию, примерно перпендикулярную друг другу, а центральный линкер образует протяженную альфа-спираль в кристаллической структуре. , [5] [6] , но остается в значительной степени неупорядоченным в растворе. [9] C-домен имеет более высокую аффинность связывания с Ca 2+ , чем N-домен. [10] [11]
Кальмодулин структурно очень похож на тропонин C , другой Ca 2+ -связывающий белок, содержащий четыре мотива EF-hand. [5] [12] Однако тропонин C содержит дополнительную альфа-спираль на своем N-конце и конститутивно связан со своей мишенью, тропонином I. Поэтому он не демонстрирует такого же разнообразия распознавания мишеней, как кальмодулин.
Способность кальмодулина распознавать огромный спектр белков-мишеней во многом обусловлена его структурной гибкостью. [13] В дополнение к гибкости центрального линкерного домена, N- и C-домены подвергаются конформационному циклированию «открыто-закрыто» в связанном с Ca 2+ состоянии. [9] Кальмодулин также демонстрирует большую структурную изменчивость и подвергается значительным конформационным флуктуациям при связывании с мишенями. [14] [15] [16] Более того, преимущественно гидрофобная природа связывания кальмодулина с большинством его мишеней позволяет распознавать широкий спектр последовательностей целевых белков. [14] [17] В совокупности эти особенности позволяют кальмодулину распознавать около 300 белков-мишеней [18] , демонстрирующих различные мотивы последовательностей, связывающихся с CaM.



Связывание Ca 2+ EF-руками вызывает открытие N- и C-доменов, что обнажает гидрофобные поверхности, связывающиеся с мишенью. [6] Эти поверхности взаимодействуют с комплементарными неполярными сегментами белков-мишеней, обычно состоящими из групп объемистых гидрофобных аминокислот, разделенных 10–16 полярными и/или основными аминокислотами. [18] [14] Гибкий центральный домен кальмодулина позволяет белку обертываться вокруг своей мишени, хотя известны альтернативные способы связывания. «Канонические» мишени кальмодулина, такие как киназы легкой цепи миозина и CaMKII , связываются только с белком, связанным с Ca 2+ , тогда как некоторые белки, такие как каналы NaV и белки IQ-мотива , также связываются с кальмодулином в отсутствие Са 2+ . [14] Связывание кальмодулина вызывает конформационные перестройки в целевом белке посредством «взаимно индуцированного соответствия», [19] что приводит к изменениям в функции целевого белка.
Связывание кальция кальмодулином демонстрирует значительную кооперативность , [5] [11], что делает кальмодулин необычным примером мономерного (одноцепочечного) кооперативно связывающегося белка. Кроме того, связывание с мишенью изменяет аффинность связывания кальмодулина с ионами Ca 2+ , [20] [21] [22] , что обеспечивает сложное аллостерическое взаимодействие между Ca 2+ и взаимодействиями связывания с мишенью. [23] Это влияние связывания с мишенью на аффинность Ca 2+ , как полагают, позволяет активировать Ca 2+ белков, которые конститутивно связаны с кальмодулином, таких как Ca 2+ -активированные калиевые (SK) каналы с малой проводимостью. [24]
Хотя кальмодулин в основном действует как белок, связывающий Са 2+ , он также координирует ионы других металлов. Например, в присутствии типичных внутриклеточных концентраций Mg 2+ (0,5–1,0 мМ) и концентраций Ca 2+ в покое (100 нМ) сайты связывания Ca 2+ кальмодулина по крайней мере частично насыщаются Mg 2+ . [25] Этот Mg 2+ замещается более высокими концентрациями Ca 2+ , генерируемыми сигнальными событиями. Аналогичным образом, Ca 2+ сам по себе может быть вытеснен ионами других металлов, такими как трехвалентные лантаноиды, которые связываются с карманами связывания кальмодулина даже сильнее, чем Ca 2+ . [26] [27] Хотя такие ионы искажают структуру кальмодулина [28] [29] и, как правило, не имеют физиологического значения из-за их нехватки in vivo , они, тем не менее, нашли широкое научное применение в качестве репортеров структуры и функции кальмодулина. [30] [31] [26]
Кальмодулин опосредует многие важные процессы, такие как воспаление , обмен веществ , апоптоз , сокращение гладких мышц , внутриклеточное движение, кратковременную и долговременную память , а также иммунный ответ . [32] [33] Кальций участвует во внутриклеточной сигнальной системе, действуя как диффундирующий вторичный мессенджер для первоначальных стимулов. Он делает это путем связывания различных мишеней в клетке, включая большое количество ферментов , ионных каналов , аквапоринов и других белков. [4] Кальмодулин экспрессируется во многих типах клеток и может располагаться в различных субклеточных местах, включая цитоплазму , внутри органелл или ассоциироваться с плазмой или мембранами органелл, но он всегда обнаруживается внутриклеточно. [33] Многие белки, с которыми связывается кальмодулин, не способны сами связывать кальций и используют кальмодулин в качестве сенсора кальция и преобразователя сигнала. Кальмодулин также может использовать запасы кальция в эндоплазматическом ретикулуме и саркоплазматическом ретикулуме . Кальмодулин может подвергаться посттрансляционным модификациям, таким как фосфорилирование , ацетилирование , метилирование и протеолитическое расщепление , каждое из которых потенциально может модулировать его действие.

Кальмодулин играет важную роль в соединении сокращений возбуждения (EC) и инициировании цикла поперечных мостиков в гладких мышцах , что в конечном итоге вызывает сокращение гладких мышц. [34] Чтобы активировать сокращение гладких мышц, головка легкой цепи миозина должна быть фосфорилирована. Это фосфорилирование осуществляется киназой легкой цепи миозина (MLC) . Эта киназа MLC активируется кальмодулином, когда она связывается с кальцием, таким образом делая сокращение гладких мышц зависимым от присутствия кальция за счет связывания кальмодулина и активации киназы MLC. [34]
Другой способ влияния кальмодулина на сокращение мышц заключается в контроле движения Ca 2+ через мембраны клеток и саркоплазматического ретикулума . Са2 + -каналы , такие как рианодиновый рецептор саркоплазматического ретикулума, могут ингибироваться кальмодулином, связанным с кальцием, что влияет на общий уровень кальция в клетке . [35] Кальциевые насосы выводят кальций из цитоплазмы или хранят его в эндоплазматическом ретикулуме , и этот контроль помогает регулировать многие последующие процессы.
Это очень важная функция кальмодулина, поскольку он косвенно играет роль во всех физиологических процессах, на которые влияет сокращение гладких мышц , таких как пищеварение и сокращение артерий (что помогает распределять кровь и регулировать кровяное давление ). [36]
Кальмодулин играет важную роль в активации киназы фосфорилазы , что в конечном итоге приводит к отщеплению глюкозы от гликогена гликогенфосфорилазой . [37]
Кальмодулин также играет важную роль в липидном обмене , влияя на кальцитонин . Кальцитонин представляет собой полипептидный гормон, который снижает уровень Ca 2+ в крови и активирует каскады G-белков , что приводит к образованию цАМФ. Действие кальцитонина можно блокировать путем ингибирования действия кальмодулина, что позволяет предположить, что кальмодулин играет решающую роль в активации кальцитонина. [37]
Са 2+ /кальмодулин-зависимая протеинкиназа II (CaMKII) играет решающую роль в типе синаптической пластичности, известном как долговременная потенциация (LTP), которая требует присутствия кальция/кальмодулина. CaMKII способствует фосфорилированию рецептора AMPA , что повышает чувствительность рецепторов AMPA. [38] Кроме того, исследования показывают, что ингибирование CaMKII мешает LTP. [38]
.jpg/440px-Sorghum_bicolor_(4171536532).jpg)
В то время как дрожжи имеют только один ген CaM, растения и позвоночные содержат эволюционно консервативную форму генов CaM. Разница между растениями и животными в передаче сигналов Ca 2+ заключается в том, что растения содержат расширенное семейство CaM в дополнение к эволюционно консервативной форме. [39] Кальмодулины играют важную роль в развитии растений и адаптации к стимулам окружающей среды.
Кальций играет ключевую роль в структурной целостности клеточной стенки и мембранной системы клетки. Однако высокие уровни кальция могут быть токсичными для клеточного энергетического метаболизма растения, и, следовательно, концентрация Ca 2+ в цитозоле поддерживается на субмикромолярном уровне за счет удаления цитозольного Ca 2+ либо в апопласт , либо в просвет внутриклеточных органелл. . Импульсы Ca 2+ , создаваемые за счет увеличения притока и оттока, действуют как клеточные сигналы в ответ на внешние раздражители, такие как гормоны, свет, гравитация, абиотические стрессовые факторы, а также на взаимодействие с патогенами. [40]
Растения содержат белки, родственные CaM (CML), помимо типичных белков CaM. CML имеют аминокислотное сходство с типичными CaM примерно на 15%. Arabidopsis thaliana содержит около 50 различных генов ХМЛ, что приводит к вопросу о том, какой цели служат эти разнообразные белки в клеточной функции. Все виды растений демонстрируют такое разнообразие генов ХМЛ. Различные CaM и CML различаются по своей способности связывать и активировать ферменты, регулируемые CaM, in vivo . Также обнаружено, что CaM или CML расположены в разных компартментах органелл.
У арабидопсиса белок DWF1 играет ферментативную роль в биосинтезе брассиностероидов, стероидных гормонов растений, необходимых для роста. Между CaM и DWF1 происходит взаимодействие, [ необходимы разъяснения ] , и DWF1, будучи неспособным связывать CaM, не может обеспечить фенотип регулярного роста у растений. Следовательно, CaM необходим для функции DWF1 в росте растений.
Известно также, что белки, связывающие CaM, регулируют репродуктивное развитие растений. Например, СаМ-связывающая протеинкиназа табака действует как негативный регулятор цветения. Однако эти CaM-связывающие протеинкиназы также присутствуют в апикальной меристеме побега табака, и высокая концентрация этих киназ в меристеме вызывает задержку перехода растения к цветению.
Киназа рецептора S -локуса (SRK) представляет собой еще одну протеинкиназу, которая взаимодействует с CaM. SRK участвует в реакциях самонесовместимости, вовлеченных во взаимодействие пыльцы и пестика у Brassica .
Цели CaM у Arabidopsis также участвуют в развитии пыльцы и оплодотворении. Транспортеры Ca 2+ необходимы для роста пыльцевых трубок . Следовательно, постоянный градиент Ca 2+ поддерживается на вершине пыльцевой трубки для удлинения во время процесса оплодотворения. Точно так же CaM также важен в верхушке пыльцевой трубки, где его основная роль заключается в управлении ростом пыльцевой трубки.
Са 2+ играет важную роль в образовании клубеньков у бобовых. Азот — важнейший элемент, необходимый растениям и многим бобовым, неспособным самостоятельно фиксировать азот, вступает в симбиотическое соединение с азотфиксирующими бактериями, восстанавливающими азот до аммиака. Для установления взаимодействия бобовых и ризобий необходим фактор Nod, который продуцируется бактериями Rhizobium . Фактор Nod распознается волосковыми клетками корня, которые участвуют в образовании клубеньков у бобовых. Характерно участие Ca 2+ -ответов различной природы в распознавании Nod-фактора. Вначале происходит поток Ca 2+ на кончике корневого волоса, за которым следуют повторяющиеся колебания Ca 2+ в цитозоле, а также вокруг ядра происходит всплеск Ca 2+ . DMI3, важный ген для сигнальных функций Nod-фактора, расположенных ниже сигнатуры всплеска Ca 2+ , может распознавать сигнатуру Ca 2+ . Кроме того, несколько генов CaM и CML у Medicago и Lotus экспрессируются в клубеньках.
Среди разнообразного спектра защитных стратегий, которые растения используют против патогенов, очень распространена передача сигналов Ca 2+ . Уровни свободного Ca 2+ в цитоплазме повышаются в ответ на патогенную инфекцию. Сигнатуры Ca 2+ такой природы обычно активируют защитную систему растений, индуцируя связанные с защитой гены и гиперчувствительную гибель клеток. CaM, CML и CaM-связывающие белки являются одними из недавно идентифицированных элементов сигнальных путей защиты растений. Некоторые гены ХМЛ в табаке , фасоли и томатах чувствительны к патогенам. CML43 представляет собой белок, родственный CaM, который, выделенный из гена APR134 в устойчивых к болезням листьях Arabidopsis для анализа экспрессии генов, быстро индуцируется при инокуляции листьев Pseudomonas syringae . Эти гены также обнаружены в томатах ( Solanum lycopersicum ). CML43 из APR134 также связывается с ионами Ca 2+ in vitro, что показывает, что CML43 и APR134, следовательно, участвуют в Ca 2+ -зависимой передаче сигналов во время иммунного ответа растений на бактериальные патогены. [41] Экспрессия CML9 у Arabidopsis thaliana быстро индуцируется фитопатогенными бактериями, флагеллином и салициловой кислотой. [42] Экспрессия соевых SCaM4 и SCaM5 в трансгенном табаке и арабидопсисе вызывает активацию генов, связанных с устойчивостью к патогенам, а также приводит к усилению устойчивости к широкому спектру патогенных инфекций. Этого нельзя сказать о SCaM1 и SCaM2 сои, которые являются высококонсервативными изоформами CaM. Белок At BAG6 представляет собой CaM-связывающий белок, который связывается с CaM только в отсутствие Ca 2+ , а не в его присутствии. BAG6 отвечает за сверхчувствительную реакцию запрограммированной гибели клеток, чтобы предотвратить распространение патогенной инфекции или ограничить рост патогена. Мутации в белках, связывающих CaM, могут привести к серьезным последствиям для защитной реакции растений на патогенные инфекции. Циклические нуклеотидзависимые каналы (CNGC) представляют собой функциональные белковые каналы в плазматической мембране, которые имеют перекрывающиеся сайты связывания CaM, транспортирующие двухвалентные катионы, такие как Ca 2+ . Однако точная роль позиционирования CNGC на этом пути защиты растений до сих пор неясна.
Изменение внутриклеточных уровней Ca 2+ используется в качестве признака разнообразных реакций на механические раздражители, осмотические и солевые воздействия, а также холодовые и тепловые шоки. Различные типы клеток корня демонстрируют различную реакцию Ca 2+ на осмотический и солевой стресс, и это подразумевает клеточную специфичность структуры Ca 2+ . В ответ на внешний стресс КаМ активирует глутаматдекарбоксилазу (GAD), которая катализирует превращение L -глутамата в ГАМК. Жесткий контроль синтеза ГАМК важен для развития растений, и, следовательно, повышенный уровень ГАМК может существенно повлиять на развитие растений. Следовательно, внешний стресс может влиять на рост и развитие растений, и КаМ участвует в этом пути, контролируя этот эффект. [ нужна цитата ]
Растение сорго является хорошо зарекомендовавшим себя модельным организмом и может адаптироваться в жарких и засушливых условиях. По этой причине его используют в качестве модели для изучения роли кальмодулина в растениях. [43] Сорго содержит проростки, которые экспрессируют богатый глицином РНК-связывающий белок , SbGRBP. Этот конкретный белок можно модулировать, используя тепло в качестве стрессора. Его уникальное расположение в ядре клетки и цитозоле демонстрирует взаимодействие с кальмодулином, требующее использования Ca 2+ . [44] Подвергая растение различным стрессовым условиям, оно может вызвать подавление различных белков , которые позволяют растительным клеткам переносить изменения окружающей среды. Показано, что эти модулированные стрессовые белки взаимодействуют с CaM. Гены CaMBP , экспрессируемые в сорго, представлены как «модельная культура» для исследования устойчивости к жаре и засухе .
В исследовании Arabidopsis thaliana сотни различных белков продемонстрировали возможность связываться с CaM в растениях. [43]
Кальмодулин принадлежит к одной из двух основных групп кальцийсвязывающих белков, называемых белками рук EF . Другая группа, называемая аннексинами , связывает кальций и фосфолипиды, такие как липокортин . Многие другие белки связывают кальций, хотя связывание кальция не считается их основной функцией в клетке.