Т-клетки являются одним из важных типов лейкоцитов иммунной системы и играют центральную роль в адаптивном иммунном ответе . Т-клетки можно отличить от других лимфоцитов по наличию рецептора Т-клеток (TCR) на их поверхности .
Т-клетки рождаются из гемопоэтических стволовых клеток , [1] обнаруженных в костном мозге . Развивающиеся Т-клетки затем мигрируют в вилочковую железу для развития (или созревания). Т-клетки получили свое название от тимуса . [2] [3] После миграции в тимус клетки-предшественники созревают в несколько различных типов Т-клеток. Дифференцировка Т-клеток продолжается и после того, как они покинули тимус. Группы специфических дифференцированных подтипов Т-клеток выполняют множество важных функций по контролю и формированию иммунного ответа .
Одной из этих функций является иммуноопосредованная гибель клеток, и она осуществляется двумя основными подтипами: CD8+ «киллерами» (цитотоксическими) и CD4+ «помощниками» Т-клетками. (Они названы в честь присутствия белков клеточной поверхности CD8 или CD4 .) CD8+ Т-клетки, также известные как «Т-клетки-киллеры», цитотоксичны – это означает, что они способны непосредственно убивать инфицированные вирусом клетки, а также раковые клетки. CD8+ Т-клетки также способны использовать небольшие сигнальные белки, известные как цитокины , для рекрутирования других типов клеток при формировании иммунного ответа. Другая популяция Т-клеток, CD4+ Т-клеток, действует как «клетки-помощники». В отличие от Т-клеток-киллеров CD8+, Т-хелперные Т-клетки CD4+ функционируют путем дальнейшей активации В-клеток памяти и цитотоксических Т-клеток, что приводит к усилению иммунного ответа. Специфический адаптивный иммунный ответ, регулируемый Т - клеткой, зависит от ее подтипа (например, Т-хелпер1, Т-хелпер2, Т-хелпер17, регуляторная Т-клетка) [4] , который отличается типами секретируемых ими цитокинов. [2]
Регуляторные Т-клетки — это еще одна особая популяция Т-клеток, обеспечивающая критический механизм толерантности , посредством которого иммунные клетки способны отличать вторгающиеся клетки от «собственных». Это предотвращает неадекватную реакцию иммунных клеток против собственных клеток, известную как « аутоиммунный » ответ. По этой причине эти регуляторные Т-клетки также называют «супрессорными» Т-клетками. Эти же регуляторные Т-клетки также могут быть использованы раковыми клетками для предотвращения распознавания опухолевых клеток и иммунного ответа против них.
Все Т-клетки происходят из c-kit + Sca1 + гемопоэтических стволовых клеток (HSC), которые находятся в костном мозге. В некоторых случаях источником может быть печень плода во время эмбрионального развития . Затем HSC дифференцируются в мультипотентные предшественники (MPP), которые сохраняют потенциал стать как миелоидными , так и лимфоидными клетками . Затем процесс дифференцировки переходит к общему лимфоидному предшественнику (CLP), который может дифференцироваться только в Т-, В- или NK-клетки. [5] Эти клетки CLP затем мигрируют через кровь в тимус, где они приживляются: Отныне они известны как тимоциты , незрелая стадия Т-клетки.
Самые ранние клетки, попавшие в тимус, обычно называют дважды негативными , поскольку они не экспрессируют ни корецептор CD4 , ни CD8 . Вновь прибывшие клетки CLP представляют собой клетки CD4 - CD8 - CD44 + CD25 - ckit + и называются клетками-предшественниками тимуса (ETP). [6] Эти клетки затем подвергаются циклу деления и подавляют c-kit и называются клетками с двойной негативностью (DN1). Чтобы стать Т-клетками, тимоциты должны пройти несколько стадий ДН, а также положительный и отрицательный отбор.
Двойно-негативные тимоциты можно идентифицировать по поверхностной экспрессии CD2 , CD5 и CD7 . Тем не менее, во время двойной негативной стадии экспрессия CD34 прекращается и экспрессируется CD1 . Экспрессия CD4 и CD8 делает их дважды положительными и созревает в клетки CD4+ или CD8+.
Критическим шагом в созревании Т-клеток является создание функционального рецептора Т-клеток (TCR). Каждая зрелая Т-клетка в конечном итоге будет содержать уникальный TCR, который реагирует на случайный образец, позволяя иммунной системе распознавать множество различных типов патогенов . Этот процесс важен для развития иммунитета к угрозам, с которыми иммунная система раньше не сталкивалась, поскольку из-за случайных изменений всегда будет хотя бы один TCR, соответствующий любому новому патогену.
Тимоцит может стать активной Т-клеткой только тогда, когда он переживет процесс развития функционального TCR. TCR состоит из двух основных компонентов: альфа- и бета-цепей. Оба они содержат случайные элементы, предназначенные для создания самых разных TCR, но из-за такого огромного разнообразия их необходимо протестировать, чтобы убедиться, что они вообще работают. Сначала тимоциты пытаются создать функциональную бета-цепь, проверяя ее на соответствие «фиктивной» альфа-цепи. Затем они пытаются создать функциональную альфа-цепочку. После того, как рабочий TCR создан, клетки должны проверить, правильно ли их TCR идентифицирует угрозы, и для этого необходимо распознать главный комплекс гистосовместимости организма (MHC) в процессе, известном как положительный отбор. Тимоцит также должен гарантировать, что он не реагирует неблагоприятно на «собственные» антигены , что называется негативным отбором. Если и положительный, и отрицательный отбор успешны, TCR становится полностью работоспособным, и тимоцит становится Т-клеткой.
На стадии DN2 (CD44 + CD25 + ) клетки активируют гены рекомбинации RAG1 и RAG2 и перестраивают локус TCRβ , объединяя гены рекомбинации VDJ и гены константной области в попытке создать функциональную цепь TCRβ. По мере того, как развивающийся тимоцит достигает стадии DN3 (CD44 - CD25 + ), тимоцит экспрессирует инвариантную α-цепь, называемую пре-Tα, наряду с геном TCRβ. Если перестроенная β-цепь успешно спаривается с инвариантной α-цепью, вырабатываются сигналы, которые прекращают реаранжировку β-цепи (и заглушают альтернативный аллель). [7] Хотя эти сигналы требуют присутствия pre-TCR на поверхности клетки, они не зависят от связывания лиганда с pre-TCR. Если цепи успешно спариваются, образуется пре-TCR, и клетка подавляет CD25, и ее называют клеткой DN4 (CD25 - CD44- ) . Затем эти клетки подвергаются циклу пролиферации и начинают перестраивать локус TCRα на стадии двойного положительного результата .
Процесс положительного отбора занимает 3–4 дня и происходит в коре тимуса. [8] Дважды положительные тимоциты (CD4 + /CD8 + ) мигрируют глубоко в кору тимуса , где они презентируются аутоантигенами . Эти аутоантигены экспрессируются кортикальными эпителиальными клетками тимуса на молекулах MHC, которые находятся на поверхности кортикальных эпителиальных клеток. Только тимоциты, которые хорошо взаимодействуют с MHC-I или MHC-II, получат жизненно важный «сигнал выживания», тогда как те, которые не могут взаимодействовать достаточно сильно, не получат сигнала и погибнут из-за пренебрежения. Этот процесс гарантирует, что выжившие тимоциты будут иметь «родство к MHC», что означает, что они могут выполнять полезные функции в организме, реагируя на молекулы MHC, помогая иммунным ответам. Подавляющее большинство развивающихся тимоцитов не проходят положительный отбор и погибают во время этого процесса. [9]
Судьба тимоцита определяется в ходе положительного отбора. Двойно-положительные клетки (CD4 + /CD8 + ), которые хорошо взаимодействуют с молекулами MHC класса II , в конечном итоге становятся CD4 + «клетками-помощниками», тогда как тимоциты, которые хорошо взаимодействуют с молекулами MHC класса I, созревают в CD8 + «клетки-киллеры». Тимоцит становится клеткой CD4 + за счет подавления экспрессии его рецепторов на поверхности клетки CD8. Если клетка не потеряет свой сигнал, она продолжит подавлять CD8 и станет CD4 + . Клетки CD8 + и CD4 + теперь являются одиночными положительными клетками. [10]
Этот процесс не фильтрует тимоциты, которые могут вызвать аутоиммунитет . Потенциально аутоиммунные клетки удаляются с помощью следующего процесса негативной селекции, который происходит в мозговом веществе тимуса.
Отрицательный отбор удаляет тимоциты, способные прочно связываться с «собственными» молекулами MHC. Тимоциты, пережившие положительный отбор, мигрируют к границе коркового и мозгового вещества тимуса. Находясь в мозговом веществе, им снова представлен аутоантиген, представленный комплексом MHC медуллярных эпителиальных клеток тимуса (mTEC). [11] mTECs должны быть положительными в отношении аутоиммунного регулятора (AIRE + ), чтобы правильно экспрессировать аутоантигены из всех тканей организма на своих пептидах MHC класса I. Некоторые mTEC фагоцитируются дендритными клетками тимуса ; это делает их AIRE - антигенпрезентирующими клетками (APC), позволяющими презентировать аутоантигены на молекулах MHC класса II (положительно отобранные CD4 + клетки должны взаимодействовать с этими молекулами MHC класса II, поэтому APC, которые обладают MHC класса II, должны быть присутствует для отрицательной селекции CD4 + Т-клеток). Тимоциты, слишком сильно взаимодействующие с аутоантигеном, получают апоптотический сигнал, который приводит к гибели клеток. Однако некоторые из этих клеток отбираются и становятся Treg- клетками. Остальные клетки покидают тимус в виде зрелых наивных Т-клеток , также известных как недавние эмигранты из тимуса. [12] Этот процесс является важным компонентом центральной толерантности и служит для предотвращения образования аутореактивных Т-клеток, которые способны вызывать аутоиммунные заболевания у хозяина.
β-селекция является первой контрольной точкой, где тимоцитам, способным образовывать функциональный пре-TCR (с инвариантной альфа-цепью и функциональной бета-цепью), разрешается продолжить развитие в тимусе. Затем положительный отбор проверяет, что тимоциты успешно реаранжировали свой локус TCRα и способны распознавать молекулы MHC с соответствующим сродством. Негативный отбор в мозговом веществе затем устраняет тимоциты, которые слишком сильно связываются с аутоантигенами, экспрессируемыми на молекулах MHC. Эти процессы отбора обеспечивают толерантность иммунной системы к себе. Типичные наивные Т-клетки, покидающие тимус (через кортикомедуллярное соединение), являются самоограничивающимися, самотолерантными и единично положительными.
Около 98% тимоцитов погибают во время процессов развития в тимусе из-за неудачи положительного или отрицательного отбора, тогда как остальные 2% выживают и покидают тимус, чтобы стать зрелыми иммунокомпетентными Т-клетками. [13] С возрастом тимус производит меньше клеток. Поскольку в среднем возрасте тимус сокращается примерно на 3% [14] в год, происходит соответствующее снижение производства наивных Т-клеток в тимусе, в результате чего расширение и регенерация периферических Т-клеток играют большую роль в защите пожилых людей.
Т-клетки сгруппированы в ряд подмножеств в зависимости от их функции. Т-клетки CD4 и CD8 отбираются в тимусе, но подвергаются дальнейшей дифференцировке на периферии в специализированные клетки, имеющие разные функции. Подпопуляции Т-клеток изначально определялись по функциям, но также имели связанные с ними закономерности экспрессии генов или белков.

Т-хелперные клетки (Т - клетки) помогают другим лимфоцитам, включая созревание В-клеток в плазматические клетки и В-клетки памяти , а также активацию цитотоксических Т-клеток и макрофагов . Эти клетки также известны как CD4 + Т-клетки , поскольку они экспрессируют гликопротеин CD4 на своей поверхности. Т-хелперы активируются, когда им презентируются пептидные антигены молекулами MHC класса II , которые экспрессируются на поверхности антигенпрезентирующих клеток (APC). После активации они быстро делятся и выделяют цитокины , которые регулируют или помогают иммунному ответу. Эти клетки могут дифференцироваться в один из нескольких подтипов, выполняющих разные роли. Цитокины направляют Т-клетки в определенные подтипы. [15]
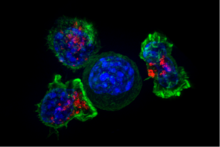
Цитотоксические Т-клетки (TC - клетки, CTL, Т-киллеры, Т-киллеры) разрушают инфицированные вирусом клетки и опухолевые клетки, а также участвуют в отторжении трансплантата . Эти клетки характеризуются экспрессией белка CD8 на их клеточной поверхности. Цитотоксические Т-клетки распознают свои мишени путем связывания с короткими пептидами ( длиной 8-11 аминокислот ), связанными с молекулами MHC класса I , присутствующими на поверхности всех ядросодержащих клеток. Цитотоксические Т-клетки также продуцируют ключевые цитокины IL-2 и IFNγ. Эти цитокины влияют на эффекторные функции других клеток, в частности макрофагов и NK-клеток.
Антиген-наивные Т-клетки размножаются и дифференцируются в память и эффекторные Т-клетки после того, как они встречают родственный антиген в контексте молекулы MHC на поверхности профессиональной антигенпрезентирующей клетки (например, дендритной клетки). Чтобы этот процесс произошел, во время встречи с антигеном должна присутствовать соответствующая костимуляция. Исторически считалось, что Т-клетки памяти относятся либо к эффекторному, либо к центральному подтипу памяти, каждый из которых имеет свой собственный отличительный набор маркеров клеточной поверхности (см. ниже). [19] Впоследствии были обнаружены многочисленные новые популяции Т-клеток памяти, включая тканерезидентные Т-клетки памяти (Trm), стволовые клетки памяти TSCM и Т-клетки виртуальной памяти. Единственная объединяющая тема для всех подтипов Т-клеток памяти заключается в том, что они долгоживущие и могут быстро размножаться до большого количества эффекторных Т-клеток при повторном воздействии родственного им антигена. Благодаря этому механизму они обеспечивают иммунной системе «память» против ранее встречавшихся патогенов. Т-клетки памяти могут быть либо CD4 + , либо CD8 + и обычно экспрессируют CD45RO . [20]
Подтипы Т-клеток памяти:
Регуляторные Т-клетки имеют решающее значение для поддержания иммунологической толерантности . Их основная роль заключается в отключении Т-клеточного иммунитета к концу иммунной реакции и подавлении аутореактивных Т-клеток , которые избежали процесса негативной селекции в тимусе.
Описаны два основных класса CD4 + T -рег -клеток — FOXP3 + T- reg -клетки и FOXP3 - T - reg- клетки.
Регуляторные Т-клетки могут развиваться либо во время нормального развития в тимусе и тогда известны как Treg-клетки тимуса, либо могут индуцироваться периферически и называются Treg-клетками периферического происхождения. Эти два подмножества ранее назывались «естественными» и «адаптивными» (или «индуцированными») соответственно. [26] Обе подгруппы требуют экспрессии фактора транскрипции FOXP3 , который можно использовать для идентификации клеток. Мутации гена FOXP3 могут предотвратить развитие регуляторных Т-клеток, вызывая смертельное аутоиммунное заболевание IPEX .
Некоторые другие типы Т-клеток обладают супрессивной активностью, но не экспрессируют FOXP3 конститутивно. К ним относятся клетки Tr1 и Th3 , которые, как полагают, возникают во время иммунного ответа и действуют путем производства подавляющих молекул. Клетки Tr1 связаны с IL-10, а клетки Th3 — с TGF-бета . Недавно к этому списку добавились клетки Th17 . [27]
Врожденные Т-клетки или нетрадиционные Т-клетки представляют собой некоторые подмножества Т-клеток, которые по-разному ведут себя в иммунитете. Они вызывают быстрые иммунные ответы независимо от экспрессии главного комплекса гистосовместимости (MHC), в отличие от своих обычных аналогов (Т-хелперных клеток CD4 и цитотоксических Т-клеток CD8), которые зависят от распознавания пептидных антигенов в контексте молекулы MHC. В целом существует три большие популяции нетрадиционных Т-клеток: NKT-клетки, MAIT-клетки и гамма-дельта-Т-клетки. Теперь их функциональные роли уже хорошо известны в контексте инфекций и рака. [28] Кроме того, эти субпопуляции Т-клеток используются во многих методах лечения злокачественных опухолей, таких как, например, лейкемия. [29]
Естественные Т-клетки-киллеры (NKT-клетки – не путать с естественными киллерными клетками врожденной иммунной системы) соединяют адаптивную иммунную систему с врожденной иммунной системой . В отличие от обычных Т-клеток, которые распознают белково-пептидные антигены, представленные молекулами главного комплекса гистосовместимости (MHC), NKT-клетки распознают гликолипидные антигены, представленные CD1d . После активации эти клетки могут выполнять функции, приписываемые как хелперным, так и цитотоксическим Т-клеткам: выработка цитокинов и высвобождение цитолитических/клеточных молекул. Они также способны распознавать и уничтожать некоторые опухолевые клетки и клетки, зараженные вирусами герпеса. [30]
Связанные со слизистой оболочкой инвариантные Т-клетки (MAIT) обладают врожденными эффекторными свойствами. [31] [32] У людей клетки MAIT обнаруживаются в крови, печени, легких и слизистой оболочке , защищая от микробной активности и инфекций. [31] Белок , подобный MHC класса I , MR1 , отвечает за представление продуцируемых бактериями метаболитов витамина B клеткам MAIT. [33] [34] [35] После презентации чужеродного антигена с помощью MR1 клетки MAIT секретируют провоспалительные цитокины и способны лизировать бактериально инфицированные клетки. [31] [35] Клетки MAIT также могут быть активированы посредством MR1-независимой передачи сигналов. [35] В дополнение к врожденным функциям, эта подгруппа Т-клеток поддерживает адаптивный иммунный ответ и имеет фенотип, подобный памяти. [31] Кроме того, считается, что клетки MAIT играют роль в аутоиммунных заболеваниях , таких как рассеянный склероз , артрит и воспалительные заболевания кишечника , [36] [37] , хотя окончательные доказательства еще не опубликованы. [38] [39] [40] [41]
Гамма-дельта-Т-клетки (γδ-Т-клетки) представляют собой небольшую подгруппу Т-клеток, которые обладают TCR γδ, а не αβ TCR на поверхности клетки. Большинство Т-клеток экспрессируют цепи αβ TCR. Эта группа Т-клеток гораздо реже встречается у людей и мышей (около 2% от общего числа Т-клеток) и обнаруживается в основном в слизистой оболочке кишечника , в популяции интраэпителиальных лимфоцитов . У кроликов, овец и кур количество γδ Т-клеток может достигать 60% от общего числа Т-клеток. Антигенные молекулы, активирующие γδ Т-клетки, до сих пор по большей части неизвестны. Однако γδ Т-клетки не ограничены MHC и, по-видимому, способны распознавать целые белки, а не требуют, чтобы пептиды были представлены молекулами MHC на APC . Некоторые мышиные γδ Т-клетки распознают молекулы MHC класса IB. Т-клетки γδ человека, которые используют фрагменты генов Vγ9 и Vδ2, составляют основную популяцию γδ-Т-клеток в периферической крови. Эти клетки уникальны тем, что они специфически и быстро реагируют на набор непептидных фосфорилированных предшественников изопреноидов , называемых фосфоантигенами , которые продуцируются практически всеми живыми клетками. Наиболее распространенными фосфоантигенами клеток животных и человека (включая раковые клетки) являются изопентенилпирофосфат (IPP) и его изомер диметилаллилпирофосфат (DMPP). Многие микробы, помимо IPP и DMAPP, производят активное соединение гидрокси-DMAPP ( HMB-PP ) и соответствующие мононуклеотидные конъюгаты. Растительные клетки продуцируют оба типа фосфоантигенов. Препараты, активирующие Т-клетки Vγ9/Vδ2 человека, включают синтетические фосфоантигены и аминобисфосфонаты , которые активируют эндогенный IPP/DMAPP.
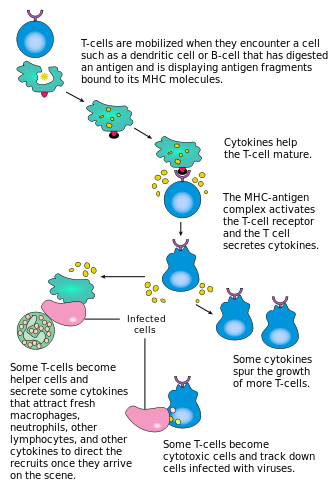
Активация CD4 + Т-клеток происходит посредством одновременного взаимодействия рецептора Т-клеток и костимулирующей молекулы (например , CD28 или ICOS ) на Т-клетке с помощью пептида главного комплекса гистосовместимости (MHCII) и костимулирующих молекул на Т-клетке. АПК . Оба необходимы для создания эффективного иммунного ответа; в отсутствие совместной стимуляции передача сигналов Т-клеточным рецептором сама по себе приводит к анергии . Сигнальные пути, расположенные ниже костимулирующих молекул, обычно включают путь PI3K , генерирующий PIP3 на плазматической мембране и рекрутирующий домен PH , содержащий сигнальные молекулы, такие как PDK1 , которые необходимы для активации PKC-θ и возможной продукции IL-2 . Оптимальный ответ CD8 + Т-клеток зависит от передачи сигналов CD4 + . [43] Клетки CD4 + полезны для начальной антигенной активации наивных Т-клеток CD8 и поддержания CD8 + Т-клеток памяти после острой инфекции. Следовательно, активация CD4 + Т-клеток может быть полезна для действия CD8 + Т-клеток. [44] [45] [46]
Первый сигнал обеспечивается связыванием рецептора Т-клеток с родственным ему пептидом, представленным на MHCII на APC. MHCII ограничен так называемыми профессиональными антигенпрезентирующими клетками , такими как дендритные клетки, B-клетки и макрофаги, и это лишь некоторые из них. Пептиды, презентируемые CD8 + Т-клеткам молекулами MHC класса I, имеют длину 8–13 аминокислот; пептиды, презентируемые CD4 + клеткам молекулами MHC класса II, длиннее, обычно составляют 12–25 аминокислот [47] , поскольку концы связывающей щели молекулы MHC класса II открыты.
Второй сигнал исходит от костимуляции, при которой поверхностные рецепторы АПК индуцируются относительно небольшим количеством стимулов, обычно продуктов патогенов, но иногда и продуктов распада клеток, таких как некротические тельца или белки теплового шока . Единственным костимулирующим рецептором, конститутивно экспрессируемым наивными Т-клетками, является CD28, поэтому костимуляция этих клеток происходит от белков CD80 и CD86 , которые вместе составляют белок B7 (B7.1 и B7.2 соответственно) на БТР. Другие рецепторы экспрессируются при активации Т-клетки, такие как OX40 и ICOS, но их экспрессия во многом зависит от CD28. Второй сигнал разрешает Т-клетке реагировать на антиген. Без него Т-клетка становится анергической , и ей становится труднее активироваться в будущем. Этот механизм предотвращает неадекватные реакции на себя, поскольку аутопептиды обычно не подвергаются подходящей совместной стимуляции. Как только Т-клетка была соответствующим образом активирована (т.е. получила сигнал один и сигнал два), она изменяет экспрессию на своей клеточной поверхности различных белков. Маркеры активации Т-клеток включают CD69, CD71 и CD25 (также маркер Treg-клеток) и HLA-DR (маркер активации Т-клеток человека). Экспрессия CTLA-4 также усиливается на активированных Т-клетках, которые, в свою очередь, конкурируют с CD28 за связывание с белками B7. Это механизм контрольной точки, предотвращающий чрезмерную активацию Т-клеток. Активированные Т-клетки также меняют профиль гликозилирования клеточной поверхности. [48]
Рецептор Т-клеток существует в виде комплекса нескольких белков. Фактический рецептор Т-клеток состоит из двух отдельных пептидных цепей, которые производятся независимыми генами альфа- и бета-рецепторов Т-клеток ( TCRα и TCRβ ). Другими белками в комплексе являются белки CD3 : гетеродимеры CD3εγ и CD3εδ и, что наиболее важно, гомодимер CD3ζ, который имеет в общей сложности шесть мотивов ITAM . Мотивы ITAM на CD3ζ могут фосфорилироваться с помощью Lck и, в свою очередь, рекрутировать ZAP-70 . Lck и/или ZAP-70 также могут фосфорилировать тирозины многих других молекул, не в последнюю очередь CD28, LAT и SLP-76 , что позволяет агрегировать сигнальные комплексы вокруг этих белков.
Фосфорилированный LAT рекрутирует SLP-76 на мембрану, где он затем может приносить PLC-γ , VAV1 , Itk и потенциально PI3K . PLC-γ расщепляет PI(4,5)P2 на внутреннем листке мембраны с образованием активных посредников диацилглицерина ( DAG ), инозитол-1,4,5-трифосфата ( IP3 ); PI3K также действует на PIP2, фосфорилируя его с образованием фосфатидлиинозитол-3,4,5-трифосфата (PIP3). DAG связывает и активирует некоторые PKC. Наиболее важной в Т-клетках является PKC-θ, имеющая решающее значение для активации факторов транскрипции NF-κB и AP-1. IP3 высвобождается из мембраны с помощью PLC-γ и быстро диффундирует, активируя рецепторы кальциевых каналов в ЭР , что индуцирует высвобождение кальция в цитозоль. Низкий уровень кальция в эндоплазматическом ретикулуме вызывает кластеризацию STIM1 на мембране ЭР и приводит к активации каналов CRAC клеточной мембраны, что позволяет дополнительному кальцию поступать в цитозоль из внеклеточного пространства. Этот агрегированный цитозольный кальций связывает кальмодулин, который затем может активировать кальциневрин . Кальцинеурин, в свою очередь, активирует NFAT , который затем транслоцируется в ядро. NFAT представляет собой фактор транскрипции , который активирует транскрипцию плейотропного набора генов, наиболее примечательным из которых является IL-2, цитокин, который способствует долгосрочной пролиферации активированных Т-клеток.
PLC-γ также может инициировать путь NF-κB . DAG активирует PKC-θ, которая затем фосфорилирует CARMA1, заставляя ее разворачиваться и функционировать как каркас. Цитозольные домены связывают адаптер BCL10 через домены CARD (домены активации и рекрутирования каспаз); который затем связывает TRAF6, который убиквитинирован по адресу K63. : 513–523 [49] Эта форма убиквитинирования не приводит к деградации белков-мишеней. Скорее, он служит для рекрутирования NEMO, IKKα и -β, а также TAB1-2/TAK1. [50] TAK 1 фосфорилирует IKK-β, который затем фосфорилирует IκB, обеспечивая убиквитинирование K48: приводит к протеасомной деградации. Затем Rel A и p50 могут проникнуть в ядро и связать ответный элемент NF-κB. Это в сочетании с передачей сигналов NFAT позволяет полностью активировать ген IL-2. [49]
Хотя в большинстве случаев активация зависит от распознавания антигена TCR, были описаны альтернативные пути активации. Например, было показано, что цитотоксические Т-клетки активируются при воздействии на них других Т-клеток CD8, что приводит к толеризации последних. [51]
Весной 2014 года на Международной космической станции в рамках миссии SpaceX CRS-3 был запущен эксперимент « Активация Т-клеток в космосе » (TCAS) для изучения того, как «на недостатки иммунной системы человека влияет среда микрогравитации». [52]
Активация Т-клеток модулируется активными формами кислорода . [53]
Уникальной особенностью Т-клеток является их способность различать здоровые и аномальные (например, инфицированные или раковые) клетки в организме. [54] Здоровые клетки обычно экспрессируют большое количество собственных pMHC на своей клеточной поверхности, и хотя рецептор антигена Т-клеток может взаимодействовать, по крайней мере, с подмножеством этих собственных pMHC, Т-клетки обычно игнорируют эти здоровые клетки. Однако, когда эти самые клетки содержат даже незначительное количество pMHC, полученного из патогена, Т-клетки способны активироваться и инициировать иммунные ответы. Способность Т-клеток игнорировать здоровые клетки, но реагировать, когда эти же самые клетки содержат pMHC, полученный из патогена (или рака), известна как дискриминация антигена. Молекулярные механизмы, лежащие в основе этого процесса, являются спорными. [54] [55]
Причины дефицита Т-клеток включают лимфоцитопению Т-клеток и/или дефекты функции отдельных Т-клеток. Полная недостаточность функции Т-клеток может быть результатом наследственных заболеваний , таких как тяжелый комбинированный иммунодефицит (ТКИД), синдром Оменна и гипоплазия хрящевых волос . [56] Причины частичной недостаточности функции Т-клеток включают синдром приобретенного иммунодефицита (СПИД) и наследственные состояния, такие как синдром ДиДжорджа (DGS), синдромы хромосомных поломок (CBS), а также комбинированные заболевания В-клеток и Т-клеток, такие как атаксия- телеангиэктазия (АТ) и синдром Вискотта-Олдрича (СВА). [56]
Основными патогенами, вызывающими озабоченность при дефиците Т-клеток, являются внутриклеточные патогены , включая вирус простого герпеса , микобактерии и листерии . [57] Кроме того, грибковые инфекции также более распространены и тяжелы при дефиците Т-клеток. [57]
Рак Т-клеток называется Т-клеточной лимфомой и составляет примерно один из десяти случаев неходжкинской лимфомы . [58] Основными формами Т-клеточной лимфомы являются:
Истощение Т-клеток — плохо определенный или неоднозначный термин. [59] [60] Существует три подхода к его определению. [59] «Первый подход в первую очередь определяет как истощенные клетки, которые демонстрируют одну и ту же клеточную дисфункцию (как правило, отсутствие ожидаемого эффекторного ответа). Второй подход в первую очередь определяет как истощенные клетки, которые производятся по определенной причине (обычно, но не обязательно хроническое воздействие антигена. Наконец, третий подход в первую очередь определяет как истощенные клетки, которые имеют одни и те же молекулярные маркеры (обычно белок запрограммированной гибели клеток 1 [PD-1])». [59]
Дисфункциональные Т-клетки характеризуются прогрессирующей потерей функции, изменениями профилей транскрипции и устойчивой экспрессией ингибирующих рецепторов. Сначала клетки теряют способность продуцировать IL-2 и TNFα , что сопровождается потерей высокой пролиферативной способности и цитотоксического потенциала и в конечном итоге приводит к их делеции. Истощение Т-клеток обычно указывает на более высокие уровни CD43 , CD69 и ингибирующих рецепторов в сочетании с более низкой экспрессией CD62L и CD127 . Истощение может развиться при хронических инфекциях, сепсисе и раке. [61] Истощенные Т-клетки сохраняют свое функциональное истощение даже после повторного воздействия антигена. [62]
Истощение Т-клеток может быть вызвано несколькими факторами, такими как постоянное воздействие антигена и отсутствие помощи Т-клеток CD4. [63] Воздействие антигена также влияет на течение истощения, поскольку более длительное время воздействия и более высокая вирусная нагрузка увеличивают тяжесть истощения Т-клеток. Для установления истощения требуется не менее 2–4 недель воздействия. [64] Еще одним фактором, способным вызвать истощение, являются ингибирующие рецепторы, в том числе белок 1 запрограммированной гибели клеток (PD1), CTLA-4 , белок 3 Т-клеточной мембраны (TIM3) и белок гена активации лимфоцитов 3 (LAG3). [65] [66] Растворимые молекулы, такие как цитокины IL-10 или TGF-β, также способны вызывать истощение. [67] [68] Последними известными факторами, которые могут играть роль в истощении Т-клеток, являются регуляторные клетки. Treg- клетки могут быть источником IL-10 и TGF-β и, следовательно, могут играть роль в истощении Т-клеток. [69] Кроме того, истощение Т-клеток возвращается после истощения Treg-клеток и блокады PD1. [70] Истощение Т-клеток также может возникнуть во время сепсиса в результате цитокинового шторма. Позже, после первоначального заражения, противовоспалительные цитокины и проапоптотические белки начинают защищать организм от повреждений. Сепсис также несет в себе высокую антигенную нагрузку и воспаление. На этой стадии сепсиса истощение Т-клеток увеличивается. [71] [72] В настоящее время проводятся исследования, направленные на использование блокады ингибирующих рецепторов при лечении сепсиса. [73] [74] [75]
В то время как во время инфекции истощение Т-клеток может развиться после постоянного воздействия антигена после трансплантации трансплантата, аналогичная ситуация возникает и с присутствием аллоантигена. [76] Было показано, что реакция Т-клеток снижается со временем после трансплантации почки. [77] Эти данные свидетельствуют о том, что истощение Т-клеток играет важную роль в толерантности трансплантата, главным образом, за счет истощения аллореактивных CD8 Т-клеток. [72] [78] Несколько исследований показали положительное влияние хронической инфекции на приживление трансплантата и его долгосрочную выживаемость, частично опосредованное истощением Т-клеток. [79] [80] [81] Также было показано, что истощение Т-клеток реципиента обеспечивает достаточные условия для переноса NK-клеток . [82] Хотя есть данные, показывающие, что индукция истощения Т-клеток может быть полезна для трансплантации, она также несет в себе недостатки, среди которых можно назвать увеличение количества инфекций и риск развития опухоли. [83]
Во время рака истощение Т-клеток играет роль в защите опухоли. Согласно исследованиям, некоторые рак-ассоциированные клетки, а также сами опухолевые клетки могут активно вызывать истощение Т-клеток в месте опухоли. [84] [85] [86] Истощение Т-клеток также может играть роль в рецидивах рака, как это было показано на примере лейкемии. [87] Некоторые исследования показали, что можно предсказать рецидив лейкемии на основе экспрессии ингибирующих рецепторов PD-1 и TIM-3 Т-клетками. [88] Многие эксперименты и клинические испытания были сосредоточены на блокаторах иммунных контрольных точек в терапии рака, причем некоторые из них были одобрены как действующие методы лечения и в настоящее время используются в клинической практике. [89] Ингибирующие рецепторы, на которые нацелены эти медицинские процедуры, жизненно важны при истощении Т-клеток, и их блокирование может обратить вспять эти изменения. [90]
Т-клетки... получили свое [название] от органов, в которых они развиваются. Т-клетки развиваются [созревают] в тимусе