Фасциолез — паразитарная червячная инфекция, вызываемая обыкновенным печеночным сосальщиком Fasciola hepatica , а также Fasciola gigantica . Заболевание является растительным трематодным зоонозом [3] и классифицируется как забытая тропическая болезнь (NTD). [4] [5] Оно поражает людей, но его основными хозяевами являются жвачные животные , такие как крупный рогатый скот и овцы [4] Заболевание протекает в четыре отдельные фазы: начальная инкубационная фаза от нескольких дней до трех месяцев с небольшими или отсутствующими симптомами; инвазивная или острая фаза, которая может проявляться: лихорадкой, недомоганием, болью в животе, желудочно-кишечными симптомами, крапивницей, анемией , желтухой и респираторными симптомами [6] Позднее заболевание переходит в латентную фазу с меньшим количеством симптомов и в конечном итоге в хроническую или обструктивную фазу спустя месяцы или годы. [7] [8] В хроническом состоянии заболевание вызывает воспаление желчных протоков , желчного пузыря и может вызвать образование желчных камней, а также фиброз . [4] Хотя хроническое воспаление связано с повышением заболеваемости раком, неясно, связан ли фасциолез с повышенным риском рака. [9]
До половины инфицированных не проявляют никаких симптомов, [4] и диагностика затруднена, поскольку яйца глистов часто не обнаруживаются при исследовании кала. [4] Методы обнаружения включают исследование кала, обнаружение специфических антител к паразитам или радиологическую диагностику, а также лапаротомию . В случае подозрения на вспышку может быть полезно отслеживать историю питания, что также полезно для исключения дифференциальных диагнозов. [4] Исследование кала, как правило, бесполезно, поскольку яйца глистов редко можно обнаружить в хронической фазе инфекции. Яйца появляются в кале впервые между 9–11 неделями после заражения. Причина этого неизвестна, и также трудно различить различные виды фасциол, а также отличить их от эхиностом и фасциолопсисов . [4] Большинство иммунодиагностических тестов обнаруживают инфекцию с очень высокой чувствительностью, и поскольку концентрация падает после лечения, это очень хороший диагностический метод. [4] Клинически невозможно дифференцировать от других заболеваний печени и желчи . Радиологические методы позволяют обнаружить поражения как при острой, так и при хронической инфекции, в то время как лапаротомия позволяет обнаружить поражения, а также иногда яйца и живых глистов. [4]
Из-за размера паразита, как взрослая F. hepatica : 20–30 × 13 мм (0,79–1,18 × 0,51 дюйма) или взрослая F. gigantica: 25–75 × 12 мм (0,98–2,95 × 0,47 дюйма), фасциолез является большой проблемой. [4] Количество симптомов зависит от того, сколько червей и на какой стадии находится инфекция. Уровень смертности является значительным как среди крупного рогатого скота (67,55%), так и среди коз (24,61%), [10] но в целом низок среди людей. [ необходима цитата ] Лечение триклабендазолом было высокоэффективным против взрослых червей, а также различных развивающихся стадий. [4] [6] Празиквантел не эффективен, а старые препараты, такие как битионол, умеренно эффективны, но также вызывают больше побочных эффектов. Вторичная бактериальная инфекция, вызывающая холангит, также вызывает беспокойство и может быть вылечена антибиотиками, а токсемия может быть вылечена преднизолоном . [4]
Люди заражаются, употребляя в пищу растения, выращенные в воде, в первую очередь дикий кресс-салат в Европе или ипомею в Азии. Заражение также может произойти при питье загрязненной воды с плавающей молодой фасциолой или при использовании посуды, вымытой загрязненной водой. [4] Культурные растения не распространяют болезнь в той же степени. Заражение человека встречается редко, даже если уровень заражения высок среди животных. Особенно высокие показатели заражения человека были обнаружены в Боливии, Перу и Египте, и это может быть связано с употреблением определенных продуктов питания. [4] Вакцины для защиты людей от заражения фасциолой не существует . [11] Профилактические меры в первую очередь заключаются в лечении и иммунизации скота, который должен быть хозяином жизненного цикла червей. Ветеринарные вакцины находятся в стадии разработки, и их использование рассматривается рядом стран из-за риска для здоровья человека и экономических потерь в результате заражения скота. [4] Другие методы включают использование моллюскицидов для уменьшения количества улиток, которые действуют как переносчики, но это нецелесообразно. [4] Было показано, что образовательные методы, направленные на сокращение потребления дикого кресс-салата и других водных растений, эффективны в районах с высоким уровнем заболеваемости. [4]
Фасциолез встречается в Европе, Африке, Америке, а также в Океании. [4] Недавно мировые потери производительности животных из-за фасциолеза были консервативно оценены в более чем 3,2 млрд долларов США в год. [12] Фасциолез в настоящее время признан новым заболеванием человека: Всемирная организация здравоохранения (ВОЗ) подсчитала, что 2,4 миллиона человек инфицированы фасциолой , а еще 180 миллионов находятся в группе риска. [13]

Течение фасциолеза у человека имеет 4 основные фазы: [7]
Эта фаза может развиться через месяцы или годы после первичного заражения. Взрослые сосальщики в желчных протоках вызывают воспаление и гиперплазию эпителия. Возникающий холангит и холецистит в сочетании с большим телом сосальщика достаточны для того, чтобы вызвать механическую обструкцию желчных протоков. В этой фазе желчная колика , боль в эпигастрии , непереносимость жирной пищи, тошнота, желтуха, зуд , болезненность в правом верхнем квадранте живота и т. д. являются клиническими проявлениями, неотличимыми от холангита , холецистита и желчнокаменной болезни другого происхождения. Увеличение печени может быть связано с увеличением селезенки или асцитом. В случае обструкции желчный пузырь обычно увеличен и отёчен с утолщением стенки (Ref: Hepatobiliary Fascioliasis: Sonographic and CT Findings in 87 Patients During the InitialPhase and Long-Term Follow-Up. Adnan Kabaalioglu, Kagan Ceken, Emel Alimoglu, Rabin Saba, Metin Cubuk, Gokhan Arslan, Ali Apaydin. AJR 2007; 189:824–828). Фиброзные спайки желчного пузыря с соседними органами встречаются часто. Часто встречается литиаз желчного протока или желчного пузыря, а камни обычно мелкие и множественные. [7]
Ветеринарные клинические [15] признаки фасциолеза всегда тесно связаны с инфицирующей дозой (количеством проглоченных метацеркарий). У овец, как наиболее распространенного окончательного хозяина, клиническая картина делится на 4 типа: [16] [17]
В крови при всех типах фасциолеза могут наблюдаться анемия , гипоальбуминемия и эозинофилия . [17] Повышение активности ферментов печени , таких как глутаматдегидрогеназа (ГЛДГ), гамма-глутамилтрансфераза (ГГТ) и лактатдегидрогеназа (ЛДГ), обнаруживается при подостром или хроническом фасциолезе через 12–15 недель после попадания метацеркарий в организм. [18] [19] Экономический эффект фасциолеза у овец заключается во внезапной гибели животных, а также в снижении набора веса и производства шерсти. [20] [21] У коз и крупного рогатого скота клинические проявления аналогичны таковым у овец. Однако приобретенная устойчивость к инфекции F. hepatica хорошо известна у взрослого крупного рогатого скота. [22] [23] Телята восприимчивы к заболеванию, но обычно требуется более 1000 метацеркарий, чтобы вызвать клинический фасциолез. В этом случае заболевание похоже на овечье и характеризуется потерей веса, анемией, гипоальбуминемией и (после заражения 10 000 метацеркариями) смертью. [24] Значение фасциолеза крупного рогатого скота заключается в экономических потерях, вызванных браковкой печени при убое, и производственных потерях, особенно из-за снижения привеса. [25]
У овец, а иногда и у крупного рогатого скота, поврежденная ткань печени может быть инфицирована бактериями Clostridium C. novyi типа B. Бактерии выделяют токсины в кровоток, что приводит к так называемой черной болезни . Лечения не существует, и смерть наступает быстро. Поскольку C. novyi распространена в окружающей среде, черная болезнь встречается везде, где популяции печеночных сосальщиков и овец пересекаются. [26]

Фасциолез вызывают две дигенетические трематоды F. hepatica и F. gigantica . Взрослые сосальщики обоих видов локализуются в желчных протоках печени или желчного пузыря . F. hepatica имеет размеры от 2 до 3 см и имеет космополитное распространение . F. gigantica имеет размеры от 4 до 10 см в длину, а распространение вида ограничено тропиками и было зарегистрировано в Африке, на Ближнем Востоке, в Восточной Европе, а также в Южной и Восточной Азии. [28] У домашнего скота в Японии были описаны диплоидные (2n = 20), триплоидные (3n = 30) и химерные сосальщики (2n/3n), многие из которых размножаются партеногенетически . В результате этой неясной классификации сосальщики в Японии обычно называются Fasciola spp. [29] Недавние отчеты, основанные на анализе митохондриальных генов, показали, что японские Fasciola spp. более тесно связан с F. gigantica, чем с F. hepatica . [30] В Индии вид под названием F. jacksoni был описан у слонов . [31]
Инфицирование человека F. hepatica определяется наличием промежуточных хозяев-улиток, домашних травоядных животных, климатическими условиями и пищевыми привычками человека. [32] Овцы, козы и крупный рогатый скот считаются основными животными- резервуарами . Хотя другие животные могут быть инфицированы, они обычно не очень важны для передачи заболевания человеку. С другой стороны, некоторые авторы наблюдали, что ослы и свиньи способствуют передаче заболевания в Боливии. [33] Среди диких животных было показано, что перидоместиальная крыса ( Rattus rattus ) может играть важную роль в распространении, а также в передаче паразита на Корсике . [34] Во Франции нутрия ( Myocastor coypus ) была подтверждена как дикий резервуарный хозяин F. hepatica . [35] Люди заражаются при употреблении в пищу водных растений, содержащих инфекционные церкарии . [36] Известно, что несколько видов водных овощей являются переносчиками заражения человека. В Европе сообщалось, что Nasturtium officinale (обыкновенный кресс-салат), Nasturtium sylvestre , Rorippa amphibia (дикий кресс-салат), Taraxacum dens leonis ( листья одуванчика ), Valerianella olitoria (салат ягнёнка) и Mentha viridis ( мята колосистая ) являются источниками заражения человека. [7] В северном боливийском Альтиплано некоторые авторы предположили, что несколько водных растений, таких как bero-bero (кресс-салат), algas ( водоросли ), kjosco и tortora, могут служить источником заражения человека. [37] Поскольку церкарии F. hepatica также инкапсулируются на поверхности воды, люди могут быть инфицированы, выпивая свежую неочищенную воду, содержащую церкарии. [32] Кроме того, экспериментальное исследование показало, что люди, употребляющие сырые блюда из свежей печени, инфицированной молодыми трематодами, могут быть инфицированы. [38]

Промежуточными хозяевами F. hepatica являются пресноводные улитки из семейства Lymnaeidae . [28] [39] Улитки из семейства Planorbidae выступают в качестве промежуточных хозяев F. hepatica очень редко. [3]
Развитие инфекции у окончательного хозяина делится на две фазы: паренхиматозную (миграционную) и билиарную. [16] Паренхиматозная фаза начинается, когда эксцистированные молодые сосальщики проникают в стенку кишечника. После проникновения в кишечник сосальщики мигрируют в брюшную полость и проникают в печень или другие органы. F. hepatica имеет сильную предрасположенность к тканям печени. [17] Иногда могут встречаться эктопические расположения сосальщиков, такие как легкие, диафрагма , стенка кишечника, почки и подкожная клетчатка. [24] [32] Во время миграции сосальщиков ткани механически разрушаются, и вокруг миграционных путей сосальщиков возникает воспаление . Вторая фаза (билиарная фаза) начинается, когда паразиты попадают в желчные протоки печени. В желчных протоках сосальщики созревают, питаются кровью и производят яйца. Гипертрофия желчных протоков, связанная с обструкцией просвета, возникает в результате повреждения тканей. [ необходима цитата ]
Механизмы резистентности изучались несколькими авторами на разных видах животных. Эти исследования могут помочь лучше понять иммунный ответ на F. hepatica у хозяина и необходимы для разработки вакцины против паразита. Установлено, что крупный рогатый скот приобретает резистентность к контрольному заражению F. hepatica и F. gigantica , когда он был сенсибилизирован первичной патентованной или сокращенной лекарственной инфекцией. [22] Устойчивость к фасциолезу была также зарегистрирована у крыс. [40] С другой стороны, овцы и козы не устойчивы к повторному заражению F. hepatica . [41] [42] Однако есть данные, что две породы овец, в частности индонезийская тонкохвостая овца и красная масайская овца, устойчивы к F. gigantica . [43] [44]
Большинство иммунодиагностических тестов выявляют инфекцию и имеют чувствительность выше 90% на всех стадиях заболевания. Кроме того, концентрация антител быстро падает после лечения, и антитела не обнаруживаются в течение года после лечения, что делает его очень хорошим диагностическим методом. [4] У людей диагностика фасциолеза обычно осуществляется паразитологически путем обнаружения яиц трематоды в кале, а также иммунологически с помощью ИФА и вестерн-блоттинга . Копрологические исследования кала сами по себе, как правило, недостаточны, поскольку у инфицированных людей важные клинические проявления проявляются задолго до того, как яйца обнаруживаются в кале. [ необходима цитата ]
Более того, при многих человеческих инфекциях яйца трематоды часто не обнаруживаются в фекалиях, даже после многократных исследований фекалий. [32] [45] Кроме того, яйца F. hepatica , F. gigantica и Fasciolopsis buski морфологически неотличимы. [45] Поэтому иммунологические методы, такие как ИФА и иммуноферментный электротрансферный блоттинг, также называемый вестерн-блоттингом, являются наиболее важными методами диагностики инфекции F. hepatica . Эти иммунологические тесты основаны на обнаружении видоспецифических антител из сыворотки . Используемые антигенные препараты в основном были получены из экстрактов экскреторных/секреторных продуктов взрослых червей или с частично очищенными фракциями. [46] В последнее время использовались очищенные нативные и рекомбинантные антигены, например, рекомбинантная катепсин L -подобная протеаза F. hepatica . [47]
Методы, основанные на обнаружении антигена (циркулирующего в сыворотке или в фекалиях), встречаются реже. Кроме того, биохимические и гематологические исследования сыворотки человека подтверждают точный диагноз (эозинофилия, повышение уровня печеночных ферментов). Также можно использовать ультразвуковое исследование и рентген брюшной полости, биопсию печени и пунктат желчного пузыря (ссылка: аспирация желчного пузыря под контролем УЗИ: новый диагностический метод билиарного фасциолеза. A. Kabaalioglu, A. Apaydin, T. Sindel, E. Lüleci. Eur. Radiol. 9, 880±882 (1999). Ложный фасциолез (псевдофасциолез) относится к наличию яиц в стуле, что является результатом не фактической инфекции, а недавнего употребления инфицированной печени, содержащей яйца. Эту ситуацию (с ее потенциалом для ошибочной диагностики) можно избежать, если пациент будет соблюдать диету без печени за несколько дней до повторного исследования стула. [46]
У животных прижизненная диагностика основана преимущественно на исследовании фекалий и иммунологических методах. Однако необходимо учитывать клинические признаки, биохимический и гематологический профиль, сезон, климатические условия, эпидемиологическую ситуацию и исследования улиток. [16] [28] Как и у людей, исследования фекалий не являются надежными. Более того, яйца трематоды обнаруживаются в фекалиях через 8–12 недель после заражения. Несмотря на это, исследование фекалий по-прежнему остается единственным используемым диагностическим инструментом в некоторых странах. В то время как копрологическая диагностика фасциолеза возможна с 8 по 12 неделю после заражения (WPI), специфические антитела к F. hepatica распознаются с помощью ИФА или вестерн-блоттинга через 2–4 недели после заражения. [48] [49] Таким образом, эти методы обеспечивают раннее обнаружение инфекции. [ необходима цитата ]
В некоторых районах действуют или планируются специальные программы контроля. [11] Типы мер контроля зависят от условий (таких как эпидемиологические, экологические и культурные факторы). [11] Строгий контроль за ростом и продажей кресс-салата и других съедобных водных растений важен. Отдельные люди могут защитить себя, не употребляя в пищу сырой кресс-салат и другие водные растения, особенно из эндемичных пастбищ. [11] Путешественникам в районы с плохой санитарией следует избегать пищи и воды, которые могут быть загрязнены (испорчены). [11] Овощи, выращенные на полях, которые могли быть орошены загрязненной водой, следует тщательно готовить, как и внутренности потенциально инфицированных животных. [11]
Несколько препаратов эффективны при фасциолезе, как у людей, так и у домашних животных. Препаратом выбора при лечении фасциолеза является триклабендазол , представитель семейства бензимидазольных антигельминтиков . [ 50] Препарат работает, предотвращая полимеризацию молекулы тубулина в цитоскелетные структуры , микротрубочки . Устойчивость F. hepatica к триклабендазолу была зарегистрирована в Австралии в 1995 году [51] и Ирландии в 1998 году. [52]
Лечение празиквантелом неэффективно. [53] [54] Имеются сообщения о случаях успешного применения нитазоксанида при лечении фасциолеза человека в Мексике. [55] Имеются также сообщения об успешном применении битионола . [56]
Нитазоксанид был признан эффективным в ходе испытаний, но в настоящее время не рекомендуется к применению. [4]
Только клорсулон и альбендазол одобрены для использования при лечении домашних животных в Соединенных Штатах, но доступные фаскициды, используемые во всем мире, также включают триклабендазол , нетобимин, клозантел, рафоксанид , нитроксинил и оксиклозанид ; однако этот список доступных препаратов имеет некоторые недостатки. [57] Клозантел, нитроксинил и оксиклозанид неэффективны против молодых печеночных сосальщиков и должны использоваться только для лечения подострых и хронических инфекций. Триклабендазол эффективен для уничтожения сосальщиков любого возраста, но чрезмерное использование привело к повышению устойчивости к этому препарату, поэтому его следует использовать только для лечения ранних инфекций, а более поздние стадии лечить другими фаскиолицидами. [58] Время лечения имеет решающее значение для успеха и определяется факторами окружающей среды и анализом ожидаемого распространения и распространенности заболевания. Например, в европейских странах, где имеется большое количество овец, компьютерные системы предсказывают, когда фасциолез, скорее всего, окажет наибольшее влияние на популяцию овец и сколько овец, скорее всего, будет поражено. Прогнозы зависят от угадывания того, когда возникнут условия окружающей среды, наиболее благоприятствующие размножению паразитов, такие как количество осадков, эвапотранспирация и соотношение влажных и сухих дней в определенном месяце. Если ожидается возникновение тяжелых инфекций, лечение овец следует начинать в сентябре/октябре, затем снова в январе/феврале и, наконец, в апреле/мае; количество вылупляющихся яиц трематод минимально в это время, поскольку им требуется теплая, влажная среда, что делает лечение более эффективным. [57]
Фасциолез человека и животных встречается во всем мире. [28] В то время как фасциолез животных распространен в странах с высоким содержанием крупного рогатого скота и овец, фасциолез человека встречается, за исключением Западной Европы, в развивающихся странах. Фасциолез встречается только в районах, где существуют подходящие условия для промежуточных хозяев. [ необходима цитата ]
Исследования, проведенные в последние годы, показали, что фасциолез человека является важной проблемой общественного здравоохранения . [32] Фасциолез человека был зарегистрирован в странах Европы, Америки, Азии, Африки и Океании. Частота случаев заболевания людей растет в 51 стране на пяти континентах. [7] [8] Глобальный анализ показывает, что ожидаемая корреляция между фасциолезом животных и человека проявляется только на базовом уровне. Высокая распространенность среди людей не обязательно обнаруживается в районах, где фасциолез является большой ветеринарной проблемой. Например, в Южной Америке гиперэндемики и мезоэндемики встречаются в Боливии и Перу, где ветеринарная проблема менее важна, в то время как в таких странах, как Уругвай, Аргентина и Чили, фасциолез человека носит только спорадический или гипоэндемический характер . [8]
В Европе фасциолез человека встречается в основном во Франции, Испании, Португалии и бывшем СССР. [8] Франция считается важной эндемичной для человека зоной. Всего в девяти французских больницах с 1970 по 1982 год было зарегистрировано 5863 случая фасциолеза человека. [59] Что касается бывшего Советского Союза, то почти все зарегистрированные случаи были из Республики Таджикистан . [8] Несколько статей касались фасциолеза человека в Турции. [60] Недавно в некоторых частях Турции было проведено серологическое исследование фасциолеза человека. Распространенность заболевания была серологически установлена на уровне 3,01% в провинции Анталья и от 0,9 до 6,1% в провинции Испарта , средиземноморском регионе Турции. [61] В других европейских странах фасциолез носит спорадический характер, и возникновение заболевания обычно сочетается с поездками в эндемичные районы. [ необходима ссылка ]
В Северной Америке заболевание встречается очень спорадически. В Мексике было зарегистрировано 53 случая. В Центральной Америке фасциолез является проблемой для здоровья человека на островах Карибского бассейна, особенно в зонах Пуэрто-Рико и Кубы. Провинция Пинар-дель-Рио и провинция Вилья-Клара являются регионами Кубы, где фасциолез был гиперэндемичным. В Южной Америке фасциолез человека является серьезной проблемой в Боливии, Перу и Эквадоре. Эти страны Анд считаются районом с самой высокой распространенностью фасциолеза человека в мире. Известные гиперэндемичные районы человека локализованы преимущественно на высокой равнине, называемой Альтиплано . В Северном Боливийском Альтиплано распространенность, обнаруженная в некоторых общинах, достигала 72% и 100% в копрологических и серологических исследованиях соответственно. [7] В Перу F. hepatica у людей встречается по всей стране. Самая высокая распространенность была зарегистрирована в Арекипе , долине Мантаро , долине Кахамарка и регионе Пуно . [3] В других странах Южной Америки, таких как Аргентина, Уругвай, Бразилия, Венесуэла и Колумбия, фасциолез у человека, по-видимому, носит спорадический характер, несмотря на высокую распространенность фасциолеза у крупного рогатого скота. [ необходима ссылка ]
В Африке случаи фасциолеза у людей, за исключением северных районов, не часто регистрировались. Самая высокая распространенность была зафиксирована в Египте, где болезнь распространена в общинах, проживающих в дельте Нила . [3]
В Азии большинство случаев заболевания людей было зарегистрировано в Иране, особенно в провинции Гилян на Каспийском море . Было упомянуто, что в Иране было выявлено более 10 000 случаев заболевания людей. В Восточной Азии фасциолез человека, по-видимому, носит спорадический характер. Несколько случаев были зарегистрированы в Японии, Корее, Вьетнаме и Таиланде. [7]
В Австралии человеческий фасциолез встречается очень редко (задокументировано всего 12 случаев). В Новой Зеландии F. hepatica никогда не обнаруживался у людей. [7]
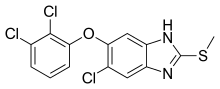
Для борьбы с фасциолезом у животных использовался ряд препаратов. Препараты различаются по своей эффективности, способу действия, цене и жизнеспособности. Фасциоциды (препараты против Fasciola spp.) делятся на пять основных химических групп: [62]
Триклабендазол (Фазинекс) считается наиболее распространенным препаратом из-за его высокой эффективности против взрослых, а также молодых особей сосальщиков. Триклабендазол используется для борьбы с фасциолезом скота во многих странах. Тем не менее, длительное ветеринарное применение триклабендазола вызвало появление резистентности у F. hepatica . У животных резистентность к триклабендазолу была впервые описана в Австралии [63] , позже в Ирландии [64] и Шотландии [65] и совсем недавно в Нидерландах. [66] Учитывая этот факт, ученые начали работать над разработкой нового препарата. Недавно новый фасциолицид был успешно испытан на естественно и экспериментально инфицированном скоте в Мексике. Этот новый препарат называется «Соединение Альфа» и по химическому составу очень похож на триклабендазол. [67] Страны, где неоднократно сообщалось о фасциолезе скота: [ необходима цитата ]
8 сентября 2007 года ветеринарные чиновники в Южном Котабато , Филиппины, заявили, что лабораторные тесты образцов от коров, буйволов и лошадей в 10 городах провинции и единственном городе показали уровень заражения в 89,5%, что является внезапным ростом положительных случаев среди крупного рогатого скота из-за неустойчивых погодных условий в этом районе. Их необходимо лечить немедленно, чтобы предотвратить осложнения с суррой и геморрагической септицемией . Сурра уже поразила все барангаи города Суралла . [68]