В неорганической химии бикарбонат ( рекомендованная ИЮПАК номенклатура: гидрокарбонат [2] ) является промежуточной формой при депротонировании угольной кислоты . Это многоатомный анион с химической формулой H C O.−
3.
Бикарбонат играет решающую биохимическую роль в физиологической буферной системе pH . [3]
Термин «бикарбонат» был придуман в 1814 году английским химиком Уильямом Хайдом Волластоном . [4] [5] Имя продолжает жить как тривиальное имя .
Бикарбонат-ион (гидрокарбонат-ион) представляет собой анион с эмпирической формулой HCO.−
3и молекулярная масса 61,01 дальтон ; он состоит из одного центрального атома углерода , окруженного тремя атомами кислорода в тригональном плоском расположении, с атомом водорода, присоединенным к одному из атомов кислорода. Изоэлектронен азотной кислоте HNO .
3. Ион бикарбоната несет отрицательный формальный заряд и представляет собой амфипротонную разновидность, обладающую как кислотными, так и основными свойствами. Это одновременно сопряженное основание угольной кислоты H.
2СО
3; и сопряженная кислота CO2−
3, карбонат- ион, как показывают эти равновесные реакции:
Бикарбонатная соль образуется, когда положительно заряженный ион присоединяется к отрицательно заряженным атомам кислорода иона, образуя ионное соединение . Многие бикарбонаты растворимы в воде при стандартной температуре и давлении ; в частности, бикарбонат натрия участвует в общем количестве растворенных твердых веществ , что является общим параметром для оценки качества воды . [6]
Бикарбонат ( HCO−
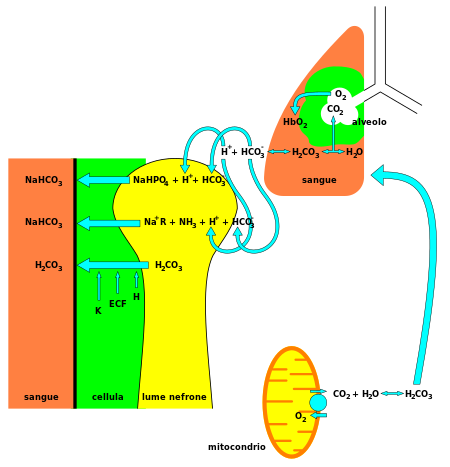
3) является жизненно важным компонентом рН- буферной системы [3] организма человека (поддержания кислотно-основного гомеостаза ). 70–75% CO 2 в организме превращается в угольную кислоту (H 2 CO 3 ), которая является сопряженной кислотой HCO .−
3и может быстро превратиться в него. [ нужна цитата ]
Угольная кислота является центральным промежуточным продуктом , а бикарбонат – в сочетании с водой, ионами водорода и диоксидом углерода – образует эту буферную систему, которая поддерживается в летучем равновесии [3] , необходимом для обеспечения быстрой устойчивости к изменениям pH как в кислой, так и в кислотной среде. и основные направления. Это особенно важно для защиты тканей центральной нервной системы , где изменения pH, слишком сильно выходящие за пределы нормального диапазона в любом направлении, могут оказаться катастрофическими (см. ацидоз или алкалоз ). Недавно также было продемонстрировано, что клеточный метаболизм бикарбоната может регулироваться с помощью передачи сигналов mTORC1. [7]
Кроме того, бикарбонат играет ключевую роль в пищеварительной системе. Он повышает внутренний pH желудка после того, как очень кислые пищеварительные соки закончили переваривание пищи. Бикарбонат также регулирует pH в тонком кишечнике. Он высвобождается из поджелудочной железы в ответ на гормон секретин для нейтрализации кислого химуса , поступающего в двенадцатиперстную кишку из желудка. [8]
Бикарбонат является доминирующей формой растворенного неорганического углерода в морской воде [9] и в большинстве пресных вод. По существу, это важный поглотитель в углеродном цикле .
Некоторые растения, такие как Чара , используют карбонат и производят карбонат кальция (CaCO 3 ) в результате биологического метаболизма. [10]
В экологии пресной воды сильная фотосинтетическая активность пресноводных растений при дневном свете высвобождает газообразный кислород в воду и в то же время производит ионы бикарбоната. Они повышают pH до тех пор, пока при определенных обстоятельствах степень щелочности не станет токсичной для некоторых организмов или не сделает токсичными другие химические компоненты, такие как аммиак . В темноте, когда фотосинтез не происходит, в процессе дыхания выделяется углекислый газ, и новые ионы бикарбоната не образуются, что приводит к быстрому падению pH.
Поток ионов бикарбоната из горных пород, выветриваемых углекислотой дождевой воды, является важной частью углеродного цикла .
Наиболее распространенной солью бикарбонат-иона является бикарбонат натрия NaHCO 3 , который широко известен как пищевая сода . При нагревании или воздействии кислоты , такой как уксусная кислота ( уксус ), бикарбонат натрия выделяет углекислый газ . Его используют в качестве разрыхлителя при выпечке .
Бикарбонат аммония используется при производстве пищеварительного печенья .
В диагностической медицине содержание бикарбоната в крови является одним из нескольких показателей состояния кислотно-щелочной физиологии организма. Его измеряют вместе с хлоридом , калием и натрием для оценки уровня электролита в панельном тесте электролита (который имеет действующую процедурную терминологию , CPT, код 80051).
Параметр стандартной концентрации бикарбоната (SBC e ) представляет собой концентрацию бикарбоната в крови при P a CO 2 40 мм рт. ст. (5,33 кПа), полном насыщении кислородом и 36 °C. [11]

Наиболее распространенным показателем качества воды является концентрация общего содержания растворенных веществ (TDS).