Благородные газы (исторически инертные газы , иногда называемые аэрогенами [1] ) являются членами 18-й группы периодической таблицы : гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe), радон (Rn) и, в некоторых случаях, оганесон (Og). При стандартных условиях первые шесть из этих элементов представляют собой одноатомные газы без запаха и цвета с очень низкой химической активностью и криогенными точками кипения. Свойства седьмого, нестабильного, элемента, Og, неопределенны.
Инертность благородных газов , или тенденция не реагировать с другими химическими веществами , является результатом их электронной конфигурации : их внешняя оболочка валентных электронов «заполнена», что дает им небольшую тенденцию участвовать в химических реакциях . Известно, что существует всего несколько сотен соединений благородных газов . По той же причине [ необходимо разъяснение ] атомы благородных газов малы, и единственная межмолекулярная сила между ними — очень слабая сила дисперсии Лондона , поэтому их точки кипения все криогенные, ниже 165 К (−108 °C; −163 °F). [2]
Инертность благородных газов делает их полезными, когда химические реакции нежелательны. Например, аргон используется в качестве защитного газа при сварке и в качестве наполнителя в лампах накаливания . Гелий используется для обеспечения плавучести дирижаблей и воздушных шаров . Гелий и неон также используются в качестве хладагентов из-за их низких температур кипения . Промышленные количества благородных газов, за исключением радона, получают путем их отделения от воздуха с использованием методов сжижения газов и фракционной перегонки . Гелий также является побочным продуктом добычи природного газа . Радон обычно выделяют из радиоактивного распада растворенных соединений радия , тория или урана .
Седьмым членом группы 18 является оганесон, нестабильный синтетический элемент , химия которого до сих пор не определена, поскольку только пять очень короткоживущих атомов (t 1/2 = 0,69 мс) когда-либо были синтезированы (по состоянию на 2020 год [3] ). ИЮПАК использует термин «благородный газ» взаимозаменяемо с «группой 18» и, таким образом, включает оганесон; [4] однако, из-за релятивистских эффектов , оганесон, как прогнозируется, будет твердым веществом при стандартных условиях и достаточно реакционноспособным, чтобы функционально не квалифицироваться как «благородный». [3] В остальной части этой статьи термин «благородный газ» следует понимать как не включающий оганесон, если это специально не упомянуто.[обновлять]
Благородный газ — перевод немецкого существительного Edelgas , впервые использованного в 1900 году Гуго Эрдманном [5] для обозначения их чрезвычайно низкого уровня реакционной способности. Название проводит аналогию с термином « благородные металлы », которые также обладают низкой реакционной способностью. Благородные газы также упоминались как инертные газы , но это название устарело, поскольку теперь известно много соединений благородных газов . [6] Редкие газы — еще один используемый термин, [7] но он также неточен, поскольку аргон составляет довольно значительную часть (0,94% по объему, 1,3% по массе) атмосферы Земли из-за распада радиоактивного калия-40 . [8]
Пьер Жанссен и Джозеф Норман Локьер открыли новый элемент 18 августа 1868 года, рассматривая хромосферу Солнца , и назвали его гелием в честь греческого слова, обозначающего Солнце, ἥλιος ( hḗlios ). [9] В то время химический анализ был невозможен , но позже было обнаружено, что гелий является благородным газом. До них, в 1784 году, английский химик и физик Генри Кавендиш обнаружил, что воздух содержит небольшую долю вещества, менее реакционноспособного, чем азот . [10] Спустя столетие, в 1895 году, лорд Рэлей обнаружил, что образцы азота из воздуха имеют другую плотность , чем азот, полученный в результате химических реакций . Вместе с шотландским ученым Уильямом Рамзаем из Лондонского университетского колледжа лорд Рэлей выдвинул теорию о том, что азот, извлеченный из воздуха, смешивается с другим газом, что привело к эксперименту, в ходе которого был успешно выделен новый элемент, аргон, от греческого слова ἀργός ( argós , «праздный» или «ленивый»). [10] Благодаря этому открытию они поняли, что в периодической таблице отсутствует целый класс газов . Во время своих поисков аргона Рамзаю также удалось впервые выделить гелий при нагревании клевеита , минерала. В 1902 году, приняв доказательства существования элементов гелия и аргона, Дмитрий Менделеев включил эти благородные газы в качестве группы 0 в свою систему элементов, которая позже стала периодической таблицей. [11]
Рамзай продолжил поиск этих газов, используя метод фракционной перегонки для разделения жидкого воздуха на несколько компонентов. В 1898 году он открыл элементы криптон , неон и ксенон и назвал их в честь греческих слов κρυπτός ( kryptós , «скрытый»), νέος ( néos , «новый») и ξένος ( ksénos , «чужой») соответственно. Радон был впервые обнаружен в 1898 году Фридрихом Эрнстом Дорном [ 12] и был назван эманацией радия , но не считался благородным газом до 1904 года, когда было обнаружено, что его характеристики аналогичны характеристикам других благородных газов. [13] Рэлей и Рамзай получили Нобелевские премии 1904 года по физике и химии соответственно за открытие благородных газов; [14] [15] По словам Дж. Э. Седерблома, тогдашнего президента Королевской шведской академии наук , «открытие совершенно новой группы элементов, ни один представитель которой не был известен с какой-либо определенностью, является чем-то совершенно уникальным в истории химии, являясь по сути прогрессом в науке особой значимости». [15]
Открытие благородных газов помогло в развитии общего понимания атомной структуры . В 1895 году французский химик Анри Муассан попытался провести реакцию между фтором , наиболее электроотрицательным элементом, и аргоном, одним из благородных газов, но потерпел неудачу. Ученые не могли приготовить соединения аргона до конца 20-го века, но эти попытки помогли разработать новые теории атомной структуры. Извлекая уроки из этих экспериментов, датский физик Нильс Бор предположил в 1913 году, что электроны в атомах расположены в оболочках, окружающих ядро , и что для всех благородных газов, за исключением гелия, самая внешняя оболочка всегда содержит восемь электронов. [13] В 1916 году Гилберт Н. Льюис сформулировал правило октета , которое заключило, что октет электронов во внешней оболочке является наиболее стабильной компоновкой для любого атома; эта компоновка сделала их нереакционноспособными с другими элементами, поскольку им не требовалось больше электронов для завершения их внешней оболочки. [16]
В 1962 году Нил Бартлетт открыл первое химическое соединение благородного газа — гексафтороплатинат ксенона . [17] Вскоре после этого были открыты соединения других благородных газов: в 1962 году для радона был открыт дифторид радона ( RnF
2), [18] который был идентифицирован с помощью радиоактивных индикаторов и в 1963 году для криптона, дифторид криптона ( KrF
2). [19] Первое стабильное соединение аргона было получено в 2000 году, когда при температуре 40 К (−233,2 °C; −387,7 °F) образовался фторгидрид аргона (HArF). [20]
В октябре 2006 года ученые из Объединенного института ядерных исследований и Ливерморской национальной лаборатории им. Лоуренса успешно создали синтетическим путем оганесон , седьмой элемент в 18-й группе, [21] путем бомбардировки калифорния кальцием. [22]
Благородные газы имеют слабую межатомную силу и, следовательно, имеют очень низкие температуры плавления и кипения . Все они являются одноатомными газами при стандартных условиях , включая элементы с большими атомными массами , чем многие обычно твердые элементы. [13] Гелий обладает несколькими уникальными качествами по сравнению с другими элементами: его температура кипения при 1 атм ниже, чем у любого другого известного вещества ; это единственный известный элемент, проявляющий сверхтекучесть ; и это единственный элемент, который не может быть затвердевшим при охлаждении при атмосферном давлении [29] (эффект, объясняемый квантовой механикой , поскольку его энергия нулевой точки слишком высока, чтобы допустить замерзание ) [30] - давление в 25 стандартных атмосфер (2500 кПа ; 370 фунтов на квадратный дюйм ) должно быть применено при температуре 0,95 К (−272,200 °C; −457,960 °F), чтобы превратить его в твердое тело [29] , в то время как при комнатной температуре требуется давление около 113 500 атм (11 500 000 кПа; 1 668 000 фунтов на квадратный дюйм) . [31] Благородные газы вплоть до ксенона имеют несколько стабильных изотопов ; Криптон и ксенон также имеют встречающиеся в природе радиоизотопы , а именно 78Kr, 124Xe и 136Xe, все они имеют очень большую продолжительность жизни (> 10 21 лет) и могут подвергаться двойному захвату электронов или двойному бета-распаду . Радон не имеет стабильных изотопов ; его самый долгоживущий изотоп, 222Rn , имеет период полураспада 3,8 дня и распадается с образованием гелия и полония , который в конечном итоге распадается на свинец . [13] Оганесон также не имеет стабильных изотопов, и его единственный известный изотоп 294Og очень короткоживущий (период полураспада 0,7 мс). Температуры плавления и кипения увеличиваются спускаясь вниз по группе.

Атомы благородных газов , как и атомы в большинстве групп, неуклонно увеличивают свой атомный радиус от одного периода к другому из-за увеличения числа электронов . Размер атома связан с несколькими свойствами. Например, потенциал ионизации уменьшается с увеличением радиуса, поскольку валентные электроны в более крупных благородных газах находятся дальше от ядра и, следовательно, не удерживаются так плотно вместе атомом. Благородные газы имеют самый большой потенциал ионизации среди элементов каждого периода, что отражает стабильность их электронной конфигурации и связано с их относительной неактивностью в химическом отношении . [23] Однако некоторые из более тяжелых благородных газов имеют потенциал ионизации достаточно мал, чтобы быть сопоставимыми с потенциалами других элементов и молекул . Именно понимание того, что ксенон имеет потенциал ионизации, аналогичный потенциалу молекулы кислорода , привело Бартлетта к попытке окислить ксенон с помощью гексафторида платины , окислителя, который , как известно, достаточно силен, чтобы реагировать с кислородом. [17] Благородные газы не могут принять электрон для образования стабильных анионов ; то есть они имеют отрицательное сродство к электрону . [32]
Макроскопические физические свойства благородных газов определяются слабыми силами Ван-дер-Ваальса между атомами. Сила притяжения увеличивается с размером атома в результате увеличения поляризуемости и уменьшения потенциала ионизации. Это приводит к систематическим групповым тенденциям: по мере спуска по группе 18 увеличивается атомный радиус, а вместе с ним увеличиваются межатомные силы , что приводит к увеличению температуры плавления, кипения, энтальпии испарения и растворимости . Увеличение плотности происходит из-за увеличения атомной массы . [23]
Благородные газы являются почти идеальными газами при стандартных условиях, но их отклонения от закона идеального газа дали важные подсказки для изучения межмолекулярных взаимодействий . Потенциал Леннарда-Джонса , часто используемый для моделирования межмолекулярных взаимодействий , был выведен в 1924 году Джоном Леннардом-Джонсом из экспериментальных данных по аргону до того, как развитие квантовой механики предоставило инструменты для понимания межмолекулярных сил из первых принципов . [33] Теоретический анализ этих взаимодействий стал поддающимся обработке, поскольку благородные газы являются одноатомными, а атомы сферическими, что означает, что взаимодействие между атомами не зависит от направления или изотропно .

Благородные газы бесцветны, не имеют запаха, вкуса и не воспламеняются при стандартных условиях . [34] Когда-то они были обозначены как группа 0 в периодической таблице, поскольку считалось, что их валентность равна нулю, что означает, что их атомы не могут соединяться с атомами других элементов для образования соединений . Однако позже было обнаружено, что некоторые из них действительно образуют соединения, из-за чего эта метка вышла из употребления. [13]
Как и другие группы, члены этого семейства демонстрируют закономерности в своей электронной конфигурации , особенно на внешних оболочках, что приводит к тенденциям в химическом поведении:
Благородные газы имеют полные электронные оболочки валентности . Валентные электроны являются самыми внешними электронами атома и обычно являются единственными электронами, которые участвуют в химических связях . Атомы с полными электронными оболочками валентности чрезвычайно стабильны и поэтому не склонны образовывать химические связи и имеют небольшую тенденцию к приобретению или потере электронов . [35] Однако более тяжелые благородные газы, такие как радон, удерживаются вместе менее прочно электромагнитной силой , чем более легкие благородные газы, такие как гелий, что облегчает удаление внешних электронов из тяжелых благородных газов.
В результате полной оболочки благородные газы могут использоваться в сочетании с обозначением электронной конфигурации для формирования обозначения благородного газа . Для этого ближайший благородный газ, который предшествует рассматриваемому элементу, записывается первым, а затем электронная конфигурация продолжается с этой точки вперед. Например, электронная нотация фосфора - 1s 2 2s 2 2p 6 3s 2 3p 3 , в то время как обозначение благородного газа - [Ne] 3s 2 3p 3 . Эта более компактная нотация облегчает идентификацию элементов и короче, чем запись полного обозначения атомных орбиталей . [36]
Благородные газы пересекают границу между блоками — гелий является s-элементом , тогда как остальные члены являются p-элементами — что необычно для групп ИЮПАК . Все остальные группы ИЮПАК содержат элементы из одного блока каждая. Это вызывает некоторые несоответствия в тенденциях по всей таблице, и на этом основании некоторые химики предложили переместить гелий в группу 2 , чтобы он был с другими s 2 элементами, [37] [38] [39], но это изменение не было принято в целом.
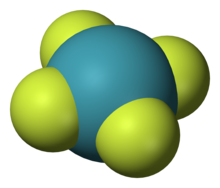
Благородные газы показывают крайне низкую химическую реактивность ; следовательно, было образовано всего несколько сотен соединений благородных газов . Нейтральные соединения , в которых гелий и неон участвуют в химических связях, не были образованы (хотя существуют некоторые гелийсодержащие ионы , и есть некоторые теоретические доказательства для нескольких нейтральных гелийсодержащих ионов), в то время как ксенон, криптон и аргон показали лишь незначительную реактивность. [40] Реакционная способность следует порядку Ne < He < Ar < Kr < Xe < Rn ≪ Og.
В 1933 году Лайнус Полинг предсказал, что более тяжелые благородные газы могут образовывать соединения с фтором и кислородом. Он предсказал существование гексафторида криптона ( KrF
6) и гексафторид ксенона ( XeF
6) и предположил, что октафторид ксенона ( XeF
8) может существовать как нестабильное соединение, и предположил, что ксеновая кислота может образовывать перксенатные соли. [41] [42] Было показано, что эти предсказания в целом точны, за исключением того, что XeF
8в настоящее время считается как термодинамически , так и кинетически нестабильным. [43]
Соединения ксенона являются наиболее многочисленными из образованных соединений благородных газов. [44] Большинство из них имеют атом ксенона в степени окисления +2, +4, +6 или +8, связанный с высоко электроотрицательными атомами, такими как фтор или кислород, как в дифториде ксенона ( XeF
2), тетрафторид ксенона ( XeF
4), гексафторид ксенона ( XeF
6), тетраоксид ксенона ( XeO
4) и перксенат натрия ( Na
4XeO
6). Ксенон реагирует с фтором, образуя многочисленные фториды ксенона в соответствии со следующими уравнениями:
Некоторые из этих соединений нашли применение в химическом синтезе в качестве окислителей ; XeF
2, в частности, коммерчески доступен и может использоваться в качестве фторирующего агента. [45] По состоянию на 2007 год было идентифицировано около пятисот соединений ксенона, связанного с другими элементами, включая органоксеноновые соединения (содержащие ксенон, связанный с углеродом), и ксенон, связанный с азотом, хлором, золотом, ртутью и самим ксеноном. [40] [46] Соединения ксенона, связанного с бором, водородом, бромом, йодом, бериллием, серой, титаном, медью и серебром, также наблюдались, но только при низких температурах в матрицах благородных газов или в сверхзвуковых струях благородных газов. [40]
Радон более реактивен, чем ксенон, и образует химические связи легче, чем ксенон. Однако из-за высокой радиоактивности и короткого периода полураспада изотопов радона на практике было образовано лишь несколько фторидов и оксидов радона. [47] Радон идет дальше к металлическому поведению, чем ксенон; дифторид RnF 2 является высокоионным, а катионный Rn 2+ образуется в растворах фторида галогена. По этой причине кинетические затруднения затрудняют окисление радона за пределами состояния +2. Похоже, что только эксперименты с трассерами увенчались успехом, вероятно, образовав RnF 4 , RnF 6 и RnO 3 . [48] [49] [50]
Криптон менее реактивен, чем ксенон, но сообщалось о нескольких соединениях с криптоном в степени окисления +2. [40] Дифторид криптона является наиболее заметным и легко охарактеризованным. В экстремальных условиях криптон реагирует с фтором, образуя KrF 2 согласно следующему уравнению:
Соединения, в которых криптон образует одинарную связь с азотом и кислородом, также были охарактеризованы [51], но они стабильны только при температурах ниже −60 °C (−76 °F) и −90 °C (−130 °F) соответственно. [40]
Атомы криптона, химически связанные с другими неметаллами (водородом, хлором, углеродом), а также с некоторыми поздними переходными металлами (медью, серебром, золотом), также наблюдались, но только либо при низких температурах в матрицах благородных газов, либо в сверхзвуковых струях благородных газов. [40] Аналогичные условия использовались для получения первых нескольких соединений аргона в 2000 году, таких как фторгидрид аргона (HArF), и некоторых, связанных с поздними переходными металлами медью, серебром и золотом. [40] По состоянию на 2007 год не было известно ни одной стабильной нейтральной молекулы, включающей ковалентно связанный гелий или неон. [40]
Экстраполяция периодических тенденций предсказывает, что оганесон должен быть наиболее реактивным из благородных газов; более сложные теоретические обработки указывают на большую реактивность, чем предполагают такие экстраполяции, до такой степени, что применимость дескриптора «благородный газ» была поставлена под сомнение. [52] Ожидается, что оганесон будет скорее похож на кремний или олово в группе 14: [53] реактивный элемент с общим +4 и менее распространенным +2 состоянием, [54] [55] который при комнатной температуре и давлении является не газом, а скорее твердым полупроводником. Для подтверждения этих предсказаний потребуются эмпирические / экспериментальные испытания. [24] [56] (С другой стороны, флеровий , несмотря на то, что находится в группе 14, как прогнозируется, будет необычайно летучим, что предполагает свойства, подобные свойствам благородного газа.) [57] [58]
Благородные газы, включая гелий, могут образовывать стабильные молекулярные ионы в газовой фазе. Простейшим является молекулярный ион гидрида гелия , HeH + , открытый в 1925 году. [59] Поскольку он состоит из двух наиболее распространенных элементов во Вселенной, водорода и гелия, считалось, что он естественным образом встречается в межзвездной среде , и он был наконец обнаружен в апреле 2019 года с помощью бортового телескопа SOFIA . Помимо этих ионов, существует множество известных нейтральных эксимеров благородных газов. Это такие соединения, как ArF и KrF, которые стабильны только в возбужденном электронном состоянии ; некоторые из них находят применение в эксимерных лазерах .
В дополнение к соединениям, где атом благородного газа участвует в ковалентной связи , благородные газы также образуют нековалентные соединения. Клатраты , впервые описанные в 1949 году, [60] состоят из атома благородного газа, захваченного в полостях кристаллических решеток некоторых органических и неорганических веществ. Основным условием их образования является то, что гостевые атомы (благородного газа) должны иметь соответствующий размер, чтобы поместиться в полостях кристаллической решетки хозяина. Например, аргон, криптон и ксенон образуют клатраты с гидрохиноном , но гелий и неон не образуют, потому что они слишком малы или недостаточно поляризуемы , чтобы удерживаться. [61] Неон, аргон, криптон и ксенон также образуют клатратные гидраты, в которых благородный газ захвачен льдом. [62]
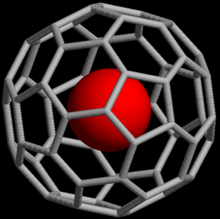
Благородные газы могут образовывать эндоэдральные фуллереновые соединения, в которых атом благородного газа заключен внутри молекулы фуллерена . В 1993 году было обнаружено, что когда C
60, сферическая молекула, состоящая из 60 атомов углерода , подвергается воздействию благородных газов при высоком давлении, комплексы , такие как He@C
60может быть сформирован ( обозначение @ указывает, что Он содержится внутри C
60но не ковалентно связаны с ним). [63] По состоянию на 2008 год были созданы эндоэдральные комплексы с гелием, неоном, аргоном, криптоном и ксеноном. [64] Эти соединения нашли применение в изучении структуры и реакционной способности фуллеренов с помощью ядерного магнитного резонанса атома благородного газа. [65]

Соединения благородных газов, такие как дифторид ксенона ( XeF
2) считаются гипервалентными , поскольку они нарушают правило октета . Связывание в таких соединениях можно объяснить с помощью модели трехцентровой четырехэлектронной связи . [66] [67] Эта модель, впервые предложенная в 1951 году, рассматривает связывание трех коллинеарных атомов. Например, связывание в XeF
2описывается набором из трех молекулярных орбиталей (МО), полученных из p-орбиталей на каждом атоме. Связывание происходит из-за комбинации заполненной p-орбитали от Xe с одной наполовину заполненной p-орбиталью от каждого атома F , что приводит к заполненной связывающей орбитали, заполненной несвязывающей орбитали и пустой антисвязывающей орбитали. Самая высокая занятая молекулярная орбиталь локализована на двух конечных атомах. Это представляет собой локализацию заряда, которая облегчается высокой электроотрицательностью фтора. [68]
Химия более тяжелых благородных газов, криптона и ксенона, хорошо изучена. Химия более легких, аргона и гелия, все еще находится на ранней стадии, в то время как соединение неона еще не идентифицировано.
Содержание благородных газов во Вселенной уменьшается по мере увеличения их атомных чисел . Гелий является наиболее распространенным элементом во Вселенной после водорода, с массовой долей около 24%. Большая часть гелия во Вселенной образовалась во время нуклеосинтеза Большого взрыва , но количество гелия неуклонно увеличивается из-за синтеза водорода в звездном нуклеосинтезе (и, в очень небольшой степени, альфа-распада тяжелых элементов). [69] [70] Содержание гелия на Земле следует различным тенденциям; например, гелий является лишь третьим по распространенности благородным газом в атмосфере. Причина в том, что в атмосфере нет первичного гелия; из-за малой массы атома гелий не может удерживаться гравитационным полем Земли . [71] Гелий на Земле появляется в результате альфа-распада тяжелых элементов, таких как уран и торий, обнаруженных в земной коре , и имеет тенденцию накапливаться в месторождениях природного газа . [71] С другой стороны, содержание аргона увеличивается в результате бета-распада калия -40 , также обнаруженного в земной коре, с образованием аргона-40 , который является наиболее распространенным изотопом аргона на Земле, несмотря на то, что он относительно редок в Солнечной системе . Этот процесс является основой для метода датирования калия-аргона . [72] Ксенон имеет неожиданно низкое содержание в атмосфере, что было названо проблемой отсутствующего ксенона ; одна из теорий заключается в том, что отсутствующий ксенон может быть захвачен минералами внутри земной коры. [73] После открытия диоксида ксенона исследования показали, что Xe может заменять Si в кварце . [74] Радон образуется в литосфере в результате альфа-распада радия. Он может просачиваться в здания через трещины в их фундаменте и накапливаться в плохо проветриваемых помещениях. Из-за своей высокой радиоактивности радон представляет значительную опасность для здоровья; По оценкам , только в Соединенных Штатах он является причиной 21 000 случаев смерти от рака легких в год. [75] Оганесон не встречается в природе, а создается вручную учеными.
Для крупномасштабного использования гелий извлекается методом фракционной перегонки из природного газа, который может содержать до 7% гелия. [80]
Неон, аргон, криптон и ксенон получают из воздуха с использованием методов сжижения газов , чтобы преобразовать элементы в жидкое состояние, и фракционной перегонки , чтобы разделить смеси на составные части. Гелий обычно получают путем его отделения от природного газа , а радон выделяют из радиоактивного распада соединений радия. [13] Цены на благородные газы зависят от их естественного распространения, причем аргон является самым дешевым, а ксенон — самым дорогим. В качестве примера в соседней таблице приведены цены 2004 года в Соединенных Штатах для лабораторных количеств каждого газа.
Ни один из элементов этой группы не имеет биологического значения. [81]

Благородные газы имеют очень низкие температуры кипения и плавления, что делает их полезными в качестве криогенных хладагентов . [82] В частности, жидкий гелий , который кипит при 4,2 К (−268,95 °C; −452,11 °F), используется для сверхпроводящих магнитов , таких как те, которые необходимы в ядерной магнитно-резонансной томографии и ядерном магнитном резонансе . [83] Жидкий неон, хотя он и не достигает таких низких температур, как жидкий гелий, также находит применение в криогенике, поскольку имеет более чем в 40 раз большую холодопроизводительность, чем жидкий гелий, и более чем в три раза больше, чем жидкий водород. [78]
Гелий используется в качестве компонента дыхательных газов для замены азота из-за его низкой растворимости в жидкостях, особенно в липидах . Газы поглощаются кровью и тканями тела под давлением, как при подводном плавании , что вызывает анестезирующий эффект, известный как азотный наркоз . [84] Из-за его пониженной растворимости мало гелия попадает в клеточные мембраны , и когда гелий используется для замены части дыхательных смесей, таких как тримикс или гелиокс , достигается снижение наркотического эффекта газа на глубине. [85] Пониженная растворимость гелия дает дополнительные преимущества при состоянии, известном как декомпрессионная болезнь , или кессонная болезнь . [13] [86] Уменьшенное количество растворенного газа в организме означает, что меньше пузырьков газа образуется во время снижения давления при всплытии. Другой благородный газ, аргон, считается лучшим вариантом для использования в качестве газа для надувания сухого костюма для подводного плавания. [87] Гелий также используется в качестве заполняющего газа в топливных стержнях ядерных реакторов. [88]

После катастрофы дирижабля «Гинденбург» в 1937 году [89] гелий заменил водород в качестве подъемного газа в дирижаблях и воздушных шарах : несмотря на снижение плавучести на 8,6% [90] по сравнению с водородом, гелий не горюч. [13]
Во многих приложениях благородные газы используются для обеспечения инертной атмосферы. Аргон используется в синтезе соединений, чувствительных к воздуху , которые чувствительны к азоту. Твердый аргон также используется для изучения очень нестабильных соединений, таких как реактивные промежуточные продукты , путем их улавливания в инертной матрице при очень низких температурах. [91] Гелий используется в качестве среды-носителя в газовой хроматографии , в качестве наполнителя для термометров и в устройствах для измерения радиации, таких как счетчик Гейгера и пузырьковая камера . [79] Гелий и аргон обычно используются для защиты сварочных дуг и окружающего основного металла от атмосферы во время сварки и резки, а также в других металлургических процессах и в производстве кремния для полупроводниковой промышленности. [78]

Благородные газы обычно используются в освещении из-за отсутствия у них химической активности. Аргон, смешанный с азотом, используется в качестве наполнителя для ламп накаливания . [78] Криптон используется в высокопроизводительных лампочках, которые имеют более высокие цветовые температуры и большую эффективность, поскольку он снижает скорость испарения нити больше, чем аргон; галогенные лампы , в частности, используют криптон, смешанный с небольшим количеством соединений йода или брома . [78] Благородные газы светятся отличительными цветами при использовании внутри газоразрядных ламп , таких как « неоновые огни ». Эти огни называются в честь неона, но часто содержат другие газы и люминофоры , которые добавляют различные оттенки к оранжево-красному цвету неона. Ксенон обычно используется в ксеноновых дуговых лампах , которые из-за своего почти непрерывного спектра , напоминающего дневной свет, находят применение в кинопроекторах и в качестве автомобильных фар. [78]
Благородные газы используются в эксимерных лазерах , которые основаны на короткоживущих электронно-возбужденных молекулах, известных как эксимеры . Эксимеры, используемые для лазеров, могут быть димерами благородных газов, такими как Ar2 , Kr2 или Xe2 , или, что более распространено, благородный газ сочетается с галогеном в эксимерах, таких как ArF, KrF, XeF или XeCl. Эти лазеры производят ультрафиолетовый свет, который из-за своей короткой длины волны (193 нм для ArF и 248 нм для KrF) позволяет получать высокоточные изображения. Эксимерные лазеры имеют множество промышленных, медицинских и научных применений. Они используются для микролитографии и микропроизводства , которые необходимы для производства интегральных схем , а также для лазерной хирургии , включая лазерную ангиопластику и хирургию глаза . [92]
Некоторые благородные газы имеют прямое применение в медицине. Гелий иногда используется для облегчения дыхания у людей, страдающих астмой . [78] Ксенон используется в качестве анестетика из-за его высокой растворимости в липидах, что делает его более мощным, чем обычная закись азота , и потому, что он легко выводится из организма, что приводит к более быстрому выздоровлению. [93] Ксенон находит применение в медицинской визуализации легких с помощью гиперполяризованной МРТ. [94] Радон, который является высокорадиоактивным и доступен только в малых количествах, используется в радиотерапии . [13]
Благородные газы, в частности ксенон, в основном используются в ионных двигателях из-за их инертности. Поскольку ионные двигатели не приводятся в действие химическими реакциями, желательно использовать химически инертное топливо, чтобы предотвратить нежелательную реакцию между топливом и чем-либо еще в двигателе.
Оганесон слишком нестабилен, чтобы с ним работать, и не имеет известных применений, кроме исследовательских целей.
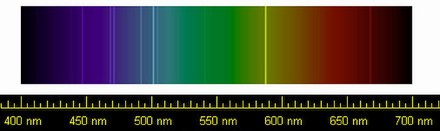
Цвет газового разряда зависит от нескольких факторов, среди которых: [95]
Элементы 18-й группы (благородные газы) не вступают в реакцию и не имеют биологического значения.