Тимус ( мн.ч .: тимусы или тимусы ) — специализированный первичный лимфоидный орган иммунной системы . Внутри тимуса созревают лимфоциты тимусных клеток или Т-клетки. Т-клетки имеют решающее значение для адаптивной иммунной системы , где организм адаптируется к определенным чужеродным захватчикам. Тимус расположен в верхней передней части грудной клетки, в переднем верхнем средостении , за грудиной и перед сердцем . Он состоит из двух долей, каждая из которых состоит из центрального мозгового вещества и внешней коры, окруженных капсулой.
Тимус состоит из незрелых Т-клеток, называемых тимоцитами , а также выстилающих клеток, называемых эпителиальными клетками , которые помогают тимоцитам развиваться. Т-клетки, которые успешно развиваются, соответствующим образом реагируют с иммунными рецепторами MHC организма (так называемый положительный отбор ), а не с белками организма (так называемый отрицательный отбор ). Тимус является самым большим и активным в неонатальный и предподростковый периоды. К раннему подростковому возрасту тимус начинает уменьшаться в размерах и активности , и ткань тимуса постепенно заменяется жировой тканью . Тем не менее, некоторое развитие Т-клеток продолжается на протяжении всей взрослой жизни.
Аномалии тимуса могут привести к уменьшению количества Т-клеток и аутоиммунным заболеваниям, таким как аутоиммунный полиэндокринный синдром 1-го типа и миастения гравис . Они часто связаны с раком ткани тимуса, называемым тимомой , или тканями, возникающими из незрелых лимфоцитов, таких как Т-клетки, называемыми лимфомой . Удаление тимуса называется тимэктомией . Хотя тимус был идентифицирован как часть тела со времен древних греков , только с 1960-х годов функция тимуса в иммунной системе стала более ясной.
Тимус — это орган, который находится за грудиной в верхней передней части груди, простираясь вверх к шее. У детей тимус розовато-серый, мягкий и дольчатый на своих поверхностях. [1] При рождении он составляет около 4–6 см в длину, 2,5–5 см в ширину и около 1 см в толщину. [2] Он увеличивается в размерах до полового созревания, когда он может иметь размер около 40–50 г, [3] [4] после чего он уменьшается в размерах в процессе, известном как инволюция . [4]
Тимус расположен в переднем средостении . [5] Он состоит из двух долей, которые встречаются в верхней средней линии и тянутся от нижней части щитовидной железы в области шеи до хряща четвертого ребра. [1] Доли покрыты капсулой. [3] Тимус лежит за грудиной, опирается на перикард и отделен от дуги аорты и крупных сосудов слоем фасции . Левая плечеголовная вена может даже быть встроена в тимус. [1] В шее он лежит спереди и по бокам от трахеи , позади грудино-подъязычной и грудино-щитовидной мышц . [1]
Тимус состоит из двух долей, слитых в середине, окруженных капсулой, которая простирается вместе с кровеносными сосудами внутрь. [2] Доли состоят из внешней коры, богатой клетками, и внутренней менее плотной мозговой части . [4] Доли разделены на более мелкие дольки диаметром 0,5-2 мм, между которыми выступают радиально расходящиеся вставки из капсулы вдоль перегородок . [1]
Кора в основном состоит из тимоцитов и эпителиальных клеток. [3] Тимоциты, незрелые Т-клетки , поддерживаются сетью тонко разветвленных эпителиальных ретикулярных клеток , которая является продолжением аналогичной сети в мозговом веществе. Эта сеть образует адвентицию кровеносных сосудов, которые входят в кору через перегородки около соединения с мозговым веществом. [1] В тимусе также присутствуют другие клетки, включая макрофаги , дендритные клетки и небольшое количество В-клеток , нейтрофилов и эозинофилов . [3]
В мозговом веществе сеть эпителиальных клеток грубее, чем в корковом веществе, а лимфоидных клеток относительно меньше. [1] Концентрические, гнездообразные тельца, называемые тельцами Гассаля (также называемые тимическими тельцами ), образуются путем скопления мозговых эпителиальных клеток. [3] Это концентрические, слоистые завитки эпителиальных клеток , количество которых увеличивается на протяжении всей жизни. [1] Это остатки эпителиальных трубок, которые вырастают из третьих глоточных карманов эмбриона, образуя тимус. [6]
Артерии , снабжающие тимус, являются ветвями внутренней грудной и нижней щитовидной артерий , а также иногда видны ветви от верхней щитовидной артерии . [2] Ветви достигают тимуса и проходят с перегородками капсулы в область между корой и мозговым веществом, где они входят в сам тимус; или, в качестве альтернативы, напрямую входят в капсулу. [2]
Вены тимуса, тимические вены , заканчиваются в левой плечеголовной вене , внутренней грудной вене и в нижних щитовидных венах . [2] Иногда вены заканчиваются непосредственно в верхней полой вене. [2]
Лимфатические сосуды идут только от тимуса, сопровождая артерии и вены. Они дренируются в плечеголовные, трахеобронхиальные и парастернальные лимфатические узлы . [2]
Нервы , иннервирующие тимус, берут начало от блуждающего нерва и шейной симпатической цепи . [2] Ветви диафрагмальных нервов достигают капсулы тимуса, но не входят в сам тимус. [2]
Две доли немного отличаются по размеру, причем левая доля обычно выше правой. Тимусная ткань может быть обнаружена разбросанной на железе или вокруг нее, а иногда и внутри щитовидной железы. [2] Тимус у детей тянется вверх по-разному, иногда до такой же высоты, как щитовидная железа. [2]
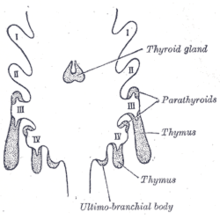
Тимоциты и эпителий тимуса имеют разное происхождение развития. [4] Эпителий тимуса развивается первым, появляясь как два выроста, по одному с каждой стороны, третьего глоточного кармана . [4] Иногда он также включает четвертый глоточный карман. [3] Они простираются наружу и назад в окружающую мезодерму и мезенхиму , полученную из нервного гребня , перед брюшной аортой . Здесь тимоциты и эпителий встречаются и соединяются с соединительной тканью. Глоточное отверстие каждого дивертикула вскоре облитерируется, но шейка колбы сохраняется в течение некоторого времени как клеточный тяж. Дальнейшая пролиферация клеток, выстилающих колбу, приводит к образованию зачатков клеток, которые окружаются и изолируются вторгающейся мезодермой. [7]
Эпителий образует мелкие дольки и развивается в губчатую структуру. На этой стадии кроветворные костномозговые предшественники мигрируют в тимус. [4] Нормальное развитие зависит от взаимодействия эпителия и кроветворных тимоцитов . Йод также необходим для развития и активности тимуса. [8]
Тимус продолжает расти после рождения, достигая относительно максимального размера к половому созреванию. [2] Он наиболее активен в эмбриональном и неонатальном периоде. [9] К половому созреванию он увеличивается до массы 20–50 граммов. [3] Затем он начинает уменьшаться в размерах и активности в процессе, называемом инволюцией тимуса . [4] После первого года жизни количество вырабатываемых Т-клеток начинает падать. [4] Жир и соединительная ткань заполняют часть объема тимуса. [2] Во время инволюции тимус уменьшается в размерах и активности. [4] Жировые клетки присутствуют при рождении, но заметно увеличиваются в размерах и количестве после полового созревания, сначала проникая в железу из стенок между дольками, затем в корковое и мозговое вещество. [4] Этот процесс продолжается до старости, когда с помощью микроскопа или человеческого глаза тимус может быть трудно обнаружить, [4] хотя обычно он весит 5–15 граммов. [3] Кроме того, появляется все больше доказательств того, что возрастная инволюция тимуса наблюдается у большинства, если не у всех, видов позвоночных, имеющих тимус, что позволяет предположить, что это эволюционный процесс, который сохранился. [40]
Атрофия обусловлена повышенным уровнем циркулирующих половых гормонов , а химическая или физическая кастрация взрослого человека приводит к увеличению размера и активности тимуса. [10] Тяжелая болезнь или заражение вирусом иммунодефицита человека также могут привести к инволюции. [3]

Тимус способствует созреванию Т-клеток , важной части иммунной системы, обеспечивающей клеточно-опосредованный иммунитет . [11] Т-клетки начинаются как кроветворные предшественники из костного мозга и мигрируют в тимус, где их называют тимоцитами . В тимусе они проходят процесс созревания, который включает обеспечение реакции клеток против антигенов («положительный отбор»), но то, что они не реагируют против антигенов, обнаруженных в тканях тела («отрицательный отбор»). [11] После созревания Т-клетки эмигрируют из тимуса, чтобы обеспечить жизненно важные функции в иммунной системе. [11] [12]
Каждая Т-клетка имеет отдельный Т-клеточный рецептор , подходящий для определенного вещества, называемого антигеном . [12] Большинство Т-клеточных рецепторов связываются с главным комплексом гистосовместимости на клетках организма. MHC представляет антиген Т-клеточному рецептору, который становится активным, если он соответствует определенному Т-клеточному рецептору. [12] Для того чтобы быть должным образом функциональной, зрелая Т-клетка должна иметь возможность связываться с молекулой MHC («положительный отбор») и не реагировать на антигены, которые на самом деле происходят из тканей организма («отрицательный отбор»). [12] Положительный отбор происходит в коре, а отрицательный отбор — в мозговом веществе тимуса. [13] После этого процесса выжившие Т-клетки покидают тимус, регулируемый сфингозин-1-фосфатом . [13] Дальнейшее созревание происходит в периферическом кровообращении. [13] Частично это происходит из-за гормонов и цитокинов, секретируемых клетками внутри тимуса, включая тимулин , тимопоэтин и тимозины . [4]
Т-клетки имеют различные Т-клеточные рецепторы. Эти различные рецепторы формируются в процессе перестройки гена рекомбинации V(D)J, стимулируемой генами RAG1 и RAG2 . [13] Этот процесс подвержен ошибкам, и некоторые тимоциты не могут вырабатывать функциональные Т-клеточные рецепторы, тогда как другие тимоциты вырабатывают Т-клеточные рецепторы, которые являются аутореактивными. [14] Если формируется функциональный Т-клеточный рецептор, тимоцит начнет одновременно экспрессировать белки клеточной поверхности CD4 и CD8 . [13]
Выживание и природа Т-клетки затем зависят от ее взаимодействия с окружающими эпителиальными клетками тимуса. Здесь рецептор Т-клетки взаимодействует с молекулами MHC на поверхности эпителиальных клеток. [13] AT-клетка с рецептором, который не реагирует или реагирует слабо, погибнет в результате апоптоза . AT-клетка, которая реагирует, выживет и будет размножаться. [13] Зрелая Т-клетка экспрессирует только CD4 или CD8, но не оба. [12] Это зависит от силы связывания между TCR и MHC класса 1 или класса 2. [13] Рецептор AT-клетки, который связывается в основном с MHC класса I, имеет тенденцию производить зрелую «цитотоксическую» CD8-положительную Т-клетку; рецептор Т-клетки, который связывается в основном с MHC класса II, имеет тенденцию производить CD4-положительную Т-клетку. [14]
Т-клетки, которые атакуют собственные белки организма, устраняются в тимусе, что называется «отрицательным отбором». [12] Эпителиальные клетки в мозговом веществе и дендритные клетки в тимусе экспрессируют основные белки из других частей организма. [13] Ген, который стимулирует это, называется AIRE . [12] [13] Тимоциты, которые сильно реагируют на собственные антигены, не выживают и погибают в результате апоптоза. [12] [13] Некоторые CD4-положительные Т-клетки, подвергшиеся воздействию собственных антигенов, сохраняются как регуляторные Т-клетки . [12]
Поскольку тимус является местом развития Т-клеток, врожденные проблемы с развитием тимуса могут привести к иммунодефициту , будь то из-за проблемы с развитием вилочковой железы или проблемы, специфичной для развития тимоцитов. Иммунодефицит может быть глубоким. [9] Потеря тимуса в раннем возрасте из-за генетической мутации (как при синдроме ДиДжорджи , синдроме CHARGE или очень редком «голом» тимусе, вызывающем отсутствие волос и тимуса [15] ) приводит к тяжелому иммунодефициту и последующей высокой восприимчивости к заражению вирусами, простейшими и грибками . [16] Голые мыши с очень редким «голым» дефицитом в результате мутации FOXN1 являются штаммом исследовательских мышей в качестве модели дефицита Т-клеток. [17]
Наиболее распространенной врожденной причиной иммунодефицита, связанного с тимусом, является делеция 22-й хромосомы , называемая синдромом ДиДжорджи . [15] [16] Это приводит к нарушению развития третьего и четвертого глоточных карманов, что приводит к нарушению развития тимуса и различным другим сопутствующим проблемам, таким как врожденный порок сердца и аномалии рта (такие как расщелина неба и заячья губа ), нарушение развития паращитовидных желез и наличие свища между трахеей и пищеводом . [16] Наблюдается очень низкое количество циркулирующих Т-клеток. [16] Состояние диагностируется с помощью флуоресцентной гибридизации in situ и лечится с помощью трансплантации тимуса . [15]
Тяжелый комбинированный иммунодефицит (ТКИД) — это группа редких врожденных генетических заболеваний, которые могут приводить к комбинированному дефициту Т-, В- и NK-клеток . [16] Эти синдромы вызваны мутациями, которые влияют на созревание гемопоэтических клеток-предшественников , которые являются предшественниками как В-, так и Т-клеток. [16] Ряд генетических дефектов могут вызывать ТКИД, включая потерю функции гена рецептора ИЛ-2 и мутацию, приводящую к дефициту фермента адениндезаминазы . [ 16]
Аутоиммунный полиэндокринный синдром 1-го типа — редкий генетический аутоиммунный синдром, возникающий в результате генетического дефекта тканей тимуса. [18] В частности, заболевание возникает из-за дефектов гена аутоиммунного регулятора (AIRE), который стимулирует экспрессию собственных антигенов в эпителиальных клетках мозгового вещества тимуса. Из-за дефектов в этом состоянии собственные антигены не экспрессируются, в результате чего Т-клетки не приспособлены переносить ткани организма и могут относиться к ним как к чужеродным, стимулируя иммунный ответ и приводя к аутоиммунитету. [18] У людей с APECED развивается аутоиммунное заболевание, которое поражает несколько эндокринных тканей, причем наиболее часто поражаемыми органами являются гипотиреоз щитовидной железы , болезнь Аддисона надпочечников и кандидозная инфекция поверхностей тела, включая внутреннюю оболочку рта и ногтей из -за дисфункции клеток TH17 , и симптомы часто начинаются в детстве. Также могут возникать многие другие аутоиммунные заболевания. [18] Лечение направлено на пораженные органы. [18]
У людей с тимомой может возникнуть мультиорганный аутоиммунитет, связанный с тимомой . При этом состоянии Т-клетки, вырабатываемые в тимусе, направлены против тканей организма. Это происходит потому, что злокачественный тимус не способен надлежащим образом обучать развивающиеся тимоциты для устранения аутореактивных Т-клеток. Это состояние практически неотличимо от реакции «трансплантат против хозяина» . [19]
Миастения гравис является аутоиммунным заболеванием, чаще всего вызванным антителами, которые блокируют ацетилхолиновые рецепторы , участвующие в передаче сигналов между нервами и мышцами . [20] Она часто связана с гиперплазией тимуса или тимомой, [20] с антителами, вырабатываемыми, вероятно, из-за Т-клеток, которые развиваются ненормально. [21] Миастения гравис чаще всего развивается в молодом и среднем возрасте, вызывая легкую утомляемость мышечных движений. [20] Исследования включают демонстрацию антител (например, против ацетилхолиновых рецепторов или мышечной специфической киназы ), а также компьютерную томографию для обнаружения тимомы или тимэктомии. [20] Что касается тимуса, удаление тимуса, называемое тимэктомией , может рассматриваться как лечение, особенно если обнаружена тимома. [20] Другие методы лечения включают увеличение продолжительности действия ацетилхолина в нервных синапсах за счет снижения скорости распада. Это делается с помощью ингибиторов ацетилхолинэстеразы, таких как пиридостигмин . [20]
Опухоли, происходящие из эпителиальных клеток тимуса, называются тимомами . [3] Чаще всего они встречаются у взрослых старше 40 лет. [3] Опухоли обычно обнаруживаются, когда они вызывают симптомы, такие как опухоль на шее или поражают близлежащие структуры, такие как верхняя полая вена ; [21] обнаруживаются в результате скрининга у пациентов с миастенией, которая имеет тесную связь с тимомами и гиперплазией; [3] и обнаруживаются как случайная находка при визуализации, такой как рентгенография грудной клетки . [21] Гиперплазия и опухоли, происходящие из тимуса, связаны с другими аутоиммунными заболеваниями, такими как гипогаммаглобулинемия , болезнь Грейвса , чистая эритроцитарная аплазия , пернициозная анемия и дерматомиозит , вероятно, из-за дефектов отрицательного отбора в пролиферирующих Т-клетках. [3] [22]
Тимомы могут быть доброкачественными; доброкачественными, но в силу расширения, проникающими за пределы капсулы тимуса («инвазивная тимома»), или злокачественными ( карцинома ). [3] Эта классификация основана на внешнем виде клеток. [3] Также существует классификация ВОЗ , но она не используется как часть стандартной клинической практики. [3] Доброкачественные опухоли, ограниченные тимусом, являются наиболее распространенными; за ними следуют локально инвазивные опухоли, а затем карциномы. [3] Существуют различия в сообщениях, при этом некоторые источники сообщают о злокачественных опухолях как о более распространенных. [22] Инвазивные опухоли, хотя технически не являются злокачественными, все же могут распространяться ( метастазировать ) в другие области тела. [3] Несмотря на то, что тимомы происходят из эпителиальных клеток, они также могут содержать тимоциты. [3] Лечение тимом часто требует хирургического вмешательства для удаления всего тимуса. [22] Это также может привести к временной ремиссии любых связанных аутоиммунных состояний. [22]
Опухоли, происходящие из Т-клеток тимуса, образуют подтип острого лимфобластного лейкоза (ОЛЛ). [23] Они похожи по симптомам, подходу к исследованию и лечению на другие формы ОЛЛ. [23] Симптомы, которые развиваются, как и другие формы ОЛЛ, связаны с дефицитом тромбоцитов , что приводит к синякам или кровотечению; иммуносупрессией, что приводит к инфекциям; или инфильтрацией клетками частей тела, что приводит к увеличению печени , селезенки , лимфатических узлов или других участков. [23] Анализ крови может выявить большое количество лейкоцитов или лимфобластов , а также дефицит других клеточных линий, таких как низкий уровень тромбоцитов или анемия . [23] Иммунофенотипирование выявит клетки, которые являются CD3 , белком, обнаруженным на Т-клетках, и поможет дополнительно различить зрелость Т-клеток. Генетический анализ, включая кариотипирование, может выявить определенные аномалии, которые могут повлиять на прогноз или лечение, такие как транслокация Филадельфия . [23] Лечение может включать несколько курсов химиотерапии , трансплантацию стволовых клеток и лечение сопутствующих проблем, таких как лечение инфекций антибиотиками и переливание крови . Очень высокие показатели лейкоцитов могут также потребовать циторедукции с аферезом . [23]
Опухоли, происходящие из небольшой популяции В-клеток, присутствующих в тимусе, приводят к первичным медиастинальным (тимическим) крупным В-клеточным лимфомам . [24] Это редкий подтип неходжкинской лимфомы , хотя по активности генов и иногда микроскопической форме они, как правило, также имеют характеристики лимфом Ходжкина . [25] Чаще всего они встречаются у молодых и людей среднего возраста, более выражены у женщин. [25] Чаще всего симптомы возникают из-за сдавления структур вблизи тимуса, таких как верхняя полая вена или верхние дыхательные пути ; когда поражаются лимфатические узлы, это часто происходит в средостении и группах шеи . [25] Такие опухоли часто обнаруживаются с помощью биопсии , которая подвергается иммуногистохимии . Это покажет наличие кластеров дифференциации , белков клеточной поверхности, а именно CD30 , с CD19 , CD20 и CD22 , и с отсутствием CD15 . Для подтверждения диагноза могут также использоваться другие маркеры. [25] Лечение обычно включает типичные схемы CHOP или EPOCH или другие схемы; схемы, как правило, включающие циклофосфамид , антрациклин , преднизон и другие химиотерапевтические средства; и потенциально также трансплантацию стволовых клеток . [25]
Тимус может содержать кисты, обычно менее 4 см в диаметре. Тимусные кисты обычно обнаруживаются случайно и, как правило, не вызывают симптомов. [3] Тимусные кисты могут возникать вдоль шеи или в груди ( средостении ). [26] Кисты обычно просто содержат жидкость и выстланы либо многими слоями плоских клеток , либо столбчатыми клетками . [26] Несмотря на это, наличие кисты может вызывать проблемы, аналогичные проблемам тимом, сдавливая близлежащие структуры, [3] а некоторые могут контактировать с внутренними стенками ( перегородками ) и их трудно отличить от опухолей. [26] При обнаружении кист исследование может включать обследование на наличие опухолей, которое может включать КТ или МРТ области, в которой предположительно находится киста. [3] [26]
Тимэктомия — это хирургическое удаление тимуса. [2] Обычной причиной удаления является получение доступа к сердцу для хирургического исправления врожденных пороков сердца в неонатальном периоде. [27] Другие показания к тимэктомии включают удаление тимом и лечение миастении. [2] У новорожденных относительный размер тимуса затрудняет хирургический доступ к сердцу и окружающим его сосудам. [27]
Удаление тимуса в младенчестве часто приводит к фатальному иммунодефициту, поскольку функциональные Т-клетки не развились. [2] [28] У детей старшего возраста и взрослых, у которых функционирует лимфатическая система со зрелыми Т-клетками, также расположенными в других лимфоидных органах, эффект снижается, но включает в себя неспособность сформировать иммунный ответ против новых антигенов, [2] увеличение числа случаев рака и увеличение смертности от всех причин. [29]
При употреблении в пищу человеком тимус животных известен как один из видов зобной железы . [30]
Тимус был известен древним грекам , и его название происходит от греческого слова θυμός ( thumos ), что означает «гнев» или на древнегреческом «сердце, душа, желание, жизнь», возможно, из-за его расположения в груди, рядом с тем местом, где субъективно ощущаются эмоции; [31] или же название происходит от травы тимьян (также на греческом θύμος или θυμάρι ), которая стала названием для «бородавчатого нароста», возможно, из-за его сходства с пучком тимьяна. [32]
Гален был первым, кто заметил, что размер органа меняется на протяжении жизни человека. [33]
В девятнадцатом веке состояние было идентифицировано как status thymicolymphaticus , определяемое увеличением лимфоидной ткани и увеличенным тимусом. Считалось, что это является причиной синдрома внезапной детской смерти, но теперь это устаревший термин. [34]
Важность тимуса в иммунной системе была открыта в 1961 году Жаком Миллером , который хирургическим путем удалил тимус у однодневных мышей и наблюдал последующий дефицит популяции лимфоцитов, впоследствии названных Т-клетками в честь органа их происхождения. [35] [36] До открытия его иммунологической роли тимус считался «эволюционной случайностью», не имеющей функционального значения. [14] Роль тимуса в обеспечении переносимости зрелых Т-клеток тканями организма была раскрыта в 1962 году, когда было обнаружено, что Т-клетки трансплантированного тимуса у мышей демонстрируют толерантность к тканям донорской мыши. [14] В-клетки и Т-клетки были идентифицированы как разные типы лимфоцитов в 1968 году, и был понят тот факт, что Т-клетки требуют созревания в тимусе. [14] Подтипы Т-клеток (CD8 и CD4) были идентифицированы к 1975 году. [14] Способ созревания этих подклассов Т-клеток — позитивный отбор клеток, функционально связанных с рецепторами MHC — был известен к 1990-м годам. [14] Важная роль гена AIRE и роль негативного отбора в предотвращении созревания аутореактивных Т-клеток были поняты к 1994 году. [14]
В последнее время достижения иммунологии позволили более полно понять функцию тимуса в созревании Т-клеток. [14]
Тимус присутствует у всех челюстных позвоночных , где он претерпевает такое же сокращение с возрастом и играет ту же иммунологическую функцию, что и у других позвоночных. Недавно, в 2011 году, в жабрах личинок миног была обнаружена дискретная тимус-подобная лимфоэпителиальная структура, названная тимоидом . [37] Миксины обладают прототимусом, связанным с глоточными велярными мышцами, который отвечает за различные иммунные реакции. [38]
Тимус также присутствует у большинства других позвоночных с похожей структурой и функцией, как у человеческого тимуса. Сообщалось, что второй тимус в шее иногда встречается у мыши [39] Как и у людей, тимус морской свинки естественным образом атрофируется, когда животное достигает зрелого возраста, [40] но бестимусная безволосая морская свинка (которая возникла в результате спонтанной лабораторной мутации) вообще не имеет тимической ткани, а полость органа заменяется кистозными пространствами. [41]
![]() В статье использован текст, находящийся в открытом доступе, со страницы 1273 20-го издания «Анатомии Грея» (1918 г.)
В статье использован текст, находящийся в открытом доступе, со страницы 1273 20-го издания «Анатомии Грея» (1918 г.)
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )