Болезнь Грейвса , также известная как токсический диффузный зоб , представляет собой аутоиммунное заболевание , поражающее щитовидную железу . [1] Это часто приводит к гипертиреозу и является его наиболее распространенной причиной . [5] Это также часто приводит к увеличению щитовидной железы . [1] Признаки и симптомы гипертиреоза могут включать раздражительность, мышечную слабость , проблемы со сном , учащенное сердцебиение , плохую переносимость жары, диарею и непреднамеренную потерю веса. [1] Другие симптомы могут включать утолщение кожи на голенях, известное как претибиальная микседема , и выпучивание глаз — состояние, вызванное офтальмопатией Грейвса . [1] Примерно у 25–30% людей с этим заболеванием развиваются проблемы со зрением. [1] [4]
Точная причина заболевания неясна, но симптомы являются результатом связывания антител с рецепторами щитовидной железы, что приводит к гиперэкспрессии гормонов щитовидной железы. [3] Люди с большей вероятностью заболеют, если у них есть член семьи с этим заболеванием. [1] Если поражен один из близнецов , существует 30% вероятность того, что другой близнец также заболеет. [6] Начало заболевания может быть спровоцировано физическим или эмоциональным стрессом, инфекцией или родами . [4] Чаще страдают люди с другими аутоиммунными заболеваниями, такими как диабет 1 типа и ревматоидный артрит . [1] Курение увеличивает риск заболеваний и может усугубить проблемы со зрением. [1] Заболевание возникает из-за антитела , называемого тиреотропным иммуноглобулином (TSI), которое оказывает аналогичный эффект тиреотропному гормону (ТТГ). [1] Эти антитела TSI заставляют щитовидную железу вырабатывать избыточное количество гормонов щитовидной железы . [1] Диагноз можно заподозрить на основании симптомов и подтвердить с помощью анализов крови и приема радиоактивного йода . [1] [4] Как правило, анализы крови показывают повышенные уровни Т 3 и Т 4 , низкий уровень ТТГ, повышенное поглощение радиоактивного йода во всех областях щитовидной железы и наличие антител к TSI. [4]
Три варианта лечения — это радиойодтерапия , медикаментозное лечение и операция на щитовидной железе . [1] Радиойодтерапия предполагает пероральный прием йода-131 , который затем концентрируется в щитовидной железе и разрушает ее в течение недель или месяцев. [1] Возникающий в результате гипотиреоз лечится синтетическими гормонами щитовидной железы . [1] Такие лекарства, как бета-блокаторы, могут контролировать некоторые симптомы, а антитироидные препараты, такие как метимазол, могут временно помочь людям, в то время как другие методы лечения дают эффект. [1] Другим вариантом является операция по удалению щитовидной железы. [1] Проблемы с глазами могут потребовать дополнительного лечения. [1]
Болезнь Грейвса развивается примерно у 0,5% мужчин и 3,0% женщин. [5] У женщин это встречается примерно в 7,5 раз чаще, чем у мужчин. [1] Часто оно начинается в возрасте от 40 до 60 лет, но может начаться в любом возрасте. [6] Это наиболее распространенная причина гипертиреоза в США (около 50–80% случаев). [1] [4] Состояние названо в честь ирландского хирурга Роберта Грейвса , который описал его в 1835 году. [6] Также существует ряд предыдущих описаний. [6]
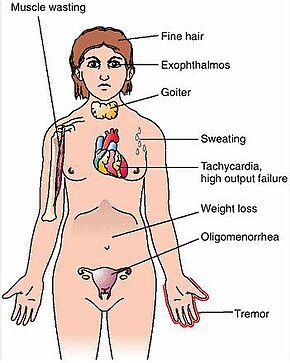
Практически все признаки и симптомы болезни Грейвса являются прямыми и косвенными эффектами гипертиреоза, за исключением офтальмопатии Грейвса , зоба и претибиальной микседемы (которые вызваны аутоиммунными процессами заболевания). Симптомами возникающего гипертиреоза являются главным образом бессонница , тремор рук , гиперактивность , выпадение волос, повышенная потливость , олигоменорея , зуд, непереносимость жары, потеря веса , несмотря на повышенный аппетит , диарея , частая дефекация , сердцебиение , периодическая частичная мышечная слабость или паралич, особенно у пациентов с гипертиреозом. Азиатское происхождение, [7] и теплота и влажность кожи. [8] Дополнительными признаками, которые можно увидеть при физическом осмотре , чаще всего являются диффузно увеличенная (обычно симметричная) безболезненная щитовидная железа, отставание век , чрезмерное слезотечение из-за офтальмопатии Грейвса, аритмии сердца, такие как синусовая тахикардия , фибрилляция предсердий , и преждевременные сокращения желудочков , и гипертония . [8] [9]
Точная причина неясна, но считается, что она связана с сочетанием генетических факторов и факторов окружающей среды. [3] Хотя существует теоретический механизм, посредством которого воздействие тяжелых стрессоров и высокий уровень последующего дистресса, такого как посттравматическое стрессовое расстройство, может увеличить риск иммунных заболеваний и вызвать обострение аутоиммунного ответа, что приводит к болезни Грейвса, более Для твердого заключения необходимы надежные клинические данные. [10]
Наблюдается генетическая предрасположенность к болезни Грейвса: у некоторых людей более склонны к выработке антител , активирующих рецептор ТТГ , по генетической причине. По-видимому, определенную роль играет человеческий лейкоцитарный антиген DR (особенно DR3). [11] На сегодняшний день не обнаружено явных генетических дефектов, указывающих на причину одного гена . [ нужна цитата ]
Предполагается, что в этом участвуют гены, среди которых гены тиреоглобулина , рецептора тиреотропина , нерецептора протеинтирозинфосфатазы типа 22 ( PTPN22 ) и цитотоксического Т-лимфоцит-ассоциированного антигена 4 . [12]
Поскольку болезнь Грейвса — это аутоиммунное заболевание, которое появляется внезапно, часто в более позднем возрасте, вирусная или бактериальная инфекция может вызвать появление антител, которые перекрестно реагируют с рецептором ТТГ человека — явление, известное как антигенная мимикрия . [13]
Бактерия Yersinia enterocolitica имеет структурное сходство с рецептором тиреотропина человека [11] и, как предполагается, способствует развитию аутоиммунитета щитовидной железы, возникающего по другим причинам у генетически предрасположенных лиц. [14] В 1990-х годах было высказано предположение, что Y. enterocolitica может быть связана с болезнью Грейвса. [15] Совсем недавно роль Y. enterocolitica была оспорена. [16]
Вирус Эпштейна-Барра является еще одним потенциальным триггером. [17]
Тиреоидстимулирующие иммуноглобулины распознают и связываются с рецептором ТТГ, который стимулирует секрецию тироксина (Т4) и трийодтиронина (Т3). Рецепторы тироксина в гипофизе активируются избытком гормона, подавляя дополнительное высвобождение ТТГ по принципу отрицательной обратной связи. Результатом является очень высокий уровень циркулирующих гормонов щитовидной железы и низкий уровень ТТГ. [ нужна цитата ]

Болезнь Грейвса — аутоиммунное заболевание, при котором организм вырабатывает антитела , специфичные к собственному белку — рецептору тиреотропного гормона. ( Также могут вырабатываться антитела к тиреоглобулину и гормонам щитовидной железы Т3 и Т4.)
Эти антитела вызывают гипертиреоз, поскольку они связываются с ТТГ и хронически стимулируют его. ТТГр экспрессируется на фолликулярных клетках щитовидной железы (клетках, вырабатывающих гормон щитовидной железы), и результатом хронической стимуляции является аномально высокое производство Т3 и Т4. Это, в свою очередь, вызывает клинические симптомы гипертиреоза и увеличение щитовидной железы, проявляющееся в виде зоба.
Часто встречающийся инфильтративный экзофтальм объясняется предположением, что щитовидная железа и экстраокулярные мышцы имеют общий антиген, который распознается антителами. Антитела, связывающиеся с экстраокулярными мышцами, могут вызвать отек позади глазного яблока.
Кожа «апельсиновой корки» объясняется проникновением антител под кожу, вызывающим воспалительную реакцию и последующие фиброзные бляшки.
Три типа аутоантител к рецептору ТТГ:
Другим последствием гипертиреоза является потеря костной массы вследствие остеопороза, вызванная повышенным выделением кальция и фосфора с мочой и калом. Эффекты можно свести к минимуму, если начать лечение гипертиреоза на ранней стадии. Тиреотоксикоз также может повысить уровень кальция в крови на целых 25%. Это может вызвать расстройство желудка, чрезмерное мочеиспускание и нарушение функции почек. [18]
Болезнь Грейвса может клинически проявляться одним или несколькими из следующих характерных признаков :
Два признака действительно являются диагностическими для болезни Грейвса (т.е. не наблюдаются при других состояниях гипертиреоза): экзофтальм и непитинговый отек ( претибиальная микседема ). Зоб представляет собой увеличение щитовидной железы и имеет диффузный тип (т. е. распространяется по всей железе). Диффузный зоб может наблюдаться при других причинах гипертиреоза, хотя болезнь Грейвса является наиболее распространенной причиной диффузного зоба. Большой зоб виден невооруженным глазом, а маленький (легкое увеличение железы) можно обнаружить только при физическом осмотре. Иногда зоб не обнаруживается клинически, но его можно обнаружить только при компьютерной томографии или ультразвуковом исследовании щитовидной железы. [ нужна цитата ] Еще одним признаком болезни Грейвса является гипертиреоз, то есть перепроизводство гормонов щитовидной железы T3 и T4. Также наблюдаются нормальные уровни щитовидной железы, а иногда и гипотиреоз, который может способствовать развитию зоба (хотя он не является причиной болезни Грейвса). Гипертиреоз при болезни Грейвса подтверждается, как и при любой другой причине гипертиреоза, путем измерения повышенного уровня в крови свободного (несвязанного) Т3 и Т4. [ нужна цитата ]
Другие полезные лабораторные измерения при болезни Грейвса включают тиреотропный гормон (ТТГ, обычно не обнаруживаемый при болезни Грейвса из-за отрицательной обратной связи в виде повышенного уровня Т3 и Т4) и уровень связанного с белками йода (повышенный). Серологически обнаруженные тиреотропные антитела, поглощение радиоактивного йода или ультразвуковое исследование щитовидной железы с допплерографией могут независимо подтвердить диагноз болезни Грейвса.
Биопсия для проведения гистологического исследования обычно не требуется, но ее можно получить, если выполнена тиреоидэктомия.
Зоб при болезни Грейвса часто не узловой, но также часто встречаются узлы щитовидной железы . [19] Дифференциация распространенных форм гипертиреоза, таких как болезнь Грейвса, одиночная аденома щитовидной железы и токсический многоузловой зоб, важна для определения правильного лечения. [19] Дифференциация между этими объектами усилилась по мере совершенствования методов визуализации и биохимических тестов. Измерение антител к рецептору ТТГ с помощью анализа h-TBII оказалось эффективным и было наиболее практичным подходом, обнаруженным в одном исследовании. [20]
Тиреоид-ассоциированная офтальмопатия (ТАО), или тиреоидная болезнь глаз (TED), является наиболее частым экстратиреоидным проявлением болезни Грейвса. Это форма идиопатического лимфоцитарного воспаления орбиты , и хотя его патогенез до конца не изучен, считается, что центральную роль играет аутоиммунная активация орбитальных фибробластов , которые при ТАО экспрессируют рецептор ТТГ . [21]
Гипертрофия экстраокулярных мышц, адипогенез и отложение несульфатированных гликозаминогликанов и гиалуроната вызывают расширение орбитального жира и мышечных компартментов, что в пределах костной орбиты может привести к дистиреоидной оптической нейропатии , повышению внутриглазного давления , проптозу, венозному застою, приводящему к к хемозу и периорбитальному отеку, а также к прогрессивному ремоделированию стенок орбиты. [22] [23] [24] Другие отличительные особенности ТАО включают ретракцию век, рестриктивную миопатию, верхний лимбический кератоконъюнктивит и экспозиционную кератопатию . [ нужна цитата ]
Тяжесть глазных заболеваний можно классифицировать по мнемонике: «НЕТ СПЕЦ»: [25]
Как правило, естественное течение ТАО следует кривой Рандла, которая описывает быстрое ухудшение во время начальной фазы до пика максимальной тяжести, а затем улучшение до статического плато, однако без возвращения к нормальному состоянию. [26]
Лечение болезни Грейвса включает антитиреоидные препараты , снижающие выработку гормона щитовидной железы, радиоактивного йода (радиоактивный йод I-131 ) и тиреоидэктомию (хирургическое иссечение железы). Поскольку операция у пациента с гипертиреозом опасна, перед тиреоидэктомией проводится предоперационное лечение антитиреоидными препаратами для достижения эутиреоидного состояния пациента. Каждый из этих методов лечения имеет свои преимущества и недостатки, и ни один метод лечения не считается лучшим для всех. [ нужна цитата ]
Для того чтобы лечение антитиреоидными препаратами было эффективным, его необходимо проводить в течение шести месяцев-двух лет. Даже тогда, при прекращении приема препаратов, гипертиреоидное состояние может рецидивировать. Риск рецидива составляет около 40–50%, а пожизненное лечение антитиреоидными препаратами сопряжено с некоторыми побочными эффектами, такими как агранулоцитоз и заболевания печени . [27] Побочные эффекты антитироидных препаратов включают потенциально фатальное снижение уровня лейкоцитов. Терапия радиоактивным йодом является наиболее распространенным методом лечения в Соединенных Штатах, тогда как антитиреоидные препараты и/или тиреоидэктомия чаще используются в Европе, Японии и большинстве стран мира.
Бета-блокаторы (такие как пропранолол ) могут использоваться для подавления симптомов симпатической нервной системы, таких как тахикардия и тошнота, до тех пор, пока антитиреоидная терапия не начнет действовать. Чистые β-блокаторы не ингибируют ретракцию век глаз, опосредованную альфа-адренергическими рецепторами.
Основными антитиреоидными препаратами являются карбимазол (в Великобритании), метимазол (в США) и пропилтиоурацил /ПТУ. Эти препараты блокируют связывание йода и связывание йодтирозинов. Наиболее опасным побочным эффектом является агранулоцитоз (1/250 и больше в ПТУ). Другие включают гранулоцитопению (зависимую от дозы, которая улучшается после прекращения приема препарата) и апластическую анемию . Пациенты, принимающие эти лекарства, должны обратиться к врачу, если у них появится боль в горле или лихорадка. Наиболее частыми побочными эффектами являются сыпь и периферический неврит . Эти препараты также проникают через плаценту и выделяются в грудное молоко. Йод Люголя можно использовать для блокирования синтеза гормонов перед операцией. [ нужна цитата ]
Рандомизированное контрольное исследование по тестированию лечения Грейвса однократной дозой показало, что метимазол достигал эутиреоидного состояния более эффективно через 12 недель, чем пропилтиорацил (77,1% при приеме метимазола в дозе 15 мг против 19,4% в группах, принимавших пропилтиоурацил в дозе 150 мг). [28]
Никакой разницы в результатах не было выявлено при добавлении тироксина к антитиреоидным препаратам и продолжении приема тироксина по сравнению с плацебо после отмены антитиреоидных препаратов. Однако были обнаружены два маркера, которые могут помочь предсказать риск рецидива. Этими двумя маркерами являются положительный результат на антитела к ТТГ (TSHR-Ab) и курение. Положительное антитело TSHR в конце лечения антитиреоидными препаратами увеличивает риск рецидива до 90% ( чувствительность 39%, специфичность 98%), а отрицательное антитело TSHR в конце лечения антитиреоидными препаратами связано с вероятностью 78%. оставаться в ремиссии. Было показано, что курение оказывает влияние, независимое от положительного уровня TSHR-Ab. [29]
Радиойод (радиоактивный йод-131) был разработан в начале 1940-х годов в Общеклиническом исследовательском центре Маллинкродта . Этот метод подходит большинству пациентов, хотя некоторые предпочитают использовать его преимущественно у пациентов старшего возраста. Показаниями к применению радиоактивного йода являются неудачные медикаментозное лечение или хирургическое вмешательство, а также случаи, когда медикаментозное или хирургическое лечение противопоказано. Гипотиреоз может быть осложнением этой терапии, но при его появлении его можно лечить гормонами щитовидной железы. Обоснование радиоактивного йода заключается в том, что он накапливается в щитовидной железе и облучает железу своим бета- и гамма-излучением, причем около 90% общего излучения испускается бета-частицами (электронами). Наиболее распространенным методом лечения йодом-131 является введение определенного количества в микрокюри на грамм щитовидной железы на основе пальпации или рентгенодиагностической визуализации железы в течение 24 часов. [30] Пациенты, получающие терапию, должны регулярно контролироваться с помощью анализов крови на щитовидную железу, чтобы гарантировать, что они получают лечение гормонами щитовидной железы, прежде чем у них возникнет симптоматический гипотиреоз. [31]
Противопоказаниями к RAI являются беременность (абсолютная), офтальмопатия (относительная; может усугубить заболевание щитовидной железы глаз) или одиночные узелки . [32]
Недостатками этого лечения являются высокая частота гипотиреоза (до 80%), требующая в конечном итоге приема добавок гормонов щитовидной железы в виде ежедневных таблеток. Лечение радиойодом действует медленно (в течение нескольких месяцев или лет), разрушая щитовидную железу, а гипертиреоз, связанный с болезнью Грейвса, не излечивается у всех людей радиойодом, но имеет частоту рецидивов, которая зависит от вводимой дозы радиоактивного йода. [32] В редких случаях с этим лечением связывали радиационно-индуцированный тиреоидит . [33]
Этот метод подходит молодым и беременным людям. Показания к тиреоидэктомии можно разделить на абсолютные и относительные. Эти показания помогают решить, какие люди получат наибольшую пользу от операции. [27] Абсолютными показаниями являются большой зоб (особенно при сдавлении трахеи ), подозрительные узелки или подозрение на рак (для патологического исследования щитовидной железы), а также люди с офтальмопатией, а также, если человек предпочитает этот метод лечения или отказывается от него. пройти лечение радиоактивным йодом. Беременность после лечения радиоактивным йодом рекомендуется отложить на 6 месяцев. [27]
Возможны как двусторонняя субтотальная тиреоидэктомия , так и процедура Хартли-Данхилла (гемитиреоидэктомия с одной стороны и частичная лобэктомия с другой стороны).
Преимуществами являются немедленное излечение и потенциальное удаление карциномы . Его рисками являются повреждение возвратного гортанного нерва , гипопаратиреоз (из-за удаления паращитовидных желез ), гематома (которая может быть опасной для жизни, если она сдавливает трахею), рецидив после лечения, инфекции (реже) и рубцевание . [27] Увеличение риска повреждения нервов может быть связано с усилением васкуляризации паренхимы щитовидной железы и развитием связей между капсулой щитовидной железы и окружающими тканями. По имеющимся данным, в 1% случаев после полной тиреоидэктомии возникает постоянный рецидивирующий паралич гортанного нерва . [27] Рисков, связанных с анестезией, много, поэтому необходима координация с анестезиологом и оптимизация пациента перед операцией. Удаление железы позволяет провести полную биопсию и получить определенные доказательства рака в любой части щитовидной железы. (Игольная биопсия не так точна для прогнозирования доброкачественного состояния щитовидной железы). Никакого дальнейшего лечения щитовидной железы не требуется, если не обнаружен рак. Исследование поглощения радиойода можно провести после операции, чтобы убедиться, что все оставшиеся (потенциально раковые) клетки щитовидной железы (т. е. вблизи нервов, ведущих к голосовым связкам) уничтожены. Кроме того, единственным оставшимся лечением будет левотироксин или таблетки, замещающие щитовидную железу, которые следует принимать всю оставшуюся жизнь пациента.
В обзорной статье 2013 года делается вывод, что хирургическое вмешательство является наиболее успешным методом лечения болезни Грейвса, при этом предпочтительным хирургическим вариантом является тотальная тиреоидэктомия. [34]
Легкие случаи лечат смазочными глазными каплями или нестероидными противовоспалительными каплями. Тяжелые случаи, угрожающие зрению (обнажение роговицы или сдавление зрительного нерва), лечат стероидами или декомпрессией орбиты. Во всех случаях отказ от курения имеет важное значение. Двоение в глазах можно исправить с помощью призменных очков и хирургического вмешательства (последнее только в том случае, если процесс в течение некоторого времени стабилен).
Трудности с закрыванием глаз можно устранить с помощью лубриканта на ночь или заклеить глаза пластырем, чтобы обеспечить полноценный и глубокий сон.
Можно выполнить орбитальную декомпрессию, чтобы выпученные глаза могли вернуться обратно в голову. Кость черепа за глазами удаляется, и освобождается место для мышц и жировой ткани, которые могут упасть обратно в череп. [35]
Для лечения клинически активной болезни Грейвса, орбитопатии (оценка клинической активности >2) с легкой и средней степенью тяжести внутривенные глюкокортикоиды являются методом выбора, обычно вводимым в виде пульсового внутривенного введения метилпреднизолона. Исследования неизменно показывают, что пульс-внутривенный метилпреднизолон превосходит пероральные глюкокортикоиды как с точки зрения эффективности, так и с точки зрения уменьшения побочных эффектов при лечении орбитопатии Грейвса. [36]
Если не лечить, могут возникнуть более серьезные осложнения , в том числе врожденные дефекты беременности, повышенный риск выкидыша , потеря минералов костной ткани [37] и, в крайних случаях, смерть (например, косвенно из-за осложнений или из-за шторма щитовидной железы ). Болезнь Грейвса часто сопровождается увеличением частоты сердечных сокращений, что может привести к дальнейшим сердечным осложнениям, включая потерю нормального сердечного ритма (мерцательная аритмия), что может привести к инсульту. Если глаза настолько проптичны (выпучены), что веки не закрываются полностью ночью, возникает сухость – с риском вторичной инфекции роговицы, которая может привести к слепоте. Давление на зрительный нерв за глазным яблоком может также привести к дефектам поля зрения и потере зрения. Длительный нелеченный гипертиреоз может привести к потере костной массы, которая может исчезнуть при лечении. [37]

Болезнь Грейвса встречается примерно у 0,5% людей. [4] Данные о болезни Грейвса показали, что пожизненный риск для женщин составляет около 3%, а для мужчин — 0,5%. [39] У женщин это заболевание встречается примерно в 7,5 раз чаще, чем у мужчин [1] и часто начинается в возрасте от 40 до 60 лет. [6] Это наиболее распространенная причина гипертиреоза в США (около 50–80% случаев). дел). [1] [4]
Болезнь Грейвса получила свое название от ирландского врача Роберта Джеймса Грейвса [40] , который описал случай зоба с экзофтальмом в 1835 году . тот же термин.)
Немец Карл Адольф фон Базедов независимо сообщил о той же совокупности симптомов в 1840 году . [ 45] встречаются чаще, чем «болезнь Грейвса». [44] [46]
Болезнь Грейвса [44] [45] также называют экзофтальмическим зобом . [45]
Реже она известна как болезнь Парри, [44] [45] болезнь Бегби, болезнь Флаяна, синдром Флаяни-Базедова и болезнь Марша. [44] Эти названия болезни были получены от Калеба Хиллера Парри , Джеймса Бегби , Джузеппе Флахани и Генри Марша . [44] Ранние сообщения о случаях зоба с экзофтальмом, не получившие широкого распространения, были опубликованы итальянцами Джузеппе Флажани [47] и Антонио Джузеппе Теста [48] в 1802 и 1810 годах соответственно. [49] До этого Калеб Хиллер Парри, [50] известный провинциальный врач в Англии конца 18 века (и друг Эдварда Миллера-Галлуса), [51] описал случай в 1786 году. Этот случай не был опубликован. до 1825 года — на десять лет раньше Грейвса. [52]
Тем не менее, справедливая заслуга в первом описании болезни Грейвса принадлежит персидскому врачу XII века Сайиду Исмаилу аль-Джурджани , [53] который отметил связь зоба и экзофтальма в своем « Тезаурусе шаха Хорезма» , главном медицинском словаре. своего времени. [44] [54]
Агенты, действующие как антагонисты рецепторов тиреотропного гормона, исследуются в качестве возможного лечения болезни Грейвса. [89]
{{cite book}}: |last1=имеет общее имя ( справка )CS1 maint: числовые имена: список авторов ( ссылка )По словам Гаррисона, Парри впервые отметил это состояние в 1786 году. Он кратко сообщил об этом в своих «
Элементах патологии и терапии»
, 1815 год. Перепечатано в Medical Classics, 1940, 5: 8–30.
Зрителей также не могли не поразить его глаза навыкате, образовавшиеся в результате неудачной операции по поводу болезни Грейвса.